盐酸左氧氟沙星缓释滴眼液的毒性及刺激性反应Δ
2010-08-06王文彤陶遵威天津市医药科学研究所天津市300020
张 娜,高 萍,王文彤,陶遵威,郑 夺(天津市医药科学研究所,天津市 300020)
盐酸左氧氟沙星是第3代氟喹诺酮类抗菌药物,具有水溶性好、活性强、广谱、毒副作用低等特点,对细菌性结膜炎和角膜炎等眼科感染有良好的疗效,具有广泛的临床应用前景[1]。本文选用壳聚糖和胶原蛋白为增效剂及增稠剂制备了盐酸左氧氟沙星缓释滴眼液,延缓了其在眼部释药时间,提高了生物利用度,并参考GB/T 16886.5-2003《医疗器械生物学评价第5部分:体外细胞毒性试验》[2]中试验方法评价了该滴眼液的体外细胞毒性,参照《药理实验方法学》评价了其急性毒性和皮肤刺激反应[3],保证安全给药的同时还为进一步开展临床试验提供了科学依据。
1 材料
1.1 细胞与动物
小鼠成纤维细胞(简称L-929细胞,中国药品生物制品检定所);昆明种小白鼠,♂♀各半,体质量17~20 g,合格证号:SCXK(京)2007-0001;大耳白兔,♂♀各半,体质量2.0~2.5 kg,合格证号:SCXK(京)2005-0002,均由北京维通利华实验动物技术有限公司提供。
1.2 试药
RPMI 1640细胞培养液(美国GIBCO公司);胎牛血清和胰蛋白酶(美国Sigma公司);高密度聚乙烯(江门市新会区浩天工贸有限公司,批号:081218);琼脂粉(北京三药科技开发公司生产,批号:061219);0.9%氯化钠注射液(中国大冢制药有限公司,批号:8C93B);盐酸左氧氟沙星缓释滴眼液(自制,批号:081011、081012、081013,规格:15 mg·5 mL-1)。
1.3 仪器
MLS-3750型高压蒸汽灭菌器和MCO-18AIC(UV)型CO2培养箱均由日本Sanyo公司提供;W-7401超净工作台(德国Steag公司);TMS型倒置显微镜(日本Nikon公司)。
2 方法
2.1 体外细胞毒性试验
2.1.1 样品的制备。试验样品:将0.1 mL盐酸左氧氟沙星缓释滴眼液滴在直径10 mm的8层滤纸圆片上;阴性对照:直径为10 mm的高密度聚乙烯圆片;阳性对照:涂有邻苯二甲酸二辛酯的直径为10 mm的聚氯乙烯圆片;生理盐水对照:将0.1 mL生理盐水滴在直径10 mm的8层滤纸圆片上。
2.1.2 操作步骤。采用琼脂扩散法[2]检测细胞毒性:取正常传代的L-929细胞10 mL,接种于直径为90 mm的培养皿内,每皿接种细胞3×106个,在37℃、5%CO2培养箱培养24 h后,弃去原培养液,加入10 mL琼脂培养基(3%琼脂与2倍的RPMI 1640细胞培养液按1∶1混合),待其凝固后,每一平皿内放阴、阳性及生理盐水对照各1片、试验样品2片、平行操作5皿,于37℃、5%CO2培养箱再培养24 h,弃去所有样品(试验样品,阴、阳性及生理盐水对照),用0.01%中性红染色20 min后进行结果评定。
2.1.3 评定指标[2]。用倒置显微镜观察试验样品和阴、阳性及生理盐水对照圆片下及周围褪色区域,并按表1所示指标评价每一样品的褪色指数和溶解指数,再按表2确定各组细胞毒性反应的分级,表1、表2见下。

表1 褪色指数和溶解指数评价标准Tab 1 Evaluation standard of fading index and dissolving index
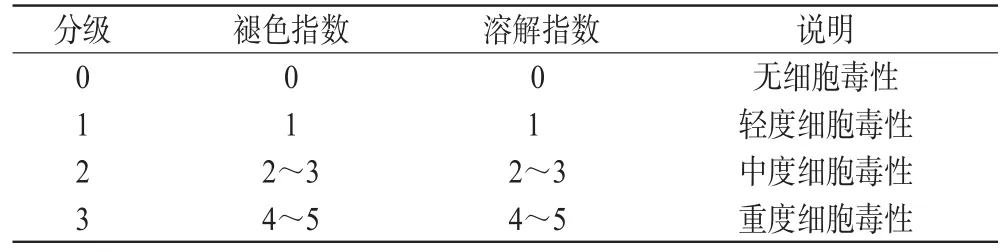
表2 细胞反应分级评价标准Tab 2 Evaluation standard for the grade of cellular reaction
2.2 急性毒性实验[3]
选小鼠20只,平均分为供试品组和空白对照组,每组10只,均采用静脉注射方式给药,供试品组以盐酸左氧氟沙星缓释滴眼液按15 mg·kg-1给药1次,相当于成人临床日用量的(成人每日盐酸左氧氟沙星为4.5 mg,按成人体质量60 kg计算,剂量为0.075 mg·kg-1)200倍;空白对照组给相同体积的生理盐水。注射完毕后,观察14 d小鼠的一般状态和死亡数,并记录体质量变化。
2.3 皮肤刺激反应实验
2.3.1 实验步骤。选用大耳白兔12只,实验前24 h剪剃其背部脊柱两侧被毛备皮,去毛范围为3 cm×3 cm,随机分为皮肤完好组和皮肤破损组,每组6只,另在皮肤破损组兔的脊柱两侧用无菌针头划成“#”,以渗血为准。采用同体左右侧自身对照,将盐酸左氧氟沙星缓释滴眼液滴到2.5 cm×2.5 cm的纱布块上,敷贴在左侧背部,阴性对照将生理盐水滴到2.5 cm×2.5 cm的纱布块上,敷贴在右侧背部,用半封闭性包扎带固定6 h,每次用量均为1.5 mg·d-1,每天1次,连续用药7 d。末次用药24 h后,用温水去除残留药物,分别于1、24、48、72 h连续观察并记录涂药部位有无红斑及水肿等情况。
2.3.2 评定指标。红斑和水肿按以下标准进行评分[3]:无红斑0分,红斑勉强可见为1分,红斑明显可见2分,严重红斑3分,紫红色红斑并有焦痂形成4分;无水肿0分,水肿勉强可见1分,边缘高出周围皮肤的水肿2分,皮肤隆起约1 mm、轮廓清楚的水肿为3分,皮肤隆起1 mm以上范围扩大的水肿4分。平均分值=(红斑反应总分+水肿反应总分)/每组动物数,按平均分值进行刺激强度[4]评价,皮肤刺激强度评价标准见表3。

表3 皮肤刺激强度评价标准Tab 3 Evaluated standard of skin irritation
3 结果
3.1 体外细胞毒性
各组褪色指数和溶解指数结果详见表4。
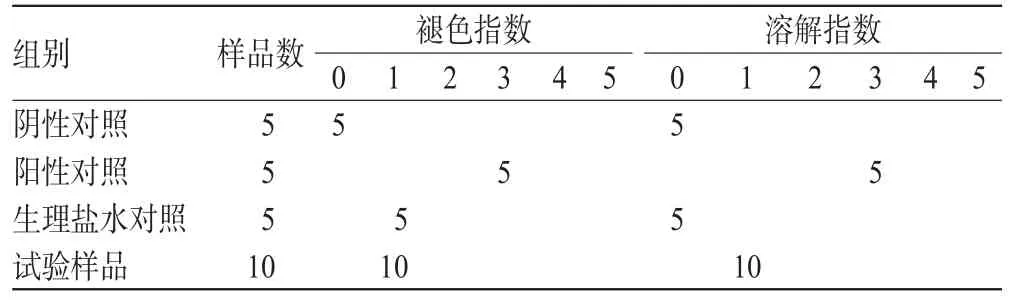
表4 各组细胞褪色指数和溶解指数结果Tab 4 Results of fading index and dissolving index
由表4分析可知,阴性对照、阳性对照、生理盐水对照、试验样品的细胞毒性反应分别为0、2、1、1级。
3.2 急性毒性
注射后小鼠在观察期状况良好,活动、食欲正常,呼吸平稳,无惊厥、瘫痪和死亡等毒性反应,小鼠体质量日渐增加。利用SPSS统计软件将空白对照组和供试品组每天的体质量进行组间t检验分析,结果见表5。
表5 各组小鼠体质量比较(g,±s,n=10)Tab 5 Comparison of body weight of mic(eg,±s,n=10)

表5 各组小鼠体质量比较(g,±s,n=10)Tab 5 Comparison of body weight of mic(eg,±s,n=10)
空白对照组17.7±0.5 18.5±0.8 20.2±0.8 21.9±0.8 23.6±0.8 26.6±0.7 31.6±0.6时间/d 1 2 3 5 7 1 0 14供试品组17.5±0.6 18.3±1.0 19.7±1.1 21.3±1.3 22.8±1.3 25.6±1.5 30.4±1.5
由表5可知,供试品组与空白对照组小鼠在14 d内体质量变化没有明显差异,表明该滴眼液对实验小鼠体质量没有明显影响。
3.3 皮肤刺激反应
除去敷贴物后1、24、48、72 h,观察各部位皮肤组织反应情况,皮肤完好组兔用药侧、对照侧皮肤均未发现红斑及水肿,皮肤刺激强度评价均为无刺激性(平均分值为0)。破损皮肤组1、24 h时仅有1只出现红斑和水肿,48 h后反应平均分值均为0,5 d后伤口均愈合,基本恢复正常状态,皮肤刺激评价均为无刺激性(平均分值均小于0.50),具体结果见表6。
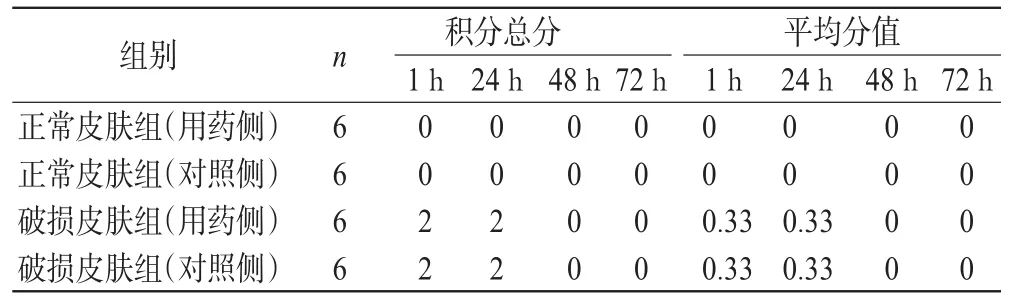
表6 各组小鼠皮肤刺激实验结果Tab 6 Results of dermal irritation test of each group
4 讨论
本课题首次将壳聚糖和胶原蛋白同时与盐酸左氧氟沙星配方组合制备盐酸左氧氟沙星缓释滴眼液。壳聚糖为甲壳类动物中提取的天然多糖甲壳素的脱乙酰产物,壳聚糖的加入不但增加了药液的黏度,延长了药物在眼内的滞留时间,增加了药物的吸收,而且该物质本身具有消炎、抑菌、止血等功能[4];另外有文献[5]数据表明,大、小白鼠口服壳聚糖的半数致死剂量(LD50)>16 g·kg-1,与蔗糖相当,长期毒性实验亦无明显毒性发生,未发现诱变性、皮肤刺激性和过敏反应发生。胶原蛋白是连接组织的主要结构蛋白,胶原蛋白不仅可以作为载体使药物在眼部缓慢释放,而且还可以促进角膜上皮细胞损伤的修复和细胞生长[6],另外胶原蛋白溶液是一种无毒、无刺激、无过敏性的安全新型外用药物[7]。壳聚糖和胶原蛋白作为新型、安全的生物材料,在眼科疾病治疗中发挥着越来越重要的作用。
盐酸左氧氟沙星缓释滴眼液的体外细胞毒性、急性毒性和皮肤刺激反应均符合相关国家规范和要求,本实验研究证明了该滴眼液用药的安全性,为进一步深入研究和推广应用提供了的科学实验依据。
[1]汪荣军.左氧氟沙星眼用凝胶的制备[J].安徽医药,2006,10(2):141.
[2]GB/T16886.5-2003,中华人民共和国国家标准[S].
[3]徐叔云,卞如濂,陈 修.药理实验方法学[M].北京:人民卫生出版社,2001:227.
[4]赖善城,卢雪梅.加替沙星壳聚糖滴眼液的制备及质量控制[J].中国药房,2005,16(24):1 870.
[5]曾 健,李晓辉,黄钺华,等.壳聚糖DCX-16的初步安全性评价[J].中国药房,2005,16(3):172.
[6]刘慧玲,王 栋,章金刚.胶原蛋白在临床医学中的应用[J].北京生物医学工程,2005,24(3):239.
[7]冯国基,潘建明,吴晓斌,等.胶原溶液的安全性试验研究[J].广东药学,1995,5(4):39.
