薄层色谱“一条”法检测99Tcm药物的放化纯度
2010-07-18王吉欣张艳华
王吉欣,张艳华
(北京大学临床肿瘤学院北京肿瘤医院暨北京市肿瘤防治研究所,北京 100142)
99Tcm-MDP作为一种有效的骨显像剂,在临床已应用多年,但99Tcm-MDP注入体内后,全身放射性本底很高,需等待2~3 h本底下降后,才能进行骨显像。怀疑是由于99Tcm-MDP放化纯度偏低导致。薄层色谱(TLC)“一条(onestrip)”法[1-2],可以在一条硅胶板上将主产品及多种杂质如游离锝、锝锡胶体及可能存在的相对分子质量相差较大的其他杂质分离清楚后,按组分分段测定放射性,并计算放化纯度。此“一条”法曾用于检测99Tcm-PYM,具有分离组分准确、可信,分离效果较好的优点。故于2002年采用此法试测由原子高科股份有限公司(京原)提供的99Tcm-MDP,用传统的放射性自显影(Radioautography,简称自显影)观察斑点,按锝锡胶体、标记物、游离锝分离清楚的三段,分别刮板测放射性,并计算其放化纯度为26%。2008年采用免洗胶片自显影法,检查99Tcm-MDP等6种常见锝药物用此“一条”法的分离效果,并定性估测99Tcm-MDP的放化纯度。2009年用同法复查3种锝药物,目的是试用一种方法测定多种锝药物,达到放化纯度检测的规范化和统一化。
1 实验材料
2008 年 用99Tcm-MDP、99TcmO4-、99Tcm-DTPA 、99Tcm-EC 、99Tcm-MIBI 和99Tcm-MAA 6种药物由北京欣科思达医药科技有限公司(简称京欣)提供,2009年用99Tcm-DTPA和99Tcm-MIBI均为京欣产品,99Tcm-MDP为京原与京欣两种产品,所有药物注射液的pH均接近生理盐水(4.5~7.0);SG硅胶板:青岛海洋化工厂产品,切成1 cm×10 cm硅胶条备用;曝光用免洗胶片:ISP International Specialty Products Inc提供,切成1 cm×10 cm;其他化学试剂均为北京化工厂产品。
2 实验方法
采用上行TLC法,固定相为硅胶条,流动相为V(10%醋酸铵)∶V(甲醇)=1∶1。用微量注射器分别取材料中所提供的6种锝药物,每次2μL,分3~5次点样,斑点直径小于4mm,趁斑点未干时立即放入色谱槽的流动相中,展开约6 cm取出,用吹风机干燥后,将硅胶条与免洗胶片全部紧密接触,用两条比硅胶条大些的玻璃片夹住,并用橡皮筋缠紧,自显影24 h,取下胶片,测量胶片上各斑点中心与原点的距离,计算R f,实验重复4次,取平均值,以±s表示。
3 结 果
3.1 6种常见99Tcm药物的自显影
2008年,TLC“一条”法后的自显影采用免洗胶片代替传统的X光胶片,共测定了6种锝药物(含99TcmO4-),99Tcm-DTPA 测 2次,其余各测1次,结果示于图1。由图1可以看出,除99Tcm-MAA保留在原点未被分开外,另5种锝药物的组分均可被分开。按在硅胶条上展开后,标记主要产物与原点间的距离由大到小依次为99TcmO4-、99Tcm-EC 、99Tcm-MDP 、99Tcm-DTPA(1为2009-05-13产品,2为2009-05-16产品)和99Tcm-MIBI,表明移动距离与标记物的相对分子质量相关,也进一步说明此法可用于检测多种锝药物。按图1计算99Tcm-MDP的Rf为0.7,肉眼观察其放化纯度偏低,但高于2002年测定结果;99Tcm-DTPA 2次自显影的斑点颜色深浅不同,表明其放化纯度有差异。
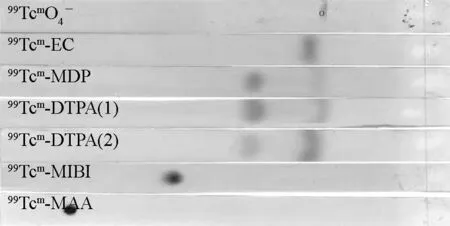
图1 6种常用锝药物的放射性自显影
3.2 部分99Tcm药物的复查
2009年用上述方法对99Tcm-MDP、99Tcm-DTPA和99Tcm-MIBI进行复查,每种药物重复4次,其自显影图像示于图2。由 4次图像计算Rf,结果显示,99Tcm-DTPA 和99Tcm-MIBI均与2008年检测结果相同,分别为 0.78±0.02和0.39±0.03;99Tcm-MDP的检测结果与2008年的相差甚大,其自显影斑点始终在原点附近,Rf接近于零,其组分未被分开。

图2 3种锝药物的TLC自显影
4 讨论与建议
4.1 99Tcm标记药物应先被分离完全,再定量测定其放化纯度
上述结果表明,用自显影法检查 TLC,除99Tcm-MAA外,实验所用“一条”法可以将锝药物的各种组分分开,与Vera的图示分析结果[3]相符合。此后按各组分分段检测放射性计数,进而可定量计算药物的放化纯度。
4.2 即使在药盒保质期内,也应在标记完成后检测其放化纯度
2002年和2008年99Tcm-MDP的放化纯度都偏低,但其组分可以分开,而2009年观察到组分未分开,这可能是由于99Tcm-MDP是具有锝锡胶体特性的复合物,因标记用MDP药盒有效期为52周,药盒内氯化亚锡含量随贮存时间增加而降低,因此可能导致标记产品的R f发生显著变化。这种变化用两条法(一条测游离锝,另一条测锝锡胶体)难以测出,且其所测定的放化纯度通常>90%。因此,即使在MDP药盒贮存有效期内进行标记,也要在标记后用于临床前检测其放化纯度。
4.3 发展检测99Tcm药物放化纯度的高效薄层色谱法
2005年Lep ri等[4]提出了改善分离效率的高效薄层色谱法(HPTLC法),此法采用颗粒度较小(2~10μm)的硅胶板和较小的点样体积(0.1~0.2μL,点样原点约1.0 mm);Gocan[5]和张玉奎[6]等认为,限制点样原点尺寸是 TLC分离和精确定量的关键。与HPTLC法相比,本方法的不足之处是试样溶液的放射性浓度较低,加样总体积也较小,只有2 m L,虽然多次点样,点样直径也未达到1.0mm的要求。
生产单位拥有众多的专业放化人才、大量放射性浓度的锝药物和检测放化纯度必需的仪器设备,有条件继续研究此项工作。可以比较多种固定相与流动相的组合,找出最佳层析体系及简便的操作方法,并进一步促进锝药物放化纯度检测方法的规范化。
致谢:本工作承蒙中国人民解放军总医院附一院核医学科欧阳巧洪主任、藩茹等同志长期来提供场所、试样和北方免疫试剂研究所孟福英同志的大力支持,北京大学第一医院核医学科王荣福主任、张春丽副主任、阎萍同志及本院药剂科、放疗科物理组等有关同志的鼎力帮助,在此表示衷心感谢!
[1] 张艳华,黄天贵,黄俊星,等.99Tcm-PYM的制备、动物实验及临床研究[J].北京医科大学学报,1997,29:150-152.
[2] Huang TQ,Zhang YH,Wang JX,et al.Pingyangmycin as a99mTCCarrier in Tumor Localization[J].Nucl Med Biol,1995,22:537-542.
[3] Vera DR.Radionuclide p roduction&radiopharmaceuticals[R/OL].[2008-01-31].http:∥dep ts.washington.edu/uwm ip/Week-5/Radiopharms.pdf.
[4] Lepri L,Cincinelli A.TLC Sorbents[C]//Cazes J.Encyclopedia of Chromatography:Vol.Ⅱ.2nd ed.New York:Tay lor&Francis G roup,2005:1 645-1 649.
[5] Gocan S.Sample app lication in TLC[C]//Cazes J.Encyclopedia of chromatography:Vol.Ⅱ.2nd ed.New York:Taylor&Francis Group LLC,2005:1 480-1 486.
[6] 张玉奎,张维冰,邹汉法主编.分析化学手册:第六分册[M].第二版.北京:化学工业出版社,2000:118-125.
