冠状动脉分叉病变的CT分型
2010-06-05白启才,李珊,杨庭树等
欧洲分叉病变俱乐部(EBC)对冠状动脉分叉病变的定义是:病变邻近或累及较大分支开口,该分支血管对于该患者有明显功能价值(与症状有关、存在大量存活心肌、提供侧支循环以及对左心功能意义重大等),在介入治疗过程中不可以丢失。分叉病变分型的意义在于指导单支架或双支架治疗策略的选择。本研究旨在应用多排螺旋CT对冠状动脉分叉病变进行分型,为介入治疗策略的选择提供理论依据。
1 资料与方法
1.1 病例选择 2008-01~2008-12在解放军总医院导管室行择期PCI并在术前进行冠状动脉CT血管造影(CTA)的患者。排除标准:成像欠佳(血管欠清晰、血管分级支数<4级、较多伪影影响判断)、严重钙化影响管腔评估,分支血管<2.0mm及在10mm内有另外一个分支发出、既往行冠状动脉旁路移植术和冠状动脉内支架置入患者。最后共35例患者35处分叉病变入组本研究。CTA至PCI的平均时间9.71±6.79d。入组病例临床情况:男性29例(82.9%),女性6例(17.1%),平均年龄 54.71±9.22岁,高血压 24例(68.57%),糖尿病患者5例(14.29%),高脂血症患者9例(25.71%),仍吸烟者6例(17.14%),稳定型心绞痛患者2例(5.71%),不稳定型心绞痛患者 33例(94.29%)。
1.2 MDCT siemens公司32排螺旋CT,准直器宽32mm×0.6mm,机架旋转一周 420ms,层厚0.625mm,螺距0.20~0.29,球管电压120kV,管电流180mAs。采用飞焦技术采集重建,重建视野36cm,重建矩阵512×512。造影剂优维显,用量1.5mg I/kg,注射流速 3.5~4.0ml/s。所有后重建处理在AW4.1工作站完成,重建方法:最大密度投影法(maximum intensity,MIP)。
1.3 CTA图像分析 测量分叉两侧病变血管外弹力膜面积(EEM CSA)、最小管腔面积(MLA)、参照血管外弹力膜面积(病变节段近端和远端10mm内最接近正常并且没有大的分支发出的部位,取平均数为参照血管面积)、斑块分布弧度。并计算:斑块负荷(plaque burden)=(EEM CSA-MLA)/EEM CSA×100%,偏心指数(eccentric index,EI)=斑块最厚值/斑块最薄值(>2.0为偏心斑块,<2.0为向心斑块)、重塑指数(remodeling index,RI)=病变处EEM CSA/参照血管EEM CSA(>1.05为正性重塑,<1.05为负性重塑)。
1.4 统计分析 应用SPSS11.5统计软件进行数据分析,计量资料以均数±标准差表示,行正态检验后两样本比较采用t检验,多样本比较采用方差分析,计数资料采用卡方检验,对多变量间关系采用多元线性逐步回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 主支血管(MV)分叉近端和远端斑块性质定性分析 结果显示分叉近端和远端斑块性质无明显区别(表1)。CT影像和冠状动脉造影见图1。

表1 分叉近端及远端斑块定性分析

图1 A.CT下前降支分叉病变示病变累及主支血管分叉远端、近端及分支血管开口;B.分叉远端血管横断面示主支血管钙化斑块,分支血管纤维斑块;C.冠状动脉造影示前降支分叉病变累及主支血管分叉远端、近端及分支血管开口
2.2 主支血管分叉近端和远端定量分析 结果显示入选病例分叉近端和远端斑块负荷无明显区别,病变及参照血管外弹力膜面积、偏心指数、重塑指数、斑块分布弧度有明显区别(表2、图2)。
2.3 冠状动脉分叉病变CTA分型 见图3。
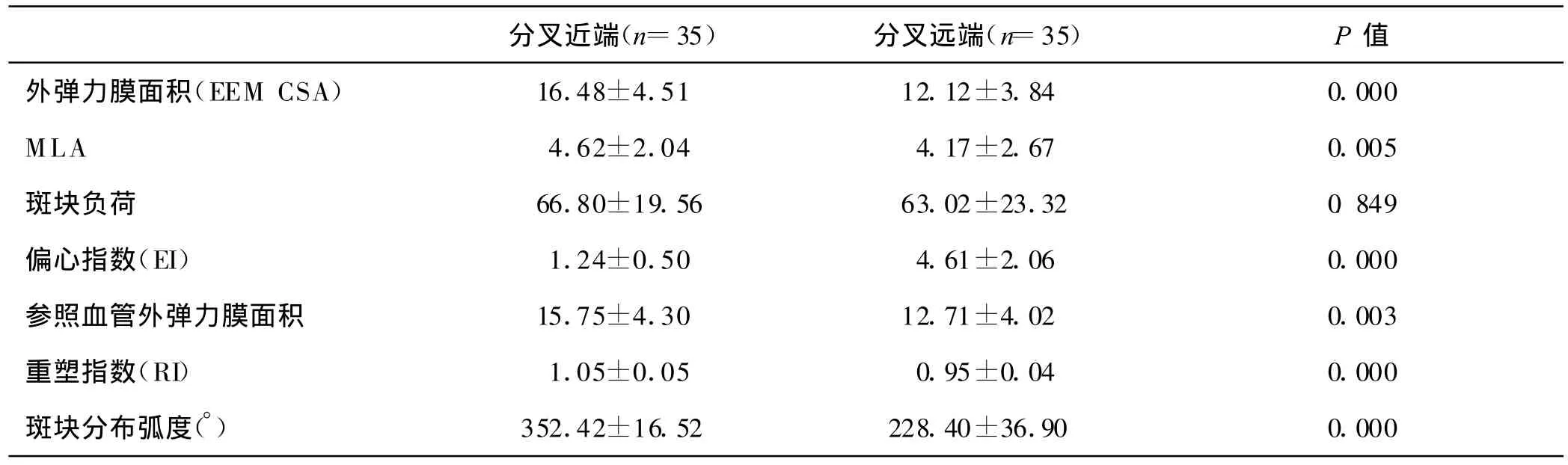
表2 分叉近端及远端定量分析
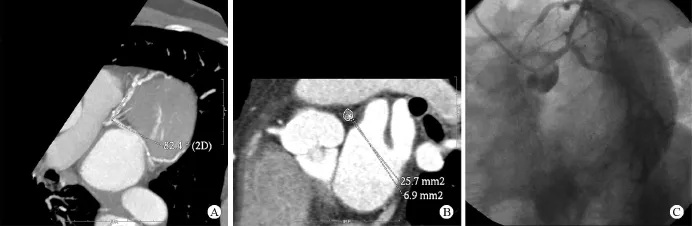
图2 A.CT示左主干分叉病变,测量主支血管与分支血管所成角度;B.CT测量分叉近端主支血管最小管腔面积和血管外弹力膜面积;C.冠状动脉造影示左主干分叉病变累及左主干远端、前降支开口及回旋支开口

图3 冠脉分叉病变CTA分型
3 讨论
分叉病变在冠状动脉介入治疗(PCI)中占15%~16%,由于分叉病变手术成功率低、术中并发症高(分支闭塞)、术后再狭窄率高(尤其分支开口)[1,2],一直是冠状动脉介入领域颇具挑战性的病变。分叉病变介入治疗策略主要有两种:①单支架术,有分支闭塞风险;②双支架术:无分支闭塞风险,但技术难度加大,急性、亚急性、晚期血栓风险增高。因此分叉病变治疗策略的制定对减少术中并发症、术后主要心脏不良事件(MACE)和靶病变血运重建率(TLR)至关重要。既往分叉病变分型有Lefevre分型、Duke分型、Sanborn分型、Safian分型等,分型的主要依据是病变在分叉部位的解剖分布,但是这些分型都是基于冠状动脉造影(CAG)的结果。由于CAG显示的是被造影剂充填的管腔轮廓,冠状动脉粥样硬化斑块的三维空间分布是CAG检测的盲区,这使得既往的分型与“真实世界”有一定差距。近年来随着冠状动脉影像检测技术的迅猛发展,新型的形态学检测手段如血管内超声(IVUS)、光学相干断层成像(OCT)、多排螺旋CT(MDCT)等能够确定斑块的空间分布构型,弥补了CAG在形态学检测方面的空缺。尤其MDCT,随着硬件设备的改进,分辨率进一步提高,向实现冠状动脉影像学发展的终极目标——用无创手段检测斑块形态学,又迈进了一步。本研究中我们对冠状动脉分叉病变的空间分布构型进行分析,提出新型的分叉病变CT分型。
研究入选35处冠状动脉分叉病变,根据CT值对主支血管分叉近端和远端斑块性质进行定性分析比较。病变分类根据先前文献报道:组织学检查显示含丰富脂质的斑块CT值较低为42±12Hu,纤维斑块居中为70±21Hu,钙化斑块最高为715±328Hu。研究显示分叉近端和远端斑块性质无明显区别。
研究中对主支血管分叉近端和远端血管进行了定量分析,结果显示二者斑块负荷无明显区别(66.80±19.56%,63.02±23.32%,P=0.849),但病变血管EEM-CSA(16.48±4.51 mm2,12.12±3.84 mm2,P=0.000)、参照血管EEM-CSA(15.75±4.30 mm2,12.71±4.02 mm2,P=0.003)偏心指数(1.24±0.50,4.61±2.06,P=0.000)、斑块分布弧度(352.42±16.52,228.40±36.90,P=0.000)、重塑指数(1.05±0.05,0.95±0.04,P=0.000)有明显区别。冠状动脉自然走行呈锥形,每 10mm长度管腔缩小1.1±1.2mm2(9±10%),这一规律在前降支更明显,每10mm长度管腔可能缩小 2.1±1.5mm2(10±6%)[3]。分叉病变处,两分支大小的总和大约是分叉前的1.5倍。IVUS也证实冠状动脉分叉部位的血管直径符合Murry定律,即:PMV(mm)=[DMV(mm)+SB(mm)]×0.6。本研究中分叉近端病变和参照外弹力膜面积分别是远端的1.36、1.24倍。分叉远端斑块偏心指数明显高于分叉近端,以及分叉两端斑块分布弧度的差别,都显示分叉远端斑块多呈偏心性分布,而分叉近端斑块呈向心性分布。另外,分叉近端血管多表现为正性重塑和无重塑,而分叉远端血管多表现为负性重塑或无重塑。既往研究显示,正性重塑多提示不稳定的病变,即软斑块,而负性重塑提示稳定的病变,即钙化斑块或纤维斑块。国内盖鲁粤等[4]的IVUS分叉病变研究显示分叉近端斑块多呈360°向心性环周分布,分叉远端斑块呈偏心性分布,多占1/2~2/3管周,斑块主要分布在分叉嵴的对侧,极少累及分叉嵴。
研究中我们提出下列分叉病变的CT分型。A型:真性分叉病变,主支血管分叉近端向心性斑块、远端偏心性斑块、分支开口偏心斑块,分支开口斑块与主支分叉远端斑块均位于分叉嵴对侧壁;B型:主支血管分叉近端向心性斑块、分支开口偏心斑块,位于分叉嵴对侧壁;C型:主支血管分叉远端偏心斑块,分支开口偏心斑块,斑块均位于分叉嵴对侧壁;D型:主支血管分叉近端向心性斑块和远端偏心斑块,分叉远端斑块位于分叉嵴对侧壁,分支开口无病变;E型:主支血管分叉近端向心性斑块;F型:主支血管分叉远端偏心斑块,位于分叉嵴对侧壁。本研究中,上述6种分型各占 22.86%(8/35)、34.28%(12/35)、14.29%(5/35)、11.43%(4/35)、8.57%(3/35)、8.57%(3/35)。该分型对于介入治疗的指导意义在于:A、B、C型分叉病变均累及分支开口,属分支闭塞高危的病变。尤其是A型,在所有类型中介入治疗操作中分支闭塞可能性最大,应提前导丝保护,必要时可在分支内放置球囊,与主支支架球囊行对吻扩张,对于A型病变,可能多需要双支架术;B型分支闭塞的危险性仅次于A型,处理原则同A型;C型如分支开口自身病变轻微,则分支受影响的可能性小,因为主支分叉远端斑块移位至分支开口的可能性小;D、E型介入操作中分支完全闭塞可能性小;E型病变主支置入支架相对安全,几乎不可能挤压分支,单支架置入安全、可靠。
近年来心血管介入治疗更倾向于对易损病变而不是狭窄程度的干预,使得各种有创的腔内影像检查技术迅速发展。MDCT作为一种无创的形态学检查手段,具有IVUS、OCT等有创检查无法比拟的优势。我们的研究首次提出新型的冠状动脉分叉病变CT分型,弥补了CAG二维成像的不足,对指导介入治疗策略的选择有显著的临床价值。
[1]Meier B,Gruntig AR,King SB III,et al.Risk of side branch occlusion during coronary angioplasty.Am J Cardiol,1984,53:10-14.
[2]Vetrovec GW,Cowley M J,Wolfgang TC,et al.Effects of percutaneous transluminal coronary angioplasty in lesionassociated branches.Am Heart J,1985,109:921-925.
[3]Javier SP,Mintz GS,Popma JJ,et al.Intravascular ultrasound assessment of the magnitude and mechanism of coronary artery and lumen tapering.Am J Cardiol 1995,75:177-180.
[4]李珊,盖鲁粤,杨庭树,等.冠状动脉分叉病变斑块分布特点的血管内超声研究.中国循环杂志,2007,22(1):329-332.
