溶胶-凝胶法制备的Li1 .15V3O8的电化学性能
2010-06-01任政娟王青春
任政娟,王青春,水 淼,舒 杰
(宁波大学材料科学与化学工程学院,浙江宁波 315211)
层状结构Li1+xV3O8的比容量高、嵌锂性能好、成本低[1]。Li1+xV3O8包含VO6八面体和VO5畸变三角双锥两个基本单元[2]。一般情况下,Li+占据八面体位置,当更多的Li+嵌入时,多余的 Li+进入四面体位置。八面体中的Li+通过强离子键与V3O8层连接,强离子键使晶体结构在充放电时更稳定。溶胶-凝胶法制备Li1+xV3O8多用柠檬酸作螯合剂。岳鸿飞[1]以柠檬酸溶胶-凝胶法在550℃下烧结18 h,所得产物的首次放电比容量达251.2 mAh/g,但循环30次后衰减了19.86%。Z.J.Wu等[3]用柠檬酸作螯合剂,讨论了n(Li)∶n(V)和体系pH对产物的影响。也可用EDTA[1]、甘氨酸[4]作螯合剂,但本文作者尚未见到用酒石酸的报道。
基于这些研究工作中存在的衰减性能较差的问题,本文作者通过溶胶-凝胶法制备了Li1.15V3O8,比较了用柠檬酸和酒石酸作螯合剂对产物电化学性能的影响。
1 实验
1.1 正极材料Li1.15V3O8的制备
按Li1.15V3O8的化学计量比称取NH4VO3(国药集团,AR)、Li2CO3(国药集团,AR),在80℃的蒸馏水中混合,再滴加物质的量与总金属离子相等的螯合剂饱和柠檬酸(国药集团,AR)或酒石酸溶液(国药集团,AR)。以300 r/min的转速搅拌约1 h,用浓氨水(国药集团,AR)调节反应体系的pH值至7左右,在60℃下继续搅拌形成溶胶,最后在80℃下浓缩,得到凝胶。将凝胶在120℃下真空(<133 Pa,下同)干燥5 h,得到膨松的、泡沫状 Li1.15V3O8前驱体,再在550℃下焙烧3 h,自然冷却,得到Li1.15V3O8。
1.2 正极的制备和电池的组装
按质量比75∶15∶10将制备的Li1.15V3O8、炭黑(深圳产,电池级)、聚偏氟乙烯(上海产,≥99.9%)混匀,滴入 N-甲基吡咯烷酮(上海产,AR),以200 r/min的转速搅拌成粘稠的浆液,再涂覆在0.02 mm厚的铝箔(上海产,≥99.9%)上,待表面比较干燥后,用DGW100型对辊机(深圳产)压实,在120℃下真空干燥约5 h,裁成直径为1.4 cm正极片。每片正极含4.2 mg活性物质。
以金属锂片(江西产,≥99.9%)为负极,Celgard 2400膜(美国产)为隔膜,1 mol/L LiPF6/DMC+EMC+EC(质量比1∶1∶1,张家港产,≥99.9%)为电解液,在充满氩气的干燥手套箱中组装CR2016型扣式电池。
1.3 结构分析和性能测试
红外光谱用FTIR-8900型傅立叶变换红外光谱仪(日本产,分辨率为4 cm-1)进行测试,KBr压片,测试范围为 4 000~400 cm-1;用 TG/DTA 6300型微热分析仪(日本产)观察前驱体的失重,参比物为α-Al2O3,流动空气,以 5℃/min的速率升温至 800℃;用 D8 Focus型 X射线衍射仪(德国产)进行物相分析,CuKα,扫描速率为0.01(°)/s;用XL30型扫描电子显微镜(荷兰产)观察材料的形貌,加速电压为20 kV。
充放电测试在CT2001A电池测试系统(武汉产)上进行,电流为0.14 mA(0.1 C),电压为1.8~3.9 V;交流阻抗测试在CHI660B电化学工作站(上海产)上进行,初始电压为开路电压,交流振幅为5 mV,频率为105~0.01 Hz。
2 结果与讨论
2.1 前驱体的红外及热分析
图1为前驱体的红外谱图。

图1 (x=0.15)不同前驱体的红外谱图Fig.1 IR spectra of different precursors
从图1可知,两种前驱体的红外图谱相似。曲线a在3 450 cm-1处有 1个强峰,曲线 b在 3 200 cm-1和 3 400 cm-1附近有2个吸收峰,与柠檬酸有 1个羟基,酒石酸有2个羟基一致。在1 400 cm-1和1 600 cm-1区域的吸收光谱,存在羧酸盐的特征不对称伸缩振动吸收带(Vas)和对称伸缩振动吸收带(Vs),分别在1 380 cm-1和1 598 cm-1处。它们的存在,说明前驱体中形成了羧酸盐,证明 VO2+和 Li+已与螯合剂形成了配位化合物。1 000~500 cm-1处的系列峰与V cm-1左右的峰,是空气中CO2的吸收峰。
前驱体的热分析测试结果见图2。
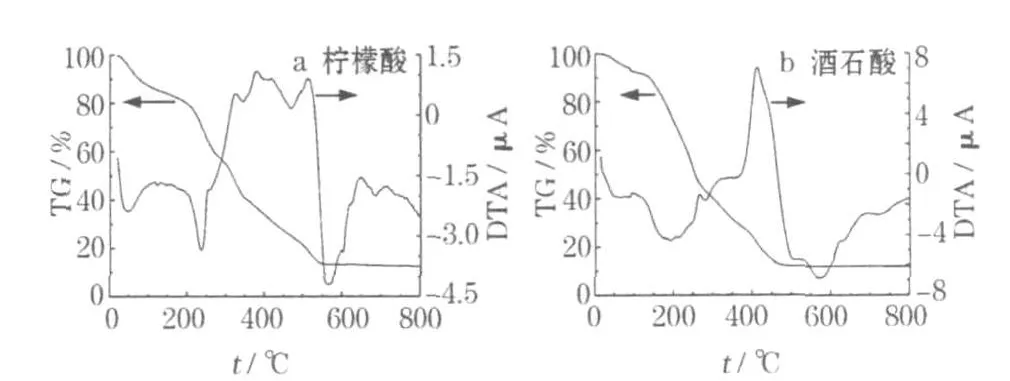
图2 不同前驱体的TG-DTG曲线Fig.2 TG-DTG curves of different precursors
从图2a可知,在用柠檬酸的前驱体的TG曲线上,从室温到260℃的失重是吸附水和结合水的脱去所致,对应DTG曲线在50℃左右有1个吸热峰,是吸附水的脱去所致。在200~260℃明显的吸热峰,是结合水的脱去所致。在260~550℃的失重情况比较复杂:首先在310~420℃出现的一系列小放热峰,可能是柠檬酸的氧化燃烧放热所致;在450~520℃又有1个放热峰,可能是形成的前驱体分解放热,形成Li1.15V3O8并释放NH3、CO2等气体所致。在550~650℃有1个明显的放热峰,但相应TG曲线上无明显的失重,可能是Li1.15V3O8的晶型转变导致的放热。TG曲线在550℃以后为恒定直线,说明此温度后生成了稳定的Li1.15V3O8。
图2b的趋势与图2a大体相似,但在400~450℃出现1个明显的放热峰,是酒石酸氧化燃烧放热和形成Li1.15V3O8所致。在450℃时就开始形成Li1.15V3O8,说明用酒石酸作螯合剂,可在更低的温度下形成结构较完整的Li1.15V3O8。
2.2 热分解产物的结构及形貌分析
图3是Li1.15V3O8粉末的XRD图。
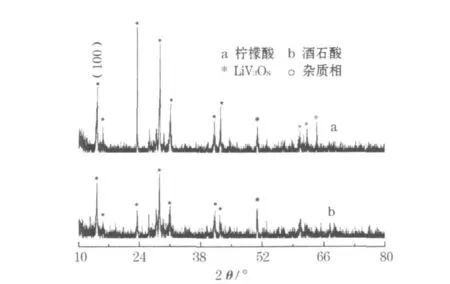
图3 不同Li1.15V3O8粉末的XRD图Fig.3 XRD patterns of different Li1.15V3O8powders
从图 3可知,曲线在 14.02°、23.38°、28.48°、30.96°和41.02°附近处均出现了 LiV3O8的特征峰,且曲线b的衍射峰强度更低。在择优取向(100)晶面,曲线b的衍射峰强度也更低,峰宽度更大,表明用酒石酸制备的Li1.15V3O8结晶度较低,粒径小,主相为LiV3O8。曲线a在60°和65°附近有明显的杂质峰,说明用柠檬酸制备的Li1.15V3O8的纯度不高。对锂钒氧化物而言,较小的晶面衍射峰强度和粒度,可缩短离子扩散路径,有利于 Li+的嵌脱[5]。
图4是Li1.15V3O8粉末的SEM图。

图4 不同Li1.15V3O8粉末的SEM图Fig.4 SEM photographs of different Li1.15V3O8powders
从图4可知,两种样品的表面形貌相似,为较光滑的椭球形。用柠檬酸、酒石酸制备的Li1.15V3O8粉末,粒径分别约为200~250 nm和 100 nm。
2.3 Li1.15V3O8的电化学性能测试
正极材料Li1.15V3O8的0.1 C首次放电曲线见图5。

图5 不同Li1.15V3O8的0.1 C首次放电曲线Fig.5 0.1 C initial discharge curves of different Li1.15V3O8
从图5可知,用柠檬酸、酒石酸制备的 Li1.15V3O8,首次放电比容量分别为134.06 mAh/g和190.17 mAh/g。嵌入锂的物质的量x可由式(1)计算。

式(1)中,C为比容量,F为法拉第常数,M是Li1.15V3O8的相对分子质量。由式(1)计算可知,放电结束时,用柠檬酸、酒石酸制备的样品,锂的嵌入量 x分别为1.44、2.05,即最终放电产物分别为Li2.59V3O8、Li3.2V3O8。图5中,用柠檬酸制备的样品有多个放电平台,放电过程中存在多次固溶体转变的过程。综合XRD分析的结果(图3),用酒石酸制备的样品结晶度小、晶化程度低、Li+扩散路径短,比容量较高。
正极材料Li1.15V3O8的0.1 C循环性能见图6。

图6 不同 Li1.15V3O8的 0.1 C循环性能Fig.6 0.1 C cycle performance of different Li1.15V3O8
从图6可知,用柠檬酸制备的Li1.15V3O8第50次循环的比容量为92.00 mAh/g,容量衰减率为31.37%;用酒石酸制备的Li1.15V3O8的放电比容量折线上升,在第32次和第47次循环时均为最高值210.99 mAh/g,第50次循环的比容量为204.44 mAh/g,比最高值衰减了3.10%。产生这一现象的原因,可能是用酒石酸制备的Li1.15V3O8在循环过程中产生了新物相,有利于Li+的可逆嵌脱。
2.4 Li1.15V3O8的交流阻抗测试
Li1.15V3O8的交流阻抗谱见图7。
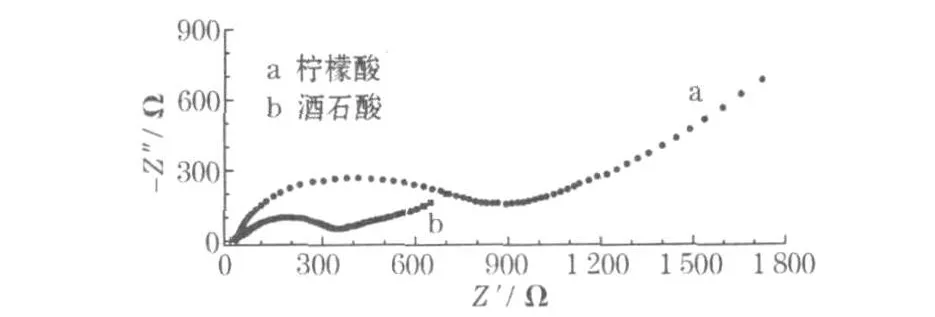
图7 不同Li1.15V3O8的交流阻抗谱Fig.7 AC impedance plots of different Li1.15V3O8
从图7可知,用柠檬酸制备的Li1.15V3O8导电率低、内阻大;用酒石酸制备的Li1.15V3O8导电率高、内阻小。电荷转移阻抗小,有利于克服动力学限制,提高Li1.15V3O8活性颗粒的嵌锂程度,表现出较高的比容量和较好的循环性能。
3 结论
以Li2CO3、NH4VO3为原料、用柠檬酸作螯合剂得到前驱体,经550℃灼烧 3 h得到正极材料 Li1.15V3O8。组装的电池的 0.1 C首次放电比容量为134.06 mAh/g,第 50次循环时,容量衰减率为31.37%。用酒石酸作螯合剂制备的Li1.15V3O8,以0.14 mA在1.8~3.8 V充放电,首次放电比容量为190.17 mAh/g,最高比容量为第32次和第47次循环时的210.99 mAh/g。在50次循环过程中,容量折线上升,循环性能较好。
致谢:感谢许伟老师在分析测试方面的帮助和宋岳、徐丹同学在材料制备方面的帮助。
[1]YUE Hong-fei(岳鸿飞).正极材料 LiV3O8的合成与性能研究[D].Beijing(北京):Graduate School of the Chinese Academy of Science(中国科学院研究生院),2007.
[2]de Picciotto L A,Adendorff K T,Liles D C,et al.Structural characterization of Li1+xV3O8insertion electrodes by single-crystal X-ray diffraction[J].Solid State Ionics,1993,62(3-4):297-307.
[3]Wu Z J,Zhao X B,Tu J,et al.Synthesis of Li1+xV3O8by citrate sol-gel route at low temperature[J].J Alloys Compd,2005,403(1):345-348.
[4]LI Zhi-xian(李枝贤),HAN Kun-ming(韩坤明),LU Dao-rong(鲁道荣),et al.高容量锂离子电池正极材料 Li1+xV3O8的制备及改性研究[J].Metallic Functional Materials(金属功能材料),2007,14(4):15-18.
[5]Jin K,Tskahiro K,Ysaushi K,et al.Lithium insertion behaviour of Li1+xV3O8with different degrees of crystallinity[J].J Power Sources,1999,81-82:448-453.
