表面改性Si3N4粉末在水相体系中的分散性能
2010-05-31银锐明范景莲刘勋单成
银锐明 , 范景莲,刘勋,单成
(1. 中南大学 粉末冶金国家重点实验室,湖南 长沙,410083;2. 湖南工业大学 包装与材料工程学院,湖南 株洲,412008)
氮化硅陶瓷具有高强度、高耐磨损和高抗热震性能、低膨胀系数、耐腐蚀及抗氧化等优异性能,是在极为恶劣和高温环境下应用的理想工程结构材料之一。但 Si3N4为共价键化合物,自扩散系数低,较难烧结,其烧结温度通常在1 850 ℃以上[1-2]。目前,通过添加烧结助剂等方法可将烧结温度降到 1 500~1 600 ℃,并提高Si3N4陶瓷的断裂韧性[3-4]。材料力学性能与颗粒尺寸紧密相关,研究表明[5]:加入纳米级颗粒后,材料的力学性能会成倍地增加,同时,材料的烧结温度降低。采用传统球磨法将纳米烧结助剂加入 Si3N4粉末中,一方面容易混入其他杂质,另一方面,由于纳米颗粒分布不均且易团聚,烧结后难以获得理想的材料微观组织。采用液相沉积法将纳米助剂均匀包覆在陶瓷颗粒表面,则可使纳米颗粒在陶瓷颗粒表面固化而防止团聚,并改善陶瓷界面的润湿性,在烧结制备陶瓷过程中各相界面反应特性相同,晶粒生长一致,大大提高显微组织的均匀性[6-9]。然而,Si3N4粉末在水相体系的分散性能很差,而液相沉淀法实现纳米颗粒均匀包覆的关键条件之一是要获得分散性良好的Si3N4粉末悬浮液。液相中颗粒之间存在的力有范德华引力及颗粒双电层静电排斥力等作用力[10]。颗粒双电层静电排斥力有利于提高粉末颗粒在水相体系中的分散性能,主要由颗粒表面性质决定。对 Si3N4颗粒表面改性,以提高颗粒双电层静电与排斥力,获得分散性能良好的Si3N4颗粒悬浮液。为此,本文作者以改善 Si3N4粉末在水相体系中的分散性能为目的,通过高温氧化对 Si3N4粉末表面进行改性,并对其在水相体系中的分散机理进行研究。
1 实验方法
1.1 原料
原料为:日产ube sn-e10型Si3N4粉末(α相),平均粒径d50为1.3 μm);氨水,分析纯;蒸馏水。
1.2 Si3N4表面氧化改性
将电阻炉升温至1 000 ℃后,将样品粉末置入炉中分别氧化3,6,9和13 h,然后取出空冷。
1.3 分散性能表征
制备待测粉末的悬浮液,超声波与机械搅拌0.5 h后静置1 h,取上层清液80 mL,将水蒸干,即得上层清液 80 mL中未沉淀粉末质量 m,则未沉淀率 F=m/0.08 (g/L)。用F可以评价颗粒在水相体系中的分散能力,即F越大,则沉降越慢,分散效果就越好;反之,分散效果就差。
1.4 性能测试
采用美国FEI公司生产的Tecnai G2 20AEM型透射电镜对粉末微观结构进行观察,待测粉末经酒精分散,滴加到铜网上,经太阳灯照射烘干后测试;采用日本理学电机株式会社的 D/max 2550型 XRD衍射仪,Cu Kα辐射,连续扫描方式采样,扫描速度为 4(°)/min;采用美国力可公司产的TC-436氮/氧分析仪对氧化前后粉末氧含量进行测试;采用 DELSA44osx型Zetaplus电位仪测量颗粒粉末的表面电位,待测粉末悬浮液质量浓度为5 mg/L,测试前超声波与机械搅拌0.5 h;采用美国Thermo公司生产的NEXUS670型傅里叶红外光谱仪对粉末进行红外光谱测量。
2 结果与讨论
2.1 氧化时间对Si3N4氧含量的影响
Sheehan[11]认为界面反应和混合扩散控制着 Si3N4粉末的氧化速率。界面反应可以在一定范围内得到较低的线性氧化速率和较高的活化能。混合扩散是指O2扩散控速过程或N2扩散控速过程,氧化速率应呈抛物线变化。图1所示为Si3N4粉末经不同时间氧化后的氧含量变化。图1表明:随着氧化时间的延长,Si3N4粉末的氧含量呈近似线性增加。由此认为:Si3N4粉末在空气中于1 000 ℃氧化,氧化时间在13 h内,Si3N4粉末的氧化速率主要受界面反应所控制。

图1 Si3N4粉末经不同时间t氧化后氧含量w(O)的变化Fig.1 Variation of oxygen content of Si3N4 powder after oxidation at 1 000 ℃ for different oxidation times
2.2 XRD及TEM分析
图2 所示为未经氧化处理的Si3N4粉末与在空气中于1 000 ℃氧化9 h后Si3N4粉末的XRD衍射谱。图2表明:表面氧化处理前后衍射峰基本相同,均只出现Si3N4衍射峰,但表面氧化处理后的Si3N4衍射峰强度较弱。其原因是氧化的Si3N4粉末表面生成SiO2等氧化物,使其强度下降,而该氧化物含量太少或处于非晶态,难以从XRD谱中识别。
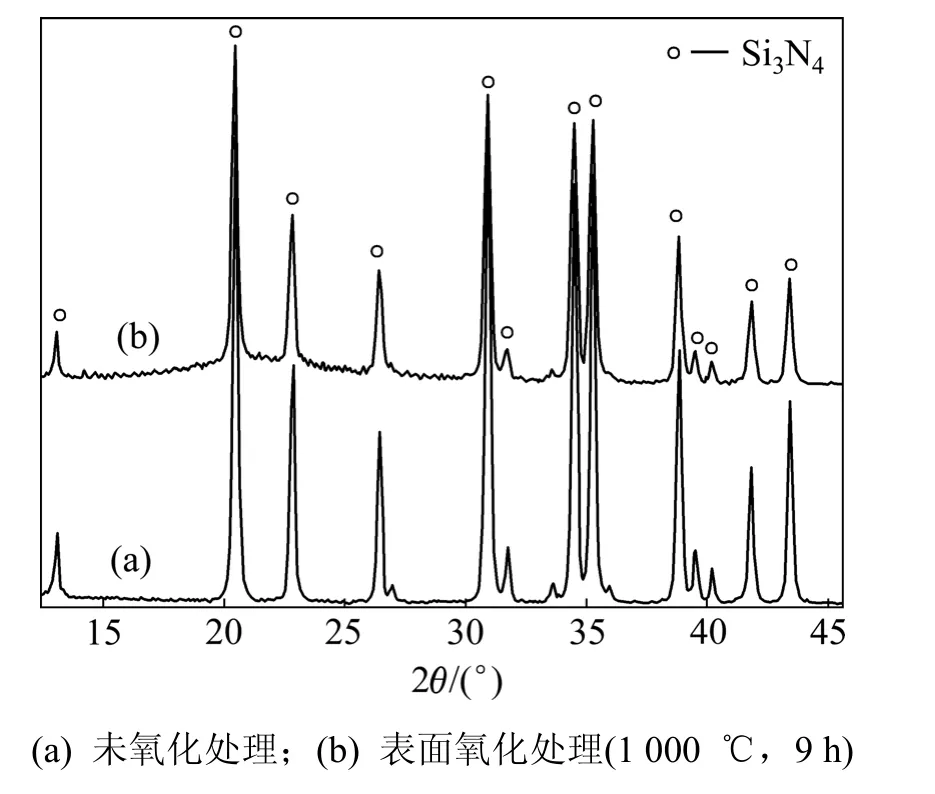
图2 Si3N4粉末的XRD谱Fig.2 XRD patterns of Si3N4 powers
图3所示为在空气中于1 000 ℃保温9 h氧化后Si3N4粉末的TEM像。图3显示:颗粒的壳体与芯部界面分明,为不同物质构成。Balat等[12-13]对 Si3N4粉末的氧化进行研究,发现Si3N4氧化有2个不同的区域:一个是“钝化氧化”区域,形成SiO2保护层,发生质量增加现象;另一个是“活化氧化”区域,有SiO气体生成,试样存在质量损失现象。“活化氧化”和“钝化氧化”之间的转变主要受氧分压和温度的影响,Si3N4粉末在空气中于1 000 ℃氧化是属于“钝化氧化”,其表层有 SiO2等氧化保护层形成,由此可判断:图3中颗粒芯部为Si3N4,壳体为SiO2等氧化物。

图3 在空气中于1 000 ℃保温9 h氧化后Si3N4粉末的TEM像Fig.3 TEM image of Si3N4 powder at 1 000 ℃for 9 h in air
2.3 氧化时间对粉末在水相体系中的 Zeta电位及分散性的影响
图4 所示为Si3N4粉末在空气中于1 000 ℃下氧化时间与其在水相体系中Zeta电位的关系。由图4可见:未经表面氧化的Si3N4粉末的表面Zeta电位绝对值很低,仅为1.63 mV,经氧化的Si3N4粉末的Zeta电位的绝对值显著增加,均在20.387 mV以上,并且随着氧化时间的延长,其值先缓慢上升,在氧化时间 9 h为最大,随后下降。
图5所示为Si3N4粉末在空气中于1 000 ℃时氧化时间与未沉淀率F的关系。图5表明:未氧化Si3N4粉末悬浮液的未沉淀率 F即分散性能很低,只有0.052 5 g/L,分散性能非常差。经氧化处理的Si3N4粉末悬浮液的F即分散性能得到显著提高,F均在20 g/L以上。此外,随着氧化时间的延长,Si3N4在水相体系中的未沉淀率即分散性能先上升,当氧化时间为 9 h时,达到最大,随后下降。由此可见:对Si3N4粉末表面氧化改性,Si3N4粉末表面双电层发生了变化,荷负电性增加,粒子间排斥力增大,直接影响到粒子间的分散性能,使得氧化时间对 Si3N4粉末在水相体系中的Zeta电位的绝对值与分散稳定性的变化趋势一致。
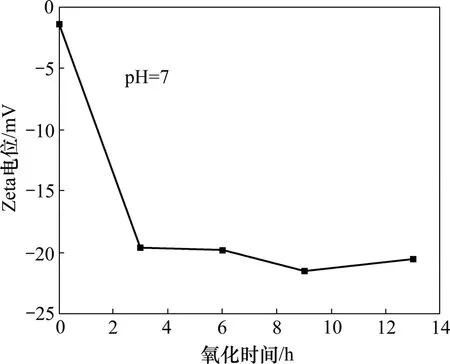
图4 Si3N4粉末在空气中于1 000 ℃下氧化时间与Zeta电位的关系Fig.4 Relationship between Zeta potential of Si3N4 powder and oxidation time at 1 000 ℃ in air
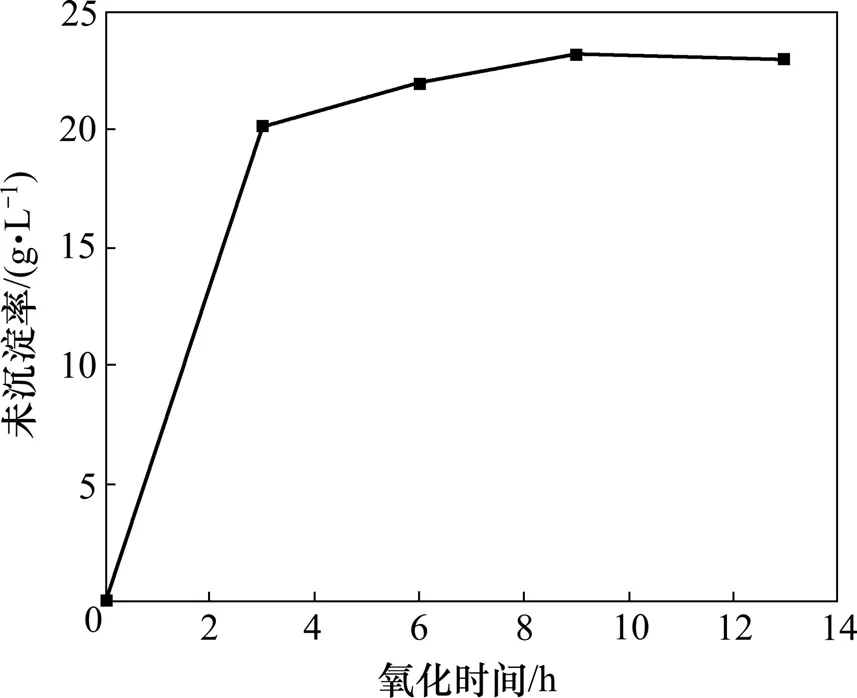
图5 Si3N4粉末在1 000 ℃时氧化时间与未沉淀率的关系Fig.5 Relationship between not precipitation rate of Si3N4 powder and oxidation time at 1 000 ℃
2.4 红外光光谱分析
图6 所示为Si3N4粉末在1 000 ℃氧化不同时间后的红外漫反射光谱。图6显示:各曲线在800~1 100 cm-1波数内有很强的吸收宽峰,代建清等[14]认为该峰主要是 Si—N键振动所产生,不同氧化时间处理的Si3N4峰值强度相当,对应的吸收峰随氧化时间的延长而宽化。氧化后在波数1 100~1 250 cm-1处出现了新的吸收峰,闻骆[15]认为该峰是由Si—O非对称伸缩振动所引起,其由一强带(1 080~1 100 cm-1)及一弱带(1 160~1 250 cm-1)组成,峰值强度随着氧化时间的延长而增强。氧化前后的 Si3N4粉末在波数 683及 600 cm-1左右均有 2个中等强度的吸收峰,林仕伟等[13]认为这是由Si—O—Si键振动引起的,氧化3 h后其振动峰较未氧化的 Si3N4粉末的振动峰略有降低,但随着氧化时间的延长,其振动峰值又逐步上升。
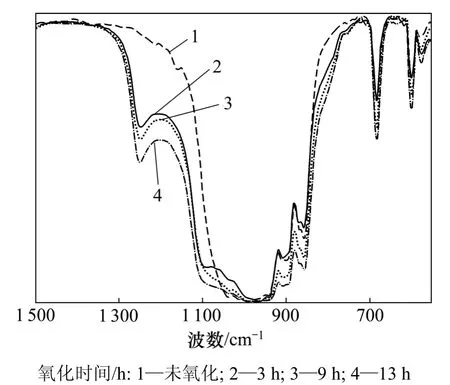
图6 Si3N4粉末在1 000 ℃氧化不同时间后的红外吸收光谱Fig.6 Infrared absorption spectra of Si3N4 powder after oxidation at 1 000 ℃ for different times
纯氮化硅表面为叔胺(Si3N)结构,故红外光谱能检测到较强的Si—N键吸收峰。由于该类结构在空气中具有反应活性,使得暴露在空气中的氮化硅颗粒与空气中的氧和水汽发生缓慢反应,在颗粒表面生成一层很薄的富氧层,富氧层的组成介于 SiO2和 Si2N2O之间,厚度为 3~5 nm,故而红外光谱能检测到Si—O—Si键振动所引起的较强的吸收峰。在Si3N4粉末氧化初期,Si—O—Si键在高温过程发生断裂,形成 Si—O键,其断裂分解的速度大于 Si—N键被氧化生成Si—O—Si键的速度,故在氧化初期Si3N4的红外光谱中出现了新的较强的 Si—O键振动峰,而Si—O—Si键振动峰略有下降。但随着高温氧化时间进一步延长,Si3N4表层Si—N键在高温不断被氧化,形成的 Si—O—Si键增多,Si—O 键与 Si—O—Si键振动峰都增强。
2.5 结果讨论
经高温氧化后,Si3N4粉末在水相体系中的 Zeta电位绝对值与分散性能显著提高。而红外光谱显示,氧化前后 Si3N4粉末表面基团都有振动峰较强的Si—N键与Si—O—Si键,但经氧化后Si3N4粉末表面出现较强的Si—O键振动峰。
代健清等[16]认为:Si3N4颗粒在水相体系中的荷电机理归因于其表面基团的离解反应,Si—O—Si键为憎水性的基团,憎水性基团不仅影响颗粒表面的电荷密度,而且使颗粒与水之间的界面能增加,大大降低其在水相体系中的分散性能,故未氧化的 Si3N4粉末在水相体系中的 Zeta电位绝对值极低,分散性能极差。然而,Si3N4经高温空气中氧化后,产生了大量的Si—O键基团,其易于在水中离解成 Si—OH键,有利于粉料颗粒表面在水中带有负电荷,从而造成颗粒表面负电荷升高,即其电位绝对值升高,而使其在水相体系中的分散性能提高。
Si3N4颗粒在氧化后期出现表面电位绝对值下降、分散性能变差的现象。原因是 Si3N4在水相体系中的Zeta电位与分散性能在水相体系中受表面的憎水性基团Si—O—Si键与Si—O键基团在水中形成的亲水基团Si—OH键的共同影响,对分散性能分别起到促进与遏制的作用。红外光谱显示:在氧化初期,Si—O键基团振动峰值强度上升较为明显,Si—O—Si键振动峰略有下降;在氧化后期,Si—O—Si键振动峰强度上升较明显。由此可见:Si—O—Si键与Si—O键对经氧化的 Si3N4粉末在水相体系中的分散性能的遏制与促进作用在氧化9 h后基本达到平衡,在氧化9 h前,Si—O键由于数量上升很快,平衡向Si—O键作用方向移动。在氧化9 h后,Si—O—Si键的数量开始明显增加,平衡略向Si—O—Si键作用方向移动。
3 结论
(1) Si3N4粉末在空气中于1 000 ℃氧化,氧化时间在 13 h内,Si3N4的氧化速率主要受界面反应所控制。
(2) Si3N4粉末表面氧化改性使得 Si3N4表面双电层发生了很大的变化,荷负电性增加,粒子间排斥力增大,直接影响到粒子间的分散性能。
(3) 经氧化的 Si3N4在水相体系中的 Zeta电位与分散性能受其表面的憎水性基团Si—O—Si键与在水相体系中由Si—O键形成的亲水基团Si—OH键共同影响。
[1] Pasupuleti S, Peddetti R, Santhanam S, et al. Toughening behavior in a carbon nanotube reinforced silicon nitride composite[J]. Materials Science and Engineering A, 2008,491(1/2): 224-229.
[2] Tian C, Liu N, Lu M. Thermal shock and thermal fatigue behavior of Si3N4-TiC nano-composites[J]. International Journal of Refractory Metals and Hard Materials, 2008, 26(5): 478-484.[3] Vila M, Carrapichano J M, Gomes J R, et al. Ultra-high performance of DLC-coated Si3N4rings for mechanical seals[J].Wear, 2008, 265(5/6): 940-944.
[4] Belmonte M, Pablos de A, Osendi M I, et al. Effects of seeding and amounts of Y2O3:Al2O3additives on grain growth in Si3N4ceramics [J]. Materials Science and Engineering A, 2008,475(1/2): 185-189.
[5] 张立德, 牟季美. 纳米材料和纳米结构[M]. 北京: 科学出版社, 2001: 497-503.ZHANG Li-de, MOU Ji-mei. Nanometer material and nanostructures[M]. Beijing: Science Press, 2001: 497-503.
[6] Fon W C W. Thermal properties of nano- and microstructures[D].Pasadena California: California Institute of Technology, 2004.
[7] 银锐明, 范景莲, 刘勋, 等. 非均相沉淀-热还原法制备铁包覆氮化硅颗粒复合粉末[J]. 中南大学学报: 自然科学版, 2008,39(1): 7-11.YIN Rui-ming, FAN Jing-lian, LIU Xun, et al. Preparation of Fe-coated Si3N4composite powders by heterogeneous precipitation-thermal reduction process[J]. Journal of Central South University: Science and Technology, 2008, 39(1): 7-11.
[8] Zou G Z, Cao M S, Zhang L, et al. A nanoscale core-shell of β-SiCP-Ni prepared by electroless plating at lower temperature[J].Surface and Coatings Technology, 2006, 201(1/2): 108-112.
[9] Zhang S P, Dong, D W, Su Y, et al. Preparation of core shell particles consisting of cobalt ferrite and silica by sol-gel process[J]. Journal of Alloys and Compounds, 2006, 415(1/2):257-260.
[10] Rumpf H. Particle technology[M]. Toronto: Chapman & Hall,1990: 116-120.
[11] Sheehan J E. Passive and active oxidation of hot-pressed silicon nitride materials with two magnesia contents[J]. J Amer Ceram Soc, 1982, 65(7): 111-115.
[12] Balat M, Czerniak M, Berjoan R. Oxidation of silicon nitride under standard air or microwave-excited air at high temperature and low pressure[J]. J Mater Sci, 1997, 32(5): 1187-1193.
[13] 林仕伟, 司文捷, 彭志坚, 等. 硅基陶瓷材料高温氧化理论的回顾[J]. 材料科学与工程, 2002, 20(2): 268-272.LIN Shi-wei, SI Wen-jie, PENG Zhi-jian, et al. Review for the research on the oxidation theory of silicon-based materials at ultrahigh temperature[J]. Materials Science and Engineering,2002, 20(2): 268-272.
[14] 代建清, 黄勇, 谢志鹏, 等. 氮化硅粉末的傅里叶变换红外光谱研究[J]. 光谱实验室, 2001, 18(1): 78-83.DAI Jian-qing, HUANG Yong, XIE Zhi-peng, et al. FTIR study of Si3N4powder[J]. Chinese Journal of Spectroscopy Laboratory,2001, 18(1): 78-83.
[15] 闻辂. 矿物红外光谱学[M]. 重庆: 重庆大学出版社, 1989:114.WEN Lu. Infrared spectra of minerals[M]. Chongqing:Chongqing University Press, 1989: 114.
[16] 代建清, 黄勇. 酸洗和热氧化对氮化硅粉料表面特性与浆料流变性能的影响[J]. 无机材料学报, 2008, 23(1): 165-170.DAI Jian-qing, HUANG Yong. Effects of acid-leaching and thermal oxidation on surface characteristics and aqueous dispersibility of silicon nitride powders[J]. Journal of Inorganic Materials, 2008, 23(1): 165-170.
