局部晚期鼻咽癌同期放化疗及辅助化疗的临床研究
2010-05-28付杰胡超苏
付杰 胡超苏
1.上海复旦大学附属肿瘤医院,复旦大学肿瘤学系放疗科;2.上海交通大学附属第六人民医院, 上海市第六人民医院放疗科
局部晚期鼻咽癌同期放化疗及辅助化疗的临床研究
付杰1,2胡超苏1
1.上海复旦大学附属肿瘤医院,复旦大学肿瘤学系放疗科;2.上海交通大学附属第六人民医院, 上海市第六人民医院放疗科
背景与目的:NCCN指南推荐晚期鼻咽癌应予以同期放化疗联合辅助化疗,本研究旨在评估改良同期放化疗及辅助化疗对局部晚期鼻咽癌患者的疗效、急性不良反应及其依从性情况。方法:2003年11月—2005年4月间,共收集67例Ⅲ、Ⅳ期局部晚期鼻咽癌患者进入同期放化疗加辅助化疗的治疗研究,放疗采用常规分割每周5次,总剂量(70~74)Gy/(35~37)次。在放疗期间第1、5周应用2个周期同期化疗(DDP 25 mg/m2·d-1,第1~3天和5-FU 300 mg/m2·d-1,第1~3天),在治疗的第10、13和16周继续3个周期辅助化疗(DDP 25 mg/m2·d-1,第1~3天和5-FU 450 mg/m2·d-1,第1~3天)。结果:67例患者中位随访时间20个月(11~27个月)。2年总生存率和无瘤生存率分别为91.75% 和 81.56%,Ⅲ、Ⅳ期患者2年总生存率、无瘤生存率相比差异无统计学意义(96%∶87.65%,P=0.334;92.16%∶69.35%,P=0.2358)。全部患者完成放疗,完成5个周期的化疗患者47例(70.1%),同期化疗中完成2个周期的化疗患者56例(83.6%),辅助化疗完成3个周期的化疗患者48例(71.6%)。同期放化疗期间Ⅲ度以上急性不良反应分别为:白细胞减少15例(21.4%),恶心呕吐2例(3.0%),黏膜炎症56例(83.6%),皮肤反应10例(15.0%)。辅助放化疗期间Ⅲ度以上急性不良反应分别为:白细胞减少13例(19.4%),贫血1例(1.5%)。结论:初步结果表明对于Ⅲ、Ⅳ期局部晚期鼻咽癌患者而言,该同期放化疗和辅助化疗方案依从性高,不良反应相对较低,早期疗效较好。长期疗效将进一步随访更新。
鼻咽癌; 化学疗法; 放射疗法
远处转移和局部复发是局部晚期鼻咽癌治疗失败的主要原因,患者的5年生存率只有15%~45%[1-2]。在我国鼻咽癌多为低分化鳞状细胞癌,对化疗较敏感,理论上化疗有可能杀灭体内微小转移病灶,同时化疗药物对放疗还有增加敏感性的作用,放疗联合化疗有可能提高鼻咽癌的疗效。目前对局部晚期鼻咽癌NCCN指南推荐同期放化疗联合辅助化疗。本研究通过对67例局部晚期鼻咽癌同期放化疗临床研究,探讨局部晚期鼻咽癌患者对改良的治疗方案耐受性和早期疗效,为局部晚期鼻咽癌新治疗方案的Ⅲ期临床试验设计提供依据。
1 资料和方法
1.1 临床资料 收集2003年11月—2005年4月就诊于复旦大学附属肿瘤医院共有67例鼻咽癌患者的临床资料。其中男性48例,女性19例;年龄28~73岁,平均年龄46.6岁。患者分期按AJCC 2002标准,其中T1期8例,T2期12例,T3期22例,T4期25例;N0期8例,N1期23例,N2期28例,N3期8例。病理分期Ⅲ期34例,Ⅳ期33例。
1.2 方法
1.2.1 放射治疗 对患者采取仰卧位下热塑料面罩固定,常规或CT模拟定位,采用同中心常规分割照射技术,每日分割剂量为2 Gy/次,每周5次。根据临床检查和CT/MRI确定靶区及照射范围,设计照射野。鼻咽原发灶采用60Co γ线(Theratron 780-C照射仪,购自加拿大AECL公司)或6MV直线加速器(型号:2 300 C/D,购自美国Varian公司)X线。颈部淋巴结区域照射采用60Co或6 MV X线+深部X线治疗机(180 Kv,HVL 0.95 mm Cu)或9~12 Mev电子线。鼻咽部剂量计算参考点为等中心点,颈部及双锁骨上区域剂量计算参考点为皮下3 cm处。脊髓受量≤45 Gy。鼻咽部原发灶36 Gy后缩野避开脊髓和脑干,全疗程总剂量为70~74 GY/35~37次,7~7.5周完成。对各种原因导致患者放射治疗中断,疗程延长≥5 d者则给予增加1 d的治疗剂量。颈部淋巴结转移时,给予根治剂量(65~70 Gy)照射。无淋巴结转移者照射量为50~55 Gy。
1.2.1 化疗 采用同期化疗(DDP 25 mg/m2·d-1,第1~3天和5-FU 300 mg/m2·d-1,第1~3天;每28 d为1个周期,共2个周期)及辅助化疗(DDP 25 mg/m2·d-1,第1~3天和5-FU 450 mg/m2·d-1,第1~3天;每21 d为1个周期,共3个周期),化疗前常规应用止吐药(5-HT抑制剂、胃复安和皮质激素等)。采用CTCAE3.0标准评定治疗不良反应。
1.3 统计处理 统计采用SPSS 10.0统计软件。用Kaplan-Meier法计算全组患者的生存率和无瘤生存率,Ⅲ、Ⅳ期患者2年总生存率、无病生存率比较采用Log-Rank检验。
2 结 果
2.1 放化疗实施情况 全部患者接受设计放疗剂量。其中58例(86.6%)无中断。9例患者放疗中断在1周之内。1例患者放疗结束后6个月颈部复发接受手术治疗。2例患者加用后装放疗。其中完成了2~5个周期的化疗患者分别为2例(3%)、4例(6%)、7例(10.4%)和47例(70.1%)。同期化疗中完成2个周期化疗的患者56例(83.6%),其中30例(44.8%)患者按时完成2个周期同期化疗,20例(29.9%)患者延期1周以内,6例(9%)患者延期1周以上;辅助化疗完成3个周期化疗的患者48例(71.6%),其中39例(58.2%)患者按时完成3个周期化疗,8例(11.9%)患者延期1周以内,1例(1.5%)患者延期1周以上;43例(64.2%)患者按时完成2个周期化疗,11例(16.4%)患者延期1周以内,3例(4.5%)患者延期1周以上;43例(64.2%)患者按时完成化疗1个周期,13例(19.4%)患者延期1周以内,2例(3.0%)患者延期1周以上;提示本组患者按治疗计划实施情况明显优于文献报告[11],患者有较好的依从性。患者同期放化疗期间体重下降为4.17(3.26~5.07)kg。同期放化疗期间53例(79.1%)患者需要补液支持治疗,辅助化疗期间28例(41.8%)患者需要补液支持治疗的。
2.2 不良反应 同期放化疗期间Ⅲ度及以上急性不良反应分别为:白细胞减少15例(21.4%);恶心呕吐2例(3.0%);黏膜炎症56例(83.6%);皮肤反应10例(15.0%)。辅助放化疗期间Ⅲ度及以上急性不良反应分别为:白细胞减少13例(19.4%);贫血1例(1.5%)(表1)。
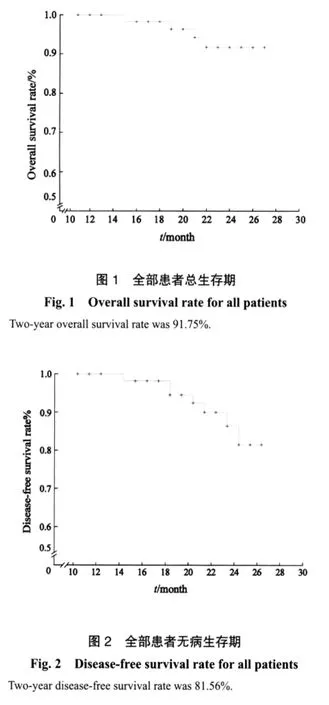
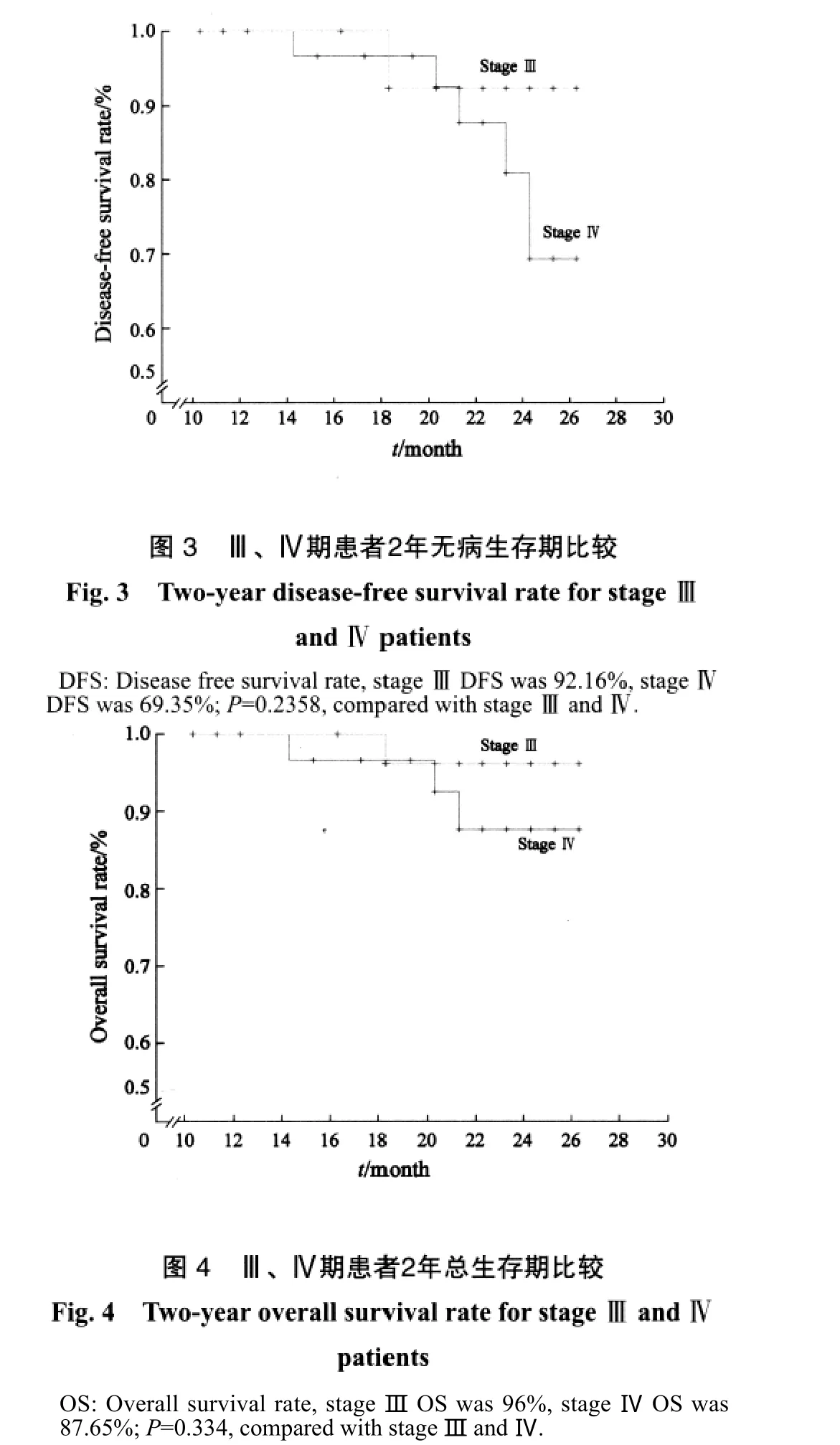
2.3 生存分析 所有生存患者均随访到2006年3月,共随访11~27个月,中位随访时间20个月,2年总生存率、无病生存率分别为91.75%和81.56%。死亡4例,远处转移3例。Ⅲ、Ⅳ期患者2年总生存率相比,差异无统计学意义(96%∶87.65%,P=0.334),无病生存率(92.16%∶69.35%,P=0.2358),见图1~4。
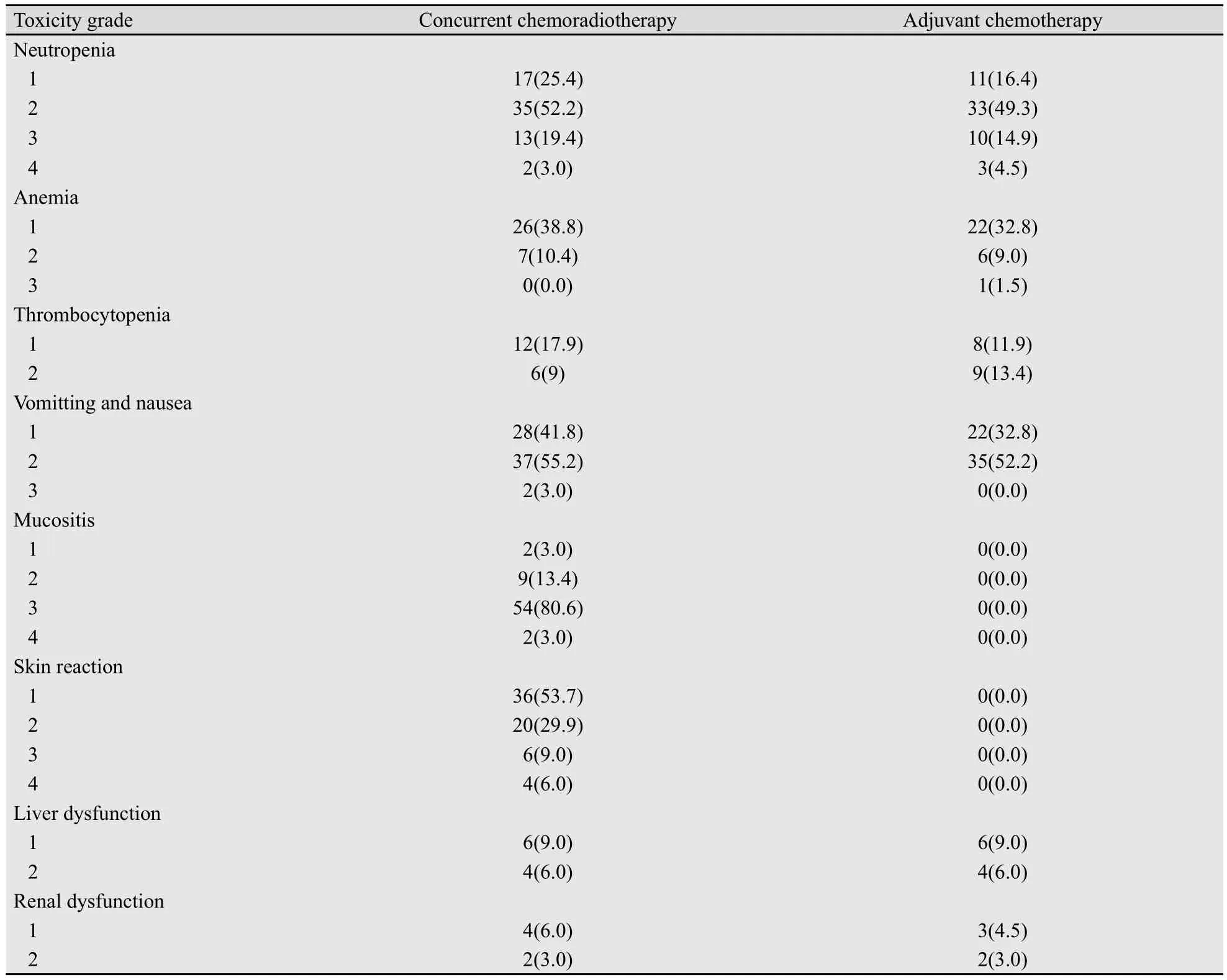
表 1 治疗相关急性不良反应Tab. 1 Acute toxicity events related to the treatment n(%)
3 讨 论
Meta分析[3-4]显示同期放化疗可以提高10%~20%局部晚期鼻咽癌患者5年生存益处。0099试验首次证实与单纯放疗相比,同期化疗加辅助化疗3年总生存率提高了31%[5],但该研究中55%患者为高分化鳞癌,且仅有55%患者完成了预定辅助化疗,与我国鼻咽癌现状不同(90%以上病例为低分化鳞癌)。一些试验探索了0099试验方案对亚洲患者疗效与不良反应。Lee等[6]报道同期放化疗组与单纯放疗组3年无病生存率分别为72%∶62%(P=0.027),主要是改善了局部控制(92%∶82%,P=0.005);52%患者完成预定同期化疗和76%的患者完成预定辅助化疗。急性及晚期不良反应同期化疗组均明显高于单纯放疗组(84%∶53%,P<0.01;28%∶13%,P=0.024)。尽管明显增加了放射治疗的不良反应,但该作者认为局部晚期鼻咽癌亚洲患者可耐受0099试验化疗方案并提高了局部控制率,没有提高早期生存率。该方案新加坡研究显示[7],54%患者(31/57)接受了预期的治疗,11%患者治疗中断,同时2例出现治疗相关死亡。笔者却认为亚洲患者可耐受该方案。该方案香港研究报告[8]显示75.7%患者(74例)完成了同期化疗,47.3%完成辅助化疗。Ⅲ级及以上急性不良反应分别为造血系统25例(33.8%),黏膜反应19例(25.7%),皮肤6例(8.1%),5年累计晚期损伤发生率为44.3%。为了改善患者依从性,降低不良反应和方便治疗,Cheng等[9]报道了亚洲患者改良方案的疗效,放疗同期DDP(60 mg/m2)和5-FU(600 mg/m2)化疗2个周期;放疗后行2个周期的DDP(100 mg/m2)和5-FU(1 000 mg/m2)联合化疗。107例患者(Ⅲ~Ⅳ期者占70.0%)的5年生存率、无瘤生存率和局部区域控制率分别为84.1%、74.4%和89.7%。98%患者完成了4个周期化疗。73.0%患者发生了Ⅲ级及以上急性黏膜不良反应,23.0%患者需要放置胃管。15.0%患者发生了Ⅲ级以上呕吐,1%患者发生了Ⅲ级及以上的白细胞减少。Lin等[10]报道了284例Ⅲ、Ⅳ期亚洲患者改良化疗方案的疗效,2个周期同期化疗(DDP 20 mg/m2·d-1,第1~3天;5-FU 400 mg/m2·d-1,第1~3天)。5年生存率、无进展生存率提高了18.1%。Ⅲ级及以上急性黏膜不良反应为45.4%,Ⅲ级及以上白细胞减少为4.3%,笔者认为同期化疗适用于低危患者,对高危患者仍不足,因此有理由对高危患者采用辅助化疗。Chan等[11-12]研究了每周小剂量DDP(40 mg/m2)同期化疗和放疗治疗Ⅱ、Ⅲ期鼻咽癌的疗效。2年无进展生存率提高了7.0%,主要是改善了T3、T4期患者的疗效。更新报道显示中位随访5.5年,总生存率提高了13.0%(P=0.04),无进展生存提高了10.0%(P=0.059),主要是T3和T4期患者疗效获得改善。
上述临床试验显示同期放化疗在改善治疗效果的同时,都不可避免地增加了急性不良反应,特别是黏膜和血液的不良反应。回顾性分析显示我国鼻咽癌患者与外国患者的临床表现和预后存在差异,提示两者之间的内在生物学行为不同[13]。尽管文献报告提示亚洲患者可以耐受0099试验方案,但均都不同程度增加了治疗的不良反应,且有治疗相关的死亡发生,因此该方案对于我国的患者情况可能不一定适用。为了提高患者的治疗效果同时降低不良反应,本研究采用改良化疗方案,期望降低急性不良反应,同时提高疗效,结果显示中位随访时间20个月,所有患者均接受放疗剂量。本研究中的治疗实施情况明显优于文献报道[5],患者有较好的依从性。本研究结果显示在血液、胃肠道、黏膜及肝肾功能等方面的不良反应方面较文献报道均较轻。与0099试验相比,本研究中的患者的耐受性明显改善,文献报告在亚洲患者中应用0099试验方案需要放置鼻胃管的占48.0%[14],而本研究中仅应用补液支持治疗就可以使患者耐受。
本研究的初步结果显示2年总生存率和无瘤生存率分别为91.75%和81.56%,其中死亡4例,转移3例。Ⅲ、Ⅳ期患者2年总生存率 96%∶87.65%(P=0.334),和无病生存率92.16%∶69.35%(P=0.2358)。Ⅳ期患者疗效与上述文献报告相比略低,主要原因可能是研究样本量较小的情况下出现了4例患者死亡,其中1例是Ⅲ期(N2)另外的3例是Ⅳ期(N3)。提示本研究对于N分类较晚的患者在治疗前采用新的影像学检查例如CT+MRI、PET来评价可能会更为全面,同时采取一些新的化疗药物及其治疗手段如靶向治疗(C225)等可能提高其疗效。目前的结果为早期临床疗效报告,长期疗效将进一步随访更新。
[1]Mould RF, Tai TH. Nasopharyngeal carcinoma: treatments and outcomes in the 20th century[J]. Br J Radiol, 2002, 75:307-339.
[2]严洁华, 徐国镇. 鼻咽癌[M]//殷蔚伯, 谷铣之, 主编. 肿瘤放射治疗学, 第3 版, 北京: 中国协和医科大学出版社,2002: 537-573.
[3]Langendijk JA, Leemans CR, Buter J, et al. The additional value of chemotherapy to radiotherapy in locally advanced nasopharyngeal carcinoma: a meta-analysis of the published literature[J]. J Clin Oncol, 2004, 22(22): 4604-4612.
[4]Baujat B, Audry H, Bourhis J, et al. Chemotherapy in locally advanced nasopharyngeal carcinoma: an individual patient data meta-analysis of eight randomized trials and 1753 patients[J].Int J Radiat Oncol Biol Phys, 2006, 64(1): 47-56.
[5]Al-sarraf M, Leblane M, Giri PG, et al. Chemoradiotherapy versus radiotherapy in patients with advanced nasopharyngeal cancer phase Ⅲ randomized intergroup study 0099[J]. J Clin Oncol, 1998, 16(4): 1310-1317.
[6]Lee AW, Lau WH, Tung SY, et al. Preliminary results of a randomized study on therapeutic gain by concurrent chemotherapy for regionally-advanced nasopharyngeal carcinoma: NPC-9901 Trial by the Hong Kong Nasopharyngeal Cancer Study Group[J]. J Clin Oncol, 2005, 23(28): 6966-6975.
[7]Tan EH, Chua ET, Wee J, et al. Concurrent chemoradiotherapy followed by adjuvant chemotherapy in Asian patients with nasopharyngeal carcinoma: toxicities and preliminary results[J]. Int J Radiat Oncol Biol Phys, 1999, 45(3): 597-601.
[8]田野, 蔡清淟, 岑信棠. 局部晚期鼻咽癌同期放化疗的疗效分析[J]. 中华肿瘤杂志, 2005, 27(7): 429-431.
[9]Cheng SH, Jian JJ, Tsai SY, et al. Long-term survival of nasopharyngeal carcinoma following concomitant radiotherapy and chemotherapy[J]. Int J Radiat Oncol Biol Phys, 2000,48(5): 1323-1330.
[10]Lin JC, Jan JS, Hsu CY, et al. Phase Ⅲ study of concurrent chemoradiotherapy versus radiotherapy alone for advanced nasopharyngeal carcinoma: positive effect on overall and progression-free survival[J]. J Clin Oncol, 2003, 21: 631-637.
[11]Chan AT, Teo PM, Ngan RK, et al. Concurrent chemotherapy-radiotherapy compared with radiotherapy alone in locoregionally advanced nasopharyngeal carcinoma:progression-free survival analysis of a phase Ⅲ randomized trial[J]. J Clin Oncol, 2002, 20: 2038-2044.
[12]Chan A, Teo P, Leung S, et al. Final results of a phaseⅢ randomized study of concurrent weekly cisplatin-RT versus RT alone in locoregionally advanced nasopharyngeal carcinoma(NPC)[J]. Proc Am Soc Clin Oncol, 2004, 23:492.
[13]Su CK, Wang CC. Prognostic value of Chinese race in nasopharyngeal cancer[J].Int J Radiat Oncol Biol Phys,2002, 54(3): 752-758.
[14]Mala B, Lillian LS, Gregory RP, et al. Tolerability of the Intergroup 0099 (INT 0099) regimen in locally advanced nasopharyngeal cancer with a focus on patients' nutritional status[J]. Int J Radiat Oncol Biol Phys, 2004, 60(4): 1127-1136.
Concurrent chemoradiotherapy followed by adjuvant chemotherapy for locally advanced nasopharyngeal carcinoma
FU Jie,HU Chao-su(Department of Radiation Oncology, Cancer Hospital, Fudan University Shanghai 200032, China)
HU Chao-su E-mail:hucsu62@yahoo.com
Background and purpose:Concurrent chemoradiotherapy followed by adjuvant chemotherapy have been administrated to locally advance nasopharyngeal carcinoma according to the NCCN guidelines. This study specifically evaluated the efficacy, toxicity and compliance of modified concurrent chemoradiotherapy followed by adjuvant chemotherapy in locally advanced nasopharyngeal carcinoma (NPC).Methods:From Nov. 2003 to Apr.2005, 67 patients with stage Ⅲ and Ⅳ locally advanced nasopharyngeal carcinoma (NPC) were enrolled in this study. A total dosage of radiation, 70-74 Gy, was given in 35-37 fractions in 5 fractions per week. Two cycles of chemotherapy,consisting of cisplatin 25 mg/m2•d-1and 5-f l uorouracil 300 mg/m2•d-1were delivered simultaneously with radiotherapy on the day 1-3 during week 1 and 5. Three cycles of adjuvant chemotherapy, consisting of cisplatin 25 mg/m2•d-1and fl uorouracil 450 mg/m2•d-1, were also given, starting on day 1-3 during week 10, 13 and 16.Results:The median follow-up was 20 months (ranged from 11 to 27 months). The 2-year overall survival rate and the 2-year diseasefree survival rate were 91.75% and 81.56% respectively. The 2-year overall survival rate was 96% for stage Ⅲ and 87.65% for stage Ⅳ(P=0.334). The 2-year disease-free survival rate was 92.16% for stage Ⅲ and 69.35% for stage Ⅳrespectively (P=0.2358). The compliance rates were 100% for radiotherapy, 47 cases (70.1%) for all chemotherapy,56 cases (83.6%) for concurrent chemotherapy and 48 cases (71.6%) for adjuvant chemotherapy. The main gradeⅢ/Ⅳ acute toxicity events during concurrent chemoradiotherapy were neutropenia in 15 patients (21.4%), vomitting and nausea in 2 patients (3%), mucositis in 56 patients (83.6%), and grade Ⅲ skin reaction in 10(15%), respectively.The main grade Ⅲ/Ⅳ acute toxicity events during adjuvant chemotherapy were neutropenia in 13 patients (19.4%),grade 3 anemia in 2 patients (1.5%) respectively.Conclusion:The primary result showed a good compliance, lower incidences of toxicity and improved early outcome of treatments for the patients with stage Ⅲ and stage Ⅳ (M0) NPC.The ultimate therapeutic ratio will be updated according to longer follow-ups.
nasopharyngeal carcinoma; chemotherapy; radiotherapy
R739.63;R730.53;R730.55
A
1007-3639(2010)05-0369-06
胡超苏 E-mail:hucsu62@yahoo.com
2010-02-25
2010-04-02)
