链状结构金属钴单质亚微米粒子的制备及磁性能研究
2010-05-01朱路平廖桂红汪玲玲张卫东谢洪勇
朱路平, 廖桂红, 杨 洋, 汪玲玲, 张卫东, 谢洪勇
(1.上海第二工业大学城市建设与环境工程学院,上海 201209;2.中国科学院理化技术研究所, 北京100190)
0 前言
磁性材料已经历了晶态,非晶态,纳米微晶态,纳米颗粒和纳米结构材料的发展阶段。磁性材料在达到纳米级时,表现出新颖独特的物理性质,而且相关性能随材料尺寸、形貌的改变而改变。这使得其在功能材料领域展现出崭新的应用前景。作为一种重要的铁磁性材料,钴纳米结构材料在磁记录材料、微波吸收材料和永磁材料等方面的潜在应用,引起了广泛的研究兴趣[1]。近年来,对该材料的制备和性能研究非常活跃。科研工作者已用微乳液法[2-3]、气相沉积法[4-5]、多元醇法[6]、热分解前躯体法[7-8]、电纺丝法[9]、电化学沉积法[10-11]以及磁场诱导法[12]等一系列制备方法得到不同形貌和结构微纳米钴结构材料,如纳米晶、纳米棒和纳米线等。
本文在借鉴多元醇法[13]制备钴镍合金纳米线的基础上,结合前期水合肼还原工艺制备纳米镍钴合金链状结构[14]的实践,用氯化钴、水合肼为起始原料,十六烷基三甲基溴化铵(CTAB)为表面活性剂、乙二醇为溶剂,采用溶剂热法成功地制备了金属钴单质亚微米粒子。该法具有工艺简单、产物纯度高、晶相结构易于控制等特点。运用X射线粉末衍射(XRD),透射电子显微镜(TEM)及扫描电子显微镜(SEM)等手段对制得的样品进行了物相分析,表征了其形貌和结构,并用振动样品磁强计(VSM)对其静磁性能进行了研究。
1 试验部分
1.1 试剂及仪器
主要试剂:氯化钴(CoCl2·4H2O,A.R),北京化学试剂有限公司;水合肼(N2H4·H2O,C.R), 北京化学试剂有限公司;乙二醇(CH2(OH)CH2(OH),A.R),北京化学试剂有限公司;十六烷基三甲基溴化铵(CTAB,A.R),北京化学试剂有限公司;无水乙醇(CH3CH2OH,C.R),北京化学试剂有限公司。实验用水为去离子水。
采用日本理学Rigaku D/max 2500型X射线粉末衍射仪(Cu-Kα, λ =0.15406 nm)对样品进行物相表征,扫描速率为0.02°·s-1,扫描范围为30°~80°;采用日本HITACHI公司H-600型透射电子显微镜(TEM)(加速电压120 kV)对样品的尺寸进行了观测;采用日本HITACHI公司S-4800扫描电子显微镜(SEM)(加速电压10 kV)对样品的表观形貌和成分进行表征和分析。样品的静磁性能采用美国Lakeshore技术公司的7307型振动样品磁强计(VSM)进行测量。
1.2 链状结构钴单质的制备
首先将0.48 g的氯化钴、0.5 g表面活性剂CTAB置于三角烧瓶中,加入30 mL的乙二醇,充分搅拌至紫红色澄清溶液;然后在搅拌的情况下逐滴加入一定量的水合肼溶液(体积分数为40 %~50 %),滴加完毕后持续搅拌1小时,得均一的粉红色乳液;最后将得到的乳液转入聚四氟乙烯内衬得反应釜中,升温至200℃并保温6小时。热处理结束后,自然冷却至室温。分离出釜底灰黑色絮状沉积物,经无水乙醇、去离子水多次洗涤后,置于真空干燥箱中于50℃干燥24小时,得灰黑色粉状产物。
2 结果与讨论
2.1 反应机理
在乙二醇溶液中,随着水合肼溶液(体积分数为40 %~50 %)的加入,溶解的钴离子先与水合肼形成稳定的络合物[Co(N2H4)3]Cl2。当升温至200oC左右时,溶液中过量的水合肼就与钴络离子发生还原反应,生成钴纳米粒子。由于新生成的钴纳米粒子极不稳定,经“极-极”相互作用而团聚长大,同时在CTAB存在情况下,由于其较强的各向异性磁力作用,钴亚微米球进一步组装成链状结构[14]。此外,由于反应是在乙二醇溶液中进行,在加热的过程中,乙二醇本身也会呈现出一定的还原性,且体系中还生成了氮气等惰性气体,这就有效地防止了新生成的钴粒子的再氧化,因而可得到较为纯净的钴单质。钴单质生成所涉及的反应如下:
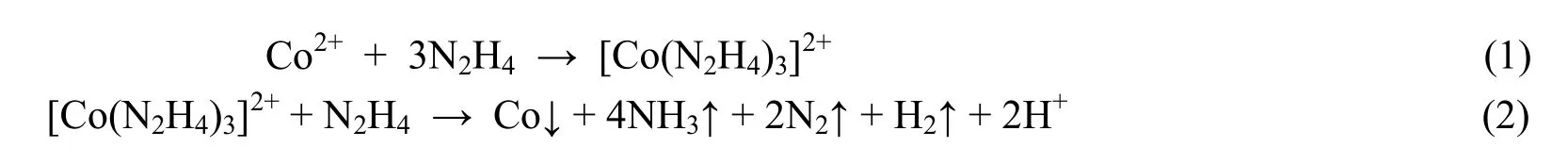
2.2 物相分析
图l(a)为溶剂热法制得样品的XRD图谱。从图上可以看出,所得到的5个衍射峰的2θ 值依次为 41.56°,44.34°,47.34°,62.72°和 75.80°,分别对应于金属钴单质的 (100),(002),(101),(102) 和(110) 晶面,与六方堆积相(hcp)的钴单质的标准图谱(JCPDS 05-0727)基本一致,因此所制得的钴单质样品可以标定为六方堆积相(hcp)结构。除钴单质的5个特征衍射峰外,没有其它杂质,如氧化钴、氢氧化钴等的衍射峰出现,表明所得到样品为纯净的钴单质。另外,样品较强的特征衍射峰,表明制得的样品具有较高的结晶度。图1(b)为样品对应的X射线能谱(EDX)图。 除了钴元素的特征锋外,没有观察到其元素的特征锋,也表明制得的样品为纯净的钴单质。
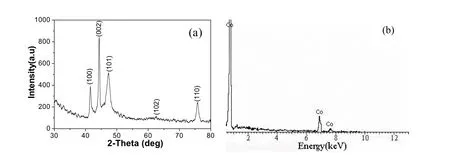
图1 样品(a)XRD及(b)EDS图Fig.1 (a)XRD and (b)EDX pattern of as-prepared products
2.3 形貌表征
图2为溶剂热法制得钴样品的电子显微镜照片。图2(a)为样品的透射电子显微镜照片。从照片可以看出,制得的钴粒子具有明显的链状结构,长度在10 μm~15 μm,构成链状结构的单个钴亚微米球的尺寸在400 nm~800 nm。图 2(a)右上角为其对应的选区电子衍射(SAED)图,其明锐的环状衍射花纹表明制得样品具有较高的结晶度,从内至外依次对应于钴单质的(100),(002),(101)和(110),这与 XRD的结果基本一致。图2(b)为制得的样品的扫描电子显微镜照片,从中可以看出大量的钴亚微米球聚集成链状结构,这与TEM的结果相一致。单个亚微米球的表面较为光滑。

图2 样品(a)TEM和(b)SEM照片Fig.2 (a)TEM and (b)SEM images of as-prepared products
2.4 静磁性能
图3是溶剂热法制备的链状结构钴单质亚微米粒子在常温下的磁滞回线。从中可以看出,制得的样品表现为铁磁性,饱和磁化强度(Ms)为 163.76 emu/g, 剩磁(Mr)为12.88 emu/g,饱和磁化强度稍小于块状钴单质 (168 emu/g);但矫顽力(Ho)较块状钴单质要高,相应的值可达104.20 Oe。该结构的钴单质有利于制备高密度的磁记忆元器件。材料的磁性能与其尺寸、形貌及结构等密切相关。因此链状结构的钴单质亚微米粒子的较大的矫顽力可能归因于其形貌的各向异性,即较大的长径比。在表面活性剂及磁场的作用下,钴亚微米粒子沿着易磁化方向进行取向组装,从而形成长链结构的聚集体,以致呈现出磁各向异性,这就使得其相应的矫顽力大于各向同性的块状钴单质。
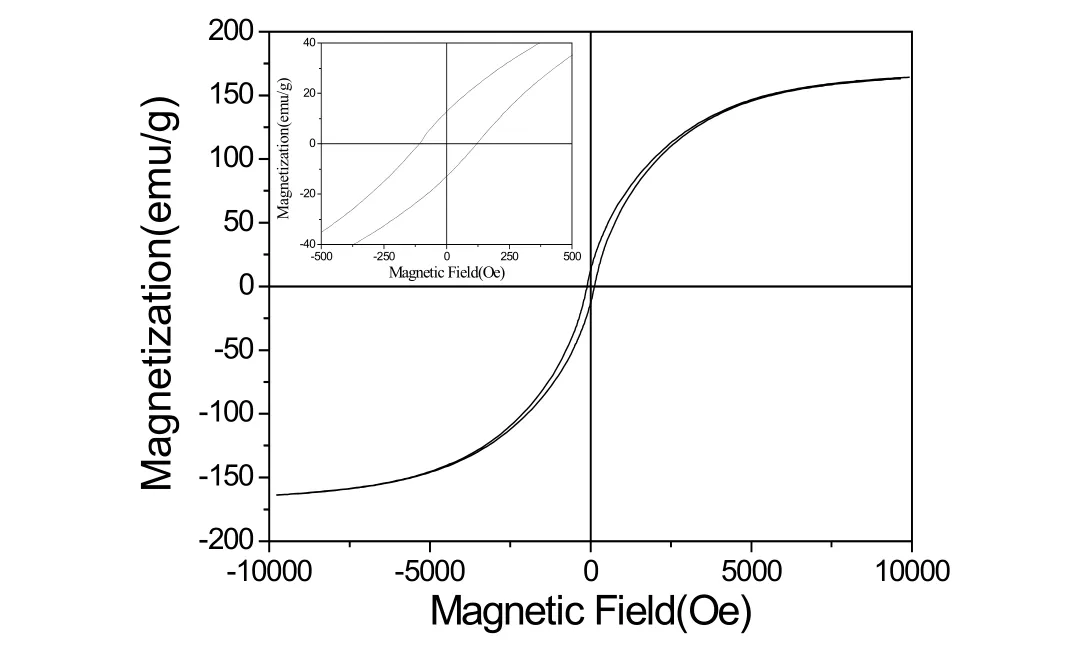
图3 样品的常温磁滞回线Fig.3 Magnetic hysteresis loop of as-prepared products
3 结 论
(1) 以氯化钴,水合肼为起始原料,CTAB为表面活性剂,采用溶剂热法制得链状结构的钴亚微米粒子,链长为10 μm~15 μm,组成链状结构的钴亚微米球粒径为400 nm~800 nm。
(2) 所制得的链状结构的钴亚微米粒子表现为铁磁性,饱和磁化强度为163.76 emu/g,相应的矫顽力较块体高,可达104.20 Oe,有望在高密度的磁记忆元器件等领域得以应用。
[1]VARGAS P, ALTBIR D,CASTRO J.Magnetism of nanosized metallic Co-clusters [J].J.Magn.Magn.Mater.,2001,226:603-605.
[2]CHEN J P, LEE K M,SORENSEN C M, et a1.Magnetic-properties of microemulsion synthesized cobalt fine particles[J].J.Appl.Phys., 1994,75(10):5876-5878.
[3]CHEN J P, SORENSEN C M, KLABUNDE K J, et a1.Enhanced magnetization of nanscale colloidal cobalt particles[J].Phys.Review B,1995, 51(17):11527-11532.
[4]GANGOPADHYAY S, HADJIPANAYIS G C, SORENSEN C M, et a1.Magnetic-properties of ultrafine Co particles [J].IEEE.Trans.Magn., 1992,28(5):3174-3176.
[5]李 华, 龚 伟.铁,钴,镍金属超微粒的制备与磁性[J].物理学报, 1991, 40(8):1356-1363.
[6]刘 飚, 官建国, 王琦, 等.多元醇还原制备Co纳米粉产品表征及机理研究[J].化学工程, 2005, 33(4):38-40, 55.
[7]DUMESTRE F, CHAUDREt B, AMIENS C, et al.Shape control of thermodynamically stable cobalt nanorods through organometallic chemistry [J].Angew.Chem., Int.Ed., 2002, 41:4286-4289.
[8]VIVEKCHAND S R C, GUNDIAH G, GOVINDARAJ A, et al.A new method for the preparation of metal nanowires by the nebulized spray pyrolysis of precursors [J].Adv.Mater., 2004, 16:1842-1845.
[9]WU H, ZHANG R, LIU X, et al.Electrospinning of Fe, Co, and Ni nanofibers:Synthesis, assembly, and magnetic properties [J].Chem.Mater.2007,19:3506-3511.
[10]CAO H, WANG L, QIU Y, et al.Generation and growth mechanism of metal (Fe, Co, Ni) nanotube arrays [J].ChemPhysChem 2006, 7:1500-1504.
[11]RIVAS J, BANTU A K M, ZARAGOZA G, et al.Preparation and magnetic behavior of arrays of electrodeposited Co nanowires [J].J.Magn.Magn.Mater., 2002, 249:220-227.
[12]ATHANASSIOU E K, GROSSMANN P, GRASS R N, et al.Template free, large scale synthesis of cobalt nanowires using magnetic fields for alignment [J].Nanotechnology, 2007, 18,165606:1-7.
[13]UNG D, VIAU G, RICOLLEAU C, et al.CoNi nanowires synthesized by heterogeneous nucleation in liquid polyol [J]Adv.Mater., 2005, 17:338-344.
[14]ZHU L P, XIAO H M, FU S Y, et al.Surfactant-assisted synthesis and characterization of novel chain-like CoNi alloy assemblies [J].Eur.J.Inorg.Chem., 2007, 25:3947-3951.
