溶液中离子浓度比较的特例及规律
2010-04-20洪晓堂
洪晓堂
(江苏教育学院附属高级中学江苏南京210036)
溶液中离子浓度比较的特例及规律
洪晓堂
(江苏教育学院附属高级中学江苏南京210036)
在历届高考中,溶液中离子浓度大小比较是必考的知识点之一。这类题目形式多变,成为很多同学解题时的难点,特别是“四离子”溶液体系中离子浓度比较更是很多同学的易错题。在分析这类问题时灵活运用电荷守恒、元素守恒和质子守恒这三大守恒是关键。下面我通过一些高考真题来具体剖析一下。
例题1(2010江苏12)常温下,用0.1000 mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1CH3COOH溶液所得滴定曲线如图。
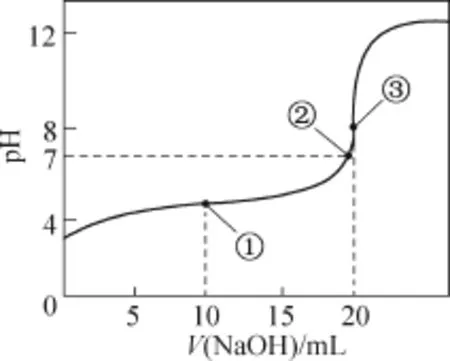
下列说法正确的是()
A.点①所示溶液中:
c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:
c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>
c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
解析选项A点①为0.001molCH3COOH和0.001molCH3COONa形成的混合溶液,根据电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),根据物料守恒:2c(Na+)=c(CH3COOH)+c(CH3COO-),两式整理后可得c(CH3COO-)+2c(OH-)=c(CH3COOH)+ 2c(H+);选项B点②时溶液呈中性,根据电荷守恒c(Na+)=c(CH3COO-);选项C点③时溶液中溶质为0.002molCH3COONa,此时溶液中离子浓度大小顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);D选项在CH3COOH溶液中滴加极少量的NaOH溶液,溶液中离子顺序就是如此。所以本题选D。
例题2(2008上海14)某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是()
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为:
c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH+4)之和
解析本题的题干中明确要求混合溶液呈酸性。A选项由于CH3COOH是弱酸,混合后溶液呈酸性;B选项,等体积、等浓度的NaOH溶液和CH3COOH溶液混合恰好生成CH3COONa,溶液呈碱性,不符合题意;C选项不符合电荷守恒;D选项加入适量氨水后,溶液可能呈酸性、中性或碱性。根据电荷守恒:c(Na+)+c(H+)+c(NH+4)= c(CH3COO-)+c(OH-),若呈酸性,则c(Na+)+c(NH+4)<c(CH3COO-),若呈中性,c(Na+)+c(NH4+)=c(CH3COO-),若呈碱性,c(Na+)+c(NH4+)>c(CH3COO-)。所以本题答案为A。
例题3(2005江苏12)常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是()
A.pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)
B.pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
C.pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.pH=7,且c(CH3COO-)>c(Na+)>c(H+)= c(OH-)
解析A选项,若pH>7,溶液中溶质可能是CH3COONa、CH3COONa和极少量CH3COOH或CH3COONa和极少量NaOH,此时c(CH3COO-)>c(H+);B选项根据电荷守恒可得;C选项,pH<7时,溶液中的溶质为CH3COONa、较过量CH3COOH,所以C选项是可能出现的结果;D选项明显的违反了电荷守恒。所以本题答案为AD。
这类题目有一个共同特点,围绕CH3COOH溶液和NaOH溶液混合后的体系中各种微粒浓度的大小关系进行比较。此类问题,我们可以灵活运用电荷守恒、元素守恒、质子守恒就可以解决。CH3COOH溶液和NaOH溶液混合后,溶液中共有4种离子,这四种离子浓度大小之间有几种可能呢?我们做一个简单探讨。
下面我们就以向0.1000mol·L-1NaOH溶液中逐滴滴加0.1000mol·L-1CH3COOH溶液为例进行分析(假设反应在常温下进行)。
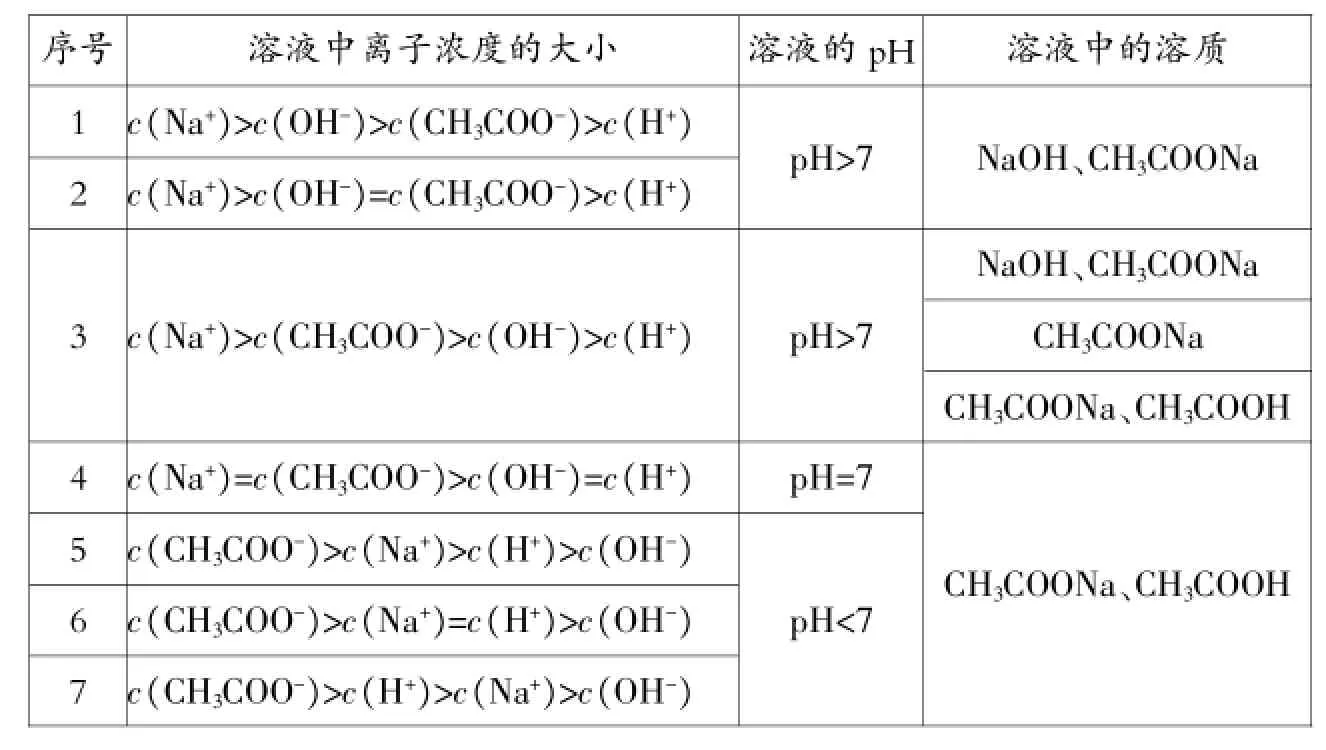
若我们把以上的离子浓度顺序理清,此类“四离子”问题就会迎刃而解。我们还可以触类旁通,利用本题的原理和三个守恒的思想去解决一定浓度的氨水和盐酸混合后溶液中NH4+、H+、OH-、Cl-四种离子浓度的大小。
文章编号:1008-0546(2010)10-0076-02中图分类号:G633.8
文献标识码:B
doi:10.3969/j.issn.1008-0546.2010.10.032
