阿魏酸糖酯体外抗氧化性质的研究
2010-03-21孙宝国曹雁平
赵 冰,张 可,王 静,*,孙宝国,曹雁平
阿魏酸糖酯体外抗氧化性质的研究
赵 冰1,张 可2,王 静1,*,孙宝国1,曹雁平1
(1. 北京工商大学化学与环境工程学院,食品添加剂与配料北京高校工程研究中心,北京 100048;2. 空军航空医学研究所,北京 100142)
采用内切木聚糖酶酶解小麦麸皮不溶性膳食纤维制备阿魏酸糖酯。研究表明阿魏酸糖酯具有螯合金属离子、清除H2O2、羟自由基、DPPH自由基的作用;与人工合成抗氧化剂BHT、VC相比,阿魏酸糖酯仍然表现出很强的抗氧化性质,而且比游离态阿魏酸的抗氧化性质高。
小麦麸皮;阿魏酸糖酯;自由基;抗氧化性质
谷物膳食对人体健康及癌症、心脏病、糖尿病[1]等的预防有重大意义,这与谷物中的膳食纤维和酚酸类物质有很大的关系。这些物质都具有潜在的抗氧化性质。阿魏酸作为谷物中含量最为丰富的一种酚酸类物质,具有很好的抗氧化性质[2]。谷物中的阿魏酸一般是以酯键与阿拉伯木聚糖的阿拉伯糖残基连接在一起的,通过适度的水解可以得到阿魏酸糖酯[3]。阿魏酸具有清除自由基、抗血栓、抗菌消炎、抑制肿瘤、防治高血压、心脏病、增强精子活力等作用[4]。通过研究表明,以结合态存在的阿魏酸具有比游离态存在的阿魏酸更好的抗氧化性质[5]。这已经引起了学者们极大的研究兴趣。
小麦作为世界上最为重要的粮食产物之一,是人体膳食的重要组成部分。近年来,我国每年大约有2000万t的小麦麸皮,作为饲料成分的经济价值很低。因此,越来越多的人将其作为膳食纤维和酚酸类物质的重要来源进行研究。本实验采用内切木聚糖酶酶解小麦麸皮不溶性膳食纤维制备阿魏酸糖酯,并研究阿魏酸糖酯的抗氧化性质,为其作为添加剂提供参考。
1 材料与方法
1.1 材料与试剂
小麦麸皮购自河北承德热河面粉厂,经粉碎过筛后备用。
内切木聚,糖酶 武汉新华扬生物有限公司;桦木木聚糖、2,,2 -联吡啶、脱氧核糖、DPPH、Amberlite XAD-2大孔吸附树脂 Sigma公司;阿魏酸 天津市精细化工研究所。实验中所用试剂均为分析纯。
1.2 仪器与设备
SHZ-82A恒温振荡器 国华电器有限公司;UV-Vis spectrophotometer SHIMADZU紫外-可见分光光度计 日本岛津公司。
1.3 方法
1.3.1 木聚糖酶酶活力的测定[3]
将预热到60℃的1mL的稀释酶液加入到同样预热到60℃的1mL 10mg/mL木聚糖溶液中,两种物质都是用50mmol/L pH5.0醋酸盐缓冲液配制而成,将其混匀后60℃反应30min,然后加入2mL 3,5-二硝基水杨酸试剂,混匀,沸水浴5min,流水快速冷却,加水定容至25mL,波长540nm处测吸光度。以木糖的质量浓度(mg/mL)为横坐标,以吸光度(A)为纵坐标,绘制标准曲线。以每分钟生成1μmol木糖所需要的酶量为一个活力单位,用U表示。
1.3.2 阿魏酸糖酯的制备
粉碎过筛的小麦麸皮经一系列处理后,制备得到不溶性膳食纤维[6-7],40℃真空干燥。再用内切木聚糖酶在适宜条件下水解不溶性膳食纤维,制备阿魏酸糖酯。将酶解液离心取上清液,用大孔吸附树脂进行纯化[8],用蒸馏水和甲醇进行洗脱。将洗脱得到的溶液收集,浓缩,再冷冻干燥,得到阿魏酸糖酯。
1.3.3 对金属离子的螯合作用[9]
将0.25mL的1mmol/L FeSO4溶液与0.25mL不同质量浓度的阿魏酸糖酯溶液(用1mmol/L pH7.4的磷酸缓冲液配制)混合后,再分别加,入0.5mL pH7.4的Tris-HCl缓冲液、0.5mL 1mg/mL 2-2 -联吡啶(用0.2mol/L HCl溶液溶解)、0.4mL 100mg/mL盐酸羟胺溶液和2.5mL无水乙醇。以EDTA作为参照物,对照为不含测试样品溶液。反应结束后用蒸馏水定容到5 m L,混匀,室温下反应10min,在波长522nm处测定其吸光度,计算其螯合能力IC50。对铁离子的螯合能力用公式(1)进行计算。

式中: A样品为反应溶液中样品或参考物质存在情况下的吸光度;A对照为测试溶液中不含样品或参考物质情况下的吸光度。公式(2)~(4)同。
1.3.4 对H2O2的清除作用[10]
用1mmol/L pH7.4的磷酸缓冲液在20℃制备H2O2溶液,H2O2的浓度在波长230nm处用比色法进行测定,该波长下H2O2的摩尔消光系数为81L/(mol·cm)[11]。取3.4mL不同质量浓度的样品液(用1mmol/L pH7.4的磷酸缓冲液配制)与600μL H2O2溶液混合,反应10min,在波长230nm处比色测定H2O2的浓度,以VC和阿魏酸作参考物质,计算其清除率IC50。样品和标准物质对H2O2的清除能力按公式(2)进行计算。

1.3.5 对羟自由基的清除作用[12]
将1mL不同浓度的样品与200μL 3mmol/L的脱氧核糖、400μL 100μmol/L的FeC13与100μmol/L的EDTA预混合(l:l,V/V)、1mmol/L 200μL H2O2、200μL l00μmol/L的VC混合。反应混合物在37℃反应60min,然后加入2mL 5mg/mL TBA溶液(用100mg/mL三氯乙酸溶液配制),混匀后,在沸水浴中加热15min,流水迅速冷却,在12000r/min离心5min,然后在波长532nm处测定上清液的吸光度。以阿魏酸作为参考物质,计算其清除率IC50。清除效果按公式(3)进行计算。

1.3.6 对DPPH自由基清除作用[13]
将0.4mL不同浓度的样品与1.6mL 100mmol/L pH7.4的Tris-HCl缓冲液、2.0mL 0.5mmol/L DPPH甲醇溶液进行混合,对照不含测试样品。摇匀后,室温下暗处反应30min,波长517nm处测定其吸光度。以BHT和阿魏酸作参考物质,计算其清除率IC50。测试样品的自由基清除能力按式(4)进行计算。
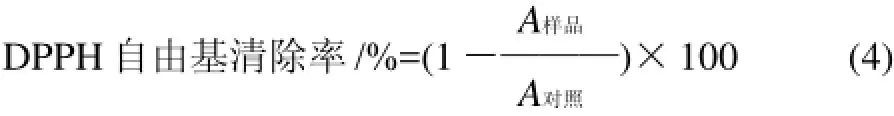
2 结果与分析
2.1 木聚糖酶的酶活力
通过测定得到木聚糖酶与木聚糖溶液反应后所得木糖的吸光度分别为0.473、0.470、0.474。得到其标准曲线方程为y=0.4405x-0.0061,R2=0.9996。计算得到木聚糖酶的酶活力为60233.33U/g。
2.2 阿魏酸糖酯对Fe2+的螯合作用
对金属离子的螯合能力是抗氧化剂的一个重要性质。酚酸类化合物的苯氧基具有很高的电荷密度,使得它能够结合带电的金属离子,从而达到螯合和稳定金属离子的效果[14]。
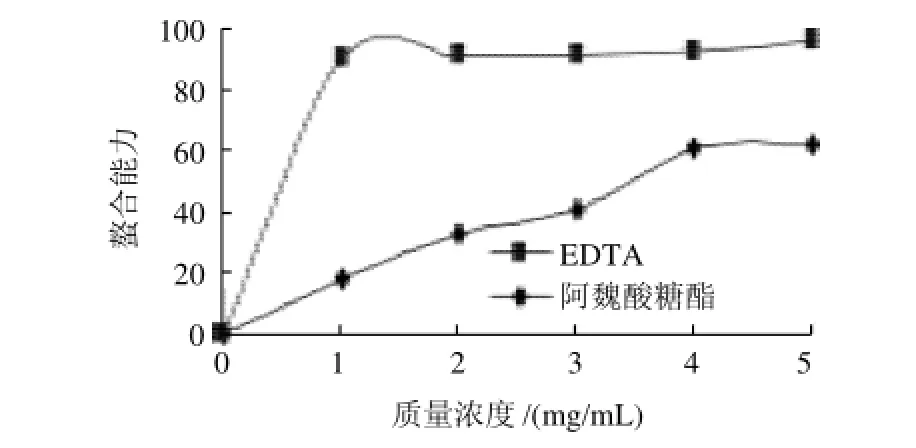
图1 阿魏酸糖酯和EDTA螯合金属离子的能力Fig.1 Comparison of ferrous chelating capacity between ferulic acid sugar esters and EDTA
从图1可,以看出,阿魏酸糖酯对Fe2+具有较强的螯合能力。2,2 -联吡啶能定量地与Fe2+形成红色螯合物,在有其他比其螯合能力更强的螯合剂存在的情况下,红色螯合物的形成将被破坏,颜色也会发生变化。因此,可以通过测定颜色的变化来研究抗氧化剂的,螯合能力。在此实验中,阿魏酸糖酯能够抑制Fe2+与2,2 -联吡,啶形成红色螯合物。由此说明,阿魏酸糖酯能够比2,2 -联吡啶优先结合Fe2+,从而表现出对Fe2+的螯合作用,阿魏酸糖酯的IC50大约为3.5mg/mL,阿魏酸糖酯对Fe2+的螯合作用呈剂量依赖关系,当阿魏酸糖酯质量浓度达到4.0mg/mL,对Fe2+的螯合能力可以达到同质量浓度EDTA的66.43%。
2.3 阿魏酸糖酯对H2O2的清除作用

图2 阿魏酸糖酯和VC对H2O2的清除能力Fig.2 Comparison of hydrogen peroxide scavenging capacity between ferulic acid sugar esters and VC

图3 阿魏酸和阿魏酸糖酯对H2O2的清除作用Fig.3 Comparison of hydrogen peroxide scavenging capacity between ferulic acid sugar esters and free ferulic acid
由图2、3可以看出,阿魏酸糖酯对H2O2的清除作用呈浓度依赖关系。与VC比较,可以发现阿魏酸糖酯表现出很高的清除作用,当阿魏酸糖酯的质量浓度达到0.5mg/mL时,其清除率可以达到同等质量浓度VC的72.97%。而与阿魏酸相比也可以发现,相同浓度下的两种物质,阿魏酸糖酯的清除作用明显高于阿魏酸,这种效果在低浓度的条件下更加明显,阿魏酸糖酯的IC50大约为0.39mmol/L,而阿魏酸的IC50大约为0.42mmol/L。由于阿魏酰基是一个良好的电子供体,它们可能加速H2O2转变成水,而显示出对H2O2的清除作用,而结合态的阿魏酸由于低聚木糖的存在,使阿魏酰基表现出更高的清除作用。
2.4 阿魏酸糖酯对羟自由基的清除作用
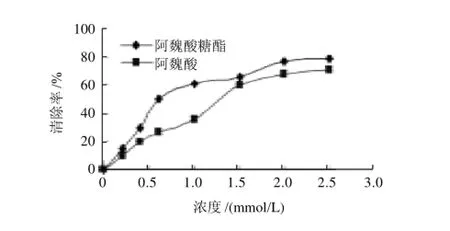
图4 阿魏酸和阿魏酸糖酯对羟自由基的清除作用Fig.4 Comparison of hydroxyl free radical scavenging capacity between ferulic acid sugar esters and free ferulic acid
如图4所示,阿魏酸糖酯对羟自由基具有明显的清除作用,其清除率与阿魏酸糖酯存在剂量依赖关系,即随着阿魏酸糖酯浓度的增加,对羟自由基的清除作用也随着增加,对于相同浓度的阿魏酸和阿魏酸糖酯来说,阿魏酸糖酯表现出更高的清除作用;阿魏酸的IC50大约为1.3mmol/L,而阿魏酸糖酯的IC50大约为0.6mmol/L,还不到阿魏酸的一半,这就表明了阿魏酸糖酯具有更优越的清除羟自由基的作用。这就使得阿魏酸糖酯可以保护食品、保健品等中的糖类物质免受羟自由基诱导的氧化损害[15]。
2.5 阿魏酸糖酯对DPPH自由基的清除作用

图5 阿魏酸糖酯和BHT对DPPH自由基清除作用Fig.5 Comparison of DPPH free radical scavenging capacity between ferulic acid sugar esters and BHT

图6 阿魏酸和阿魏酸糖酯对DPPH自由基清除作用Fig.6 Comparison of DPPH free radical scavenging capacity between ferulic acid sugar esters and free ferulic acid
从图5、6可以看出,阿魏酸糖酯对DPPH自由基具有强烈的清除作用。由图5可知,当阿魏酸糖酯的质量浓度在0~2.0mg/mL时,清除能力的增加非常明显;质量浓度超过2.0mg/mL时,清除能力增加非常缓慢,清除能力可以达到60%左右,虽然阿魏酸糖酯的清除能力不如BHT,但是作为天然无毒的物质,仍然具有很高的利用价值,而且当阿魏酸糖酯的质量浓度达到10mg/mL时,它的清除能力可以达到近70%,已经很接近BHT的清除率了。从图6可以看出,阿魏酸糖酯的清除能力高于阿魏酸,阿魏酸糖酯的IC50大约为1mmol/L,而阿魏酸的IC50大约为2.8mmol/L。
3 结 论
阿魏酸糖酯具有良好的抗氧化效果。阿魏酸糖酯具有螯合金属离子、清除H2O2、·OH、DPPH自由基的作用,在一定的浓度范围内呈剂量依赖关系,与人工合成抗氧化剂相比也不处于劣势,因此,阿魏酸糖酯具有很强的抗氧化功能,可以作为抗氧化剂进行使用。研究还发现,与游离态阿魏酸[16]相比,阿魏酸糖酯表现出高得多的抗氧化性质,这可能与阿魏酸糖酯的结构有很大关系,阿魏酸糖酯所带的低聚木糖残基和阿拉伯糖残基使阿魏酸糖酯表现出更高的生物活性,使其既具有阿魏酸的性质,又具有低聚木糖的性质。而且阿魏酸糖酯还解决了阿魏酸作为食品添加剂的水溶性问题,阿魏酸糖酯在水中具有很高的溶解性,而且具有很好的耐热性。因此,阿魏酸糖酯在添加剂行业具有广阔的应用前景。
[1]TEMPLE N J. Antioxidants and disease: More questions than answers [J]. Nutr Res, 2000, 20(3): 449-459.
[2]GRAFT E. Antioxidant potential of ferulic acid[J]. Free Radical Biol Med, 1992, 13(4): 435-448.
[3]袁小平. 酶解麦麸制备阿魏酰低聚糖及其生物活性的研究[D]. 无锡:江南大学, 2006.
[4]欧仕益, 包惠燕, 蓝志东. 阿魏酸及其衍生物的药理作用研究进展[J]. 中药材, 2001(3): 220-221.
[5]RONDIM L, PEYRAT-MAILLARD M N, MARSSET-BAGLIEN A, et al. Bound ferulic acid from bran is more bioavailable than the free compound in rat[J]. J Agric Food Chem, 2004, 52: 4338-4343.
[6]ZILLIOX C, DEBEIRE P. Hydrolysis of wheat straw by a thermostable endoxylanase: Adsorption and kinetic studies[J]. Enzyme Microb Technol, 1998, 22(1): 58-63.
[7]BUNZEL M, RALPH J, MARITA J M, et al. Diferulates as structural components in soluble and insoluble dietary fibre[J]. J Sci Food Agric, 2001, 81: 653-660.
[8]BUNZEL M, ALLERDINGS E, SINWELL V, et al. Cell wall hydroxycinnamates in wild rice(Zizania aquatica L.) insoluble dietary fible[J]. Eur Food Res Technol, 2002, 214(6): 482-488.
[9]YAMAGUCHI F, ARIGA T, YOSHIMURA Y, et al. Antioxidative and anti-glycation activity of garcinol from Garcinia indica fruit rind[J]. J Agric Food Chem, 2000, 48(2): 180-285.
[10]RUCH K J, CHENG S J, KLAUNING J E. Prevention of cytotoxicity and inhibition of intercellular communication by antioxidant catechin isolated from Chinese greenter[J]. Carcinogensis, 1989, 10(6): 1003-1008.
[11]BEERS R F, SIZER I W. A spectrofluorometric method for measuring the breakdown of hydrogen peroxide by catalase[J]. J Biol Chem, 1952, 195: 133-140.
[12]HALLIWELL B, GUTTERIDGE J M C, ARUOMA O I. The deoxyribose method: A simple test-tube asssy for determination of rate constants for reactions of hydroxyl radicals[J]. Anal Chem, 1987, 165: 215-219.
[13]BRAND-WILLIAMS W, CUVELIER M E, BERSET C. Use of a free radical method to evaluate antioxidant activity[J]. Lebensm-Wiss Technol, 1995, 28: 25-30.
[14]姚惠源, 胡敏, 袁小平, 等. 酶法制备阿魏酰低聚糖的研究[J]. 食品与机械, 2008, 24(4): 3-7.
[15]袁小平, 王静, 姚惠源. 小麦麸皮阿魏酰低聚糖对红细胞氧化性溶血抑制作用的研究[J]. 中国粮油学报, 2005, 20(1): 13-16.
[16]赵文红, 邓泽元, 范亚苇, 等. 阿魏酸体外抗氧化作用研究[J]. 食品科学, 2010, 31(1): 219-223.
Antioxidant Properties of Ferulic Acid Sugar Esters in vitro
ZHAO Bing1,ZHANG Ke2,WANG Jing1,*,SUN Bao-guo1,CAO Yan-ping1
(1. Beijing Higher Institution Engineering Research Center of Food Additives and Ingredients, School of Chemical and Environmental Engineering, Beijing Technology and Business University, Beijing 100048, China;2. Institute of Aviation Medicine, Air Force, Beijing 100142, China)
The ferulic acid sugar esters prepared from wheat bran hydrolyzed by endo-xylanase were characterized for their antioxidant properties in vitro reflected by the abilities to scavenge hydrogen peroxide as well as hydroxyl and DPPH free radicals and to chelate metals using two synthetic antioxidants, BHT and VC, as the controls. The sugar esters were found to have strong antioxidant properties, which were better than those of free ferulic acid.
wheat bran;ferulic acid sugar esters;radicals;antioxidant properties
TS202.3
A
1002-6630(2010)21-0094-04
2010-06-12
北京市教委面上项目(KM200910011002);北京市科学技术委员会科技新星项目(2008B07)
赵冰(1986—),男,硕士研究生,研究方向为农副产品资源的开发利用。E-mail:zhaobtg@163.com
*通信作者:王静(1976—),女,副教授,博士,研究方向为农副产品资源的开发利用。E-mail:jwang810@yahoo.com.cn
