电解液用量及负极添加剂对锌镍电池的影响
2010-02-28曾冬青杨占红王升威申松胜
曾冬青,杨占红,王升威,申松胜
(1.中南大学化学化工学院,湖南长沙 410083; 2.新乡联达华中电源有限公司,河南新乡 453731)
提高锌镍电池实用性能的重点在锌负极和电解液,并可归结为两类:①对锌负极的活性物质,如锌酸钙[1]、ZnO的Sn包覆物[2]等改性或再造,以降低金属锌的反应活性,抑制ZnO在碱性电解液中的不可逆溶解,但工艺复杂,尚不能大规模生产;②向锌负极或电解液中加入添加剂,对锌电极的阳极或阴极过程施加影响,无机添加剂有 In[3]、Bi、Sn等元素的氧化物、ZnSO4[4]等,有机添加剂有聚乙二醇600[5]、含氟表面活性剂[6]、吐温-20[7]、烷基数为 12~16的烷基三甲基溴化铵[8]等。对添加剂的研究多为开口或半开口体系,所得结论具有局限性,它们在密封电池中的应用值得探讨。
本文作者以六次甲基四胺(HT)、十二烷基苯磺酸钠(SDBS)、十六烷基三甲基溴化铵(CTAB)、亚硫酸钠(Na2SO3)或它们的组合为锌负极添加剂,研究了锌负极添加剂及电解液用量对密封锌镍电池的影响。
1 实验
1.1 极片的制作
将质量比为 79.6∶10.0∶7.0∶3.0∶0.4∶45.0 的 Ni(OH)2(无锡产,电池级)、CoO(无锡产,电池级)、石墨(青岛产,电池级)、聚四氟乙烯(PTFE,上海产,电池级)、羧甲基纤维素钠(CMC,上海产,电池级)和水在不断搅拌的条件下调成墨绿色浆料,用刮板将浆料均匀涂覆于1.60±0.05 mm厚的泡沫镍(无锡产,孔数PPI为70~110)基体上。在30℃下自然干燥16 h后,辊压至0.65±0.02 mm厚,再剪切为30 mm×50 mm,经清粉、点焊等工序,制得正极片。
将质量比为 69.3∶9.9∶9.9∶4.9∶3.0∶1.0∶1.0∶0.4∶0.4∶0.2∶42.0的ZnO(上海产,AR)、Zn粉(上海产,AR,300目)、自制锌酸钙[1]、石墨、PTFE、Ca(OH)2(上海产,AR)、CMC、SnO2(长沙产,AR)、六偏磷酸钠(天津产,AR)、负极添加剂和水在不断搅拌的条件下调成粘稠状浆料,通过拉浆法制得湿态负极。在30℃下自然干燥12 h后,辊压至0.30±0.01 mm厚,再剪切为34 mm×100 mm,制得负极片。以 HT(长沙产,AR)、SDBS(天津产,AR)+CTAB(长沙产,AR)+Na2SO3(长沙产,AR)(质量比为2∶1∶1)及HT+SDBS(质量比为1∶1)为添加剂的负极,依次记为负极B、C、D,不使用添加剂的负极记为负极A。
1.2 密封锌镍电池的组装
电池的设计容量为400 mAh,正极限容,正、负极容量比为1.0∶2.8。隔膜为GP-1聚乙烯微孔膜(上海产)和维纶18隔膜(河南产)两层(聚乙烯微孔膜靠近负极);电解液为6.3 mol/L KOH(广东产,AR)+1.4 mol/L NaOH(广东产,AR)+0.7 mol/L LiOH(天津产,AR),并用ZnO(上海产,AR)饱和。将正极、负极和隔膜卷绕后入壳,注入电解液后,涂油、加密封圈、点焊盖帽,封口化成,制得AA型密封锌镍电池。
化成制度:0.1C充电13 h,0.5C放电;0.5C充电2.5 h,0.5C放电;1.0C充电1 h。放电截止电压为1.400 V。
考察添加剂对电池性能的影响时,使用负极A、B、C、D的电池依次记为电池A、B、C、D,电解液用量均为2.7 g。用负极C考察电解液用量对电池循环性能的影响,添加2.0 g、2.5 g、2.7 g、2.9 g 电解液的电池依次记为电池 a、b、c、d。
1.3 密封锌镍电池的性能测试
用BK-6016A/30二次电池测试系统(广州产)对化成好的电池进行性能测试。测试条件:电流为1.0C,充电时间为68 min,限压2.300 V,放电截止电压为1.400 V,温度为20±5℃。
高温储存测试:在电热恒温鼓风干燥箱中、50℃下储存7 d,用电压测试仪(广州产)记录储存期间的开路电压,然后以1.0C放电至1.400 V,用BK-6016A/30二次电池测试系统测试储存后的放电容量;
常温储存测试:在常温下储存28 d后,用YC-2000二次电池化成柜(广州产)测试放电容量。
2 结果与讨论
2.1 锌负极添加剂对电池性能的影响
2.1.1 充放电性能
使用不同负极添加剂的电池的充、放电曲线见图1。
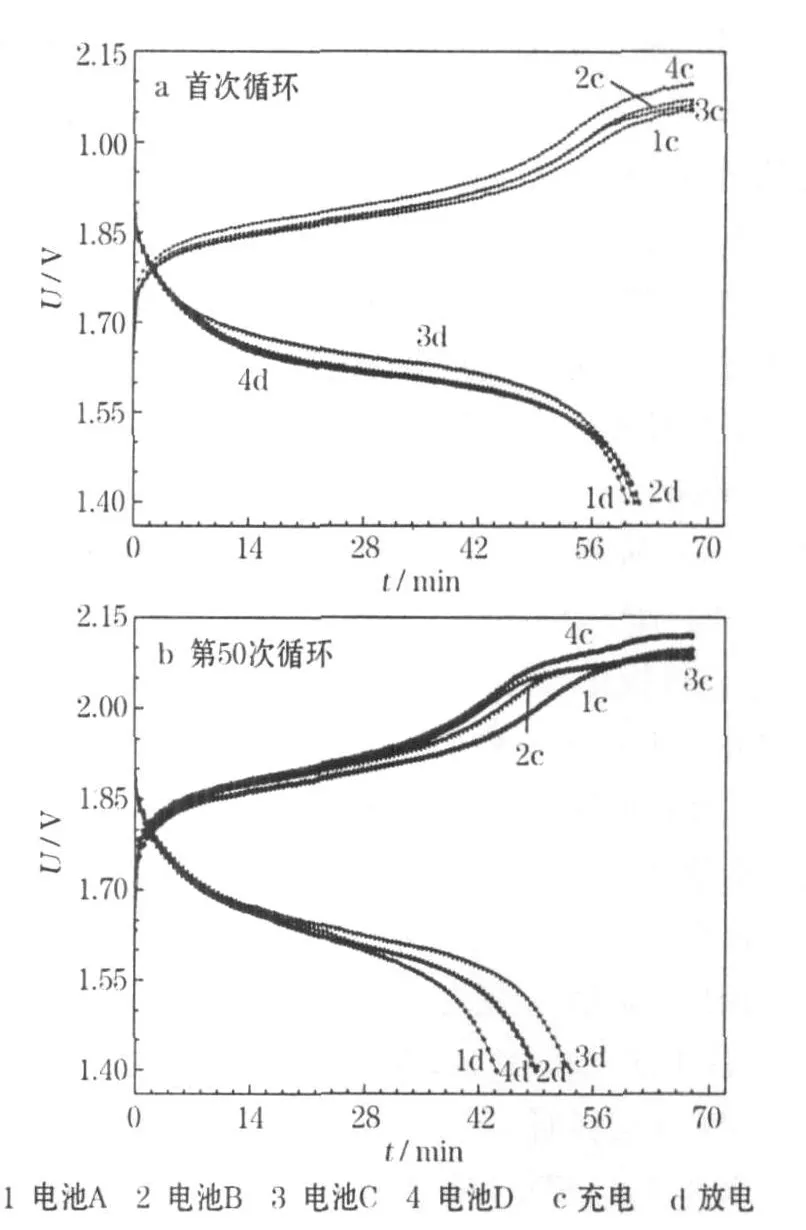
图1 使用不同负极添加剂的电池的充、放电曲线Fig.1 The charge-discharge curves of sealed Ni-Zn batteries using different anode additives
从图1可知,随着充电时间的延长,各电池的充电电压逐步增加,原因是充电过程中电极的极化不断增加。电池A的充电终止电压最低,为2.055 V,电池D的终止电压最高,为 2.097 V,电池B、C的终止电压分别为2.070 V、2.063 V。电池A、B、C的充电终止电压差别很小,电池 D较高的充电电压可能与HT的加入有关。HT为非离子有机物,在首次循环时,作为负极组成增加了电极的电阻,导致充电电压的升高。总体而言,负极添加剂对电池首次充电的影响有限。电池A的充电终止电压达到了2.097 V,比首次充电要高0.042 V,说明随着循环的深入,锌电极的变形、钝化等缺陷导致负极出现了较大的极化。充电后期,电池A在65~68 min时间段出现了电压平台,原因是正极出现过充,产生析氧。电池 D的充电终止电压为2.119 V,在63~68 min时间段有一个电压平台,电池B在此时间段也有一个充电平台,说明电池B、D均出现了过充现象。电池C在50 min时开始出现电压的缓慢增加,并在64~68 min时间段出现了电压平台。根据缓蚀的基本理论[9]可知,HT、SDBS、CTAB这类有机活性分子均可在锌负极表面形成连续的、起物理屏障作用的吸附层,使充电过程中电极/溶液界面的电荷传递变得困难,导致电极的电化学过程变得困难;同时随着充电的深入,浓差极化也逐步增加,因此充电终止电压逐步升高。HT有4个N吸附官能团,SDBS只有1个S官能团,CTAB有1个 N官能团,因此,电池D较电池B、C有更高的充电电压。SDBS与CTAB的组合,比单一物种具有更紧密的吸附层,并增加电极极化,导致出现过充现象。
从图1还可看出,在首次放电时,电池A、B、C、D的放电容量分别为 397.10 mAh、411.11 mAh、403.70 mAh、405.38 mAh,放电平台明显,约为1.650 V。从数据上看,似乎放电性能顺序为B>D>C>A,但本文作者认为,电池首次放电所给的有效信息有限,因为锌负极在化成后,往往还要经过一定的循环才能达到稳定。从这方面来说,电池的首次放电数据带有一定的偶然性,可靠性值得商榷。电池C具有较好的放电平台且平台维持的时间长,总放电时间最长,容量为351.34 mAh,是设计容量的87.8%。电池A的放电时间最短,电池B、C居中,且放电曲线相似。这表示在循环过程中,电池A由于活性物质的不可逆损失,电极表面均匀性严重下降,导致电极极化加大,放电条件恶化,使得循环容量下降,而电池B、C、D由于隔离了溶剂分子在锌负极表面的汇集,抑制了活性物质的溶解损失,改善了电极的表面状况,获得了优于电池A的循环性能。缓蚀作用的电化学理论[9]认为,有机表面活性分子在零电荷电位附近才发生强烈吸附,当电极电势偏离此值后,吸附力很快下降,最终脱附。胡俊[10]发现,电解液中加入SDBS后,电池的充电电压明显增加,但放电性能却并未受影响,原因是SDBS在放电时存在脱附。从实验结果来看,以SDBS部分代替HT不能明显改善电池的放电性能,本文作者认为原因是:在放电过程中,SDBS发生强烈的脱附,露出所占据的负极活性点,但由于具有较强表面吸附性的HT重新占据部分活性点,使电极的放电性能不能得到较大的提高。
2.1.2 循环性能
使用不同负极添加剂的电池的循环性能见图2。
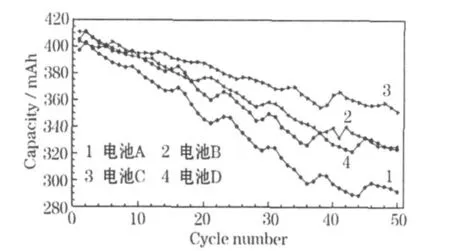
图2 使用不同负极添加剂的电池的循环性能Fig.2 Cycle performance of sealed Ni-Zn batteries using different anode additives
从图2可知,电池C的循环性能最好,电池A最差,电池B稍优于电池D。第50次循环时,电池C的放电容量为351.34 mAh,是设计容量的87.8%。电池A的放电容量为291.72 mAh,是设计容量的 72.9%。电池B、C的放电容量分别为 325.56 mAh、323.52mAh,分别是设计容量的81.4%、80.9%。这表明在多次循环后,作为添加剂的有机表面活性剂抑制了负极活性物质的溶解,改善了电极的表面状况。对电池C而言,Na2SO3的SO2-3能与电池过充产生的氧气复合,生成SO2-4,延缓锌电极的钝化。SDBS与CTAB复配,一方面两种表面活性剂离子间存在强烈的静电作用,在混合吸附时具有较强的协同效应,对水偶极层中的水分子排挤作用更大,提高了锌在碱性电解液中的抗腐蚀能力,可起到较好的缓蚀效果;另一方面,两者均为表面活性剂,具有分散作用,配合后可改善负极浆料的均匀性和流动性,得到工艺性较好的锌负极[11],为电池循环性能的提高提供保证。
2.1.3 自放电性能
锌镍电池的自放电主要是金属锌在碱性溶液中的电化学腐蚀引起的,该过程的阳极、阴极及总反应见式(1)~(3)。

有关锌镍电池自放电性能的研究较少。高温储存测电池自放电性能的基本原理是:从热力学角度看,由于电池的自放电为放热、熵增的过程,提高反应温度有利于该过程的进行。锌镍电池在自放电过程中,负极活性物质会有不可逆损失,其结果在开路电压和放电容量中有所体现。高温储存过程中,使用不同负极添加剂的电池开路电压的变化见图3。
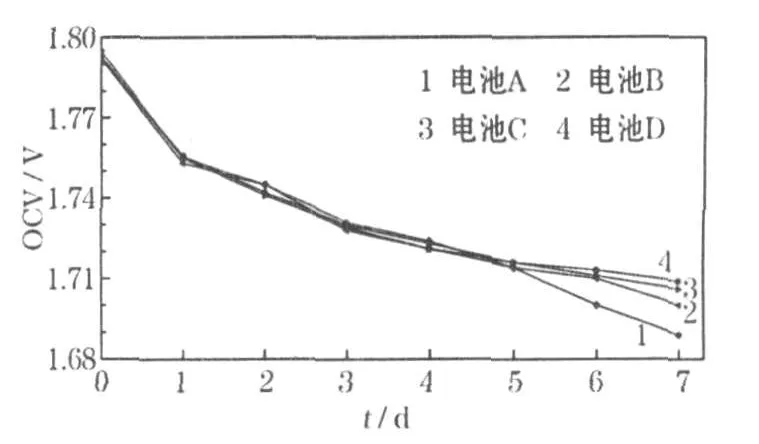
图3 使用不同负极添加剂的电池在高温储存过程中的开路电压变化Fig.3 The open circuit voltage(OCV)change of sealed Ni-Zn batteries using different anode additives during high temperature storage
从图3可知,经7 d高温储存后,电池 A、B、C、D的开路电压依次为 1.689 V、1.700 V、1.706 V、1.709 V;随着储存时间的延长,开路电压持续下降。在自放电测试中,电池由于活性物质从活性高的金属态转化为氧化态,开路电压下降得很快,随着活性物质不断转化形成氧化态保护钝化膜,电池的开路电压变化趋于平缓。总体而言,电池C、D的开路电压变化较平缓,电池B次之,电池A变化最剧烈。这主要是因为电池A中金属锌形成的氧化态保护钝化膜在碱性电解液中的溶解度较高,在储存过程中,钝化膜在不断地生成,当生成的速度小于溶解速度时,钝化膜就会遭到溶解破坏[11],使活性物质暴露于碱性溶液中,再加上高温储存使自放电反应大大加快,增加了锌的不可逆损失。电池B、C、D中有机添加剂的缓蚀作用,抑制了碱性电解液对钝化膜的溶解,保护了钝化膜的完整性,且锌的反应活性较小、损失较少。电池D的开路电压高于电池C,是因为HT的吸附能力较强,比SDBS、CTAB能更好地隔离锌与碱性电解液,提高自放电反应的能垒。电池B加入了HT,但吸附性较弱的SDBS与吸附性强的HT导致电极表面的化学环境不稳定。
电池A、B、C、D在储存后的放电容量见表1。
从表1可知,在高温储存时,电池C、D的放电容量较高,电池B居中,电池A最低。电池A、B的放电容量损失主要是活性物质损失相差较大造成的。电池C、D放电容量的变化情况与电压的变化情况相反,原因是HT虽然能隔离锌与碱性溶液的接触,抑制自放电反应,但电池D在放电过程中受到一定的阻碍,致使容量不能完全发挥,且电池C的两种添加剂具有较好的协同作用,而Na2SO3中的SO2-3能吸收镍正极释放的氧气,降低电池的内压,为负极提供较稳定的化学环境。常温储存的测试结果与高温储存的结果的一致性较好。由此可见,与常温储存测试相比,高温储存能快速测定锌镍电池的自放电性能,并得到较准确的结果。

表1 使用不同负极添加剂的电池在储存后的放电容量Table 1 The discharge capacity of sealed Ni-Zn batteries using different anode additives after storage
2.2 电解液用量对电池循环性能的影响
不同电解液用量的电池循环100次的放电容量见图4。

图4 不同电解液用量的电池循环100次的放电容量Fig.4 The discharge capacity of sealed Ni-Zn batteries with different electrolyte amount
从图4可知,电池a、b、c、d的首次放电容量分别为403.70 mAh、431.33 mAh、403.92 mAh、395.11 mAh;第 100次循环的放电容量分别为 259.60 mAh、316.67 mAh、298.54 mAh、294.10 mAh,为设计容量的 64.9%、79.1%、74.6%、73.5%。电池b的容量较高,但从整体趋势上看,电池c、d的循环性能较好,电池a则在前期(约60次)有较高的容量和较好的循环性能。对密封锌镍电池而言,过多的电解液将阻碍正极的氧气在负极的复合,因为电解液把隔膜的气孔全部淹没,使氧气的扩散变得困难,同时也使氧气与锌负极的反应面积减少。反之,过少的电解液会使隔膜的润湿不够,电极与隔膜的接触不好,电池的内阻增大,不利于容量的释放。也就是说,镍正极析出的氧气在锌负极的复合与电池内阻两个因素,决定了电解液的合适用量。从实验考察的几个用量来说,电池b达到了较佳的平衡状态。在循环后期,电解液将有一定的损耗,此时,原来处于富液态的电池c、d开始处于“亚富液”态,达到了类似于电池b的平衡状态,而电池a开始变为贫液态,隔膜和极片的润湿和接触都不好,因此,随着循环的深入,电池c、d较电池a衰减平缓。至于电池 a、b间是否有更好的平衡点,有待于进一步考察。
3 结论
锌负极同时加入十二烷基苯磺酸钠(SDBS)、十六烷基三甲基溴化铵(CTAB)、亚硫酸钠(Na2SO3)能改善密封锌镍电池的充放电性能和循环性能,第50次循环时,电池仍能保持设计容量的87.8%。添加六次甲基四胺(HT)能提高电池的高温储存性能,但放电过程受到一定的阻碍。
密封锌镍电池中电解液的最佳用量是镍正极析出的氧气在锌负极的复合度与电池内阻平衡的结果。对于设计容量为 400 mAh的电池,实验所得的较好用量为2.5 g,第 100次循环时,能保持设计容量的79.1%。
高温储存测试能快速测定锌镍电池的自放电性能,并得到较合理的结果。
[1] YANG Zhan-hong(杨占红),WANG Sheng-wei(王升威),ZENG Li-hui(曾利辉),et al.化学合成法制备锌镍电池负极材料锌酸钙[J].Journal of Central South University(Science and Technology)[中南大学学报(自然科学版)],2008,39(5):918-922.
[2] Yuan Y F,Tu J P,Wu H M,et al.Preparation,characteristics andelectrochemical performance of Sn6O4(OH)4-coated ZnO for Zn-Ni secondary battery[J].Electrochem Commun,2006,8(4):653-657.
[3] ZHOU He-bing(周合兵),YANG Mei-zhu(杨美珠),LU Dongsheng(吕东生),et al.几种缓蚀剂对锌粉缓蚀效果的比较[J].Battery Bimonthly(电池),2003,33(6):378-380.
[4] LI Jing-wei(李景威),YANG Zhan-hong(杨占红),GU Peng(谷鹏),et al.添加ZnSO4对Zn-Ni电池锌负极性能的影响[J].Battery Bimonthly(电池),2008,38(4):234-235.
[5] JIA Zheng(贾铮),ZHANG Cui-fen(张翠芬),ZHOU De-rui(周德瑞).二次碱性锌电极的复合缓蚀剂[J].Battery Bimonthly(电池),2004,34(2):111-113.
[6] GAO Cui-qin(高翠琴),HU Jing-wei(胡经纬),ZHOU Yun-hong(周运鸿).含氟表面活性剂在碱性锌电极中的应用[J].Battery Bimonthly(电池),2002,32(2):75-77.
[7] BU Xue-tao(卜雪涛),LIANG Guang-chuan(梁广川),LI Cui(李翠).锌电极有机复配缓蚀剂的性能研究[J].Electrochemistry(电化学),2006,12(2):199-204.
[8] YANG Zi-yun(杨子运),GUO Bing-kun(郭炳),XU Wei(徐微),et al.锌电极有机代汞缓蚀剂的研究[J].Battery Bimonthly(电池),2000,30(6):251-253.
[9] GAO Cui-qin(高翠琴),LUO Lie-chao(罗列超),SHI Jian-zhen(石建珍),et al.有机物添加剂对碱性锌电极的影响[J].Journal of Wuhan University(Natural Science Edition)[武汉大学学报(自然科学版)],1999,45(4):427-431.
[10]HU Jun(胡俊).密封锌镍电池产业化关键问题的研究[D].Changsha(长沙):Central South University(中南大学),2009.
[11]ZENG Li-hui(曾利辉).密封圆柱形锌镍电池负极及相关问题的研究[D].Changsha(长沙):Central South University(中南大学),2007.
