不同提取分离方法对芍药甘草汤物质组成影响的初步研究
2010-02-07方玉婷郭立玮
董 洁, 方玉婷, 郭立玮
(南京中医药大学中药复方分离工程重点实验室,江苏南京210029)
中药复方提取物本质上是一种化学复杂体系,其中包括“基本活性物质”以及与其共存的“伴生物质”[1]。目前所采用的水提醇沉,树脂吸附,膜分离等提取、精制手段其目的都是去除提取物中的伴生物质,保留基本活性物质。以上几种方法因各自技术原理不同,不仅对复方中指标性成分保留率不同且所除去的伴生物质的种类与多少也有差异。鉴于物化参数变化是伴生物质除去的这一微观过程的综合表征,本实验以芍药甘草汤为试验体系,以指标性成分的含量以及物化参数为指标,探索不同的提取、精制方法对芍药甘草汤体系中“基本活性物质”以及“伴生物质”的影响。
1 仪器与药品
高效液相色谱仪(Waters515泵,WaterU6K进样器,Waters2487紫外检测器,JS-3030江申通用汉化色谱工作站);ShimazhuLibrorAEL-40SM(十万分之一)电子天平(日本岛津),PHSJ-4A实验室pH计(上海精密科学仪器有限公司),DDSJ-308A电导率仪(上海精密科学仪器有限公司),SZD-2型智能化散射光浊度仪(上海自来水设备工程公司),NDJ-1型旋转黏度计(上海精密科学仪器有限公司);LDZ5-2型自动平衡离心机(北京医用离心机厂)。
所用药材均购自南京市药材公司,经鉴定符合《中国药典》2005版一部的规定;芍药苷对照品(供含量测定用 批号110715-200212),甘草酸对照品(供含量测定用批号110731-200306),甘草苷对照品(供含量测定用 批号 111610-200604)均购自中国药品生物制品检测所;甲醇、乙腈为色谱纯(江苏汉邦科技有限公司),其余试剂均为分析纯。
2 提取工艺
按处方比例称取各味药,浸泡0.5 h,加水煎煮3次:第1次加10倍量水,煎煮1 h;第2次加8倍量水,煎煮1 h;第3次加8倍量水,煎煮1 h,并分别用300目滤布滤过,合并滤液,得浓度为0.04 g生药/mL的水提液,待用。
3 精制工艺
水提液采用醇沉法、离心法、大孔树脂吸附法、絮凝法、微滤法、超滤法等几种常用的分离工艺精制,比较了不同精制液中指标性成分(芍药苷、甘草苷、甘草酸)含量,以及物理化学参数(pH、电导率、浊度、黏度)。
3.1 醇沉法 采用正交设计法对醇沉工艺进行优选,确定最佳醇沉工艺为:取水提液1 000 mL浓缩至1.5 g生药/mL,不断搅拌该浓缩液同时缓缓加入计算量的乙醇至含醇量达到70%,醇沉时间14 h,滤过,取上清液,挥至无醇味后,用蒸馏水定容至1 000 mL。
3.2 离心法 取水提液1 000 mL离心(3 000 r/min,12 min),倾出上清液并用蒸馏水定容至1 000 mL。
3.3 大孔树脂吸附法 以芍药苷、甘草苷、甘草酸三种成分的吸附量为指标通过考察五种不同型号树脂的静态吸附以及动态吸附-洗脱选择最佳树脂为HPD100。同时,以上述3种成分的保留率为指标通过单因素考察确定最佳工艺为:取水提液1 000 mL并浓缩至浓度为0.05 g生药/mL,取该浓缩液以1.5 mL/min的流速通过已预处理的HPD100树脂柱(树脂床的体积约125 mL),先用500 mL水洗脱,再用70%乙醇500 mL洗脱,收集醇洗脱液,挥至无醇味后,用蒸馏水定容至1 000 mL待用。
3.4 絮凝法 取水提液1 000 mL浓缩至0.16 g生药/mL,并加壳聚糖溶液(壳聚糖-醋酸-水=1∶1∶100)20 mL,静置24 h,过滤,取滤液并用蒸馏水定容至1 000 mL待用。
3.5 微滤法 取水提液1 000 mL离心(3 000 r/min,12 min),倾出上清液并用孔径为0.2 μm的中空聚偏氟乙烯膜组件以错流方式进行循环微滤,待微滤液收集到800 mL后,加入200 mL水,继续微滤直至收集到1 000 mL为止。
3.6 超滤法 取水提液1 000 mL按3.5项进行微滤后,用截留分子量为1~3万的中空聚砜纤维膜组件以错流方式进行循环超滤,待超滤液收集到约800 mL时,加入200 mL水,继续超滤,至收集到1 000 mL为止。
4 指标性成分含量及物理化学常数测定
4.1 pH测定 取样品20 mL,以校正过的精密PHSJ-4A实验室pH计测定样品的pH值。
4.2 电导率测定 取样品20 mL,在溶液温度为20℃时,测定其电导率。
4.3 浊度测定 取样品50 mL,以SZD-2型智能化散射光浊度仪测定样品的浊度值。
4.4 黏度测定 取样品20 mL,以NDJ-1型旋转黏度计测定样品在20℃时的黏度值。
4.5 固含率的测定 精密移取样品20 mL,置于已干燥至恒重的蒸发皿(W1)中,水浴蒸干,于105℃烘箱中干燥3 h,置干燥器中冷却0.5 h,迅速称重(W2),计算固含率。固含率(mg/mL)=(W2-W1)/20。
4.6 指标性成分含量测定方法
4.6.1 芍药苷测定色谱条件[2]69色谱柱为 Kromasil C18(4.6 mm ×250 mm,5 μm);流动相为乙腈 -0.1%磷酸溶液(13∶87),检测波长为230 nm,流速为1.0 mL/min。
4.6.2 甘草苷测定色谱条件[2]59-60色谱柱:Kromasil C18(4.6 mm ×250 mm,5 μm);流动相为乙腈 -1.1%冰醋酸(1∶4),检测波长为276 nm,流速为1.0 mL/min。
4.6.3 甘草酸测定色谱条件[2]59-60色谱柱:Kromasil C18(4.6 mm ×250 mm,5 μm);流动相为甲醇 -0.2 mol/mL 醋酸铵溶液-冰醋酸(67∶33∶1.5);检测波长为250 nm,流速为1.0 mL/min。
以上色谱条件经方法学考察,在所选定的浓度范围内,线性关系、精密度、稳定性、重现性均良好。

表1 固含及指标性成分含量测定结果
5 结果
5.1 固含及指标性成分含量测定结果 从固含来看,芍药甘草汤分别经过上述几种方法处理后固含明显减少,几种精制液固含由低到高的顺序为:大孔树脂洗脱液<醇沉液<超滤液<絮凝液<微滤液<离心液。从指标性成分保留率来看,不同的精制方法对指标性成分的保留率不尽相同。如:对芍药苷而言微滤法和离心法的保留率较高,但超滤法和絮凝法较低。对甘草苷、甘草酸而言离心法较为理想但超滤法的保留率较低。从浸膏中指标性成分含量来看,由于不同的精制方法对指标性成分的保留率不同以及不同精制方法的出膏率也不同,最终导致不同浸膏中指标性成分的含量存在差异。综上所述,几种方法对芍药甘草汤都有精制作用,但通过不同方法精制后芍药甘草汤体系中指标性成分的含量以及各指标性成分之间的比例都有明显改变。这种改变是否会影响芍药甘草汤整体药效,有待从药代动力学以及药效学做进一步研究。
5.2 物理化学参数测定结果
5.2.1 pH、黏度 由图1可知芍药甘草汤水提液和不同精制液的黏度变化不大。但pH在4~6有明显波动,其中超滤液和微滤液的pH最低,而大孔树脂精制液pH最高。pH不同有可能改变化学体系中蛋白质所带电荷数,以及各成分间的絮凝,沉降性能和过滤性能。有文献报道由于给药体系的pH值不同可以改变药物尤其是弱电解质药物(如盐酸小檗碱)的解离度,从而影响药物透过生物膜的难易程度,未解离的分子型药物比离子型药物易于透过生物膜[3]296。
5.2.2 电导率、浊度 浊度是表明液体澄清度的指标,泥沙,药渣碎片,微粒以及没有用的大分子胶体都能增加液体的浊度。由图2可知经过不同的方法处理后芍药甘草汤体系的浊度值大幅度下降,该结果表明几种方法都能除去体系中悬浮颗粒和胶体物质,提高澄清度。其中大孔树脂吸附法,超滤法,微滤法效果尤为明显。
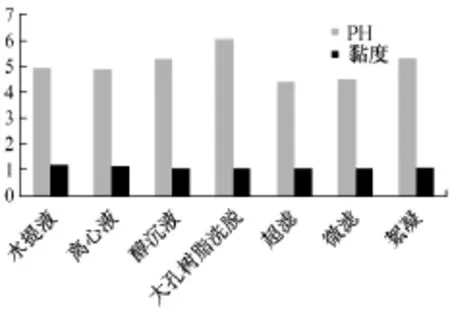
图1 pH、黏度测定结果

图2 电导率、浊度测定结果
电导率是衡量溶液体系离子多少的一个指标,也是描述胶体溶液体系变化的重要指标,与中药提取液中的带电胶体粒子(如蛋白和鞣质)密切相关。图2表明除离心液外,其他几种精制液的电导率较水提液都有改变。其中醇沉液、大孔树脂洗脱液、超滤液、絮凝液电导率有所降低,且大孔树脂洗脱液降低尤为明显,而微滤液的电导率则有所升高。有研究认为:形成离子对可促进带电药物的吸收。离子对在溶液中通过静电吸引所形成中性物质使电荷消失,药物的理化性质、亲脂性增强,易于药物透过生物膜。因而电导率是影响溶液中药物吸收的因素之一[3]29。
6 讨论
综上所述,芍药甘草汤经过不同的方法处理后其物质组成发生了很大的改变。那么如何对不同的精制方法进行科学评价?有文献报道以指标性成分含量作为评价指标,但从本文的试验结果来看,由于每一种精制方法对三种指标性成分的保留率不尽相同,因此,仅以某种指标性成分含量的高低作为评价指标缺乏一定的合理性。又有文献报道[4]伴生物质可改变基本活性物质的理化性质,从而影响生物药剂学参数,特别影响活性物质从药物处方或植物提取物中的溶出和进一步吸收。试验结果表明,不同的精制液的物理化学参数有明显的差异,也即芍药甘草汤经过不同的方法精制后,伴生物质发生了明显的改变,那么,这种伴生物质的改变将怎样影响活性物质在体内的吸收以及对活性物质从提取物中溶出有何影响我们正在做进一步研究,试图从复杂的数据中挖掘出物理化学参数和生物药剂学的相关性,尝试从物理化学参数的角度为中药的精制分离方法建立一种合理的评价体系。
[1]郭立玮,潘林梅,朱华旭.中药提取物伴生物质的生物药剂学特性及其制剂学意义[J].中草药,2007,38(8):1281.
[2]中国药典[S].2005:69.
[3]苏德森.物理药剂学[M].北京:化学工业出版社,2004:296.
[4]Rainer H M,Gesine E H著,胡晋红主译.现代给药系统的理论和实践[M].北京:人民军医出版社,2004:78.