超高温陶瓷材料的抗氧化性
2010-02-06刘东亮金永中邓建国
刘东亮 金永中 邓建国
(四川理工学院材料与化学工程系,自贡:643000;材料腐蚀与防护四川省高校重点实验室,自贡:643000)
1 引言
高温材料通常在550℃以上的温度下能承受一定应力并具有抗氧化、抗腐蚀等性能。它包括高温合金、高温陶瓷及抗氧化C/C复合材料。超高温陶瓷(ultrahigh temperature ceramics,UHTCs)是指能在2000℃以上的高温下使用的一类难熔陶瓷材料,主要是ⅣB、ⅤB族过渡金属的硼化物、碳化物及其复合材料。它们的熔点、硬度高,抗热震性好,可作超音速飞机的耐热保护材料、火箭和各种高速飞行器的燃料喷嘴、导弹外壳以及航空发动机和火箭发动机的重要承力结构件。由于这类陶瓷材料可能存在的潜在军事用途,德国和美国都禁止向中国出口[1]。在高温氧化气氛下,属于非氧化物的硼化物,碳化物陶瓷容易被氧化而失效。因而,超高温陶瓷材料的氧化就成为发展航空发动机和超音速飞机的一个瓶颈[2],阻碍了它们向高速、长寿命方向发展。从上世纪六十年代对高温材料的研究以来,提高超高温陶瓷材料的抗氧化性一直是材料研究者们关注的热点。本文结合这些研究工作对超高温陶瓷材料的抗氧化性作了述评。
2 硼化物
2.1 硼化物的结构及氧化
硼化物超高温陶瓷主要有MeB,MeB2,MeB12(Me=Ti、Zr、Hf等过渡金属),其中二硼化物最稳定。Ti、Zr、Hf的二硼化物属于AlB2六方晶体结构,结构编号C32,Pearson符号hP3,空间群P6/mmm,编号191。晶胞中金属原子的分数坐标Me(0,0,0);硼原子分数坐标B(1/3,2/3,1/2)和B(2/3,1/3,1/2)。Me原子占据六棱柱的顶角和底心位置,B原子分别处于Me原子构成的六个三棱柱中心[3]。金属原子层与B原子层交替排列,每个B原子以共价键方式与另外三个最近邻B原子结合,形成的强共价键和金属键赋予二硼化物很高的硬度和高温稳定性,以及良好的导电性和导热性。因此硼化物在保护性气氛下的使用温度可以达到2000℃以上。
在氧化气氛下,硼化物与氧结合生成更稳定的氧化物,其使用性能大大降低。Berkowitz-Mattuck[4]1966年在研究Zr、Hf二硼化物的高温氧化时提出以下反应式:
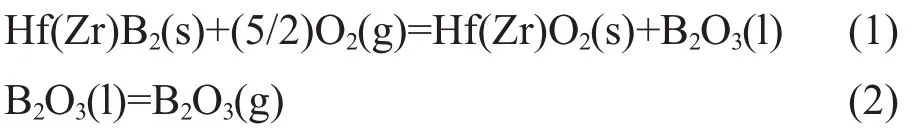
Parthasarathy等[5]针对ZrB2,HfB2和TiB2在1000~1800℃的氧化也提出了一个类似的模型。他们指出在1400℃以下,硼化物的氧化动力学过程符合抛物线规律。金属原子的氧化物构成骨架,而产生的液态氧化硼填充到骨架里、涂敷在硼化物表面。此时,氧化速率受到氧通过液态B2O3进行的扩散所控制。高温阶段,氧空位通过氧化物晶格进行的扩散过程制约着氧化速率。温度越高,B2O3的蒸发速率越大,它作为氧扩散阻碍层的作用降低,硼化物的抗氧化性下降。
其他对ZrB2、HfB2的研究[6-8]也发现在900~1100℃间,硼化物表面有一层致密氧化膜,其主要成分是ZrO2(HfO2)、B2O3,而且还有玻璃相出现。温度升高后留在氧化膜上的玻璃相减少,达到1400℃时,由于玻璃相在多孔ZrO2中的润湿性高、表面张力大使得玻璃相还剩约10%[2]。当温度升高到接近B2O3的沸点(1860℃)时有大量的空隙出现在氧化物层。氧就以这些空隙为通道,进入晶体内部发生进一步的氧化反应。因而大多数硼化物只在较低温度下具有相对好的抗氧化性,如 TiB2、ZrB2在空气中加热到1200~1400℃时没有发生严重的氧化[9]。
按理说ZrO2、HfO2的熔点很高、高温下的挥发少,是很好的抗氧化层。但在低氧分压条件下,ZrO2、HfO2会形成氧空位[10]。这些氧空位为氧进入到表层以下提供了一个通道,使硼化物的氧化继续进行。并且在表面形成的氧化物ZrO2、HfO2是不稳定的,它们会随着温度变化而发生相变,容易从硼化物表层剥落下来。因此ZrO2、HfO2不是抗氧化的理想保护层。几十年来,对硼化物氧化机理的研究,几乎都停留在这一阶段。
2.2 硼化物的抗氧化研究
2.2.1 添加SiC后的抗氧化性
迄今为止,主要是利用合金化方法在硼化物表面原位形成致密保护膜来提高其抗氧化性。因此材料工作者们一直在积极寻找合适的添加元素及其添加量。Cougherty等人[11]在上世纪60年代把SiC引入ZrB2,HfB2中,但最初的目的是细化晶粒、提高强度。由于在高温下形成的硼硅玻璃,其挥发性没有B2O3高,而且与底层氧化物(ZrO2、HfO2)的润湿性较好、粘附性较强,抗氧化性得到提高。至今,掺加硅元素仍是提高硼化物抗氧化性的主要方法,并得到广泛研究。其中SiC的高温性能比较好,成了人们的首选添加物[6,12-15]。
添加SiC后,高温下硼化物表面最外层主要由富含SiO2的玻璃层组成,内部则是氧化物(ZrO2、HfO2)层。而玻璃层能阻止氧的扩散,因此ZrB2在添加20~30%体积比的SiC后,在2000℃仍有较高的抗氧化性[16]。Ni课题组[17]首次在强磁场下注浆成型织构化的ZrB2-SiC材料,在改善显微结构的同时,发现抗氧化性呈现各向异性,且硬度更高。
对HfB2-SiC体系的研究相对较少。但也有实验表明添加SiC后的HfB2在高温下的抗氧化性也比较好[18]。
尽管添加SiC能在一定程度上提高硼化物的高温抗氧化性,但当温度在1200℃以下时,由于SiC的氧化慢,SiO2未能快速形成并进入玻璃相以阻碍氧的扩散。因而纯硼化物与添加了SiC的硼化物相比,氧化速率差别不大[2]。当温度达到1800℃以上,尤其在高温流动环境下,大部分B2O3、SiO2会因蒸发流失[19]而失去保护作用,只有靠氧化物(ZrO2、HfO2)膜作保护层。如前所述,这两种氧化物并不适合做高温抗氧化保护层。
2.2.2 添加其他物质后的抗氧化性
除了SiC以外,MoSi2在1000℃以上也有较好的抗氧化性。Savino[20]把5%体积比的MoSi2加到HfB2中后,发现在1950℃时表面有大约15μm厚的氧化硅玻璃层覆盖着下面的HfO2膜,同样也起到了一定的保护作用。
为了把氧束缚在晶格上以抑制氧化膜中氧的传输,防止氧化膜开裂和剥离以及通过相的稳定来提高氧化物膜的粘附性,可以采用添加高价离子(如Nb5+和Ta5+)的方法。而Nb2O5的熔点只有1460℃,不适合在超高温条件下使用。Ta2O5的熔点可达1880℃。加入的Ta元素可作为ZrO2、HfO2的掺杂相,其氧化物Ta2O5还可参与玻璃相的形成。Wuchina[21]和Talmy[22]等人分别把TaB、TaB2加到HfB2、ZrB2中,在1500℃时氧化膜的密度和抗氧化性都得到了提高。
Talmy等人[23]结合Si、Ta的特性,把Ta5Si3加入到ZrB2里,于1900~2200℃热压烧结。在表面产生的Ta2O5能促进硼硅玻璃的相分离,当Ta2O5的量在8~30%体积百分比时,ZrB2-Ta5Si3的氧化程度很低。加30%体积百分比的Ta5Si3时,抗氧化性最好,而且整个材料的强度、硬度也达到峰值。2008年,他们把Si3N4,Ta5Si3和TaSi2分别添加到ZrB2里在1200~1500℃间进行实验[24]。在1400℃以下,由于形成的硼硅玻璃具有阻碍氧扩散的作用,所以相对于纯ZrB2抗氧化性都得到了提高。在加Si3N4的ZrB2中,抗氧化性随着Si3N4的增多而提高。而且在这组成分中他们还加了CrB2、TaB2。由于Cr、Ta的氧化物能提高液相的温度和黏度,因此降低了氧的扩散,减少了B2O3的挥发。但在1500℃时,他们的实验显示加SiC的抗氧化性却略优于加其他几种物质。
Chen等[25]还把LaB6添加到ZrB2里,通过在表层形成La2O3·B2O3,La2O3·3B2O3和ZrO2氧化层来阻碍氧的扩散,但只在1200℃左右进行了实验。
Zhang等[26]研究了把4mol%WC加到ZrB2中的抗氧化性。在1600℃氧化3小时后,WC与ZrB2形成固溶体,通过液相烧结促进ZrO2膜的致密化,提高了ZrB2的抗氧化性。
2.2.3 多相复合
通过实验研究,发现添加单一物质的方法来提高硼化物的氧化性的效果有限。于是人们采用添加多种物质的方法,并结合易烧结性和显微结构的改善来综合考虑。Monteverde[27]为了改善HfB2在热压烧结时显微结构粗化产生的机械性能降低,把SiC加到HfB2中的同时还加入5.8%体积比的Si3N4作为烧结助剂。由于改善了显微结构,致密度增加,在1400℃以上抗氧化性显著提高。Levine等人[28]把体积比为20%SiC和20%TaSi2加入到ZrB2中于1627℃下进行氧化实验,结果发现其氧化速率比单独加SiC慢得多。Brach等人[29]把体积比为55%的AlN、15%的SiC都加入到ZrB2里,在700~900℃时,ZrB2氧化成ZrO2和B2O3,动力学过程接近抛物线规律,有抗氧化性;在1000~1100℃时,B2O3与Al2O3反应形成硼酸铝和硼硅玻璃;1200~1300℃时,硼酸铝和莫来石在表面结晶。但当温度达到1300℃时,表层破裂,不能起到很好的保护作用。Silvestroni[30]在HfB2-ZrB2和HfB2-HfC中分别加入体积比为20%的MoSi2,于1900~1950℃来改善显微结构,同时抗氧化性得到了提高。
可见,通过合金化法可以在一定程度上改善硼化物的抗氧化性,但实验温度大都离超高温较远。而且添加了其他元素后,还会降低硼化物熔点。
3 碳化物
3.1 碳化物的结构及氧化
过渡金属碳化物ZrC、HfC和TaC的熔点高于相应的硼化物、氧化物,且抗热震稳定性好、无相变,也被当作潜在的超高温材料。其中HfC和TaC的熔点极高,分别达到3890℃和3880℃,并且硬度、弹性模量也很高,因此在超高温陶瓷中受到的关注也较多。这类符合化学计量比的碳化物属于岩盐(NaCl)结构,结构编号B1,Pearson符号cF8,空间群Fm3m、编号225。两种离子各自以面心立方的形式堆积。碳原子填充在金属原子正八面体中心。晶胞中金属原子的分数坐标为Me(0,0,0);碳原子分数坐标为B(1/2,1/2,1/2)。
有关ZrC和HfC的氧化性,Berkowitz-Mattuck[31]在1967年进行了研究。他发现在10个大气压下、1790~2000℃时,HfC的氧化符合线形关系,且主要发生在晶界。Voitovich[32]研究组把ZrC和HfC在500~1200℃空气状态下进行了5小时的氧化实验。根据热力学关系,可能的热力学反应如下:

他们发现反应(3)首先发生,随后表面产生裂纹,氧与游离碳结合生成CO、CO2。Rodriguez等[33-34]用高分辨率光电子实验结合第一性原理研究了同属B1型的TiC与氧的结合情况,也证实了这一点。他们发现O被吸附在(001)面上的CMeMe空心(hollow)位最稳定。O首先取代表面的C原子,在O2充足的情况下,C被氧化成CO、CO2而挥发,进而在表面留下C空位。O可以通过这些空位与表面下的碳化物继续反应。然而在高温氧化时,反应(6)也可能发生。ZrC表面形成的氧化膜在900℃时烧结程度较高且与底层粘附紧密;但HfC表面的氧化膜在整个实验温度范围不论烧结性还是粘附性都不如ZrC。而且中间层HfCxOy中的空位浓度要高于ZrCxOy。因此在1200℃以下,HfC的抗氧化性较ZrC弱。不仅粉末烧结体的氧化如此,Shimada等人[35]研究了单晶HfC(200)面在700~1500℃的氧化也得到了类似的结果。
对于HfC在1400~2100℃的氧化,Bargeron等人[7,8,36]发现表层有三层:外层为多孔HfO2,中间是较致密的含碳氧化物(HfOxCy)层,最里面是残余碳层。其中含碳氧化物层比其他两层能更好地阻碍氧的扩散。在1500℃以下,形成的氧化物达不到烧结状态,易剥落(即“pesting”过程)。而在1800℃以上时,氧化物有一定程度的烧结,抗氧化性相对较好。此外,偏离理想化学计量比对抗氧化性也有影响,如HfC0.67形成的氧化膜比HfC0.98的要薄[16],氧化膜下面的碳化物也少孔、少裂纹、更致密。
对钽的碳化物,Desmaison-Brut等[37]比较了TaC和Ta2C在750℃和850℃的氧化行为。在TaC表层形成的Ta2O5有空隙,不能有效阻止O的扩散,没有形成钽的碳氧化物中间层,Raman光谱也未发现残余碳的存在。而Ta2C氧化后在Ta2C和Ta2O5之间有碳氧化物TaCxOy存在,它和HfCxOy一样能阻止O的扩散。因此Ta2C的抗氧化性要优于TaC。与HfC氧化形成高熔点的HfO2(2758℃)不同的是,TaC氧化形成的是较低熔点的Ta2O5(1872℃)。因此HfC看起来比TaC更适合应用在高温场合。但是在氧分压很低时,TaC表面不会氧化,而HfC上却有HfO2出现[16],此时,TaC比HfC更适合作高温材料。
3.2 碳化物的抗氧化研究
与硼化物在表面形成硼硅玻璃不同,碳化物主要靠在表层与底层之间的金属碳氧化物层来阻止O的扩散以达到抗氧化的目的。这层碳氧化物的烧结性、致密程度等对O的扩散有很大影响。相比而言,硼硅玻璃较金属碳氧化物致密,对O的扩散有更好的抑制作用。这也是迄今为止,掺硅硼化物超高温陶瓷得到广泛研究的原因之一。
受到Hf-Ta合金的抗氧化性比纯Hf高的启示,Courtright等人[38]在HfC中添加质量百分比为25%的TaC后,发现表面氧化物的形成符合抛物线规律,说明有一定的抗氧化性。在2000℃以上有CO的形成并逸出,使得表面氧化物不像Hf-Ta合金表面氧化物那样致密,而是多孔易剥落。他们还研究了添加质量百分比为7%的PrC2后HfC的氧化性。仍然发现形成的氧化物有剥落、产生裂纹。因此添加PrC2、TaC都没有明显提高HfC的高温抗氧化性。
鉴于MoSi2在高温下能在表面形成SiO2保护层,而且能促进烧结[39],有可能提高HfC的抗氧化性,Savino等[20]把5%体积比的MoSi2加到HfC中,发现MoSi2促进了烧结,烧结体密度达到理论密度的98%,而且空隙很少。表层为多层结构,有裂纹,但与底层未反应的HfC结合较牢固。最外层仍是多孔HfO2,未发现有连续的玻璃相。HfC与MoSi2之间有SiOxCy,这可能是在膜内氧分压低,MoSi2与CO作用所致。
此外,Al、Cr在高温下也能氧化成致密且具有保护作用的Al2O3、Cr2O3膜。刘东亮[40]利用第一性原理比较了在HfC中掺Al、Cr的形成能。他发现在HfC中掺Cr的稳定性要优于掺Al。而氧化往往首先发生在表面,且O原子首先置换表面的C原子,进而发生氧化。因此Liu等[41]比较了在HfC(001)面吸附Al、Cr原子的吸附能。结果表明Al、Cr更容易吸附在C原子上,而且Cr原子的吸附能要低于Al原子。因此用Cr吸附在HfC表面后,能阻止氧置换表面的C原子,抗氧化性可以得到提高。但他们未比较HfC(001)面吸附Al、Cr原子前后与O原子的相互作用。而且Al2O3、Cr2O3在超高温下的挥发速率也大[18]。因此Al2O3、Cr2O3膜仍然只能作较低温度下的抗氧化层。
尽管目前已对这类碳化物作了许多抗氧化研究,而且已有用于火箭发动机的HfC部件的报道,但抗氧化性差和难烧结等问题依然存在。这使得HfC、ZrC和TaC等材料还较难得到实际应用[42]。
4 结语
综上所述,几十年来,随着航空、航天技术的发展,超高温陶瓷材料尤其是硼化物的抗氧化性得到了较广泛的研究。硼化物主要是依靠表面形成的非晶膜(如硼硅玻璃)来阻止氧的扩散,温度过高,非晶膜失效;碳化物主要利用碳氧化物层(HfCxOy、ZrCxOy、TaCxOy)来阻止材料的进一步氧化。虽然这些措施能在一定程度上提高超高温陶瓷材料的抗氧化性,但大多数的研究表明这些材料只是在1600℃以下有较好的抗氧化性,离一般认为的超高温(>2000℃)还有较大距离。许多研究的实验环境与航空、航天的实际有较大差别:温度不是很高,很难使氧分子分解成原子氧;周围的气流不像实际中有流动等。而且,氧通过氧化膜的传输机制还不是很明确。因此,有必要从以下几方面来考虑:
(1)利用材料计算方法进行原子氧的研究。这可以克服常规实验中遇到的很难使材料与原子氧接触而产生的氧化,而且还可以利用流体动力学方法模拟材料周围有流体流动时的现象。从这些方面去探索超高温陶瓷材料的氧化机理。
(2)开展超高温陶瓷材料表面的研究。材料的氧化首先是从表面开始。分子氧、原子氧是如何与这些陶瓷材料的表面结合并进行扩散的,进而探索如何阻止超高温陶瓷表面与氧的结合和氧的扩散。
(3)结合烧结问题进行研究,寻找超高温陶瓷材料表面的最佳保护膜。用一种或多种物质进行复合,使形成的保护膜更致密、更稳定,与底层结合更牢。
1傅正义,李建保.先进陶瓷及无机非金属材料.北京:科学出版社,2007
2 Bongiorno A.,Först C.J.,Kalia R.K.,et al.A perspective on modeling materials in extreme environments:oxidation of ultrahigh-temperature ceramics.MRS Bulletin,2006,31: 410~418
3宋贵宏,杜昊,贺春林.硬质与超硬涂层.北京:化学工业出版社,2007
4 Berkowitz-Mattuck J.B.Hi gh-temperature oxidation.IIIZirconium and hafnium diborides. Journal of the Electrochemical Society,1966,113(9):908~914
5 Parthasarathy T.A.,Rapp R.A.,Opeka M.,et al.A model for the oxidation of ZrB2,HfB2and TiB2.Acta Materialia,2007, 55:5999~6010
6 Opeka M.M.,Talmy I.G.and Zaykoski J.A.Oxidation-based materials selection for 2000℃ hypersonic aerosurfaces: Theoretical considerations and historical experience.Journal of Materials Science,2004,39(19):5887~5904
7 Bargeron C.B.,Benson R.,Newman R.,et al.Oxidation mechanisms of hafnium carbide and hafnium diboride in the temperature range 1400℃to 2100℃.Johns Hopkins APL Technical Digiest,1993,14(1):29~36
8 Bargeron C.B.,Bensen R.C,Jette A.N.,et al.Oxidation of Hafnium Carbide in the Temperature Range 1400℃to 2060℃. Journal of the American Ceramic Society,1993,76(4): 1040~1046
9陈昌明,张立同,周万诚等.硼化物陶瓷及其应用.兵器材料科学与工程,1997,20(2):68~71
10 LevineS.R.,Opila E.J.,Robinso n R.C.,et al. Characterization ofan ultra-high temperature ceramic composite.NASA/TM-2004-213085,Washington,DC: NASA,2004
11 Clougherty E.V.,Pober R.L.and Kaufman L.Synthesis of oxidation resistant metal diboride composites.Transaction of the Metallurgic Society of AIME,1968,242:1077~1082
12 Tripp W.C.,Davis H.H.,Graham H.C.Effect of an SiC addition on the oxidation of ZrB2.American Ceramic Society Bulletin,1973,52:612~616
13 Hwang S.S.,Vasiliev A.L.,Padt ure N.P.Improved processing and oxidation-resistance ofZrB2ultra-high temperature ceramics containing SiC nanodispersoids. Materials Science and Engineering A,2007,464;216~224
14杨飞宇,张幸红,韩杰才等.ZrB2-SiC和Csf/ZrB2-SiC超高温陶瓷基复合材料烧蚀机理的研究.无机材料学报,2008,23(4): 734~738
15闫永杰,张辉,黄政仁等.常压烧结ZrB2-SiC复相材料的抗氧化行为研究.无机材料学报2009,24(3):631~635
16 Wuchina E.,Opila E.,Opeka M.,et al.UHTCs:Ultra-high temperatureceramicmaterialsforextreme environment applications.The Electrochemical Society Interface,2007,16 (4):30~36
17 Ni De-Wei,Zhang Guo-Jun,Kan Yan-Mei,et al.Highly textured ZrB2-based ultrahigh temperature ceramics via strong magnetic field alignment.Scripta Materialia,2009,60(8): 615~618
18 Upadhya K.,Yang J.M.and Hoffman W.Advanced materials for ultrahigh temperature structural applications above 2000℃. AFRL-PR-ED-TP-1998-007,Edwards AFB:1998
19 Hu P.,Guolin W.and Wang Z.Oxidation mechanism and resistance of ZrB2-SiC composites.Corrosion Science,2009, 51:2724~2732
20 Savino R.,Fumo M.D.S.,Silvestroni L.,et al.Arc-jet testing on HfB2and HfC-based ultra-high temperature ceramic materials.Journal of the European Ceramic Society,2008,28: 1899~1907
21 Wuchina E.J.and Opeka M.M.The Oxidation of HfC,HfN and HfB2.Electrochemical Society Proceedings,2001,12: 136~43
22 Talmy I.G.,Zaykoski J.A.,Opeka M.M.,et al.Oxidation of ZrB2ceramics with SiC and Group IV-VI transition metal diborides.Electrochemical Society Proceedings,2001,12: 144~58
23 Talmy I.G.,Zaykoski J.A.,Opeka M.M.,et al.Properties of ceramics in the system ZrB2-Ta5Si3.Journal of Materials Research,2006,21(10):2593~2599
24 Talmy I.G.,Zaykoski J.A.,Opeka M.M.High-Temperature Chemistry and Oxidation of ZrB2Ceramics Containing SiC, Si3N4,Ta5Si3and TaSi2.Journal of the American Ceramic Society,2008,91(7):2250~2257
25 Chen C.M.,Zhang L.T.,Zhou W.C.,et al.High temperature oxidation of LaB6-ZrB2eutectic in situ composite.Acta Materialia,1999,47(6):1945~1952
26 Zhang S.C.,Hilmas G.E.,Fahrenholtz W.G.Improved Oxidation Resistance of Zirconium Diboride by Tungsten Carbide Additions.Journal of the American Ceramic Society, 2008,91(11):3530~3535
27 Monteverde F.,Bellosi A.The resistance to oxidation of an HfB2-SiC composite.Journal of the European Ceramic Society,2005,25:1025~1031
28 Levine S.R.and Opila E.J.Tantalum addition to zirconium diboride for improved oxidation resistance. NASA/TM-2003-212483,Washington,D.C.,2003
29 Brach M.,Sciti D.,Balbo A.,et al.Short-term oxidation of a ternary composite in the system AlN-SiC-ZrB2.Journal of the European Ceramic Society,2005,25(10):1771~1780
30 Silvestroni L.,Sciti D.and Bellosi A.Microstructure and properties of pressureless sintered HfB2-based composites with additions of ZrB2or HfC.Advanced Engineering Materials,2007,9(10):915~920
31 Berkowitz-Mattuck J.B.High-temperature oxidation IV zirconium and hafnium carbides.Journal Electrochemical Society,1967,114:1030~1032
32 Voitovich R.F.and Pugach E.A.High-temperature oxidation of ZrC and HfC.Powder Metallurgy and Metal Ceramics, 1973,12:916~921
33 Rodriguez J.A.,Liu P.,Dvorak J.,et al.The interaction of oxygen with TiC (001):Photoemission and first-principles studies.Journal of Chemical Physics,2004,121(1):465~474
34 Rodriguez J.A.,Liu P.,Gomes J.,et al.Interaction of oxygen with ZrC (001)and VC (001):Photoemission and first-principles studies.Physics Review B,2005,72,075427
35 Shimada S.and Yunazar F.Oxidation of hafnium carbide and titanium carbide single crystals with the formation of carbon at high temperatures and low oxygen pressures.Journal of the American Ceramic Society,2000,83(4):751~728
36 Bargeron C.B.and Benson R.C.X-ray microanalysis of a hafnium carbide film oxidized at high temperature.Surface and Coatings Technology,1988,36(1-2):111~115
37 Desmaison-BrutM.,AlexandreN.andDesmaison J. Comparison of the oxidation behaviour of two dense hot isostatically pressed tantalum carbide (TaC and Ta2C) materials.Journal of the European Ceramic Society,1997, 17:1325~1334
38 Courtright E.L.,Prater J.T.,Holcomb G.R.,et al.Oxidation of hafnium carbide and hafnium carbide with additions of tantalum and praseodymium.Oxidation of Metals,1991,36 (5):423~437
39 ScitiD.,SilvestroniL.and BellosiA.High-density pressureless sintered HfC-based composites.Journal of the American Ceramic Society,2006,89(8):2668~2670
40刘东亮.Hf1-xCrxC、Hf1-xAlxC的电子结构及其稳定性.计算机与应用化学,2009,26(5):641~644
41 Liu D.,Deng J.and Jin Y.First-principles analysis of the adsorption of aluminum and chromium atoms on the HfC (001)surface.Computational Materials Science,2009,doi:10. 1016/j.commatsci.2009.09.005
42刘军,熊翔,王建营等.耐超高温材料研究.宇航材料工艺, 2005,(1):6~9
