工业盐水中总氮量的检测
2010-01-16刘忠琼
黄 彬,刘忠琼,蒲 敏
(宜宾天原集团股份有限公司,四川 宜宾 644004)
工业盐水中总氮量的检测
黄 彬,刘忠琼,蒲 敏
(宜宾天原集团股份有限公司,四川 宜宾 644004)
介绍了用过硫酸钾使有机氮和无机氮氧化为硝酸盐后,以紫外分光光度法测盐水总氮量的方法。加入标准样品浓度为0.7 mg/L以上时的回收率为98.6%~107.5%;相对标准偏差为3.52%;10 mL样品最低定量限为0.1 mg/L。该方法操作较简便,耗时较少,标准曲线线性好、准确度、精密度能满足分析检测要求。
工业盐水;总氮;硝酸盐氮;过硫酸钾;紫外分光光度法
氯碱生产系统运行过程中产生的三氯化氮,是一种极易爆炸的物质。三氯化氮主要是氨、铵盐及含铵化合物进入生产系统,在盐水电解过程的酸性条件下与氯气或次氯酸反应生成的。阻止铵化合物进入电解槽是防止三氯化氮危害的治本之法,准确测定盐水中总氮量,对消除盐水中含氮物质非常重要。现在许多企业都通过采用凯氏定氮法检测工业盐水中总氮的方式,了解工业盐水中氮化合物含量。凯氏定氮法无法测出系统中硝酸盐氮及亚硝酸盐氮等,操作繁琐,1套装置一次消化与蒸馏只能处理1个样品,测试1个样品约3 h,检测时间长,影响样品检测准确度的因素较多,对操作要求严格,平行效果较差。采用本方法,一次可消化数十个样品;消化后,只需加酸就可测试;可测试系统中氨、无机铵盐、硝酸盐氮、亚硝酸盐氮及大部分有机含氮化合物中氮的总和;具有操作简单、耗时少、准确度高等特点,特别在批量较多时更有优势。
1 实验部分[1]
1.1 原理
过硫酸钾在60℃以上水溶液中,可分解产生硫酸氢钾和原子态氧,硫酸氢钾在溶液中离解而产生氢离子,故在氢氧化钠的碱性介质中可促使分解过程趋于完全。分解出的原子态氧在120~124℃条件下,可使样品中含氮化合物的氮元素转化为硝酸盐。溶解的有机物在220 nm处也会有吸收,而硝酸根离子在275 nm处没有吸收,可用紫外分光光度法于波长220 nm和275 nm处,分别测出吸光度A220及A275,按式(1)求出校正吸光度 A。

按扣除空白后的吸光度值查校准曲线并计算总氮含量。
1.2 仪器和设备
(1)紫外分光光度计及10 mm石英比色皿;(2)医用手提式蒸汽灭菌器或家用压力锅(压力为0.11~0.14 MPa),锅内温度保持 120~124 ℃;(3)具玻璃磨口塞比色管,25 mL;(4)实验室专用移液器,1 mL;(5)滴定管,10 mL;(6)烘箱;(7)分析天平,分度值为0.1 mg;(8)电炉;(9)其他实验室常用仪器。
1.3 试剂
(1)氢氧化钠溶液,质量浓度为 200 g/L,称取20 g氢氧化钠,溶于纯水中,稀释至100 mL。
(2)氢氧化钠溶液,质量浓度为 20 g/L(将(1)溶液稀释10倍而得)。
(3)碱性过硫酸钾溶液,称取40 g过硫酸钾,溶于纯水中,另称取15 g氢氧化钠,溶于纯水中,待氢氧化钠溶液冷却至室温后,两者混合并稀释至1 000 mL,溶液存放在密闭良好的聚乙烯瓶内,于冷暗处避光保存,最长可贮存一周。
a.过硫酸钾试剂提纯方法
分析纯的过硫酸钾试剂在低于60℃的水浴下溶解于纯水中,将清澈的溶液冷却至接近0℃,抽滤。将已重结晶的过硫酸钾置于放有浓硫酸的干燥器中干燥,经过2次以上重结晶后方能达到要求。
b.碱性过硫酸钾的配制注意事项
过硫酸钾在超过60℃时,会分解失效。配制该溶液时,可分别称取过硫酸钾和氢氧化钠,分开配制,待氢氧化钠溶液冷却到室温后,再混合定容。或先配制氢氧化钠溶液,待其温度降到室温后再加入过硫酸钾溶解。
(4)盐酸溶液(1+9)。
(5)硝酸钾标准储备液,CN=100 mg/L,硝酸钾在105~110℃烘箱中干燥至恒重,在干燥器中冷却后,称取0.721 8 g,溶于纯水中,移至1 000 mL容量瓶中,用纯水稀释至标线,在0~10℃暗处保存;
(6)硝酸钾标准使用液,CN=10 mg/L(将储备液(5)用纯水稀释10倍而得,使用时配制)。
(7)硫酸溶液(1+35)。
1.4 检测方法
1.4.1 检测样品步骤
(1)用具塞玻璃瓶或聚乙烯瓶采集样品后,盖严瓶塞,以防周围空气中氨和含氮化合物的污染。所用玻璃器皿用盐酸(1+9)或硫酸(1+35)浸泡,清洗后再用纯水冲洗数次。
(2)用移液器吸取1.00 mL盐水样,置于比色管中,用无氨水稀释至10 mL。
(3)加入5 mL碱性过硫酸钾溶液(3),塞紧磨口塞用布及绳等扎紧瓶塞,以防弹出。
(4)将比色管置于医用手提蒸汽灭菌器中,加热,使压力表指针到 0.11~0.14 MPa,此时温度达120~124℃,开始计时。或将比色管置于家用压力锅中,加热至顶压阀吹气时开始计时,保持此温度加热1 h。
(5)冷却,开阀放气,移去外盖,取出比色管并冷至室温。
(6)加盐酸(1+9)1 mL,用无氨水稀释至 25 mL标线,混匀。
(7)移取部分溶液至10 mm石英比色皿中,在紫外分光光度计上,以无氨水作参比,分别在波长为220 nm与275 nm处测定吸光度。
(8)空白试验除以10 mL纯水代替试料外,采用与测定完全相同的试剂、用量和分析步骤进行操作。
1.4.2 制作标准曲线
(1)制备校准系列。用吸量管向一组比色管中,分别加入硝酸钾标准使用液 0.0,0.10,0.30,0.50,0.70,1.00,3.00,5.00,7.00,10.00 mL。 加 纯 水 稀 释 至10.00 mL。按检测样品步骤(2)~(7)进行操作。
(2)绘制校准曲线。 分别按式(2)~(4)求出除零浓度(空白)溶液外其他校准系列的校正吸光度AS和零浓度的校正吸光度Ab及其差值Ar。

式中:AS220—标准溶液在220 nm波长的吸光度;
As275—标准溶液在275 nm波长的吸光度;
Ab220—零浓度(空白)溶液在220 nm波长的吸光度;
Ab275—零浓度(空白)溶液在275 nm波长的吸光度。
按Ar值与相应的NO3-N含量(mg)绘制校准曲线。
1.5 计算
按式(5)~(7)计算得试样校正吸光度 AX。

式中:A220—样品溶液在220 nm波长的吸光度;
A275—样品溶液在275 nm波长的吸光度。
用Ax在校准曲线上查出相应的总氮量(mg),按式(8)计算样品中总氮含量(mg/L) 。

式中:m—试样测出含氮量,mg;
V—测定用试样体积,L。
2 结果与讨论
2.1 样品检测谱图分析
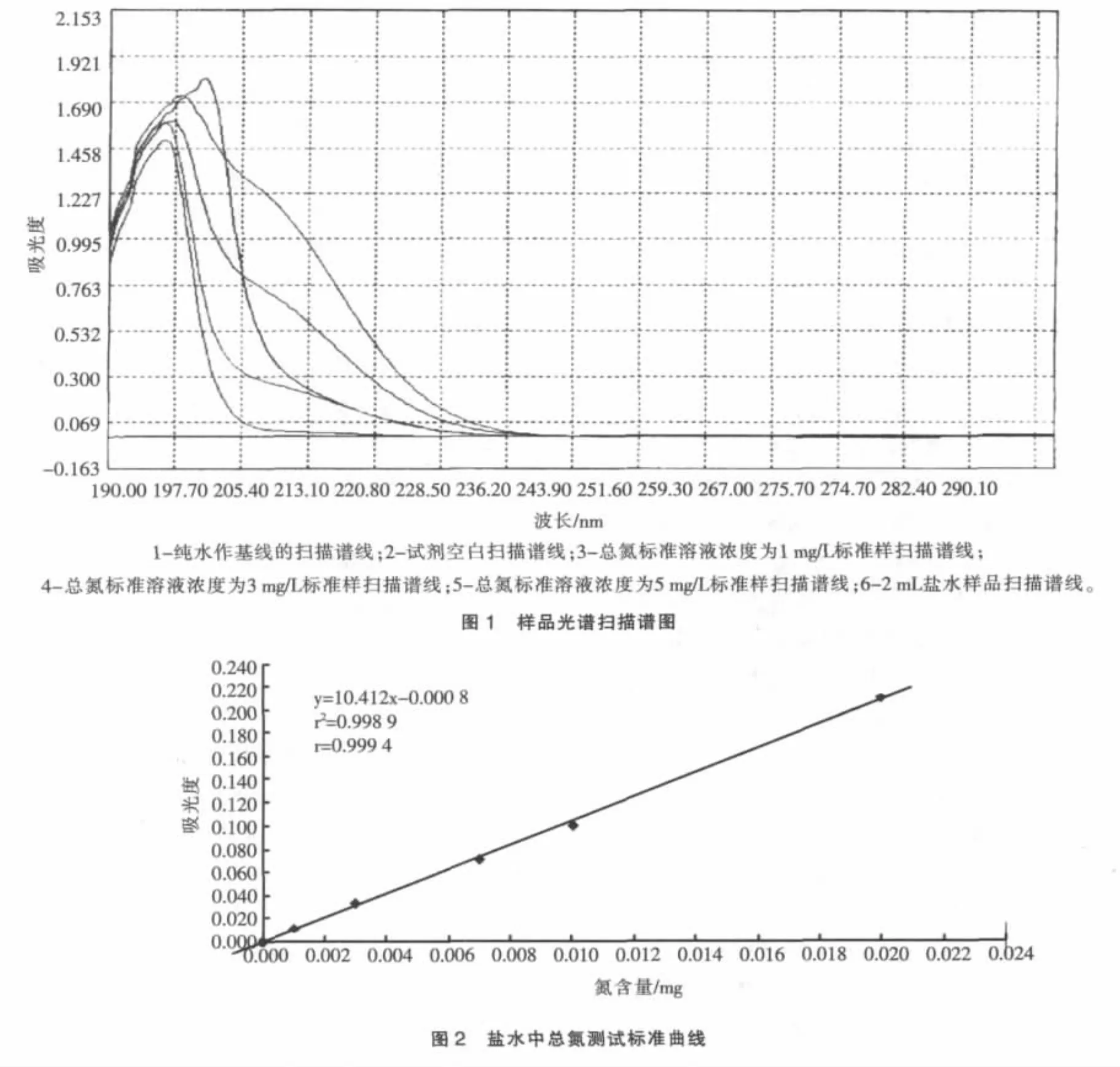
扫描谱图见图1。
从图1中可观察到,在220 nm处试剂空白不干扰检测,盐水样品在此处也无干扰峰,且吸光度随硝酸盐浓度增加而增加。
2.2 标准曲线线性
标准曲线按总氮含量高低分成两段分别制作曲线。表1、表2为制作标准曲线的测试数据。
对应表1的曲线图见图2。
对应表2的曲线图见图3。
2.3 干扰物离子影响情况实验
当盐水中常含的碘离子及溴离子达到一定浓度时,对检测有干扰。宜宾天原集团股份有限公司盐水中Br-质量浓度低于30 mg/L,I-质量浓度低于20 mg/L。将硝酸钾、氯化铵标液加入含Br-和I-的溶液中,使溶液中 Br-质量浓度为 30 mg/L,I-质量浓度为20 mg/L,氮标准物质含量浓度为0.005 mg,如参与测试样品体积为1~10 mL,则样品中氮质量浓度为5.0~0.5 mg/L,此时,测定加标回收率为80%~90%。当使氮标准浓度为0.01 mg,参与测试样品体积为1~10 mL,则样品中氮质量浓度为10~1 mg/L,测定加标回收率为97%~105%。表明在样品中氮质量浓度高于1 mg/L时,碘离子及溴离子对检测的干扰很小,可不考虑。
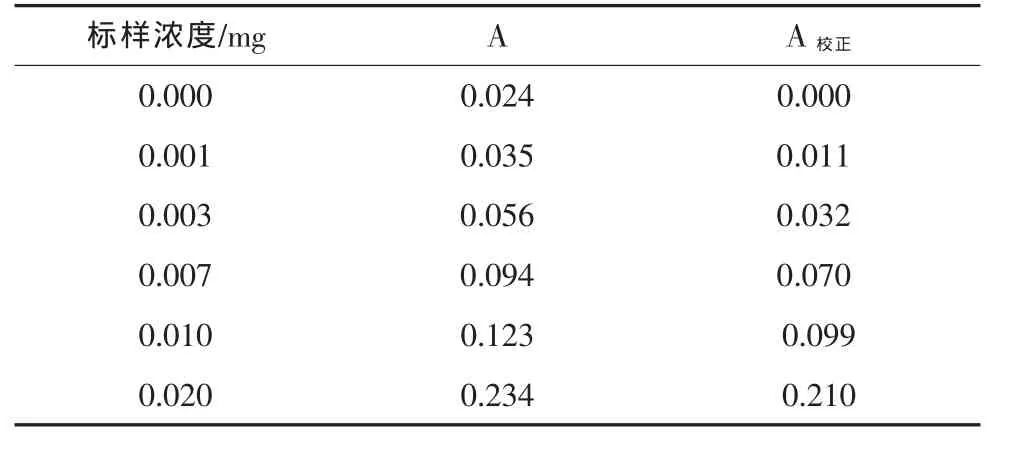
表1 标准曲线的测试数据(1)
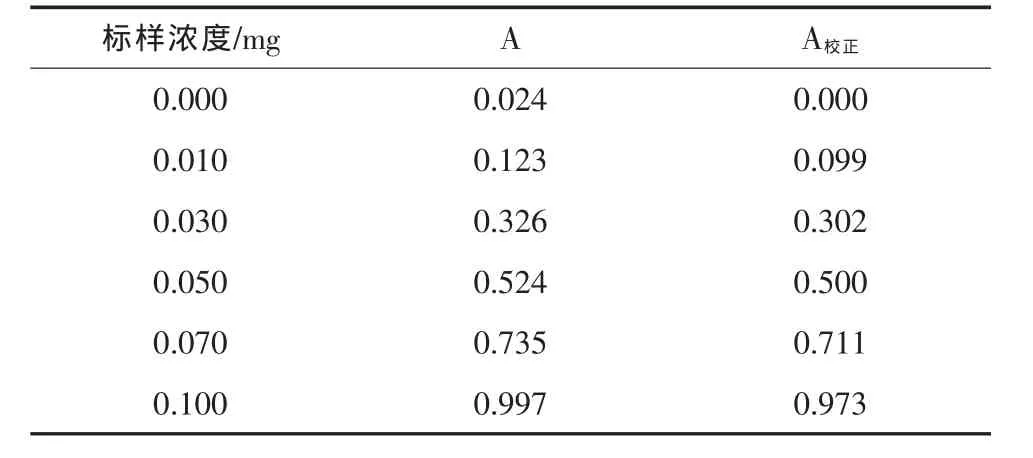
表2 标准曲线的测试数据(2)

2.4 过硫酸钾试剂提纯实验
在实验过程中,发现过硫酸钾试剂无论是分析纯还是优级纯,试剂空白吸光度值均高,分析纯试剂空白吸光度为1.4以上,优级纯试剂空白吸光度为0.569~0.801,严重干扰样品检测,无法测试低氮含量样品。
将优级纯过硫酸钾试剂重结晶提纯后,试剂空白吸光度值低于0.025,甚至可达0.007,采用重结晶提纯后的过硫酸钾试剂进行检测情况较好。
2.5 方法精密度实验
在25 mL比色管中加入 1 mL CN=10 mg/L的硝酸钾标准溶液,稀释至10 mL,然后进行消化处理,按测标准样品操作步骤进行。不同日期,不同人测8个样品,扣除试剂空白吸光度后,计算相对标准偏差。
2.6 方法的准确度实验
向1 mL盐水中加入不同量硝酸钾标样,稀释制成10 mL试液,测试加标回收率如表4所示。
从表4中可看出低含量范围(0.007 mg以下)的加标回收率稍差,这时加入标样浓度在0.7 mg/L以下,当加入标样浓度在0.7 mg/L以上时,加标回收率较好。氮含量在0.7 mg/L以下时盐水安全性好,对于测试准确度可稍放宽。
2.7 定量检测限
根据制作标准曲线线性范围,取曲线上最低点氮含量,当取10 mL样品时,样品中氮含量最低定量限为 0.1 mg/L。

表3 精密度实验结果

表4 加标回收率
2.8 水合肼在测试中的表现
用80%水合肼进行检测,通过计算样品中实际氮含量,与检测结果比较得知水合肼样品中的水合联氨不参与反应。向水合肼试样中加入硝酸钾标样,测试加标回收率得知加入标样含量较高时(氮含量≥0.01 mg),回收率为98%~102%,即使加入标样含量低(氮含量为0.005 mg),回收率也有97%~121%。说明水合肼不干扰检测。
3 结语
凯氏氮法操作繁琐,影响样品检测准确度的因素较多,如环境空气中氮、试剂中氮、蒸馏装置气密性、蒸馏速度、氨的馏出率、器皿洗涤及保存方式,操作要求严格,平行效果较差。本方法操作较简单,耗时较少,且精密度、准确度、检测限都较好,可测定亚硝酸盐氮、硝酸盐氨、无机铵盐、溶解态氨及大部分有机含氮化合物中氮的总和,但对规定的测定条件下不能完全转化为硝酸盐的有机物不能检测。对于氯碱系统进槽盐水中氮含量检测可考虑采用本法。该方法也可用来测试固体盐中总氮含量,测试方法相同,只是取样时要称量。
[1]刘 珍,黄沛成,于世林,周心如.化验员读本.第三版.北京:化学工业出版社,1998.
[2]国家环境保护局、《水和废水监测分析方法》编委会.水和废水监测分析方法.第3版.北京:中国环境科学出版社出版,1989.
Detection of total ammonia contents in industrial brine
HUANG Bin,LIU Zhong-qiong,PU Min
(Yibin Tianyuan Co.,Ltd.,Yibin 644004,China)
After oxidizing organic nitrogenous and inorganic nitrogenous to nitrate by potassium sulfate,the detection method of total ammonia in brine by ultraviolet-visible spectrophotometry was introduced.The recycle rate are 98.6%~107.5%when the concentration of standards samples was over 0.7 mg/L.the relative standards deviation was 3.52%.The lowest quantitation limit of 10 mL was 0.1 mg/L.The operation of method was simple,and took short time.The requirements of anslysi and detection were met with better standard curve linearity,accuracy and precision.
industrial brine;total ammonia;nitrate nitrogen;potassium persulfate;ultraviolet-visible spectrophotometry
TQ075+.3
B
1009-1785(2010)04-0034-04
2009-12-10
