人胰腺癌细胞株PANC1裸鼠原位模型的建立及磁共振监测
2009-11-27何伟王冬青孙维斌苏兆亮王铮超许云飞
何伟 王冬青 孙维斌 苏兆亮 王铮超 许云飞
·论著·
人胰腺癌细胞株PANC1裸鼠原位模型的建立及磁共振监测
何伟 王冬青 孙维斌 苏兆亮 王铮超 许云飞
目的建立一种稳定的人胰腺癌裸小鼠原位移植瘤模型,并探讨无创的磁共振(MRI)对其监测的应用价值。方法人胰腺癌细胞株PANC1体外常规传代后建立裸鼠皮下种植瘤模型,将皮下种植瘤制成细胞悬液,植入20只BALB/C-nu裸鼠的胰腺包膜下构建人胰腺癌原位移植模型;通过MRI检查监测模型的成瘤率、成瘤时间、肿瘤生长速度、肿瘤形态、信号变化等特征,于第7周末取肿瘤组织行病理学检查。结果接种后15 d,7只(35%)荷瘤鼠在MRI上显示成瘤,至接种后27 d,成瘤率为100%。肿瘤信号与邻近组织相比,90%(18/20)病灶T1WI呈均匀稍低信号,10%(2/20)呈等信号;75%(15/20)在T2WI呈均匀高信号。移植后2、3、4、5、6、7周经MRI测量的移植瘤体积分别为(12.6±2.4)mm3、(94.3±11.2)mm3、(175.9±82.5)mm3、(395.8±126.6)mm3、(1290.2±167.2)mm3、(1583.4±87.4)mm3。病理学检查确诊为胰腺低分化腺癌,并保持原发瘤的生物学特征。结论人胰腺癌细胞株PANC1移植瘤制成的细胞悬液种植裸小鼠胰腺包膜下制备胰腺癌模型符合人胰腺癌的特征,且易于无创监测,为临床研究提供了一个有效、稳定的体内实验体系。
胰腺肿瘤; 磁共振成像; 小鼠,裸; 肿瘤细胞系
早期发现并手术切除肿瘤是提高生存率的关键[1-3],但临床上很难完整观察及研究胰腺癌的发生发展过程。本实验在裸鼠胰腺包膜下注入人胰腺癌细胞株PANC1悬液,旨在建立人胰腺癌裸小鼠胰腺原位移植瘤模型,为胰腺癌的临床研究提供一个易于复制及便于监测的肿瘤体内实验系统。
材料和方法
一、细胞培养与裸鼠皮下瘤模型的建立
人胰腺癌细胞株PANC1购自中国科学院上海生物科学研究所,体外常规传代。BALB/C-nu裸小鼠25只,购自扬州大学农学院动物实验中心,雌性,4~6周龄,体重16~20 g,SPF级分笼饲养。其中5只裸鼠右肩部皮下种植PANC1细胞悬液建立皮下种植瘤模型。取一只肿瘤生长较快的荷瘤鼠,在无菌条件下摘取皮下种植瘤研磨制成1×108/ml的细胞悬液。取50 μl细胞悬液注入胰尾下,在超净台内20只裸鼠的胰腺包膜下。共移植。严格无菌。术后自由进食饮水。
术后每日记录裸鼠的一般状况、手术并发症,称体重,肉眼观察并触诊肿瘤的生长状况。
二、磁共振动态检查
应用Siemens Magnetom Trio Tim 3.0T超导磁共振成像仪,使用临床型乳腺线圈,对所有裸鼠术前行常规磁共振(MRI)检查,术后第3天行MRI TSE序列T1WI、T2WI横断面、冠状面及矢状面扫描,扫描参数见表1。增强扫描采用TSE-T1WI-FS序列,此后每隔3 d复查一次,直至第7周处死裸鼠。由三位影像科医师分别观察并记录肿瘤的部位、大小、形态、肿瘤信号及浸润、转移等。在T2WI测量肿瘤的最大长径(L)、宽径(W)和高径(H),按下列公式计算肿瘤体积V(mm3)。V=(4/3×π×L×W×H)×1/8[3]。
三、裸鼠原位瘤模型的病理学诊断
收集肿瘤原发灶及所有可能发生侵袭、转移的脏器,用10%中性福尔马林固定,常规石蜡包埋,以4 μm厚度连续切片,行HE染色,常规光镜检查。
结 果
一、原位移植后荷瘤鼠瘤体生长状况
20只荷瘤鼠在2周内进食、进水正常;3周后出现纳差,活动力减弱;5周后逐渐出现消瘦、皮肤干燥、恶病质等生物学特性。接种后27 d 2只荷瘤鼠意外死亡。接种后第3天,处死2只荷瘤鼠观察移植瘤的生长。移植后荷瘤鼠1、2、3、4、5、6、7周的平均体重分别为19.7、20.1、20.0、19.2、18.9、18.5、17.6 g。
二、荷瘤鼠的MRI扫描所见
制模后第3天, MRI均显示阴性结果。至15 d,7只(35%)荷瘤鼠的MRI显示左肾前上方异常信号,病灶呈不规则形,境界清晰,最小瘤灶约2 mm×3 mm×4 mm。与周围组织相比,T1WI呈不均匀稍低信号,T2WI呈均匀高信号(图1A),处死的2只荷瘤鼠的胰尾处形成不规则白色结节,质地较硬,无转移灶。移植后27 d,MRI均显示胰腺肿瘤,接种成功率为100%。肿瘤信号与邻近组织相比,90%(18/20)T1WI呈均匀稍低信号,10%(2/20)呈等信号;75%(15/20)在T2WI呈均匀高信号,10%(2/20)以高信号为主,15%(3/20)呈等低信号;增强扫描瘤灶边缘强化,中央不强化或轻度不均匀强化(图1B、C)。移植后2、3、4、5、6、7周的瘤体积分别为(12.6±2.4) mm3、(94.3±11.2) mm3、(175.9±82.5) mm3、(395.8±126.6) mm3、(1290.2±167.2) mm3、(1583.4 ±87.4) mm3,中后期生长较快。
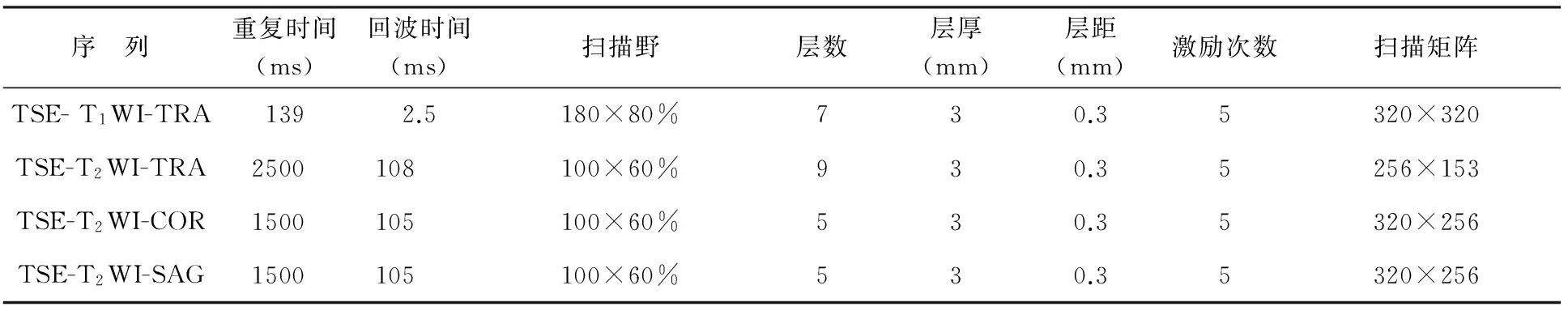
表1 荷瘤裸鼠MRI平扫序列和参数

图1同一动物模型在癌细胞移植后15(A)、27 d(B)的MRI平扫和27 d增强扫描(C)的表现
三、荷瘤鼠的病理学检查
术后27 d死亡的荷瘤鼠的胰腺肿瘤呈类圆形、分叶状或结节状,质较硬,表面血管分布较少,瘤灶与周围组织粘连,中心部位出现点状坏死腔(图2A)。术后7周荷瘤鼠的肿瘤体积明显增大,邻近器官有转移及浸润,未见明显腹水。其中2只腹膜上有多个白色小结节形成,直径在2~5 mm。
镜下见肿瘤细胞排列成实性巢片状结节,无腺腔,周围可见正常胰腺细胞。后期瘤灶肿瘤细胞层数少,中央可见大片状坏死;肿瘤细胞形态不一,呈多边形或柱形,边界清楚,胞质淡染,胞核大而圆,染色深,异型性明显,可见巨核、双核,甚至奇异形核及病理性核分裂像,符合胰腺低分化腺癌(图2B)。

图2原位移植瘤大体表现(A)及病理变化(B,HE ×200)
讨 论
评价一种模型主要根据它对人类疾病的生物学特征的复制程度[4]。人胰腺癌细胞株PANC1为恶性低分化腺癌,通过裸鼠皮下移植型、脾内注射和原位移植为常用的动物模型[5]。皮下接种简单易行,但移植瘤的生物学特性常同原发灶不同,如移植瘤常有包膜、呈局限性生长、很少发生局部或远处器官的转移等,且由于受到位置的影响, 可能会产生药物疗效的假阳性结果。脾内注射胰腺癌细胞所致的动物模型本质上并非原位,而是异地发育或旁路侵袭,以上两种模型均未能如实反映人胰腺癌形态及生物学特性。原位移植是将体外培养的胰腺癌细胞或者外科手术中采集的胰腺癌组织移植到裸鼠的胰腺部位,能最大程度地表现和肿瘤转移能力密切相关的细胞特性。异种原位移植最常用的途径有瘤细胞悬液原位注射以及外科原位种植技术(SOI技术),即采用直接来自新鲜外科标本或移植的人肿瘤组织, 通过原位种植于裸鼠体内建立肿瘤模型,SOI技术在胃、肝脏及肺的原位肿瘤模型建立中应用较多[6],但由于其对外科技术要求高,在胰腺包膜下嵌插组织块难度大,极易造成胰腺组织穿透、出血、胰漏以及组织块脱落,引起严重的手术并发症,造成裸鼠死亡或其它部位的种植。我们曾尝试使用原位种植方法建立模型,因组织块脱落,导致实验失败。后改用细胞悬液移植于裸鼠胰腺包膜下,在肿瘤细胞植入后15 d即可通过MRI无创监测到肿瘤的形成,至第27天MRI显示成瘤率为100%,与Zervox等[7]研究基本一致。移植后7周肿瘤的病理分析显示肿瘤细胞的形态、恶性生物学行为以及影像学表现均符合典型的人胰腺癌特征。同时,本实验还尝试在现有条件下使用高场强磁共振及临床型线圈对肿瘤的生长进行无创监测[8],是一种敏感、可靠的检测手段。本实验方法为更深入地研究胰腺癌发病机制、寻求新的治疗手段、筛选新型抗肿瘤药物等体内实验研究提供了较理想的荷瘤裸鼠模型与观察方法。
[1] 李晓兵.早期胰腺癌的CT和MRI诊断.国外医学·临床放射学分册,2002,25:97 -100.
[2] Peterson DL,Sheridan PJ,Brown WE Jr.Animal models for brain tumors:historical perspectives and future directions.J Neurosurg,1994,80:865-876.
[3] 王冬青,曾蒙苏,靳大勇,等.2D和3D MRI结合技术胰腺癌诊断中的应用.中华肿瘤杂志.2007,29:216-220.
[4] 吴深宝,周国雄,黄介飞,等.实验性胰腺癌动物模型研究进展,胰腺病学,2005,5:187-189.
[5] 王虹,彭卫斌,许云飞,等.人胰腺癌裸鼠模型3,0 T MRI早期表现.临床放射学杂志.2008,27:957-960.
[6] Teresa Troiani,Clorinda Schettino,Erika Martinelli,et al.The use of xenograft models for the selection of cancer treatments with the EGFR as an example.Criti Rev Onco Hematolo,2008,65:200-211.
[7] Zervox EE,Franz MG, Salhab KF,et al.Matrix metalloproteinase inhibition improves survival in an orthotopic model of human pancreatic cancer.J Gastrointest Srug,2000, 4:614-619.
[8] 王虹,彭卫斌,许云飞,等.裸鼠3.0 T MRI线圈选择的实验研究,中华放射学杂志,2008,42:1210-1212.
2009-02-12)
(本文编辑:屠振兴)
EstablishmentandmagneticresonanceimagingmonitoringoftheorthotopictransplantationnudemousemodelwithhumanpancreaticcancercelllinePANC1
HE Wei, WANG Dong-qing, SUN Wei-bin, SU Zhao-liang, WANG Zheng-chao, XU Yun-fei.
Department of Radiology, Affiliated Hospital, Medical School, Jiangsu University, Zhenjiang 212001, China
WANGDong-qing,Emailwangdongqing71@hotmail.com
ObjectiveTo establish a stable orthotopic transplantation nude mouse model of the human pancreatic cancer and to explore the role of monitoring tumor growth with noninvasive MRI.MethodsThe tumors cells suspension made by the subcutaneous injection of human pancreatic cancer cell lines PANC1 were used as the source of tissue for orthotopic implantation of tissue,and transplanted into the pancreas of 20 BALB/C- nu nude mice. After implantation, the successful rate, tumor formation time, tumor growth speed, tumor shape and the change of signal of the tumor were monitored and recorded noninvasively by MRI. At the end of the 7th week, all the specimens were examined by pathological methods.ResultsThirty-five percent (7/20) mice with implantation of primary human PANC1 adenocarcinoma cells were detected to have orthotopic implanted tumors by MRI after 15 days, and all the 20 nude mice developed pancreatic tumor within 27 days after operations, and the successful rate was 100%. Compared with adjacent normal tissue, the T1WI imaging of 90% (18/20) of all the tumors showed uniformly hypo-intense signal, 10%(2/20) showed iso-intense signal, the T2W 75% (15/20) showed uniformly hyper-intense signal. The tumor size 2, 3, 4, 5, 6, 7 weeks after implantation was (912.6±2.4)mm3, (94.3±11.2)mm3, (175.9±82.5)mm3, (395.8±126.6)mm3, (1290.2±167.2)mm3, (1583.4±87.4)mm3, respectively. Pathologic examination confirmed poorly differentiated pancreatic adenocarcinoma and it remained the primary tumor′s biologic features.ConclusionsThe orthotopic transplantation nude mouse model was in accordance with the feature of human pancreatic cancer and was easy for noninvasive monitoring, which provided an effective and stable in vivo experimental system.
Pancreatic neoplasm; Magnetic resonance imaging; Mice, nude; Tumor cell line
10.3760/cma.j.issn.1674-1935.2009.05.013
江苏省自然科学基金(BK2006080)
212001 镇江,江苏大学附属医院影像科 江苏大学临床医学院影像系
王冬青,Email:wangdongqing71@hotmail.com
