SS熊胆眼药水刺激性研究
2009-04-29刘天强肖丹何健董自亮
刘天强 肖 丹 何 健 董自亮
摘 要:目的:构建滴眼液刺激性体外评价方法,筛查SS熊胆眼药水刺激性原因并采取适宜方法解决。方法:采用兔角膜上皮细胞毒性试验(SIRC-MTT)对4种熊胆滴眼液进行评价,将结果与临床刺激性评分进行相关性分析,运用SIRC-MTT筛查SS熊胆眼药水的刺激性原因并进行解决。结果:相关系数为0.961,说明SIRC-MTT能较好评价熊胆滴眼液眼刺激性;造成熊胆眼药水刺激性较强的原因为羟苯乙酯与熊胆原液的共存;采用减少羟苯乙酯用量(调整至0.04%)、添加羧甲基纤维素钠(0.2%~0.25%)均能增加角膜上皮细胞存活率。结论:SIRC-MTT是SS有效的体外刺激性评价方法;降低羟苯乙酯用量和添加羧甲基纤维素钠均能降低熊胆眼药水的刺激性。
关键词:刺激性;熊胆眼药水;细胞毒性试验;角膜上皮细胞
中图分类号:R988.1文献标识码:A文章编号:1673-2197(2009)06-0022-04
SS熊胆眼药水由熊胆单味中药研制而成,具有清热解毒,祛翳明目的功效,主要用于治疗急、慢性卡他性结膜炎,但大多患者在使用中发现该药具有较强刺激性,严重影响了其临床用药。现今评价眼刺激性的方法为兔眼刺激法(draize test),该法具有主观性强,实验差异大等缺点[1],难以寻找出SS熊胆眼药水刺激性较强的内在原因。该研究拟建立SS新的体外刺激性评价方法,用于筛查该眼药水的刺激性原因,并解决该问题。
1 材料与方法
1.1 受试物、仪器与试剂
SS熊胆眼药水(成都某药业公司提供),熊胆粉滴眼液(某药业公司),熊胆黄芩滴眼液(黑龙江黑宝药业),复方熊胆滴眼液(长春普华药业),熊胆、羟苯乙酯、羧甲基纤维素钠(成都某药业公司提供),氯化钠、硼酸、硼砂(科龙试剂有限公司),透明质酸钠(Solarbio);二氧化碳培养箱(Thermo),超净工作台(苏州净化),倒置显微镜(奥林巴斯),自动酶标仪(BIO-RAD),DMEM低糖(GIBCO,USA),胎牛血清(甘肃民海),MTT(SIGMA,USA),F12(GIBCO,USA),青霉素(石家庄制药有限公司),链霉素(华北制药股份有限公司),L-谷氨酰胺 DMSO(SIGMA,USA)。培养基组成(20%胎牛血清, F12培养基∶DMEM低糖=3∶1,2mM/100mL谷氨酰胺,100U/mL双抗溶液)。
1.2 动物
健康白种家兔,雌雄不限,体重2500±200g,成都中医药大学动物实验中心提供。
1.3 兔角膜上皮细胞的培养[2,3]
健康白种家兔,断头放血处死后,无菌条件下摘取眼球,104U•L-1青链霉素溶液漂洗2次,,取角膜缘部上皮组织:沿角巩膜缘灰白交界后1mm处穿刺,取下包括1mm巩膜缘的眼前段组织,解剖镜下去除晶状体、虹膜等附属组织,将得到的角膜组织逐个撕取角膜内皮及后弹力层,然后沿透明角膜内1mm,环状取下2~2.5mm宽的角膜缘组织,剪成1mm×1mm×1mm大小;将组织块平铺于培养瓶中,置37℃、5%CO2恒温培养箱中培养,3d首次换液,以后隔日换液。原代培养至80%融合后,0.25%胰酶消化传代, 3d后首次换液,以后隔日换液,直至细胞融合。传代细胞(2-4代)用于实验研究。将实验用细胞以104个/孔细胞接种于96培养板中,培养(37℃、5%CO2)5d,细胞达到铺平状态。
1.4 评价方法的建立
1.4.1 市售滴眼液刺激性评价
对市售4种熊胆滴眼液临床用药状况进行分析,其刺激性评价结果见表1。
1.4.2 体外刺激性评价方法
(1)直接接触法[4]。 将培养液吸出,加入不同滴眼液溶液100μL作用20min,吸出滴眼液,PBS冲洗两次,加入含10%胎牛血清培养基180μL,20μLMTT(5mg/mL),37℃孵育4h,吸出培养基,加入150μLDMSO,570nm酶标仪测定吸光度。
(2)混合培养法[5]。将培养液吸出,加入含40μL的滴眼液样品的培养基继续培养24h,然后吸出含样品溶液的培养基,其它同直接接触法。

对照组采用PBS溶液,细胞存活率作为评价指标。细胞存活率(cell survival rates)=活细胞数/(活细胞数+死细胞数)×100%=(实验组吸光度值-空白对照组吸光度值)/(对照组吸光度值-空白对照组吸光度值)×100%。各浓度样品设6个复孔进行试验。
将由直接接触法与混合培养法评价滴眼液对兔角膜上皮细胞毒性的实验结果与临床刺激性评分进行相关性研究,选择相关性较好的方法作为本研究评价细胞毒性的方法。
1.5 刺激源筛查
熊胆眼药水刺激性源可能来自处方中不同物质之间的相互作用,也可能来自制备工艺各环节。本研究从这两个方面进行刺激源的筛查。
1.5.1处方考察
处方:熊胆粉5.0g、硼酸12.0g、硼砂0.6g、氯化钠2.2g、羟苯乙酯0.8g 按照处方,根据表2配制相应熊胆眼药水样品,采用优选的细胞毒性评价方法进行刺激性评价(样品S-1—S-7)。

1.5.2 制备工艺考察
制法:熊胆粉加注射用水100mL,加热煮沸10min,使溶解,放冷,加乙醇至含醇量为75%,静置24h,滤过,滤液回收乙醇后,备用。另取硼酸、硼砂、氯化钠、羟苯乙酯加水800mL,加热煮沸至完全溶解,滤过,滤液加入上述药液中,煮沸30min,放冷,加注射用水至1000mL,用微孔滤膜(0.22μm)滤过,分装,即得。
按照该滴眼液制备工艺,对提取时间、精制工艺、合并煎煮时间3个环节进行考察,根据相关工艺变更工艺水平配制各样品溶液。
1.6 刺激性解决方法研究
对1.5环节中筛查出的刺激性原因进行分析,并采用以下4种方法进行针对性的解决。
1.6.1 更换防腐剂
将处方中羟苯乙酯分别更换为1.5g、1.8g、2.1g山梨酸,然后按照处方要求配制样品,标记为S-8、S-9、S-10。
1.6.2 降低羟苯乙酯用量
将处方中羟苯乙酯用量调整为0.2g、0.4g、0.6g、0.8g、1.0g、1.2g,配制成不同样品。
1.6.3 添加增粘剂羧甲基纤维素钠
按照不同比例(0.05%、0.10%、0.15%、0.20%、0.25%)配制添加羧甲基纤维素钠样品。
1.6.4 添加增粘剂透明质酸钠
按照不同比例(0.02%、0.04%、0.08%、0.10%、0.20%、0.30%、0.40%)配制添加透明质酸钠的样品。
2 试验结果
2.1 方法学的确立
通过相关性分析,结果如图1、图2,混合培养法(R=0.961,F=545.409,P=0.000)评价滴眼液刺激性优于直接接触法(R=0.619,F=13.657,P=0.001),故采用混合培养法作为细胞毒性研究方法用于该实验研究。
2.2 刺激源分析结果
2.2.1 处方刺激源筛查结果
由图3可知,当样品中同时含有熊胆原液与羟苯乙酯,细胞毒性明显增加,角膜上皮细胞存活率低于70%(S-2、S-3、S-4、S-5),而当样品中无熊胆原液(S-6),或者无羟苯乙酯(S-1,S-7),角膜上皮细胞的存活率与阴性对照组(S-31)之间没有统计学意义,提示熊胆原液与羟苯乙酯共存增加了眼药水的刺激性。
2.2.2 制备工艺筛查结果
(1)对熊胆煎煮时间的考察。对采用不同煎煮时间的熊胆原液及其与处方药品混合的处方液进行试验发现,煎煮10min、20min、30min对兔角膜上皮细胞存活率的影响差异没有统计学意义。处方组角膜上皮细胞存活率均低于熊胆原液组,如图4所示。

(2)对水提醇沉工艺的考察。水提醇沉采用4因素3水平分析进行考察,结果显示各因素及各水平对角膜上皮细胞的存活率的差异没有统计学意义(数据未列出)。提取方法改用直接水提、水提离心、75%醇提,结果显示水提醇沉法、水提离心、醇提法3种方法之间没有差异(P>0.05),但均优于水提法(P<0.01),如图5所示。

(3)合并煎煮时间的考察。将熊胆原液与其它药品的混合液煎煮0~30min对兔角膜上皮细胞毒性的影响没有差异(P>0.05),当混合煎煮达60min时,样品对兔角膜上皮细胞毒性明显减小(P<0.01)。
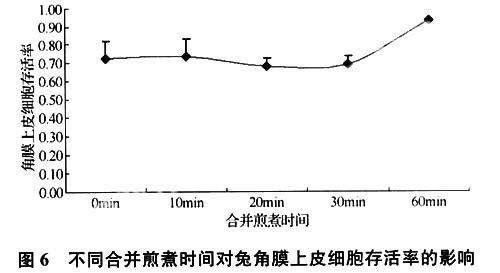
2.3 刺激性解决结果
2.3.1 更换防腐剂
将防腐剂更换为山梨酸(0.15%~0.21%),结果如图7所示,进一步增加了滴眼液的细胞毒性,对刺激性没有任何缓解作用(P<0.001)。

注:羟苯乙酯用量从左到右依次为0.2g、0.4g、0.6g、0.8g、1.0g、1.2g;处方中山梨酸用量从左到右依次为1.5g、1.8g、2.1g。
2.3.2 降低防腐剂用量
将防腐剂用量分别调整至0.02%,0.04%,0.06%与原配方0.08%比较。结果如图7所示,降低防腐剂的用量能减轻其细胞毒性,具备一定缓解刺激性的作用(P<0.05)。
2.3.3 添加羧甲基纤维素钠
由图8可知,当羧甲基纤维素钠的含量达到0.20%时,细胞存活率显著增加,刺激性减小,推测羧甲基纤维素钠含量达到0.30%刺激性将进一步降低,但由于该浓度滴眼液粘度过大不利于临床应用,所以舍弃了该浓度样品。由图8还知,含羧甲基纤维素钠0.20%~0.25%的熊胆滴眼液刺激性明显降低(P<0.01)。
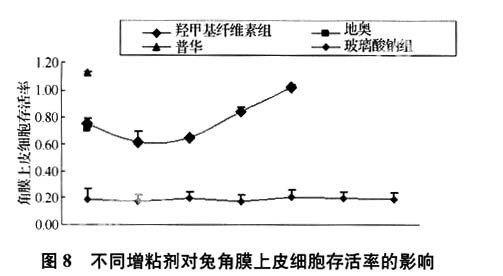
注:羧甲基纤维素钠含量从左到右依次为0.05%,0.10%,0.15%,0.20%,0.25%;增粘剂透明质酸钠从左到右依次为0.02%,0.04%,0.08%,0.10%,0.20%,0.30%,0.40%。
2.3.4 添加透明质酸钠
如图8可知,透明质酸钠含量在0.02%~0.40%对熊胆眼药水的刺激性没有明显改善作用,相反可能会增加滴眼液的刺激性(P>0.05)。
3 讨论
(1)羟苯乙酯与熊胆原液同时存在时,角膜上皮细胞存活率大大降低,且当羟苯乙酯加入熊胆原液后,熊胆原液澄明度明显增加,提示二者结合可能产生了某种化学反应,生成了细胞毒性更大的物质,需要采用进一步手段进行分析研究。
(2)该研究表明加入一定量的羧甲基纤维素钠能够明显改善其对角膜上皮细胞的毒性,而添加透明质酸钠则没有任何改善。推测羧甲基纤维素钠通过化学或物理作用减轻了胆酸成分刺激性。但熊胆眼药水的药理作用是否有所改变有待进一步研究。
(3)有研究表明,滴眼液中常用防腐剂山梨酸、苯扎溴铵和羟苯乙酯均具有一定的角膜上皮细胞毒性,其中苯扎溴铵毒性最大,羟苯乙酯毒性最小[6]。本研究采用山梨酸替代羟苯乙酯进行实验研究,结果显示其对熊胆眼药水的刺激性改善不明显,尽管有报道称透明质酸钠对由防腐剂造成的细胞毒性有明显改善作用[6],提示熊胆眼药水刺激性的产生不单纯依靠羟苯乙酯实现。这与研究中单用PBS配制不同浓度羟苯乙酯进行实验其细胞毒性较小的现象一致。
参考文献:
[1] YORK M, STEILING W. A critical review of the assessment of eye irritation potential using the Draize rabbit eye test[J]. J Appl Toxicol, 1998,18(4):233-240.
[2] 谢立信,董晓光,张德茹,等.人角膜细胞的原代培养实验研究[J].中华眼科杂志,1991,27:13.
[3] 任玫卿,栾洁.兔角膜上皮细胞体外原代培养方法的研究[J].东南大学学报,2008,27(2):90-94
[4] TAKAHASHI Y, KOIKE M, HONDA H, et al. Development of the short time exposure (STE) test: An in vitro eye irritation test using SIRC cells[J].2008, 22(3):760-70.
[5] K CHIBA I, MAKINO J. Interlaboratory Validation of the In Vitro Eye Irritation Tests for Cosmetic Ingredients (9)[J]. Evaluation of Cytotoxicity Test on HeLa Cells. Toxicol In Vitro,1999 (13)189-198.
[6] 张琛,王志昕,邓世靖,等.防腐剂对兔角结膜上皮细胞毒性及透明质酸钠保护作用的实验研究[J].眼科新进展,2008,28(2):85-89
(责任编辑:陈涌涛)
Study on the Irritation of SS Xiongdan Eye Drop
Xiao Dan,Liu Tianqiang,He Jian,Dong Ziliang
(Chengdu University of TCM, Sichuan, Chengdu 610075, China)
Abstract:Objective: Using a new irritation test established in this study to screen the cause of the irritation of SS Xiongdan eye drop (SS eye drop) and adopting proper approach to solve this problem. Methods: 4 kinds of Xiongdan eye drops were tested by the SIRC-MTT and the scores were compared with clinical evaluation, the cause of irritation of Diao eye drop was studied by the method of SIRC-MTT. Results: The correlation coefficient between SIRC-MTT score and clinical evaluation score was 0.961, whichshowed that SIRC-MTT is an effective method to evaluate irritation of Xiongdan eye drops. The cause of strong irritation of Diao eye drop is the coexistence of xiongdan liquid and ethylparaben. Decreasing the dosage of the ethylparaben (0.04) or adding CMC-Na (0.2%~0.25%)could increase the Corneal epithelial cell survival rates. Conclusion: SIRC-MTT is an effective method to evaluate irritation in vitro. Decreasing the dosage of the ethylparaben or adding CMC-Na can ease the irritation of the Diao eye drop.
Key words:Irritation;SIRC;Cytotoxicity test;SS Xiongdan Eye Dop
