氯及其化合物知识点考查剖析及复习指导
2025-03-03周丽


摘 要:“氯及其化合物”作为氧化还原反应中的重要内容,具备丰富的价态,并与实际生活紧密相连,历来是考试的热点.本论文就聚焦于此,简述了“氯及其化合物”在考试中的地位,并结合典型题目,针对“氯及其化合物”复习教学提出了针对性的建议.
关键词:高中化学;考试;“氯及其化合物”;复习指导
中图分类号:G632"" 文献标识码:A"" 文章编号:1008-0333(2025)01-0122-03
收稿日期:2024-10-05
作者简介:周丽,本科,中学一级教师,从事高中化学教学研究.
“氯及其化合物”是非金属元素及其化合物的重要内容之一,涉及知识点较多,且与化工生产、日常生活、科学技术紧密相连,历来是考试的热点,不仅出现的频率高,且占据的分值比较高.纵观以往考试题目,考查知识涵盖了氯及其化合物的性质、氯气的氧化还原反应、氯气的实验室制法等,且以选择题、填空题、推断题的形式出现在试卷中,属于基础和中档题目,直接决定了学生的考试成绩.本论文就以此切入,围绕“氯及其化合物”常见的考点,结合典型的题目展开分析与探究,旨在对读者有所帮助.
1 “氯及其化合物”的考点分析
1.1 “氯及其化合物”性质考查
氯气作为一种化学性质非常活泼的非金属单质.在“氯及其化合物”考查中,关于其性质的考查属于基础型考查,常出现于选择题目中,或者位于推理题的第一环节.学生唯有牢牢掌握其基础知识,精准把握氯气的物理性质和化学性质,才能顺利解答题目.
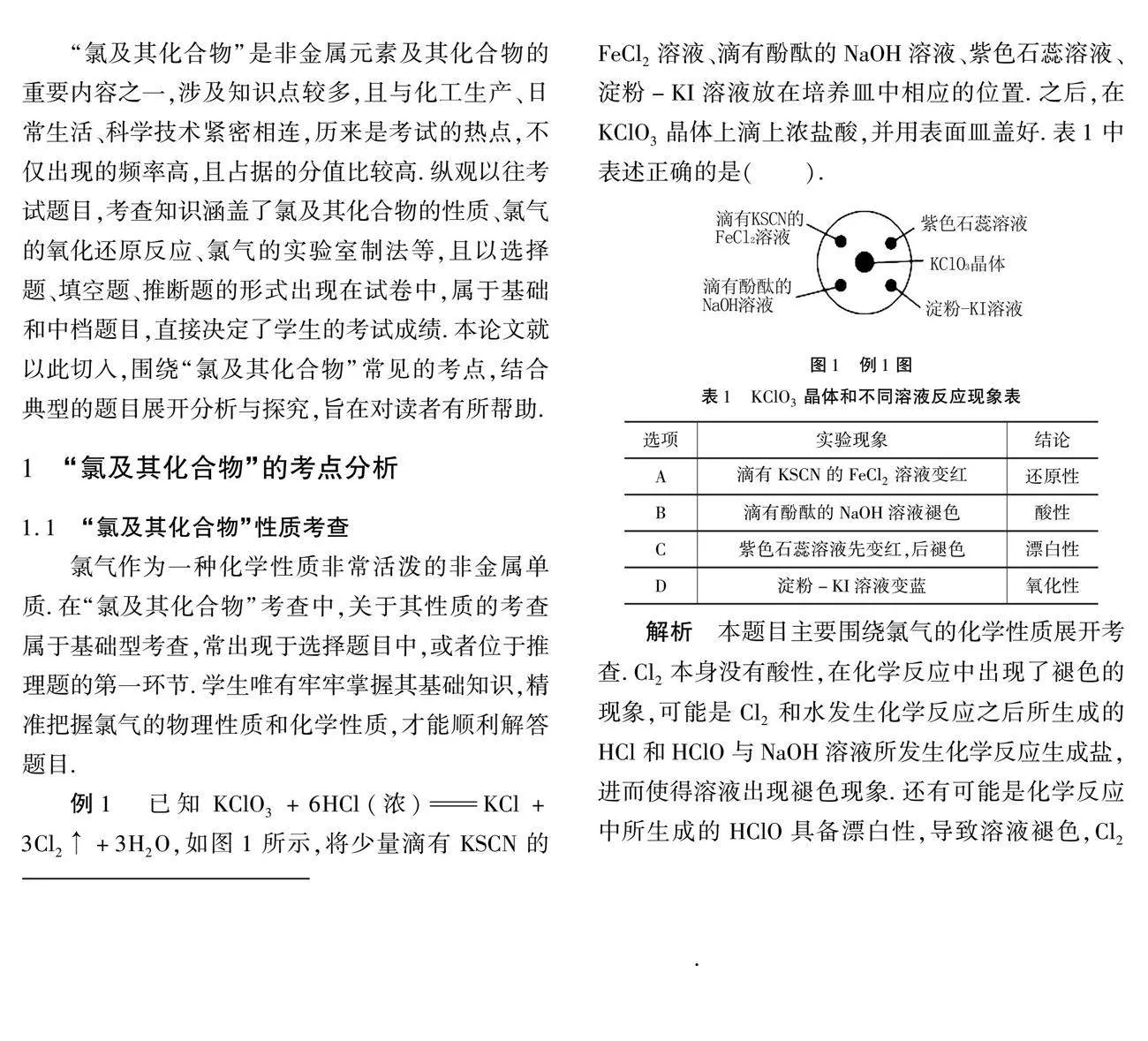
例1 已知KClO3+6HCl(浓)KCl+3Cl2↑+3H2O,如图1所示,将少量滴有KSCN的FeCl2溶液、滴有酚酞的NaOH溶液、紫色石蕊溶液、淀粉-KI溶液放在培养皿中相应的位置.之后,在KClO3晶体上滴上浓盐酸,并用表面皿盖好.表1中表述正确的是(" ).
解析 本题目主要围绕氯气的化学性质展开考查.Cl2本身没有酸性,在化学反应中出现了褪色的现象,可能是Cl2和水发生化学反应之后所生成的HCl和HClO与NaOH溶液所发生化学反应生成盐,进而使得溶液出现褪色现象.还有可能是化学反应中所生成的HClO具备漂白性,导致溶液褪色,Cl2本身不具备漂白性,而是Cl2和水反应中所生成的HClO所致.因此,该题目的正确答案为D.综上,本题目主要考查了氯气的化学性质,难度系数不大,学生只要精准掌握氯气和金属单质、非金属单质、氧化还原反应等知识点,即可轻松完成题目的解答.
1.2 氯气的实验室制法考查
氯气的实验室制法是化学考查的热点,常见于选择题、填空题目中.学生必须牢牢掌握氯气的制取原理、制取过程、实验装置和制取过程中的注意事项,才能轻松解答相关题目.
例2 实验室在制取氯气时,可利用浓盐酸和二氧化锰这两种物质,在加热条件下发生化学反应,且根据氯气可溶于水的性质进行收集.结合所学的化学知识,回答下面问题:
(1)图2中所给出的装置,是实验室制取氯气时发生、收集装置是______(填序号)
(2)制备氯气时,首先要检查装置的气密性.之后的实验操作步骤依次为______(填序号)
A.将MnO2粉末加入到烧瓶中
B.加热
C.将浓盐酸加入到烧瓶中
解析 (1)实验室在制备氯气时,所选择的药品是强化剂MnO2和浓盐酸,化学反应的条件是加热,化学反应方程式为:MnO2+4HCl(浓)
△MnCl2+Cl2↑+2H2O.在该化学反应中,装置的特点是:固体+液体△气体.因此,发生装置应选择A;在该化学反应中,由于生成的氯气密度大于空气,无法采用排水法进行收集,必须采用向上排空的方法进行收集,因此收集装置为F;第(2)问聚焦化学实验整个流程.通常,在具体的实验过程中,首先要检查装置的气密性,之后再加药品(先固体后液体),最后进行加热.由此即可得出在该实验中,接下来应该是往烧瓶中加入MnO2粉末、加入浓盐酸、加热等环节,即:ACB.
在实验室制取考查中,所涉及的知识点比较多,学生不仅要掌握制取原理、制取过程,还应注意一些常见的问题.在选择反应物时,必须选择浓盐酸,因为稀盐酸和MnO2不反应.同时,在具体的化学反应中,伴随着反应的进行,浓盐酸逐渐变稀,待其逐渐成为稀盐酸时,反应停止.因此,在化学反应过程中,盐酸中的HCl无法全部参与其中.同时,实验室制取氯气中,化学反应条件是加热,但加热不宜过高,以免出现HCl挥发.在收集氯气时,由于氯气密度大于空气,可选择向上排空气法进行收集.另外,化学实验完成之后,待化学反应停止下来之后,必须排除将残留氯气.在拆卸装置时,还应避免出现空气污染的现象.最后,在处理化学反应尾气时,可选择NaOH溶液,不能选择澄清的石灰水,因为其中含有Ca(OH)2的量比较少,吸收不够完全[1].
1.3 次氯酸和次氯酸盐的考查
次氯酸和次氯酸盐也是“氯及其化合物”中考查的重点.就次氯酸而言,其酸性比碳酸弱,具备强氧化性和不稳定性,常被用来制作消毒剂、漂白剂,如84消毒液、漂白粉等.同时,次氯酸盐极容易见光分解,久置容易在光照的条件下失效.
例3 氯可形成多种含氧酸盐,常被用来杀菌、消毒、化工等.图3是实验室中KClO3和NaCIO的制备装置.
回答下列五个问题:
(1)盛放MnO2粉末仪器名称( ),a中试剂是( ).
(2)b中所选择的加热方式是( ),c中所发生的化学反应的离子方程式( ),在该化学反应中,进行冰水浴冷却是为了( ).
(3)d的功效是( ),可选择哪一种试剂( )(Na2S、NaCl 、Ca(OH)2 、H2SO4).
(4)待到化学反应完毕后,取出b中试管,对其进行冷却结晶,( )干燥,即可得到KClO3晶体.
(5)取少量的KClO3溶液置于1号试管中,少量的NaClO溶液置于2号试管中.之后,将中性KI溶液滴加到试管中.结果发现:1号试管中溶液的颜色一直没有出现变化,2号试管中的溶液有所改变,逐渐呈现为棕色.之后,继续加入CCl4并进行振荡,静置一段时间,CCl4层呈现( )色.从这一过程中,可对KClO3、NaClO的氧化能力进行判断,即KClO3( )NaClO(填“>”或“<”).
解析 本题目属于典型的次氯酸盐考查.在(1)中,氯气发生装置,是在圆底烧瓶中完成的,因此盛放MnO2粉末的仪器就是圆底烧瓶,b中氯气和氢氧化钾发生反应,因此a中的试剂是饱和食盐水.在(2)中,b所采用的加热方式是水浴加热,根据题目意思即可得知,b中氯气和氢氧化钾是在加热水浴中所发生的化学反应,进而生成KClO3.c中是氯气和冷的NaOH发生化学反应,继而生成NaClO,在这过程中采用冷水浴的目的是防止NaClO3生成.针对(3)来说,d的作用是除去多余的氯气,预防在整个化学反应中出现污染大气的现象,在本题目所给出的选项中,只有Na2S、Ca(OH)2符合题意.针对(4)来说,冷却结晶是过滤,过滤下来就是洗涤.针对(5)来说,1号试管中溶液颜色没有发生变化,这主要是因为KClO3无法和KI溶液发生化学反应,难以氧化KI;2号试管中出现了溶液变色的现象,则表明该物质能够和KI溶液发生化学反应,并且在反应中生成了I2,加入CCl4振荡呈现紫色,表明KClO3的氧化能力小于NaClO的氧化能力.
2 “氯及其化合物”复习教学建议
首先,构建系统化的知识体系.本章节内容包含着大量的知识点,也是考试的热点.因此,教师在指导学生进行复习时,不仅要带领学生梳理单元知识点,还应立足于本章节内容和实际生活的内在联系,从某一生活情境切入,带领学生在分析生活情境问题的过程中,将相关知识点串联到一起,最终形成系统化的知识体系.同时,在这一过程中,教师还可指导学生借助思维导图工具,对单元知识点进行整理.
其次,教学内容结构化.新高考下,关于“氯及其化合物”考查的形式和内容也有所改变,更加关注学生核心素养.鉴于此,教师在引领学生进行复习时,可从真实的生活中常见的物品出发,如含氯消毒剂,进而将氯气的性质、制备、用途整合到一起,使得学生在结构化的内容中完成学习.
最后,关注课堂生成.教师在指导学生进行复习时,不仅要借助现代化的教学手段,还应充分利用课堂提问、追问等方式,关注课堂生成,并结合学生的复习效果及时调整教学方案、改进教学手段等,全面提升学生的复习效果[2].
3 结束语
综上所述,氯及其化合物在化学考试中尤为常见,或直接设置与其相关的题目,或将其融入实际问题中,题目情境灵活多变,且一环扣一环,存在一定的综合性.学生在学习该部分知识时,唯有熟练掌握该部分知识,掌握一定的解题方法和技巧,方可轻松应对考试.因此,教师在日常教学中,可结合典型的例题,基于学生的实际情况,优化复习教学指导,使得学生在日常复习中,不断提升自身的问题解答能力.
参考文献:
[1] 徐丹.氯及其化合物知识点探究[J].中学生数理化(高一使用),2021(10):41-46.
[2] 刘志勇.基于真实情境的化学复习课教学实践与反思:以“氯及其化合物”为例[J].课程教材教学研究(教育研究),2024(01):50-56.
[责任编辑:季春阳]
