骨通贴膏(热压法)毒理学实验研究
2024-09-20陈宇峰吴超权莫玉焕农学多曾森





【摘要】
目的:探讨系统评价骨通贴膏(热压法)的用药安全性。方法:通过急性毒性试验、皮肤刺激和过敏试验、小鼠嗜多染红细胞微核试验进行骨通贴膏安全性评价。结果:以骨通贴膏(热压法)样品分别给大鼠完整及破损皮肤局部外贴,含膏浆2000 mg/kgBW的一次性限量急性皮肤毒性试验,未见出现明显急性皮肤毒性反应。样品对家兔完整及破损皮肤均无刺激性;样品对豚鼠皮肤为无致敏性;微核试验用药组与阴性对照组比较,微核发生率无显著差异(P>0.05)。结论:骨通贴膏(热压法)对试验动物皮肤无刺激,不致敏,无吸收中毒,亦无潜在的致突变作用。
【关键词】
热塑性橡胶;骨通贴膏;急毒;过敏;致突变
【中图分类号】R285
【文献标志码】 A【文章编号】1007-8517(2024)16-0016-06
DOI:10.3969/j.issn.1007-8517.2024.16.zgmzmjyyzz202416005
Experimental Study on Toxicology of Gutong Plaster (Hot Pressing Method)
CHEN Yufeng1WU Chaoquan2MO Yuhuan2NONG Xueduo2ZENG Sen3
1.Guilin Huarun Tianhe Pharmaceutical Co., Ltd., Guilin 541000,China;
2.Guangxi Institute for Food and Drug Control,Nanning 530000,China;
3.Guilin Tianhe Pharmaceutical Yiwei Co. , Ltd., Guilin 541000,China
Abstract:
Objective To systematically evaluate the safety of Gutong Plaster ( hot pressing method ). Methods The safety of Gutong Plaster was evaluated by acute toxicity test, skin irritation and allergy test, mouse polychromatic erythrocyte micronucleus test. Results The samples of Gutong Plaster ( hot pressing method ) were applied to the intact and damaged skin of rats, and no obvious acute skin toxicity was observed in the one-time limited acute skin toxicity test containing 2000 mg/kg BW paste. The sample had no irritation to the intact and damaged skin of rabbits.The sample was non-allergic to guinea pig skin; there was no significant difference in the incidence of micronucleus between the micronucleus test group and the negative control group ( P>0.05 ). Conclusion Gutong Plaster ( hot pressing method ) has no irritation, no sensitization, no absorption poisoning, and no potential mutagenic effect on the skin of experimental animals.
Keywords:
Thermoplastic Rubber; Gutong Plaster; Acute Toxicity; Allergy; Mutagenesis
骨通贴膏是采用消炎、扩张毛细血管、渗透功能强的天然药物,同时辅助透皮吸收促进剂,运用现代技术加工制成的外用贴剂。主要成分有丁公藤、麻黄、当归、干姜、白芷、海风藤、乳香、三七、姜黄、辣椒、樟脑、肉桂油、金不换、薄荷脑。辅料为橡胶、氧化锌、松香、羊毛脂、黄凡士林、月桂氮卓酮等[1]。用于治疗骨质增生、肩周炎、颈(腰)椎病、风湿、关节炎、腰椎间盘突出等各种慢性骨病[2]。有祛风散寒、活血通络、消肿止痛的功效,对各种慢性骨病引起的局部疼痛、肿胀、麻木重着,或屈伸不利,或活动受限有较好的疗效[3-5]。
骨通贴膏等中药贴膏作为药物透皮制剂,与散剂等传统内服剂型相比,有使用方便、可以避免首过效应、提高患者顺应性等优点[6]。以往骨通贴膏使用的辅料为烟片胶,是天然橡胶,有异性蛋白,易导致过敏、皮肤刺激。近年来,企业对产品进行创新升级,采用热塑性橡胶作为骨通贴膏的基质材料,经过物理加热捏合而制成新型的骨通贴膏,其具有黏性适中、对皮肤的牵拉刺激作用小、过敏率低等特点,且热塑性橡胶性质稳定,不与主药起反应。为确保临床用药安全,课题组对其进行了多项毒理实验,现将实验结果报道如下。
1材料和方法
1.1材料
1.1.1检测样品骨通贴膏(热压法,批号:221103,桂林华润天和药业有限公司,制剂每贴面积为7 cm×10 cm,含膏浆1.7~1.8 g/100 cm2),外用,贴于患处,每日1次。临床按成人每日用2贴计。人推荐日剂量为2.33 cm2/kg 体重(膏浆0.042 g/kg 体重)或体表面积88.0 cm2/m2体表面积(膏浆1.58 g/m2体表面积)。空白贴膏(热塑性橡胶制成,不加药物,批号:20211222,桂林华润天和药业有限公司)用于皮肤刺激性、过敏性实验和小鼠嗜多染红细胞微核试验基质对照用。
1.1.2对照品2, 4-二硝基氯代苯(上海试剂一厂),用70%乙醇配成1%(致敏诱导用)及0.1%(激发反应用)两种浓度供试,用于皮肤过敏性实验致敏和激发用;环磷酰胺,购于上海源叶生物科技有限公司。
1.1.3动物来源急性皮肤毒性试验:SD大鼠,SPF级,♀♂各半,体重260~300 g,广西壮族自治区食品药品检验所提供,生产许可证号:SCXK桂2022-0001。多次皮肤刺激性试验:新西兰兔,普通级,♀♂各半,体重2.5~2.8 kg,广西壮族自治区食品药品检验所提供,生产许可证号:SCXK桂2022-0001。皮肤过敏性试验:Hartley豚鼠,普通级,♀♂各半,体重252~290 g,广西壮族自治区食品药品检验所提供,生产许可证号:SCXK桂2022-0001。小鼠嗜多染红细胞微核试验:小鼠,SPF级,♀♂各半,体重30~35 g,广西壮族自治区食品药品检验所提供,生产许可证号:SCXK桂2022-0001。
1.1.4仪器及其他显微镜,JJ2000电子天平,PL3001-S电子天平,CP224S型电子天平,ACS-30电子计价秤等。
1.2方法
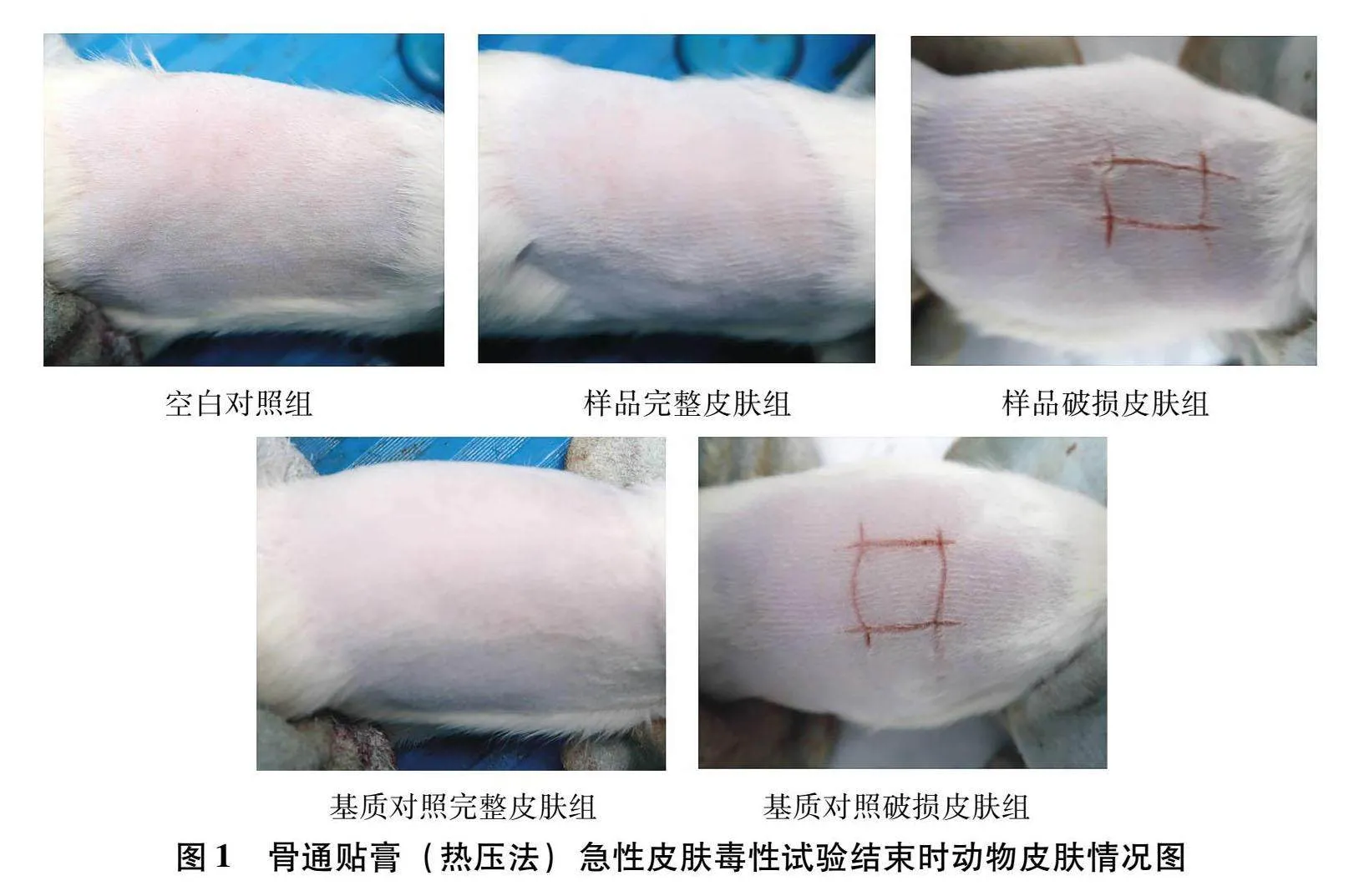
1.2.1急性皮肤毒性试验方法取上述大鼠100只(♀♂各半),每鼠背部及两侧皮肤用电动毛剪去毛,范围约10 cm×6 cm。24 h后按体重随机均分为5组,每组20只(♀♂各半):空白对照组、样品完整皮肤组、样品破损皮肤组、基质对照完整皮肤组、基质对照破损皮肤组。破损皮肤造型方法:以75%乙醇消毒去毛区皮肤,用消毒手术刀在去毛区表皮划“井”形伤口,每刀口长约2 cm,以渗血为度。两组动物均给予受试药物:按动物体重给予贴膏,给药剂量为2000 mg/kg,参照样品含膏浆重量计算相对应贴膏面积并将贴膏敷贴于去毛区皮肤区域,覆盖一层医用胶布,并用胶带包扎固定,持续24 h后除去包扎和胶布,用温水洗去皮肤药物。观察给药期间及至药后14 d大鼠的局部及全身反应等情况。
1.2.2多次皮肤刺激性试验方法取健康无皮疾的新西兰家兔24只(♀♂各半),每只家兔背部脊柱左、右两侧各1个区域皮肤去毛,每侧范围约4 cm×4 cm。24 h后按体重随机均分为4组(每组6只,♀♂各半):样品完整皮肤组、样品破损皮肤组、基质对照完整皮肤组、基质对照破损皮肤组。破损皮肤造型方法:以75%乙醇消毒去毛区皮肤,用消毒手术刀在两侧去毛区表皮划“井”形伤口,每刀口长约2 cm,以渗血为度。各组动物均给予相应受试药物:将样品贴膏及基质对照分别剪成3 cm×3 cm的试样,敷贴于各兔左侧去毛区皮肤(面积为4 cm×4 cm),用医用胶布及胶带包扎固定;右侧去毛区皮肤不做处理作为空白对照,5 h后除去试样,于除去试样1 h后观察敷贴部位的皮肤反应,评分;从第二天开始,每次敷贴前观察皮肤评分后,用电动毛剪剪毛,敷贴5 h后除去试样,于除去试样1 h后观察敷贴部位的皮肤反应,评分。连续敷贴14 d,每次除去药物后1 h,每次给药前及末次敷贴去除药物1 h、24 h、48 h、72 h(共30个观察点),观察皮肤反应并评分,评分按参考文献[7]中“皮肤刺激反应评分标准”评分记录。首先计算每一观察时间点各组积分均值,然后计算观察期限内每天每只动物刺激积分均值,并按参考文献[7]“皮肤刺激强度评价标准”判定皮肤刺激强度。
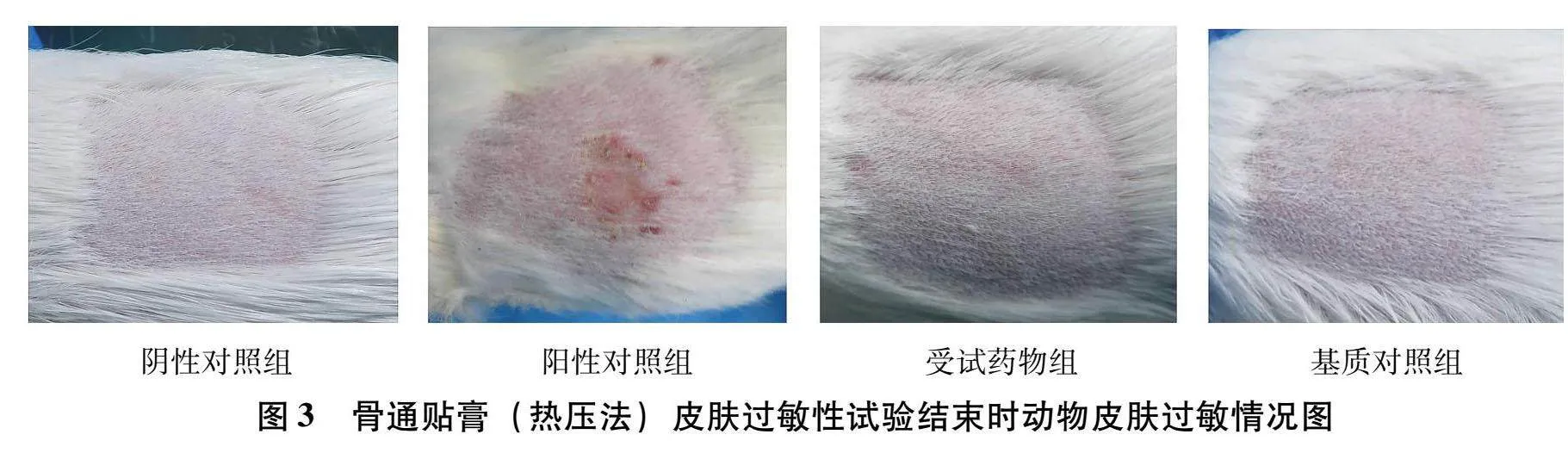
1.2.3皮肤过敏性试验方法取豚鼠60只(♀♂各半),每鼠背部脊柱右侧皮肤去毛,范围约4 cm×4 cm。24 h后按体重随机均分为受试药物组(20只,♀♂各半)、基质对照组(20只,♀♂各半)、阴性对照组(10只,♀♂各半)、阳性对照组(10只,♀♂各半),分组后即致敏给药:将试药敷贴或涂敷于左侧去毛区皮肤上;受试药物组敷贴有药膏药(分别制成3 cm×3 cm试样),阴性对照组不作处理,阳性对照组敷贴1% 2, 4-二硝基氯苯(用0.5 mL溶液浸湿3 cm×3 cm的灭菌纱布块后贴敷),并用医用胶布及胶带包扎固定;6 h后除去包扎和试药;第7天、第14天分别同法致敏给药各1次。于首次致敏给药第27天,每鼠背部脊柱左侧皮肤去毛,范围约4 cm×4 cm,并于第28天激发给药:按前述方法将对应试药(阳性组为0.1% 2, 4-二硝基氯苯)分别敷贴或涂敷于对应各组动物的左侧去毛区皮肤,并用医用胶布及胶带包扎固定;6 h后除去包扎和试药,观察即时、24 h、48 h、72 h局部皮肤的红斑、水肿等情况,按参考文献[7]主动皮肤过敏试验(ACA)试验的“皮肤过敏反应程度的评分标准”进行评分,并综合计算动物组“致敏率”,按参考文献[7]主动皮肤过敏试验(ACA)试验的“皮肤致敏性评价标准”对“致敏强度”进行评价,见表1、表2。测定开始时和结束时的动物体重。当受试物组动物出现皮肤反应积分≥2,判定该动物出现过敏反应阳性。
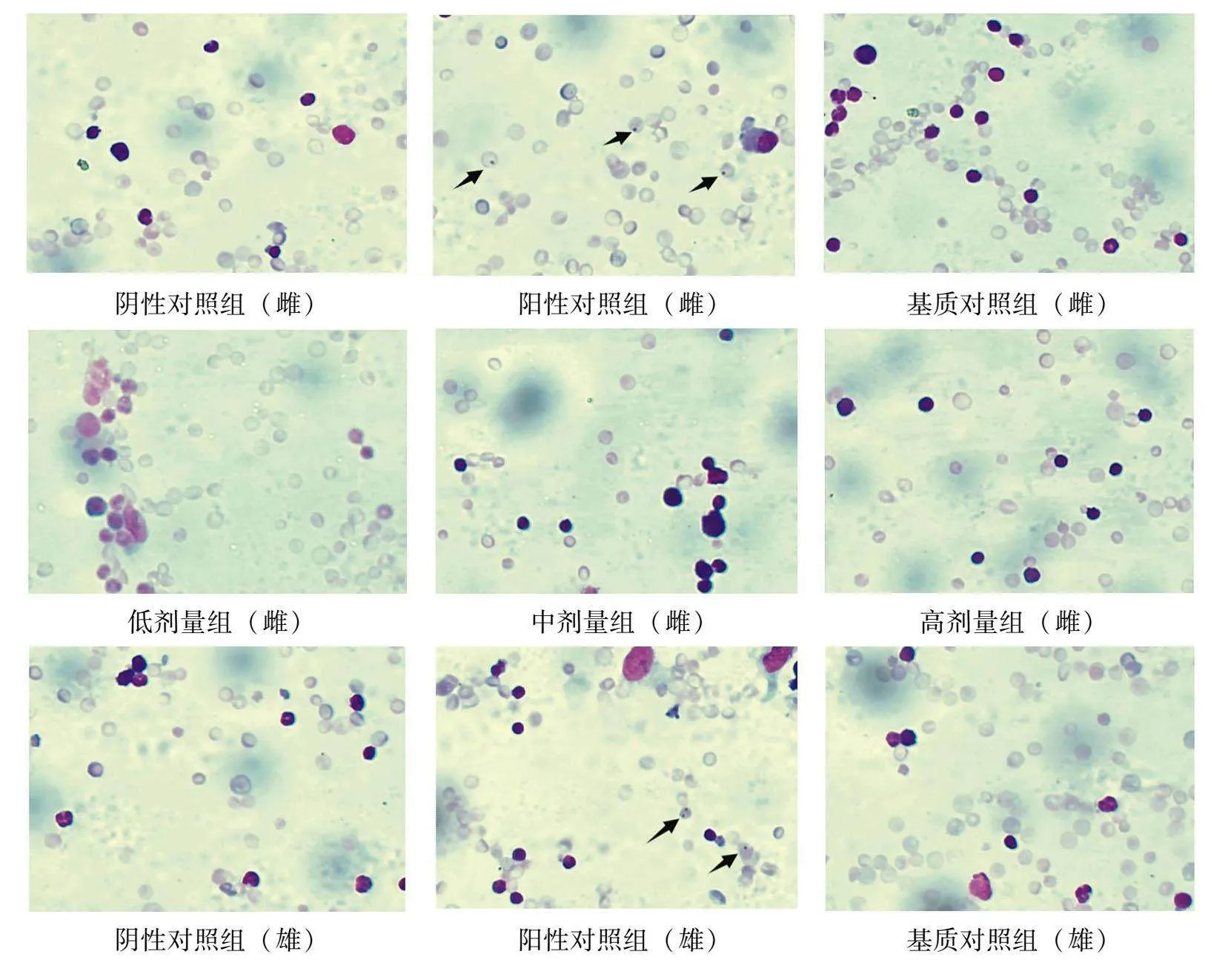
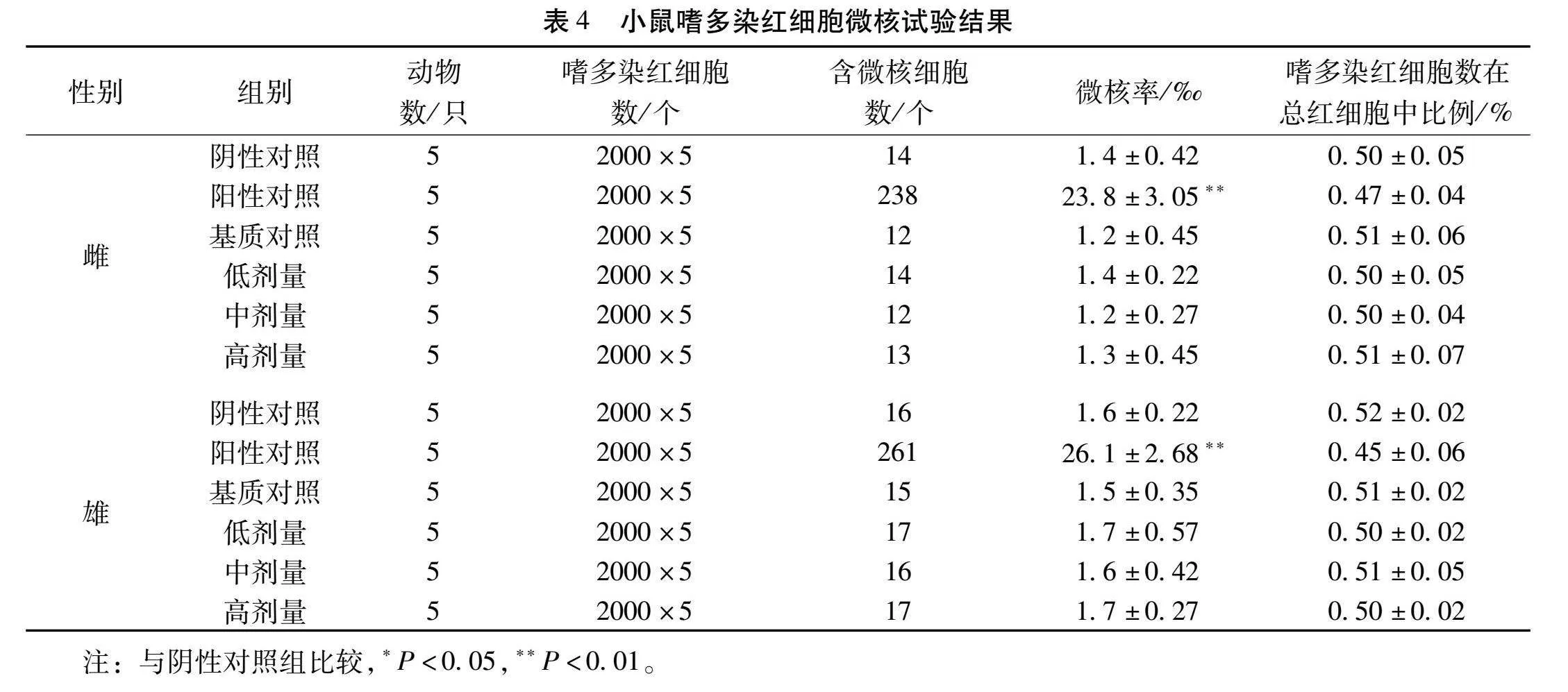
1.2.4小鼠嗜多染红细胞微核试验方法选用小鼠60只,分为6组,每组10只,雌雄各半,每鼠背部脊柱左侧皮肤去毛,范围约4 cm×4 cm。设样品三个剂量组,分别为高剂量组(4 cm×4 cm)、中剂量组(3 cm×3 cm)、低剂量组(2 cm×2 cm);另设基质对照组(3 cm×3 cm)、阴性对照组和阳性对照组。给予受试物方式:将不同规格试药敷贴于左侧去毛区皮肤上,并用医用胶带包扎固定;6 h后除去包扎和试药,每日1 次,连续7 d给予受试物,两次给受试物的间隔时间为24 h。阴性对照组不作任何处理,为空白对照。阳性对照组通过灌胃方式给予环磷酰胺(1 mg/mL),给药体积为为20 mL/kg,末次给予受试物后6 h,处死动物。取股骨骨髓涂片,在显微镜下观察,每只动物计数2000个嗜多染红细胞(PCE)中有微核的细胞数,计算微核率(‰);计数200个红细胞(RBC)数以及PCE数,计算PCE/RBC比值。
1.2.5统计学分析数据采用SPSS 16.0统计软件进行处理,雌雄分别统计,以均数加减标准差表示。对符合正态分布且方差齐的数据,则进行单因素方差分析和多重比较(SNK-q检验);对不符合正态分布或方差不齐的数据,则进行非参数检验(Kruskal-Wallis秩和检验)。其中, 遗传毒性试验结果中,微核率的比较使用泊松分布法。P<0.05表示差异有统计学意义。
2结果
2.1急性皮肤毒性试验以骨通贴膏(热压法)样品分别给大鼠完整及破损皮肤局部外贴,含膏浆2000 mg/kg BW(按体重用药剂量计,产品相当于日临床用量的48倍;按单位体表面积用药量计,此量为日临床用量的4倍)的一次性限量急性皮肤毒性试验,未见出现明显急性皮肤毒性反应。各组大鼠去除贴剂后未见给药区皮肤红斑和水肿;给药后14 d内各组大鼠的外观、行为、眼和粘膜、四肢活动、进食、排泄及呼吸、循环、自主神经、中枢神经系统等均未见明显异常;无死亡现象;未见对体重有明显影响,体重增长正常;破损皮肤组动物于6 d后伤口愈合良好。
2.2多次皮肤刺激性试验样品对完整、破损皮肤组的试验区刺激性反应平均分值均与对照区侧相近,完整皮肤组试验区、对照区每天每只动物平均总分值分别为0分、0分,破损皮肤组试验区、对照区每天每只动物平均总分值分别为0分、0分;热塑性橡胶基质对完整、破损皮肤组的试验区刺激性反应平均分值均与对照区侧相近,完整皮肤组试验区、对照区每天每只动物平均总分值分别为0分、0分,破损皮肤组试验区、对照区每天每只动物平均总分值分别为0分、0分。提示骨通贴膏及空白贴膏对家兔完整皮肤及破损皮肤均无刺激性,未见引起皮肤粗糙增厚或变薄,破损皮肤愈合良好,与对照区侧比较无显著差异。
2.3皮肤过敏性试验对于骨通贴膏样品,按标准评价,认为样品对豚鼠皮肤具有无致敏性。其组内最高反应分值为0分,与空白对照组反应相同,故认为样品所致豚鼠皮肤过敏反应程2.4小鼠骨髓嗜多染红细胞微核试验受试物各剂量组嗜多染红细胞数在总红细胞中比例与阴性对照组的差异均在20%以内,差异无统计学意义(P>0.05),表示骨通贴膏(热压法)对小鼠骨髓细胞增殖无不良影响。雌性小鼠阳性对照组微核发生率高于阴性对照组(P<0.05),雌性小鼠各剂量组与阴性对照组比较无显著性差异(P>0.05)。雄性小鼠阳性对照组微核发生率高于阴性对照组(P<0.05),雄性小鼠各剂量组与阴性对照组比较无显著性差异(P>0.05),表明骨通贴膏(热压法)在小鼠骨髓细胞微核试验中为阴性结果。结果见表4。
3讨论
热塑性橡胶,简称TPE,又称热塑性弹性体,是一类在常温下显示橡胶弹性、受热时呈可塑性的高分子材料。热塑性橡胶具有普通硫化胶的类似物性,相似的结构(均为聚异戊二烯结构),但不需硫化,可与热塑性树脂一样,用普通塑料加工方法成型,制品可回收再加工而不失其基本性能。骨通贴膏基质骨架材料为高分子聚合物,无以往天然橡胶贴膏基质中的高蛋白类物质和不饱和松香酸,可减少皮肤过敏反应[8]。热塑性橡胶黏接强度高并且低敏、低刺激、皮肤相容性好、载药量大并且适应热熔或溶剂型涂布,可配置成适宜人体皮肤生物学和透湿性要求而且不易过敏的新型基质[9]。这种新型材料的开发,给橡胶工业带来重大革新。它打破了橡胶和塑料之间的传统界限,在节能、省力和防止环境污染方面,更具经济和社会效益。
骨通贴膏热压法生产过程分为捏炼、混合、涂胶、收卷、分切和包装几个工序。热压法生产橡胶膏剂与溶剂法相比:不使用溶媒,无易燃易爆挥发性物体,安全、环保,厂房占地面积小,挥发性药物损失少,生产效率高,投资少[9-10]。中药的毒性与无毒性是中医中药理论的重要组成部分。古代和现代医生对同一种中药的毒性有不同的描述,给临床用药带来了一定的难度。究其原因,一方面可能是中药毒性的客观判定标准较少,且中药毒性的影响因素很多。例如配伍是否合理,用量是否合适,炮制工艺是否得当,剂型是否合适,这些都能影响药物的毒性。此外,中药的产地、用药部位、采收时间、贮存条件等对中药的毒性也有一定的影响[11]。研究人员常运用急性毒性实验、小鼠骨髓细胞微核试验、单次皮肤刺激试验和大鼠致畸试验等试验进行中药及保健食品安全性评价[11-12]。骨通贴膏(热压法)采用热塑性橡胶为辅料基质,运用热压法生产,辅料发生了改变,为确保临床用药安全,课题组对其进行了急毒、刺激、过敏和诱变实验研究,实验结果显示骨通贴膏(热压法)对实验动物皮肤无刺激、不致敏、无吸收中毒,亦无潜在的诱变作用,表明临床应用安全可靠,为临床用药提供了科学依据。
参考文献
[1]夏菁,谢媛媛,张宗璇,等.骨通贴膏指纹图谱及化学成分研究[J].中成药,2014,36(3): 571.
[2]丘明明. HPLC 法测定骨通贴膏中盐酸麻黄碱的含量及均匀度[J].中国药师,2010,13(5):69.
[3]万世元,奚小冰.天和骨通贴膏治疗膝骨关节炎的临床疗效评价研究[J].中国医药导刊 ,2015,17(12):1231-1234.
[4]李亮,周正新,刘安平,等.骨通贴膏治疗早、中期膝骨关节炎临床研究[J].世界最新医学信息文摘,2019,19(69):166-167.
[5]杜婕莹,曾森,王璐,等.聚异丁烯骨通贴膏经皮肤给药的安全性研究[J].中国药房,201,27(25):3512-3514.
[6]高成林,贾晓斌,陈彦,等.中药经皮给药制剂的研究进展[J].中国药房,2009,20(9):707-709.
[7]国家食品药品监督管理总局.药物刺激性、过敏性和溶血性研究技术指导原则(2014年版)[S].
[8]王永刚,关子昂,于鑑衡,等.热熔胶基质和热熔胶贴膏制备技术的应用分析[J],中国现代应用药学,2022,39(8):1088-1094.
[9]刘齐,贾晓斌,韦英杰,等.中药橡胶膏剂致敏因素分析与对策[J].中国医院药学杂志,2011,31(8):685-687,691.
[10]王永刚.橡胶贴膏剂制备方法的应用分析[J].中国实验方剂学杂志,2017,23(13):231-234.
[11]张静,黄丽华,耿秀兰.梔翘生肌软膏毒理学实验研究[J].中国卫生产业,2014,11(14):42-43.
[12]卢礼平,王欢,熊玲,等.铁皮石斛叶的安全性毒理学评价试验研究[J].中国民族民间医药,2022,31(19):12-16.
(收稿日期:2023-11-08编辑:刘斌)
