糖类与甜味剂的肠-脑轴效应研究进展及评估方法分析
2024-05-20史清照刘富强张启东柴国璧王焕丽姬凌波冯伟华宗国浩曹培健谢剑平
史清照,刘富强,张启东,范 武,柴国璧,毛 健,2,王焕丽,姬凌波,冯伟华,宗国浩,曹培健,卢 鹏,谢剑平,2,*
(1.中国烟草总公司郑州烟草研究院,河南 郑州 450001;2.北京生命科技研究院,北京 102299)
喜爱甜味是人类的本能,人类在婴儿时期就表现出明显的甜味偏好[1],而甜味引发的大脑奖赏区域神经活动和多巴胺(dopamine,DA)的释放则阐释了这一现象的深层生物学机制[2-3]。人类文明初期,甜味主要源于鲜果、蜂蜜和其他植物中的天然小分子糖类。随着农业和手工业的发展,世界各地先后以谷物、甘蔗、甜菜等为原料,创造性地开发出含有较高麦芽糖(饴)、蔗糖等糖类的甜食。《诗经》中有“周原膴膴,堇荼如饴”的诗句,以甜美的饴糖赞美周人的故土,可见早在周代饴糖已是生活中常见的食品。
随着工业革命的发生,尤其是二战后工业与农业、畜牧业的结合,全球越来越多的经济体呈现食物和营养供给日益过剩的趋势;由于对甜味的本能喜爱,高糖高甜度食品备受消费者青睐,但同时也带来了诸如糖尿病、肥胖等健康问题。国际糖尿病联盟(International Diabetes Federation,IDF)2021年统计数据显示,全球糖尿病患病率持续增长,相比于2019年,2021年全球成年糖尿病患者人数增加了16%,约占全球成年人口的10.5%[4-5]。
在这一全球健康风险背景下,许多国家开始实施政策以降低本国居民的糖类摄入量[6]。我国各级政府机构已出台多项政策或计划,呼吁人们控制日常糖分摄入、倡导减糖生活。在各方倡导下,利用甜味剂代替糖类提供甜味感受的产品在食品产业界和消费者群体中受到更多关注。甜味剂通常以更少的剂量提供与糖类同等强度的甜味,同时不影响血糖水平,也不会导致肥胖、龋齿等健康问题,满足了消费者获取甜味享受和降低健康风险的双重需求。目前全球范围内无糖或低糖类产品数量迅速增加,这些产品都应用了不同类型的甜味剂。
甜味剂根据来源分为人工甜味剂和天然甜味剂两种类型。1879年,美国约翰·霍普金斯大学研究人员偶然品尝了所合成的产物,发现其具有强烈的甜味并将其命名为“糖精”,这是首个被发现并获得大规模应用的人工甜味剂[7]。随后甜蜜素、安赛蜜、阿斯巴甜和三氯蔗糖等不同类型的人工甜味剂陆续被开发出来,且无一例外出于实验偶然。1979年,辉瑞公司投资开发出阿力甜,人工甜味剂进入更为理性的研发时代,且甜度获得更大幅度的提升。1993年纽特公司开发出纽甜,2008年日本味之素公司开发出爱德万甜,甜度分别达到了蔗糖的8 000 倍和20 000 倍[8-9]。伴随各类人工甜味剂的广泛应用,其在消化系统、神经系统、免疫系统和生殖系统等方面的安全性争议不断[10-12],近期国际癌症研究机构将阿斯巴甜列为“可能对人类致癌的物质”,这一报道引起了人们对甜味剂安全性的广泛关注。另一方面,环保主义和绿色消费理念则驱动着以糖苷类、糖醇类为代表的天然甜味剂快速发展。然而,天然甜味剂甜度相对偏低,又因原料产能限制导致生产成本相对较高,因此常与人工甜味剂搭配使用,改良产品风味。目前,人工甜味剂市场占有率仍显著高于天然甜味剂。
尽管现有甜味剂能够提供类似于糖类的风味感受和远高于糖类的甜味强度,但仍旧不能完全替代食用糖类所带来的满足感。研究发现,甜味剂的摄入可能会让人更想吃含糖的甜食[13],孕期摄入大量的甜味剂甚至会导致胎儿出生后对糖类食物产生更强烈的偏好,从而间接性地导致肥胖[14]。近二十年来,在动物行为学表现、大脑奖赏系统活动和关键神经通路激活模式等不同层面的研究中均发现人类或动物对糖类和甜味剂的行为偏好和肠-脑轴神经反应存在显著差异,明确该现象及其深层生物学机制,对于完善甜味剂的功能评估体系和指导甜味剂的创新发展都具有十分重要的意义。本文综述了糖类和甜味剂引发动物行为偏好差异及其生物学机制方面的研究进展;在此基础上,从动物行为学特征、脑区神经活动模式和关键受体激活能力3 个角度提出了完善当前甜味剂功能评估体系的方法学建议,旨在为甜味剂的功能研究与创新发展提供参考。
1 糖类与甜味剂的肠-脑轴效应差异研究
1.1 糖类与甜味剂引发的动物行为偏好差异
大多数动物都会被甜味吸引,然而面对糖类和甜味剂,动物却展现出明显的选择倾向性。在甜味受体发现之前,研究者认为味觉系统可能是导致动物对糖类和甜味剂产生偏好差异的主要原因[15-16]。然而,在针对小鼠的味觉测试中发现,蔗糖和非糖类甜味成分(甘氨酸或L-丝氨酸)同时存在时小鼠表现出对蔗糖的明显偏好[17]。48 h双瓶偏好实验结果也显示,实验过程中小鼠消耗的葡萄糖比L-丝氨酸多[18]。在对蔗糖和三氯蔗糖的对比研究中也发现了小鼠对蔗糖的偏好,经过饥饿训练的小鼠随着时间推移,取食蔗糖的次数明显增加[2]。虽然8%蔗糖溶液、0.3%甜菊糖苷溶液、10 mmol/L安赛蜜溶液、10 mmol/L三氯蔗糖溶液和10 mmol/L阿斯巴甜溶液均能引起小鼠明显的甜味偏好,但是面对甜度相同的蔗糖和安赛蜜溶液时,相同时间内小鼠对蔗糖的消耗量显著高于安赛蜜[19]。这种对糖和甜味剂的显著偏好差异在24 h内即可出现,而48 h后小鼠几乎只选择糖溶液,从而出现完全的选择倾向性[20]。
进而有研究者推断,这种对糖类和非糖类甜味物质的行为偏好差异有可能来自不同成分与甜味受体结合能力的差异[17]。然而,甜味受体的发现以及甜味感知机制的相关研究成果推翻了这一假设[21-25]。人类感知甜味的能力由异源二聚体——味觉受体第一家族成员(taste receptor family 1 member,T1R)2/T1R3介导,敲除T1R3能够去除小鼠感知甜味的能力[23,26-27]。Tan等[20]发现尽管T1R3敲除小鼠无法尝到糖和安赛蜜的甜味,但它们却依然能够在糖和安赛蜜之间倾向性地选择糖。分别将可引起野生小鼠最大偏好浓度的蔗糖、D-葡萄糖和3 种人工甜味剂(三氯蔗糖、安赛蜜和SC45647)溶液供给T1R3敲除小鼠时,48 h内小鼠对各溶液的行为偏好均消失;进一步将各溶液浓度提高到最大偏好浓度的5~10 倍时,T1R3敲除小鼠出现对蔗糖和D-葡萄糖的偏好,而对3 种人工甜味剂依然没有产生偏好;此外,在胃内输注蔗糖的同时,通过口腔供给小鼠风味溶液能使小鼠对风味溶液产生偏好,而将蔗糖替换为三氯蔗糖后,偏好则不能产生[28]。
瞬时受体电位离子通道蛋白5(transient receptor potential melastatin 5,TRPM5)、钙稳态调节蛋白(calcium homeostasis modulator,Calhm1)均是甜味信号的重要转导元素,敲除TRPM5、Calhm1基因同样可以阻断甜味信号的转导[29]。Zhang Yifeng等[30]发现敲除TRPM5小鼠对安赛蜜的偏好完全消失,而对于蔗糖和葡萄糖的舔舐次数虽有所降低,但仍然表现出行为偏好。类似的研究发现,TRPM5基因敲除小鼠保留了对蔗糖的偏好,但对三氯蔗糖的偏好消失[31]。Calhm1敲除小鼠每天消耗的蔗糖总量降低了一半,但依然形成了对蔗糖的偏好[32]。此外,以胃部灌注的方式对野生小鼠和TRPM5敲除小鼠分别进行蔗糖或三氯蔗糖刺激后,小鼠均仅对蔗糖产生偏好[2](图1)。

图1 糖和甜味剂的小鼠行为学差异Fig.1 Behavioral differences between sugars and sweeteners in mice
以上行为学实验结果表明,糖类和甜味剂均可使正常小鼠产生甜味偏好,但是相比于甜味剂,小鼠更偏爱糖;敲除小鼠的甜味受体基因或甜味信号转导基因均能阻断人工甜味剂诱发的行为偏好,但不能阻断其对糖的行为偏好。这些现象说明糖类和甜味剂使小鼠产生偏好的机制并不完全相同,存在一种不需要甜味受体参与、独立于味觉系统的神经机制调控糖偏好的形成。
1.2 糖类与甜味剂引发的动物脑区活动差异
早先人们认为肠道和大脑仅通过激素进行信号传递,激素信号可以独立于甜味感受刺激动物对糖的消费和偏好[33]。然而后来的研究表明,对胆囊收缩素A(小肠黏膜I细胞释放的一种肽类激素)受体的药理学抑制不会影响糖在胃内输注引发的偏好[34]。生长激素释放肽也曾被认为参与食物奖赏的过程,而Sclafani等[35]研究发现,生长激素释放肽受体敲除同样不会影响小鼠对糖的偏好,进而推翻了这一假设。
多项研究证明,大脑中DA释放引发的奖赏效应参与了糖类摄入的中枢反应[36-37]。在摄入糖后,能够监测到伏隔核区域DA的释放[38-40]。DA受体(D1和D2型受体)的药理学抑制也能抑制糖的摄入或消除胃内输注葡萄糖引发的条件性风味偏好[41-46]。DA信号也参与调节糖或其他营养物质如脂肪产生条件风味偏好的能力[47-49]。因此,糖引起DA奖赏环路响应是糖偏好的重要研究切入点。随着相关研究的深入,糖激活大脑释放DA的神经环路机制逐渐明晰。Mark等[50]发现胃内输注聚糖溶液可以诱发腹侧纹状体和背侧纹状体释放DA。口服和肠内输注蔗糖的研究结果均显示出中脑边缘系统和黑质纹状体系统神经元活性的增加和DA的释放[51]。研究表明,敲除TRPM5基因小鼠依然对胃内注射D-葡萄糖产生了强烈的偏好,并且30 min内检测到腹侧纹状体和背侧纹状体DA释放量增多;在胃部注射机体不可代谢的葡萄糖类似物同样能检测到DA的释放(虽然释放量有所降低),这种特异性偏好证明D-葡萄糖可以独立于味觉系统和能量产生行为偏好,并具有刺激腹侧纹状体和背侧纹状体释放DA的能力[52]。以上研究揭示了与糖信号有关的两条DA释放环路:第一条是中脑边缘系统,从腹侧被盖区(ventral tegmental area,VTA)投射到腹侧纹状体;第二条是黑质纹状体系统,从黑质致密部投射到背侧纹状体。口服和胃内输注蔗糖溶液均可激活上述两个环路神经元,促进DA释放[53]。
Tellez等[3]针对糖信号引起DA释放的进一步研究发现,这两条神经环路在感知糖和甜味剂的反应上存在差异:小鼠口腔摄入三氯蔗糖同时胃内输注三氯蔗糖或葡萄糖均可引起腹侧纹状体释放DA,然而只有胃内输注葡萄糖时才能引起背侧纹状体释放DA,这表明投射至背侧纹状体的DA神经元对糖具有选择敏感性;掺入苦味剂的三氯蔗糖溶液同时胃内输注葡萄糖能够抑制腹侧纹状体释放DA,而背侧纹状体仍有高水平的DA释放量,这也间接说明了黑质纹状体系统可能负责对糖产生奖赏反应,而中脑边缘系统可能负责对糖和甜味剂引发的甜味产生奖赏反应(图2)。Fernandes等[2]利用深脑钙成像技术监测胃内VTA多巴胺能神经元的活性,与胃内输注三氯蔗糖相比,胃内输注蔗糖可以在1~2 min内快速诱导VTA的DA神经元出现持续正向上调活性,这说明蔗糖胃内输注引发的感觉信号从肠道到大脑的传递是十分迅速的,肠-脑之间可能存在一条“信息高速公路”支撑糖引发的感觉信号传递。
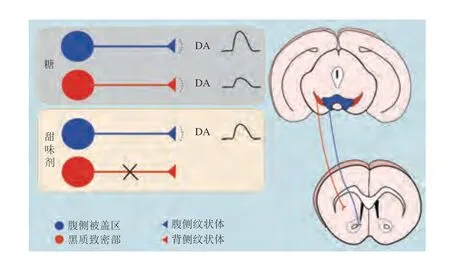
图2 糖和甜味剂感知的多巴胺能奖赏环路Fig.2 Dopaminergic reward circuits for sugar and sweetener perception
1.3 糖类与甜味剂引发的肠-脑轴神经激活模式差异
Bohórquez等[54]通过激光扫描共聚焦显微镜观察肠道内分泌细胞的神经纤维亚群时发现,一种特殊细胞亚群基部具有类似于神经元轴突的胞质突起,这些神经纤维亚群既可以作为吸收营养的平台,也可以作为分泌激素的启动平台。这些肠道内分泌细胞的发现为解释肠道和大脑的信号传导机制开辟了新的研究路径。该团队进一步研究发现肠道内分泌细胞与神经元之间的突触存在连接,这种突触之间的信号传递可能比血液中的激素释放信号更为直接,这些含有突起的肠道内分泌细胞被称为neuropod细胞;进一步追踪neuropod细胞的触体发现,这些细胞十分接近小肠和大肠的个别神经纤维,同时60%的neuropod细胞会接触感觉神经元,因此,推测这些neuropod细胞可能参与了肠道感觉信号的传递;狂犬病病毒通常被用作神经元单突触连接的可视化工具,狂犬病病毒示踪结果表明,结肠内的neuropod细胞能够被狂犬病毒成功感染,说明该病毒可以从肠道内腔到达神经系统,因此neuropod细胞和肠道神经元之间的确存在联系[55]。Kaelberer等[56]对neuropod细胞进一步研究发现,该细胞与迷走神经元之间形成的突触可以传递蔗糖或葡萄糖引发的信号:葡萄糖能够诱发neuropod细胞释放谷氨酸,并且可以引发迷走神经元的兴奋性突触后电流;沉默neuropod细胞后,葡萄糖输注诱导迷走神经在几毫秒内的快速放电则被完全消除。这些研究结果表明,大脑在几毫秒内接受来自肠道输入的糖刺激取决于neuropod细胞的谷氨酸能信号传递,然而这群细胞在糖偏好中的作用及机制至此仍未明确。
肠道中最主要的葡萄糖转运体是钠-葡萄糖共转运蛋白1(sodium-glucose cotransporter 1,SGLT1),在肠上皮细胞和肠内分泌表面均有表达。Kaelberer等[56]的研究证明SGLT1参与了葡萄糖或蔗糖刺激neuropod细胞释放神经递质谷氨酸的过程,抑制SGLT1会阻断谷氨酸的释放,而SGLT1对葡萄糖具有选择性,人工甜味剂并不能激活SGLT1。Tan等[20]从神经元活动的角度证明了SGLT1的激活能够激活对葡萄糖摄入响应的神经元,抑制SGLT1能够阻断对葡萄糖摄入偏好的形成。这些研究表明糖类摄入信号的肠-脑轴信号传递需要SGLT1参与。
Buchanan等[57]基于neuropod细胞和SGLT1受体深入研究了糖和人工甜味剂的偏好行为:近端小肠注入蔗糖、葡萄糖类似物和人工甜味剂均会快速引发迷走神经反应,沉默neuropod细胞后迷走神经反应相应消失,这表明3 类甜味物质引发的迷走神经反应均依赖于neuropod细胞。阻断SGLT1可消除蔗糖和葡萄糖类似物诱发的迷走神经反应,而阻断T1R3仅能消除人工甜味剂诱发的迷走神经反应;利用活体双光子成像和受体抑制实验确定了neuropod细胞分别通过释放谷氨酸和腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)两种不同的神经递质将蔗糖和人工甜味剂的肠道刺激传递到迷走神经的不同神经元亚群;分别提供给小鼠含有三氯蔗糖溶液和同等甜度的蔗糖溶液,小鼠表现出对蔗糖的偏好,抑制neuropod细胞或谷氨酸受体均会导致小鼠对蔗糖的偏好消失。以上研究表明,小鼠的糖偏好取决于neuropod细胞,neuropod细胞分别依赖SGLT1和甜味受体T1R3分辨出糖和人工甜味剂信号。糖类和人工甜味剂会刺激neuropod细胞分别释放谷氨酸和ATP作为神经递质,通过释放不同的神经递质激活迷走神经的不同神经元亚群,进而让大脑分辨糖和人工甜味剂。
孤束尾核(caudal portion of solitary tract nucleus,cNTS)是机体内部感知信号向大脑传递的中继器。研究表明,不同的cNTS神经元亚群可被十二指肠或胃内的葡萄糖或甲基-α-D-吡喃葡萄糖苷激活,而糖精则无法激活cNTS[58-59]。利用腺病毒携带的破伤风毒素阻断被糖激活的cNTS神经元突触传递功能后,小鼠对于糖的偏好消失,因此可以认为cNTS是小鼠对葡萄糖产生偏好的重要中继。切断双侧迷走神经可阻断cNTS神经元被激活,这表明糖摄入信号的传递需要通过迷走神经,进而通过迷走神经结状神经元传递信号并激活cNTS神经元[20]。
至此,糖类摄入信号在肠-脑轴传递的神经通路基本明晰,口腔摄入的糖类和甜味剂均能激活位于口腔的甜味受体细胞,将信息传递至中脑边缘DA系统刺激腹侧纹状体DA的释放。但进入胃和近端小肠(十二指肠)后,糖类和人工甜味剂则出现了明显差异。蔗糖或葡萄糖等能够与肠道内neuropod细胞表面SGLT1受体结合,neuropod细胞轴突释放谷氨酸激活迷走神经,迷走神经的结状神经元亚群通过单突触继续将糖摄入的信息传递到脑干cNTS神经元,进一步激活黑质纹状体系统背侧纹状体DA的释放。而人工甜味剂则与neuropod细胞表面的甜味受体T1R3结合,使neuropod细胞轴突释放神经递质ATP将信息传递到迷走神经,但并不引发脑干cNTS神经元的响应(图3)。因此,大脑可以辨别糖和甜味剂从而使个体表现出行为偏好的差异。
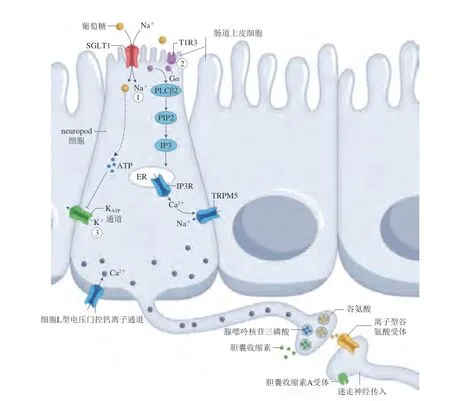
图3 肠道neuropod细胞识别糖和甜味剂的分子机制[53]Fig.3 Molecular mechanisms of discrimination between sugars and sweeteners by gut neuropod cells[53]
2 基于肠脑轴效应的甜味剂功能评估和创新研发的新方法
甜味剂和糖类的肠-脑轴效应差异是决定甜味剂能否产生长时程行为偏好的根本原因,这对于甜味剂的功能评估和创新研发意义重大。目前对是否所有的甜味剂都不能引发肠-脑轴效应尚未明确,同时新一代甜味剂研发更应该将引发肠-脑轴效应作为重要功能指标。因此,本文从3 个层面分别总结了甜味成分肠-脑轴效应相关的研究手段,提出了3 种可用于甜味剂肠-脑轴效应评估的方式,旨在为相关产业界开展甜味剂创新研发提供参考。
2.1 利用动物行为学表现的评估方式
行为学方法能够简便且直观地表征动物行为偏好。双瓶偏好实验是行为学研究中面对类似问题最常用的实验手段。例如利用野生小鼠、T1R3或TRPM5等基因敲除小鼠模型,并使用小鼠糖水偏好装置,通过监控相同时间内小鼠对含甜味剂溶液和糖溶液的消耗量或计算动物偏好指数(分析前100 次和后100 次动物舔舐甜味剂占总舔舐次数的百分比),即可有效量化小鼠对甜味剂的行为偏好。
行为学实验可以设计两种实施策略:一种是以野生小鼠为动物模型,监测野生小鼠在葡萄糖和甜味剂之间的偏好选择,如果小鼠在葡萄糖和甜味剂之间没有行为偏好,则反映甜味剂和葡萄糖同样具有激活肠-脑轴的能力(图4)。另一种是以T1R3或TRPM5等基因敲除小鼠为动物模型,监测小鼠在水和甜味剂之间的偏好选择。T1R3和TRPM5基因的敲除分别阻断了甜味感知和甜味信号传导的通路,小鼠依然能够形成对糖的偏好。因此,如果基因敲除小鼠形成了对甜味剂的偏好,即可反映该甜味剂具有激活肠-脑轴的能力。
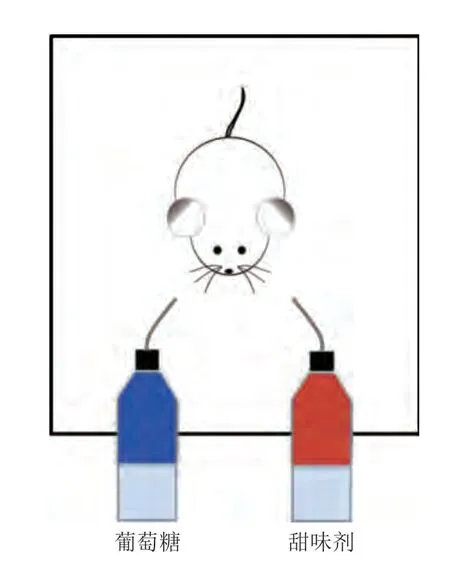
图4 双瓶偏好实验[18]Fig.4 Two-bottle preference experiment[18]
结合野生小鼠、T1R3敲除小鼠或TRPM5敲除小鼠等动物模型,利用双瓶偏好等行为学研究方法,能够从功能层面有效评估新型甜味剂激活肠-脑轴的能力。行为学实验具有设备要求低、实验操作简单、实验周期短等优势,是一种低成本高效率的甜味剂肠-脑轴激活能力评估方式。
2.2 利用脑区神经活动检测的评估方式
糖类可通过肠-脑轴激活中脑边缘系统和黑质纹状体系统释放DA产生奖赏效应;而人工甜味剂如三氯蔗糖等仅能通过口腔甜味受体激活中脑边缘系统产生奖赏效应。因此,可以通过黑质纹状体系统多巴胺能神经元的激活或DA的释放特征评估甜味剂是否具有激活肠-脑轴的能力。目前针对DA奖赏环路的研究较多,技术路线已经较为成熟。
DA神经元激活的研究方法常以DA受体标记(DATCre)的转基因小鼠为动物模型,结合立体定位仪和微量注射装置将能表征神经元活动的钙荧光指示剂注射到黑质致密部,将钙荧光蛋白特异性地表达在黑质致密部多巴胺能神经元上,利用光纤记录或双光子钙成像等技术手段监控胃内输注甜味剂后多巴胺能神经元(群体神经元或单个神经元)荧光强度的变化规律,从而反映甜味剂激活肠-脑轴的能力(图5)。通过cNTS神经元的激活也可以表征甜味剂是否具有激活肠-脑轴的能力,但孤束核位于脑干,相比于黑质纹状体系统实验操作难度较大。
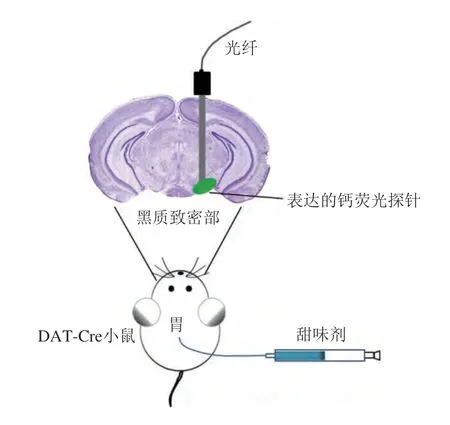
图5 以DAT-Cre小鼠为动物模型利用光纤记录甜味剂胃内输注后DA神经元的活性[2]Fig.5 DAT-Cre mice as an animal model for fiber optic recording of DA neuron activity after intragastric infusion of sweeteners[2]
通过检测黑质纹状体系统背侧纹状体区域DA的释放是奖赏环路研究另一个可选择的技术。以C57BL/6小鼠(实验室最常用的小鼠品系)为动物模型,将监测神经递质释放的DA探针表达在背侧纹状体神经元上,利用光纤记录手段,监控胃内输注甜味剂后代表性神经递质DA释放荧光强度的变化规律,进而反映甜味剂激活肠-脑轴的能力。
与行为学评估方法相比,利用脑区神经活动的评估方法能够更为直观地观察到脑区神经活动,更加客观地量化评价新型甜味剂肠-脑轴激活能力。但是,这些方法涉及到动物手术和脑区神经活动监控技术,对其及设备要求相对较高;同时,所使用的生物探针表达时间周期较长,实验的时间成本也相对较高。
2.3 利用关键受体激活能力的评估方式
SGLT1受体是糖类肠-脑轴信号产生的关键靶点,葡萄糖是SGLT1受体的特异性配体。葡萄糖通过与细胞表面的SGLT1受体结合可以引发胞内下游信号转导和细胞活性的增加,导致胞内钙离子浓度增高。近年来,受体蛋白的高效异源表达技术取得了巨大进步。异源表达细胞系统可以是人胚胎肾细胞(HEK-293)、幼仓鼠肾细胞(BHK)、绿猴肾细胞和中国仓鼠卵巢细胞(CHO)等[60-62]。当前已有研究成功构建了人胚胎肾细胞(HEK-293)SGLT家族中SGLT2基因异源表达体系[63]。因此,可以通过分子生物学技术构建SGLT1蛋白基因真核表达载体,向异源细胞系统插入表达SGLT1蛋白的基因,使细胞单一地表达SGLT1受体蛋白。进一步运用钙离子成像技术检测细胞内钙离子浓度的变化,给予甜味剂刺激后通过激光扫描共聚焦显微镜观察细胞荧光变化,从而评估甜味剂对SGLT1的激活能力。
此外,肠道neuropod细胞表达SGLT1蛋白,葡萄糖可特异性地结合SGLT1蛋白激活neuropod细胞释放谷氨酸[55,64]。因此可以通过甜味剂是否激活neuropod细胞释放谷氨酸评估甜味剂激活肠-脑轴的能力。例如将表达谷氨酸荧光探针(iGluSnFR)的细胞(如HEK-293、BHK细胞等)和neuropod细胞共培养后加入甜味剂,利用激光扫描共聚焦显微镜可以实时观察表达iGluSnFR细胞的荧光变化,以量化反映谷氨酸的释放情况,从而判断甜味剂是否具有激活肠-脑轴的能力(图6)。
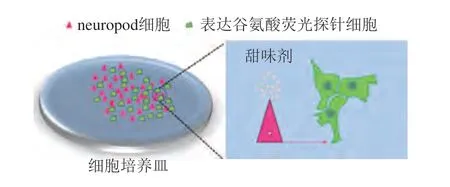
图6 Neuropod细胞和表达谷氨酸荧光探针细胞共培养[55]Fig.6 The co-culture of neuropod cells and cells expressing iGluSnFR[55]
测定关键靶点蛋白激活能力能从更深层的角度(受体、分子)评估甜味剂激活肠-脑轴的能力,所涉及技术方法依赖于构建稳定表达的异源SGLT1受体蛋白细胞株或从动物的肠道分离出neuropod细胞。细胞实验环境需要细胞培养间,并配备荧光共聚焦显微镜、细胞培养箱等一系列设备,同时要求实验人员具备专业的分子生物学技术背景和仪器操作技能。
3 结语
本文系统梳理了糖类与甜味剂引发的动物行为偏好差异、动物脑区活动差异和肠-脑轴神经激活模式差异3 个方面的研究进展,阐释了大脑可以辨别糖和甜味剂使个体表现出行为偏好差异的根本原因。基于肠-脑轴效应的宏观表现和内在机制,提出了利用动物行为学表现、脑区神经活动和关键受体激活能力3 种技术手段完善甜味剂功能评估体系的建议。关注甜味剂的肠-脑轴效应对于该领域的创新发展意义重大。
