芪丹颗粒联合盐酸二甲双胍对脾虚痰瘀型2型糖尿病患者胰岛素抵抗的影响
2024-05-17雷自红陈冬妮郭叙喜张越叶仁群
雷自红,陈冬妮,郭叙喜,张越,叶仁群
1. 广州中医药大学第七临床医学院,广东 深圳 518133
2. 深圳市宝安区中医院内分泌科,广东 深圳 518133
胰岛素抵抗(IR)是2 型糖尿病(T2DM)的发病因素之一,贯穿于T2DM 的病程始终,尤其是对于T2DM 伴肥胖的患者而言。体内慢性炎症反应与肥胖、IR,甚至T2DM 的发生密切相关[1-3]。其中脂肪组织存在的慢性低度炎症阻断了胰岛素信号转导通路,诱导IR 的发生;而同时IR 引起的高胰岛素血症又进一步加重IR 的程度,并使IR 逐步陷入恶性循环。改善脂肪组织的慢性炎症现已成为治疗以IR 为主的T2DM 的关键因素之一。因此,调控炎症因子成为研究IR 的核心环节[4],改善脂肪炎症反应将逐渐成为糖尿病治疗的新手段,常用的药物如噻唑烷二酮类、利拉鲁肽与二甲双胍等均具有抗炎作用[5-6]。有研究对脾虚痰瘀型T2DM 患者以健脾化痰、祛瘀通络为治法,证实了芪丹颗粒在改善IR 方面具有良好的疗效[7]。本研究在此基础上,进一步观察芪丹颗粒联合盐酸二甲双胍对脾虚痰瘀型T2DM 患者IR 及血清炎症因子的影响,报道如下。
1 临床资料
1.1 诊断标准符合文献[8]中T2DM 诊断标准。典型的糖尿病症状(多饮、多食、多尿和不明原因的体重下降)加上随机静脉血糖≥11.1 mmol/L;空腹静脉血糖≥7.0 mmol/L;口服葡萄糖耐量试验(OGTT)2 h静脉血糖≥11.1 mmo/L。符合上述条件中的任意1 项即可确诊,若无典型糖尿病症状者,需改日复查。
1.2 辨证标准符合脾虚痰瘀型辨证标准[9]。主症:形体肥胖;嗜食肥甘;脘腹满闷或胸闷刺痛;肢体麻木或沉重;次症:神倦懒言;气短乏力;头重眩晕;呕恶口黏;口干不欲饮;舌脉:舌质淡暗、苔白厚腻、有瘀点瘀斑、或舌下静脉迂曲青紫,脉沉滑或沉涩。符合3 项主症及3 项以上次症,结合舌脉即可辨为脾虚痰瘀证。
1.3 纳入标准符合上述诊断及辨证标准;年龄18~70 岁,健康状况良好,无严重既往病史,不限男女;根据自身的意愿参与本研究,并签署知情同意书。
1.4 排除标准1 型糖尿病;妊娠及哺乳期妇女;合并糖尿病急性并发症或严重的糖尿病慢性并发症;合并其他脏器如心、脑、肝、肾等严重病变;患有精神疾病或自行服用其他药物影响试验结果或依从性差无法配合研究。
1.5 一般资料选取2021 年12 月—2022 年12 月深圳市宝安区中医院内分泌科门诊及住院部就诊的100 例脾虚痰瘀型T2DM 患者,按随机数字表法分为对照组及治疗组各50 例。对照组男23 例,女27 例;平均年龄(47.36±7.89)岁;平均病程(4.59±2.42)年。治疗组男24 例,女26 例;平均年龄(50.98±7.76)年;平均病程(5.04±2.73)年。2 组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
2 治疗方法
对2组均进行糖尿病相关知识教育,包括患者饮食、运动、基础护理等;使用同种类降血糖药,排除使用双胍类、噻唑烷二酮类、相关含中药增敏成分制剂等胰岛素增敏剂,对于血压、血脂不达标者予以相同类别降压降脂治疗。
2.1 对照组盐酸二甲双胍(中美上海施贵宝制药有限公司,国药准字H20023370)治疗。每次0.5 g,每天2次,饭后口服。
2.2 治疗组在对照组基础上联合芪丹颗粒治疗,每次1 袋,每天2 次,分早、晚饭前温水200 mL 冲服。芪丹颗粒由深圳市宝安区中医院制剂室制备,剂型:颗粒剂;规格:每袋装18 g;制作方法:黄芪1 000 g,丹参、三七各800 g,山楂600 g,上药加水煎煮2 次,每次加10 倍量水,煎煮1.5 h,合并煎液,滤过,浓缩至相对密度1.05~1.10(60 ℃)的清膏,加入150 g 麦芽糊精,混匀,喷雾干燥。取干浸膏粉,加入适量麦芽糊精,混匀,干式制粒,整粒,制成1 000 g,分袋包装。
2组均治疗8周。
3 观察指标与统计学方法
3.1 观察指标①临床疗效。②中医证候积分。参照文献[9]拟定中医证候积分。按无、轻、中、重4个等级,主症分别计0、2、4、6分,次症分别计0、1、2、3分,对脾虚痰瘀型T2DM患者的主症和次症做总积分。总分分值42 分。③胰岛素抵抗指数(HOMAIR)、体质量指数(BMI)、腹围(AC)。IR 评估采用稳态HOMA-IR:空腹血糖[FBG(mmol/L)]×空腹胰岛素[FINS(mIU/L)] /22.5。BMI=体质量(kg)/身高平方(m2),并测量AC。④血脂总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HLD-C)。采用全自动生化分析仪测定TC、TG、LDL-C、HLD-C。⑤血清核因子-κB(NF-κB)、肿瘤坏死因子-α(TNF-α)。双抗体夹心酶联免疫吸附试验(ELISA 法)测定血清NF-κB 及TNF-α 水平,ELISA 试剂盒分别由江莱生物和博士德公司生产,编号分别为JL46013和EK0525 H。
3.2 统计学方法应用SPSS21.0 统计学软件进行数据分析。计量资料以均数±标准差(±s)表示,组内比较采用配对样本t检验,组间比较采用独立样本t检验;计数资料以百分比(%)表示,采用χ2检验。P<0.05表示差异有统计学意义。
4 疗效标准与治疗结果
4.1 疗效标准显效:中医证候积分减少率≥70%,临床症状和体征明显改善;有效:30%≤中医证候积分减少率<70%,但未达到显效标准,临床症状和体征有改善;无效:中医证候积分减少率<30%或升高,临床症状和体征无明显改善甚或加重。
4.2 2 组临床疗效比较见表1。治疗后,对照组与治疗组总有效率分别为80.00%、94.00%,2组临床疗效比较,差异有统计学意义(P<0.05)。
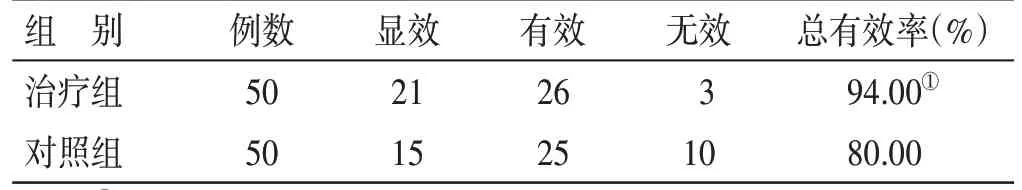
表1 2组临床疗效比较 例
4.3 2 组治疗前后中医证候积分比较见表2。治疗前,2组中医证候积分比较,差异无统计学意义(P>0.05)。治疗后,2 组中医证候积分均较治疗前下降(P<0.05),治疗组中医证候积分低于对照组(P<0.05)。
表2 2组治疗前后中医证候积分比较(± s) 分

表2 2组治疗前后中医证候积分比较(± s) 分
注:①与本组治疗前比较,P<0.05;②与对照组治疗后比较,P<0.05
治疗后5.12 ± 1.90①②7.44 ± 2.02①组 别治疗组对照组例数50 50治疗前12.32 ± 2.11 12.08 ± 2.15
4.4 2 组治疗前后HOMA-IR、BMI、AC 指标值比较见表3。治疗前,2组HOMA-IR、BMI、AC指标值比较,差异无统计学意义(P>0.05)。治疗后,2 组HOMA-IR、BMI、AC指标值均较治疗前下降(P<0.05),治疗组HOMA-IR、BMI、AC指标值均低于对照组(P<0.05)。
表3 2组治疗前后HOMA-IR、BMI、AC指标值比较(± s)

表3 2组治疗前后HOMA-IR、BMI、AC指标值比较(± s)
注:①与本组治疗前比较,P<0.05;②与对照组治疗后比较,P<0.05
AC(cm)96.86 ± 8.09 81.34 ± 5.86①②96.26 ± 7.02 89.74 ± 5.39①组 别治疗组对照组时 间治疗前治疗后治疗前治疗后例数50 50 50 50 HOMA-IR 5.69 ± 0.98 3.87 ± 1.06①②5.87 ± 1.07 4.29 ± 0.98①BMI 25.25 ± 3.23 22.61 ± 2.69①②25.10. ± 3.09 23.72 ± 2.79①
4.5 2 组治疗前后TC、TG、LDL-C、HDL-C 水平比较见表4。治疗前,2 组TC、TG、LDL-C、HDL-C 水平比较,差异无统计学意义(P>0.05)。治疗后,2 组TC、TG、LDL-C 水平均较治疗前下降(P<0.05),HLD-C 水平均较治疗前上升(P<0.05);治疗组TC、TG、LDL-C 水平均低于对照组,差异有统计学意义(P<0.05),HDL-C 水平与对照组比较,差异无统计学意义(P>0.05)。
表4 2组治疗前后TC、TG、LDL-C、HDL-C水平比较(± s) mmol/L

表4 2组治疗前后TC、TG、LDL-C、HDL-C水平比较(± s) mmol/L
注:①与本组治疗前比较,P<0.05;②与对照组治疗后比较,P<0.05
HDL-C 0.89 ± 0.09 1.13 ± 0.17①0.94 ± 0.09 1.08 ± 0.10①组 别治疗组对照组时 间治疗前治疗后治疗前治疗后例数50 50 50 50 TC 5.12 ± 0.68 3.91 ± 0.39①②5.24 ± 0.72 4.62 ± 0.55①TG 3.04 ± 0.33 1.90 ± 0.22①②2.95 ± 0.42 2.27 ± 0.17①LDL-C 3.33 ± 0.68 2.10 ± 0.52①②3.43 ± 0.62 2.90 ± 0.56①
4.6 2 组治疗前后血清NF-κB、TNF-α 水平比较见表5。治疗前,2组血清NF-κB、TNF-α水平比较,差异无统计学意义(P>0.05)。治疗后,2 组血清NF-κB、TNF-α 水平均较治疗前下降,治疗组血清NF-κB、TNF-α 治疗前后比较,差异有统计学意义(P<0.05);治疗组血清NF-κB、TNF-α 水平均低于对照组(P<0.05)。
表5 2组治疗前后血清NF-κB、TNF-α水平比较(± s) pg/mL
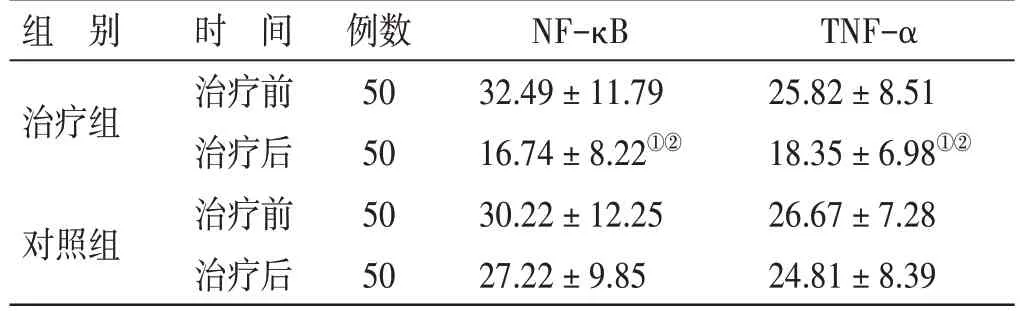
表5 2组治疗前后血清NF-κB、TNF-α水平比较(± s) pg/mL
注:①与本组治疗前比较,P<0.05;②与对照组治疗后比较,P<0.05
TNF-α 25.82 ± 8.51 18.35 ± 6.98①②26.67 ± 7.28 24.81 ± 8.39组 别治疗组对照组时 间治疗前治疗后治疗前治疗后例数50 50 50 50 NF-κB 32.49 ± 11.79 16.74 ± 8.22①②30.22 ± 12.25 27.22 ± 9.85
5 讨论
IR 的发病机制较为复杂,有研究表明,IR 的发生是一个慢性炎症过程,炎症成为肥胖与IR 的桥梁,身体在慢性炎症状态下,白色脂肪组织中脂肪细胞及巨噬细胞分泌多种炎症因子,如白细胞介素-6(IL-6)、TNF-α等[10]。这些炎症因子以自分泌、旁分泌、内分泌的形式,主要通过NF-κB 信号通路、c-Jun 氨基末端激酶(JNK)途径和双链RNA 依赖的蛋白激酶R(PKR)途径等信号转导通路抑制胰岛素信号转导,最终导致肥胖及IR 的发生发展。而其中NF-κB 信号通路是目前研究中炎症参与IR 和肥胖病发病的经典信号通路。
游离脂肪酸(FFA)作为一种脂肪因子,是脂质代谢的中间产物,其对机体能量调节、胰岛素敏感性调节及对糖脂代谢调节有一定作用。当机体摄入能量过多时,FFA为机体提供必要的能量,剩余的FFA则以脂肪的形式进行储存,当下表现为肥胖,但当机体不能耐受过多的脂肪时,脂代谢失代偿,大量的脂肪酸被释放出来,表现其脂毒性,通过启动氧化应激、线粒体自噬、炎症反应等,导致胰岛细胞的凋亡及胰岛素分泌障碍,机体对胰岛素的敏感性降低,对葡萄糖的摄取和利用受阻,促进糖原分解、糖异生,进而导致糖代谢异常,诱发IR 及糖尿病的产生。IR、T2DM 与机体内低度慢性弥漫性炎症浸润密切相关。机体内过多的FFA 能刺激TNF-α 和白细胞介素-8(IL-8)等炎症因子产生,引起炎症信号转导级联反应,激活多条炎症通路,如Toll 样受体4(TLR4)、IκB 激酶β(IKKβ)/NF-κB、JNK1 和NOD样受体P3 炎症通路等,导致靶细胞、靶器官炎症浸润,对胰岛素刺激应答障碍,胰岛素敏感性及传导受阻,糖代谢紊乱。FFA作为糖异生的底物之一,其过多的蓄积会促进糖异生的发生,同时,FFA导致的炎症因子表达上调,亦可通过上调糖异生限速酶(PEPCK)、葡萄糖-6-磷酸酶(G-6-Pase)等的表达来促进糖异生。
T2DM与IR可归属于中医消渴、脾瘅、肥胖等范畴。病因病机为过食肥甘厚味,致使脾胃虚弱,脾虚运化失常,中焦气机升降失调,津液输布异常,水液停聚,聚而成湿,停而为痰,水停痰聚,困阻气血运行,血停为瘀;痰浊瘀血积聚日久,形成肥胖,渐而发为脾瘅,最终转为消渴。由此可见脾虚湿盛为其病机关键,痰瘀内生是其重要病理因素。临床上,该类患者多摄食肥甘厚味,形体肥胖,皮肤可见紫纹,皆为脾虚而痰湿困阻,痰瘀互结的表现。根据以上病因病机,本研究以健脾化痰、袪瘀通络为基本治法,联合自制芪丹颗粒来治疗。方中黄芪健脾益气,恢复脾胃运化功能,中焦气机升降正常,津液得以输布,三七、丹参活血祛瘀通络,山楂消食健胃,化痰通络,与三七、丹参共同起到活血化痰通络,清除痰、瘀病理产物,标本兼顾,契合脾虚痰瘀病机,故而能健脾化痰、祛瘀通络。黄芪治疗IR 关联性较强的药物活性成份是槲皮素,实验研究表明,槲皮素可能通过调节AMPK/SIRT1/NF-κB 信号通路抑制氧化应激和炎症反应来改善IR、调控血糖水平[11]。丹参具有活血调经,祛瘀止痛功效,其有效成分丹参酮ⅡA 可有效降低T2DM 大鼠的血脂及炎症因子如IL-8、TNF-α 和IL-6 水平,改善机体炎症浸润状态,调节糖脂代谢情况,改善机体IR[12-13]。三七具有活血消肿止痛的功效,其有效成分包括槲皮素、豆甾醇、人参皂苷Rg1、三七皂苷R1等与信号转导和转录激活因子3(STAT3)、白细胞介素-2(IL-2)等基因相关性较强,可调控其蛋白表达,参与炎症信号通路传导,发挥其改善IR 的作用[14]。山楂健胃、行气散瘀、化浊降脂,山楂原花青素是山楂的有效成分之一,实验表明,山楂原花青素能通过阻碍磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(AKT)/NF-κB 通路信号传导,抑制NF-κB 活性,降低促炎因子表达水平,改善机体慢性低度炎症状态,调节糖脂代谢,改善IR[15]。
本研究结果显示,芪丹颗粒联合盐酸二甲双胍治疗脾虚痰瘀型T2DM 有效,在降低患者BMI、腹围、HOMA-IR 指数、血脂、血清NF-κB及TNF-α水平上均优于对照组(P<0.05),能改善患者IR,其可能通过减少促炎因子TNF-α 的分泌来抑制NF-κB 信号通路表达,改善脂肪组织的炎症刺激,减轻对胰岛素信号转导的抑制,进而达到改善IR 的目的。TNF-α 还可以通过下调脂联素水平并表现出与抵抗素一致的作用来逐步介导IR,本研究证实联合芪丹颗粒可降低TNF-α 的合成分泌,该结论与前期研究中芪丹颗粒可通过升高血清脂联素、降低抵抗素水平来改善IR的结论一致[7]。
综上,芪丹颗粒联合盐酸二甲双胍能改善脾虚痰瘀型T2DM 患者的IR,下调血清NF-κB、TNF-α水平,改善脂肪组织的炎症反应,缓解临床症状。
