综合保温护理对新生儿坏死性小肠结肠炎围手术期低体温和术后并发症的影响
2024-05-16张永倩刘红梅高丽娜郭倩倩邢民者
张永倩 刘红梅 高丽娜 郭倩倩 邢民者
新生儿坏死性小肠结肠炎(necrotizing enterocolitis of newborn,NEC)是一种严重威胁新生儿生命的肠道疾病,而且90%~95%发生于胎龄<36周的早产儿,新生儿皮下脂肪少,而体表面积与体重之比相对较大,散热速度比较快,而且体温中枢还没有完全发育[1]。此外新生儿抵抗力很弱,无有效调节和维持恒温的能力,体温也会受到外界环境的影响而发生变化[2]。同时,由于层流手术室的常温和所使用的空气对流模式,也会使身体的散热性增大。因为新生儿的手术均为全麻,随着麻醉剂的用量,会出现不同的体温变化,所以新生儿的血管收缩和寒颤是出汗时的3倍[3]。在手术之前,对皮肤进行消毒也会降低体温,而且在手术的时候,需要打开腹腔,这样会加快身体的温度下降。而围手术期体温降低又与多种并发症关系密切,包含心血管事件增加、药物代谢减慢、苏醒时间延长、凝血功能障碍、手术部位感染、住院时间延长等。成人方面主要是通过一系列被证实有效的护理干预措施用于患者围手术期护理中,并联合各种器材起到减轻手术应激反应的目的,减少低体温发生,积极预防或减少并发症,促进术后尽快康复[4-5]。新生儿和成人的围手术期综合保温体系护理研究内容总体相似,可分为术前、术中和术后3个阶段[6-7]。本研究以本院的NEC患儿为例,探讨综合护理干预对NEC患儿的协助作用,为NEC患者临床工作的开展提供参考。
1 资料与方法
1.1 一般资料 前瞻性选择2020年6月至2023年6月河北省儿童医院行新生儿坏死性小肠结肠炎病例60例,经过伦理委员会通过,签订知情同意书。入院后按数字随机分组的方式随机分为综合保温体系护理组(观察组)和常规保温组(对照组),每组30例。
1.2 纳入与排除标准
1.2.1 纳入标准:①日龄≤28 d;②符合新生儿坏死性小肠结肠炎诊断具备手术治疗指征者[8]。
1.2.2 排除标准:①合并先天性心脏病者、先天性消化道畸形者;②存在多器官功能衰竭者、合并重症急性感染者。
1.3 方法
1.3.1 常规保温组:在术前将室内温度调整到24~26℃,相对湿度控制在50%~60%,并将恒温水毯的温度调整到38~40℃,直至手术完成。缩短灭菌时间,为新生儿进行各项操作,尽可能减少无谓的接触。合理应用消毒液的用量,避免浸湿床单位。限制室内人员出入,保持手术室的温度比较稳定。
1.3.2 综合保温体系护理组
1.3.2.1 术前:除上述措施外,采取患儿入手术室前30 min调节室温27~29℃,打开充气加温仪至38℃,进行预温,接手术前通知病房护士,预加温转运患儿所需的被褥,转运至手术室途中应用40℃温盐水袋持续保温。
1.3.2.2 术中:入手术间后将患儿放入恒温水毯上并充气加温仪覆盖患儿,再覆盖预热棉被。消毒时将充气加温仪撤至下肢,避开消毒区域。头部包裹铺预加温无菌单,避免头部散热。手术结束前30 min,通知病房,调节室温27~29℃,预热保温箱,做好接收患儿准备。
1.3.2.3 术后:①麻醉苏醒期护理:拔除气管导管后,容易造成咽喉部水肿,造成气道阻塞,故应注意气道的通畅。手术结束后,患儿取下气管插管,用11000氢化可的松喷喉,15 min/次,连喷3次。在此期间,患儿应采取平躺的姿势,将头部倾斜到一侧,在肩膀下面垫上一个柔软的枕头,以便及时将鼻腔里的液体排出。观察患儿的血氧饱和度,观察患儿的呼吸、面色、肢体循环等情况,直至患儿完全苏醒。②保持体温恒定:术后给予辐射台保暖,床温28~32℃。每2~4小时测体温1次,体温>39℃时,采取降低辐射台床温,松解衣被或温水擦浴,避免使用药物降温,使体温维持在36.5~37.59℃。③维持水、电解质、酸碱平衡:在禁食的过程中,血液进行电解质和血气检测,要及时补充钾、钠、氯、钙等电解质,防止出现失衡。还要适当补充碳酸氢钠缓解酸中毒。每日以总液量为依据,制定输液计划,对输液顺序、滴速等做出合理的安排,还要考虑到抗生素滴入的时效性,并精确记录输入的排出量,确保能够实现治疗目标,使1 d内的液体能够均匀地滴入。④继续禁食和胃肠减压:在手术结束后,要坚持禁食和胃肠减压,要保证胃管通畅,不能打折,扭曲或者受压。如患儿出现呕吐、引流量减少,说明胃管不畅,需要使用注射器抽吸来调整胃管的深浅度,并准确地记录24 h内的引流量、颜色、性质。⑤预防感染:保持病室空气新鲜,温湿度适宜,口腔护理2次/d,保持患儿皮肤清洁干燥,勤换尿布,防止尿液浸湿伤口敷料,避免交叉感染,缩短病儿住院时间。⑥肠造瘘口的护理:每天都要定期换药,观察造口肠管的颜色和是否有回缩现象。通常情况下,术后48~72 h即可打开造口器。要注意造口周围皮肤的清洁和干燥,可以外用复方氧化锌油膏,起到预防皮肤糜烂的作用。
1.4 观察指标 (1)术中持续监测患儿核心体温,监测时间点分别为术前、术中30、60、90 min和术毕。(2)观察2组新生儿术后并发症:心率增快、苏醒期寒战、低氧血症、切口感染等。(3)观察2组新生儿的治疗效果、住院时间以及家属护理满意度评分。
1.5 疗效标准 干预后患儿肠道功能得到完全改善,伴有的腹胀、便血等不良症状完全消失,疗效为显效;干预后患儿肠道功能较干预前明显改善,伴有的腹胀、便血等不良症状较 治疗前明显减轻,疗效为有效;患儿未达到前述等级标准,疗效为无效。总有效率=(痊愈+显效)/总例数×100%。
2 结果
2.1 2组患儿术前、术中、术毕体温比较 术前2组患儿差异无统计学意义(P>0.05),术中及术毕2组患儿体温差异明显(P<0.05),且观察组患儿体温要高于对照组(P<0.05)。见表1。

表1 2组新生儿术前、术中、术毕体温比较 n=30,℃,
2.2 2组患儿并发症发生情况比较 试验组患儿切口感染、寒战、心率增快、低氧血症等并发症发生率均
低于对照组(P<0.05)。见表2。

表2 2组患儿并发症发生情况比较 n=30,例(%)
2.3 2组患儿治疗效果比较 2组NEC患儿治疗效果差异无统计学意义(P>0.05)。见表3。
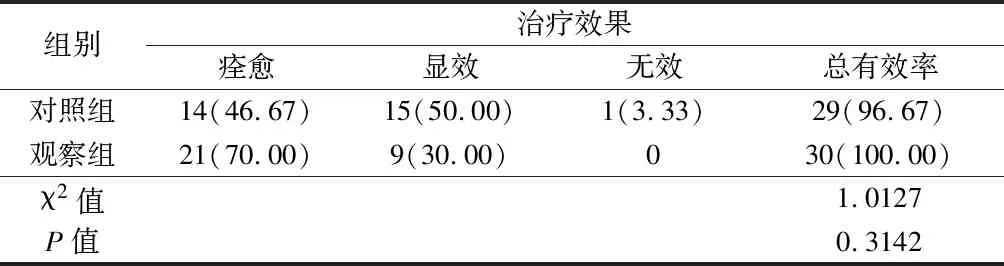
表3 2组患儿治疗效果比较 n=30,例(%)
2.4 2组患儿住院时间以及家属护理满意度评分对比 观察组患儿的家属对患儿的照顾满意程度明显高于对照组,住院天数明显少于对照组,差异均有统计学意义(P<0.05)。见表4。

表4 2组患儿住院时间以及家属护理满意度评分比较 n=30,
3 讨论
NEC是一种以肠道黏膜损伤为主要特征的继发性疾病,其病理特征是肠道黏膜缺血缺氧,导致小肠及结肠出现弥漫性或局灶性坏死。NEC常见于早产儿或者是刚出生的婴儿身上,表现为腹胀、便血,临床特征是肠道黏膜和肠道深层组织的坏死,多发生在回肠远端和结肠近端,而很少发生在小肠。部分儿童的腹透平片表现为小肠壁上的囊状积气。从临床看,NEC多呈散发,没有明显的季节变化,新生儿的排泄物也是正常的,发病时间一般在出生后2~3周,发病高峰期在出生后2~10 d;此外,男性NEC患儿要多于女性[9]。NEC有以下几种常见临床表现:(1)患儿出现腹胀,肠鸣音减弱的现象。病情不严重表现为腹胀,病情严重不仅有腹胀还会伴有肠鸣音减弱甚至消失的现象[10-11]。(2)患儿出现呕吐。(3)患儿出现腹泻、血便。有的新生儿的粪便没有明显的腹泻、血便,只有粪便中的隐血。(4)全身性表现。NEC患儿常见的症状有酸中毒、黄疸加重、休克等[12-13]。早产、缺氧、细菌感染等原因都会导致NEC。且该病病情进展快,对患儿的健康影响很大,甚至会危及生命,NEC也是导致新生儿死亡的主因[14-15]。
由于这类疾病和对象的特殊性,除了有针对性的治疗之外,还需要通过护理介入来对治疗效果进行进一步的优化[16]。梁银华等[17]对新生儿在腹腔外科手术中防止术中低体温的集束化护理应用进行了总结,与传统的围手术期护理措施相比较护理经过部分改良优化更符合新生儿手术患儿的需要,在新生儿腹部手术围手术期的护理过程中,综合保温能够安全、有效地降低儿童的心理、生理应激反应,加快儿童的康复进程,还能有效地提升儿童家属对护理工作的满意度。刘梅[18]报告了综合保温系统在新生儿剖腹手术中对低温的预防作用,综合保温系统的围手术期管理可以显著地减少患者的平均住院时间和术后并发症的发生,并提升了患者的家庭满意度。综合保温体系在NEC围手术期低体温预防研究国内未见报道。以往的常规护理在护理内容上具有盲目性和被动性,造成了护理效果不佳。目前,护理工作的质量和水平都得到了很大的提高,护理工作必须围绕护理流程进行,保证了护理的全面化、系统化。综合护理的出现弥补了常规护理的不足之处,使其护理效果得到增强,改善了患儿的预后。有相关研究证实,对NEC患儿进行有效的护理干预,可以使儿童的状况得到改善,生活质量得到提高,并且可以降低并发症的发生率[19-21]。上述结果本研究一致。
目前省内NEC率逐年增高,儿童医院外科医疗资源相对短缺,通过把综合保温体系护理理念应用在NEC手术的研究,采用综合保温体系减少新生儿死亡率,减少术后并发症,节省医疗资源,更大程度减少手术对新生儿的创伤,有助于加速新生儿的术后恢复,提高国内整体医疗水平。另外一方面减少新生儿住院时间和手术费用,具有重要的经济价值和社会价值。
