口服碳水化合物联合加速康复外科模式对结直肠癌患者围术期康复效果的影响
2024-05-16岳磊段佳文张志生孔令霞
岳磊 段佳文 张志生 孔令霞
结直肠癌与其他恶性肿瘤一样,发病原因尚未完全弄清,结肠或直肠的任何部位均可发生。据统计[1],本病的全球年病死人数居癌症死因的第2位,年约死亡88万,国内年约死亡率占全球的39.50%以上(年约病死人数为34.8万),老年人群患病率上升趋势明显,较非老年人群更高[2]。手术是延长本病患者生存期限最有效的方法,但结合实际情况来看,无论是传统手术方法,还是高清镜头下的腹腔镜手术方法,术后均有可能出现不同程度的胃肠功能障碍。学者证实,术后肠麻痹(postoperative ileus,POI)发生率高达1/8[3]。故为提升围手术期康复效果,降低其并发症、不良反应,维持肠粘膜屏障结构的完整性,抑制病原菌入侵与定居,采取必要的围手术期康复干预极为关键。熊照玉等[4]发现,术前实施预防性的碳水化合物(口服)干预可有效改善本病患者的术后胰岛素抵抗,王治国等[5]证实,在ERAS模式下实施术前口服碳水化合物干预则可促进胰岛素释放,改善氮平衡,对术后胰岛素抵抗改善有益。荟萃分析(meta)认为碳水化合物(围手术期)的安全性与有效性良好[6]。而梁德森等[7]证实,ERAS模式下的碳水化合物干预可有效缩短术后首次排气时间、住院天数,减少医疗费用支出。故本文将以联合干预的方式,探索口服碳水化合物+ERAS模式在本病围手术期康复干预中的临床疗效。报道如下。
1 资料与方法
1.1 一般资料 选取本院肿瘤科2019年1月至2021年1月收治的结直肠癌73例。随机分为口服碳水化合物组(A组36例)和口服碳水化合物+ERAS模式组(B组37例)。A组36例,男23例,女13例;年龄20~75岁,平均年龄(56.57±5.67)岁;观察组37例,男22例,女15例;年龄20~75岁,平均年龄(56.50±56.23)岁;2组年龄、性别比差异无统计学意义(P>0.05),具有可比性。诊断标准按《中国结直肠癌肝转移诊断和综合治疗指南(2020年版)》和《中国结直肠癌诊疗规范(2020年版)》拟定与执行[8-9]。课题符合《赫尔辛基宣言》[10]医学研究准则。
1.2 纳入与排除标准
1.2.1 纳入标准:①术前病理学、影像学(未发现远处血液及周围淋巴结转移)确诊为结直肠癌者;②满足手术耐受及麻醉适应证者;③术前葡萄糖耐量、空腹血糖实验正常者;④签署《知情同意书》且各项临床资料完整、有效、无残缺、破损者。
1.2.2 排除标准:①既往有结直肠癌相关放疗、化疗者;②入组前正在接受抑酸剂或免疫制剂治疗者;③结直肠癌远处转移或周围淋巴结转移者;④合并心脑血管及高血压、糖尿病、低白蛋白血症等基础性疾病者;⑤肝肾功能不全、营养不良者。
1.3 方法
1.3.1 A组:口服碳水化合物。术前1 d配伍,溶液配制配方:碳水化合物溶液(购自荷兰纽迪希亚公司)含葡萄糖、果糖、麦芽糖及多聚糖(每100 mL)各0.2、1.3、0.7、10 g;钠及钾、氯、钙、磷等微量元素(每100毫升)各0.05、0.122、0.006、0.001、0.001 g,pHWFHG为4.9。配伍完成后在特殊环境下灭菌(120~125℃,灭菌时间:0.5 h)处理,并放置在4℃环境下保存。肠道准备:术前以半流质(3~5 d)、流质(1~3 d)饮食为主,手术前1晚进行必要的灌肠[药物:复方聚乙二醇电解质散,舒泰神(北京)生物制药股份有限公司生产,批准文号:国药准字H20040034]处理。术前禁食(12 h)、禁水(8 h),术前3 h左右在医务人员的指导下口服碳水化合物(共6次)。注意事项:术中补液时,均不加葡萄糖和胰岛素。
1.3.2 B组:口服碳水化合物+ERAS模式。术前口服碳水化合物,方法同A组。ERAS模式:成立ERAS小组,以循证医学为依据,减少手术创伤及应激为核心,开展各项围手术期康复工作。首先,所有病患入组后建立QQ、微信等为主的现代信息交流平台,用于ERAS模式干预期间各项康复活动的监督与指导。其次,建立围手术期碳水化合物(口服)管护方案。联合操作如下:①评估与宣教:手术前1 d评估手术风险及病患耐受性,加强术前(手术风险与耐受性、肠道准备、禁食禁饮、麻醉用药、预防性使用抗生素、麻醉方案、手术方式等)、术中(生命体征监测、鼻胃管放置、避免术中低温、液体治疗、腹腔及尿道引流等)、术后(恶心及呕吐治疗、止痛、预防肠麻痹及促进胃肠蠕动、营养治疗、早期下床活动、出院标准、随访及结构品谷)宣教以促进术后康复。禁食禁饮:以个性化禁食禁饮为主,对无胃肠道动力障碍者,麻醉前6 h左右可适当的进食固体饮食,麻醉前2 h左右进食清流质食物;术前12 h左右口服碳水化合物(800 mL),术前2~3 h口服碳水化合物(400 mL)或水、茶、咖啡及果汁等纯液体,以减轻病患围手术期的烦躁、饥饿、口渴,降低潜在的术后胰岛素抵抗、高血糖及并发症等;术前1 h或术后清醒后可适当选用中医穴位按摩,如睛明、攒竹、合谷、太阳、承泣、风府、涌泉等穴,运动频率:4次/节,8拍/次,时间15 min,以消除身体疲劳、减缓压力等。②术后营养:尽量减少术后禁食,开展必要适当的早期场内灌食,预防术后感染,缩短住院时间。为降低术后肠麻痹风险,需辅助以必要的营养干预,术后4 h鼓励病患口服辅助进食(根据胃肠耐受量加减),促进机体氮平衡,减少术后高血糖发生率。③术后早期下床活动:为降低病患术后胰岛素抵抗及肌肉丢失,术后需避免长期卧床,完成术后止痛(NSAIDs)的同时,根据病患客观情况开展早期运动:床上运动:以缓慢运动为主,包括平躺与病床上做四肢向上运动,左侧、右侧翻身及高抬腿(抬高幅度:30°)及缓慢坐起等常规有氧运动,连续做完上述运动为1组,耗时3~5 min,1~3组/d。床边坐位:床边站立5 min后沿床旁缓慢行走,或床边坐位排便、穿衣、洗漱等模拟训练,逐步过度至病室内行走。病室内行走:5~10 min/次,2~3次/d,运动强度、次数、持续时间由弱到强、由少到多、由短至长,过度至病室走廊内散步和上楼梯(1~2层),以增强病患肌肉力量,促进康复。④出院随访:病患出院后24~48 h内进行必须进行电话随访及指导,督促其术后7~10 d来院进行必要的病理检查与评估,为抗肿瘤治疗的进一步开展提供依据。ERAS随访持续至术后1个月及以上。
1.4 观察指标
1.4.1 胃肠功能指标:采用酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)法检测手术前1天及术后第1、3、7天时的胃动素(motilin,MTL)、胰岛素样生长因子-1(Insulin-like growth factor 1,IGF-1)、二胺氧化酶(Diamine Oxidase,DAO)表达。
1.4.2 主观舒适度:含口渴、饥饿、焦虑等三项,用0~3分积分法评估,得分越高口渴、饥饿、焦虑越显著。见表1。

表1 主观舒适度评分
1.4.3 术后康复指标:首次排气时间、首次进食时间、术后住院时间。
1.4.4 术后并发症:观察项目包括肠麻痹、切口感染、吻合口瘘。
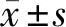
2 结果
2.1 2组MTL、IGF-1、DAO表达比较 A组手术后1、3 d时的MTL低于B组,7 d时的MTL高于B组(P<0.05);A组手术后1 d时的IGF-1低于B组,3、7 d时的IGF-1高于B组(P<0.05);A组手术后1、3 d时的DAO高于B组(P<0.05);2组组内手术前后的MTL、IGF-1、DAO相比差异显著(P<0.05)。2组其他时间段的MTL、IGF-1、DAO相比差异无统计学意义(P>0.05)。见表2。

表2 2组MTL、IGF-1、DAO表达比较
2.2 2组口渴、饥饿、焦虑等主观舒适度评分比较 A组的口渴、饥饿、焦虑等主观舒适度评分较B组更高(P<0.05)。见表3。

表3 2组口渴、饥饿、焦虑等主观舒适度评分比较 分,
2.3 2组术后并发症比较 A组术后总并发症发生率为27.78%(10.36),B组为13.51%(5/37),A组术后总并发症发生率显著高于B组(χ2=6.215,P=
0.013)。见表4。

表4 2组术后并发症比较 例(%)
3 讨论
作为一种新的理念与治疗康复模式,ERAS的获益主要体现在:加速病患临床康复,提高临床疗效,缩短住院时间,降低医疗费用、减轻社会及病患家庭负担。通过检索既往文献不难发现,ERAS模式对提升消化系统疾病患者的围手术期康复效果极有益处,如黄升等[11]发现,术后ERAS模式管理科有效提高胃十二指肠穿孔急诊患者的口服碳水化合物利用率。国外研究数据佐证,接受ERAS模式干预的结直肠癌患者的术后并发症、死亡率均非ERAS模式的结直肠癌患者相比更低(P<0.05),但需注意的是,ERAS模式应用效果的好坏,与麻醉科、外科等多学科通力合作密切相关。
对结直肠癌患者而言,术前禁食是目前国内医院常用的常规处理方法之一,原因在于术前胃排空对降低术后胃反流和误吸等并发症。
但近年来的研究证实,术前禁食是缺乏循证医学证据的,首先,固态食物的摄入有可能增加麻醉意外风险,其次,术前禁食虽然符合昼夜生物节律,对降低术后感染,减轻术前胃肠道负担有益。但从本研究结果来看,A组的各项临床治疗与B组相比更差:(1)手术前后的MTL、IGF-1、DAO表达低于B组,(2)主观舒适度评分(口渴、饥饿、焦虑)较B组偏高,(3)术后并发症较B组更高。此结果与既往研究[12]相近,提示术前口服碳水化合物联合ERAS模式可促进结直肠癌患者围手术期胃肠功能恢复,减少肠黏膜屏障损伤,提高主观舒适度,降低术后并发症。
ERAS联合口服碳水化合物的优势主要体现在以下几个方面:(1)胰岛素的敏感性与进餐相关,碳水化合物的功能与早餐基本相近,既往的动物实验研究数据发现,术前口服碳水化合物能有效增强胰岛素信号转导路径上的蛋白酪氨酸激酶(protein tyrosine kinase,PTK)、磷脂酰肌醇-3激酶(phosphatidylinositol 3 kinase,PI3K)及蛋白激酶B(protein kinase B,PKB)等[13-14]关键酶的表达和活性。同时有学者发现,在前述信号通路状态下,结直肠癌病患的术后胰岛素敏感性随之增强,外周组织中的葡萄糖转运蛋白-4(glucose transporter4,GluT4)随之转位[15],故葡萄糖的利用率便增加了。而在此基础上的研究佐证,这种作用的实现与亮氨酸代谢和PI3K/PKB/雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)mTOR通路调控受影响有关。(2)ERAS模式的核心是减少手术创伤应激及围手术期其他应激,在本模式下进行碳水化合物口服(术前)能有效改善结直肠癌患者术前禁食带来的不适应激,Wang等[16]发现,此对减轻围手术期口渴、饥饿、焦虑等均有益;碳水化合物口服(术前)可刺激结直肠癌患者胰岛素释放,减轻术后分解代谢,最终改善其胰岛素抵抗。(3)结直肠癌患者术后住院时间长短(length of postoperative hospital stay,LOS)的决定因素之一就是术后胰岛素抵抗程度[17-18],故当后者因为碳水化合物口服(术前)而得到改善后,结直肠癌患者的住院时间随之缩短,术后并发症随之降低;但文中A、B组依旧存在术后并发症,提示碳水化合物口服(术前)仍有风险,原因:液体的量和组成,这是应引起重视的。
综上所述,口服碳水化合物联合ERAS模式能有效促进结直肠癌患者围手术期胃肠功能恢复,减少肠粘膜屏障损伤,提高主观舒适度,降低术后并发症,安全性好。但本文依旧存在不足,一是样本量偏低,二是缺乏胃肠功能指标(MTL、IGF-1、DAO)与胰岛素之间的相关性分析。
