基于平均表观传播子磁共振成像鉴别WHO CNS4R较低级别胶质瘤中的CNS5胶质母细胞瘤
2024-05-14肖慧楠郑莞怡吴振兴施宇婷蒋日烽
肖慧楠 郑莞怡 吴振兴 施宇婷 徐 雪 蒋日烽▲
1.福建医科大学附属协和医院放疗科,福建福州 350001;2.福建医科大学附属协和医院放射科,福建福州 350001
胶质瘤是中枢神经系统最常见的原发性肿瘤,其中胶质母细胞瘤(glioblastoma,GBM)是恶性度最高、预后最差的一类,其中位生存期不足15个月[1]。2021年世界卫生组织(World Health Organization,WHO)发布的第五版WHO中枢神经系统肿瘤分类标准(以下简称为CNS5分类),指出异柠檬酸脱氢酶(isocitrate dehydrogenase,IDH)基因野生型弥漫性星形细胞瘤如果存在微血管增生或坏死、TERT启动子突变、EGFR基因扩增、7号染色体增加或10号染色体完全丢失,则应被诊断为GBM[2]。因此根据CNS5分类标准,部分2016年第四版修订版WHO中枢神经系统肿瘤分类标准(以下简称为CNS4R分类)为WHO Ⅱ或Ⅲ级的较低级别胶质瘤将在CNS5分类下被诊断为GBM,而尽早地精准识别这一类GBM对于患者的个体化治疗及预后至关重要。
扩散磁共振成像已成为胶质瘤无创诊断的重要手段之一。它可以辅助胶质瘤术前分型、指导制定治疗方案,并预测疗效和预后[3-4]。其中平均表观传播子磁共振成像(mean apparent propagator-magnetic resonance imaging,MAP-MRI)是近年提出的一种先进的扩散成像技术。与扩散张量成像(diffusion tensor imaging,DTI)等传统扩散技术相比,MAPMRI能更准确揭示神经组织的微观结构特征,同时能提供更丰富的定量参数[5],且已在胶质瘤分型诊断中展现出巨大优势[6]。本研究探讨MAP-MRI从CNS4R较低级别胶质瘤中鉴别CNS5下GBM的应用价值,现报道如下。
1 资料与方法
1.1 一般资料
回顾性选取福建医科大学附属协和医院(本院)2019年1月至2022年12月使用磁共振影像诊断为疑似胶质瘤的成人患者为研究对象。纳入标准:①术前影像资料完整,包括常规磁共振和扩散磁共振;②经手术或活检病理证实为胶质瘤,且CNS4R分级为Ⅱ或Ⅲ级;③进行基因检测:常规检测的关键基因(IDH1/2和1p/19q)和辅助新版分类诊断的基因(TERT、EGFR、+7/-10、CDKN、BRAF及MGMT)。排除标准:①术前影像具有明显的运动伪影;②近期接受过放、化疗。经过筛选后纳入符合CNS4R分类为Ⅱ或Ⅲ级的患者共28例。根据CNS5分类分为GBM 6例,非GBM 22例。入组患者的筛选流程见图1。本研究经本院医学伦理委员会批准(伦理审批编号:2023KY164)。
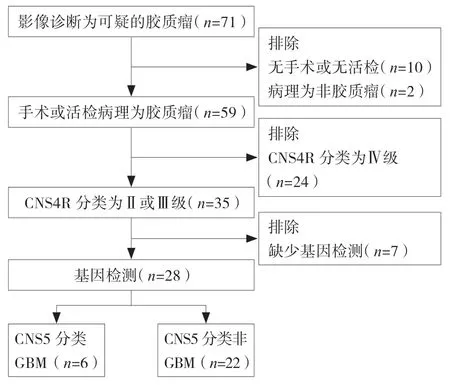
图1 入组胶质瘤患者的筛选流程图
1.2 方法
1.2.1 临床资料 收集患者的性别、年龄、是否复发胶质瘤、Karnofsky功能状态(Karnofsky performance status,KPS)评分。
1.2.2 仪器与方法 使用带有64通道磁头线圈的3.0T的MR扫描仪(MAGNETOM Prisma,Siemens Healthineers)先进行头颅结构成像。之后采用基于EPI的扩散成像序列进行图像采集,扫描参数:采用Grid采样方案来采集128个扩散q空间样本,采集14个b值包括250、500、750、1000、1250、1500、2000、2250、2500、2750、3000、3250、3500、4000 s/mm2,分别沿着3、6、4、3、12、12、6、15、12、12、4、12、24、3个方向进行采集。其他扫描参数:TR=3900 ms,TE=88 ms,FOV=230×230 mm2,GRAPPA=2,Multi-band加速因子=2,激励次数=1,体素=2.5×2.5×2.5 mm3,无层间隔,扩散采集模式=bipolar。
1.2.3 图像分析 所有的扩散图像经运动校正后,采用NeuDiLab软件分别计算出全脑MAPMRI和DTI参数图,包括均方位移(mean square displacement,MSD)、q-空间逆方差(q-space inverse variance,QIV)、回归原点概率(return to the origin probability,RTOP)、回归轴概率(return to the axis probability,RTAP)、回归平面概率(return to the plane probability,RTPP)、平均扩散率(mean diffusivity,MD)。由两名高年资的神经影像学医师对肿瘤实体区进行感兴趣区(region of interest,ROI)的勾画,并提取肿瘤实体区各参数的平均值。
1.2.4 病理、基因检测 首先由病理科医师对患者根据CNS4R进行分型,筛选出WHO Ⅱ级及Ⅲ级患者,再结合基因检测结果根据CNS5进行重新分型,分为GBM和非GBM两组。记录肿瘤的Ki-67表达阳性率。
1.3 统计学处理
使用SPSS 22.0统计学软件进行数据处理。计量资料用[M(P25,P75)]表示,采用Mann-WhitneyU检验,计数资料用[n(%)]表示,采用χ2检验。绘制受试者工作特征曲线(receiver operator characteristic curve,ROC)评估各定量参数对GBM的诊断效能。P< 0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较
本研究共纳入28例,根据CNS4R诊断为WHOⅡ级22例,WHO Ⅲ级6例。根据CNS5新分类诊断为GBM 6例,非GBM 22例。GBM组与非GBM组在性别、KPS评分、复发率以及Ki-67 标记指数(Ki-67 labeling index,Ki-67 LI)表达方面比较,差异无统计学意义(P> 0.05)。但GBM组中位年龄显著高于非GBM组,差异有统计学意义(P< 0.05)。见表1。

表1 两组患者一般资料比较
2.2 两组各定量参数比较
与非GBM组相比,GBM组肿瘤实体区的MD、QIV值显著降低,RTAP显著增高,差异有统计学意义(P< 0.05),其中以QIV和RTAP值的差异最为显著;两组肿瘤实体区的MSD、RTOP、RTPP值比较,差异无统计学意义(P> 0.05)。见表2。各定量参数在GBM组和非GBM组中数据分布的箱型图见图2。

表2 两组各定量参数比较[M(P25,P75)]
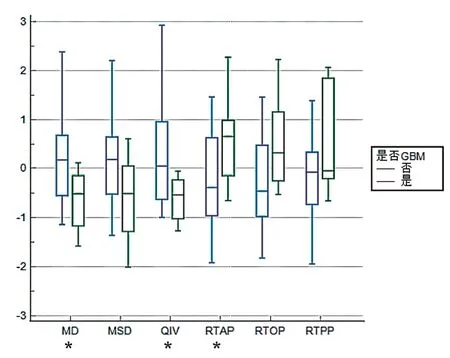
图2 各定量参数在GBM组和非GBM组中数据分布的箱型图
2.3 各定量参数对GBM预测的ROC曲线分析
QIV和RTAP均具有最大的曲线下面积(area under the curve,AUC)值,均为0.78,最佳特异度和敏感度分别为54.50%和100.00%。MD的AUC为0.77,最佳特异度和敏感度分别为50.00%和100.00%,见表3、图3。GBM和非GBM的影像学表现见图4。

表3 各定量参数对GBM预测的ROC曲线
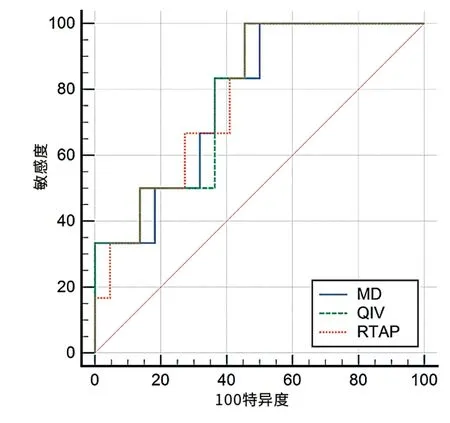
图3 ROC曲线图

图4 GBM和非GBM的影像学表现
3 讨论
MAP-MRI是近年提出的一个新的扩散模型。该模型是一个将DWI的q空间与分子位移联系起来的数学框架[7-8]。由于该模型不基于任何假设,可直接计算水分子运动的位移分布函数,因此有助于获得更准确的扩散受限和扩散速率等信息[9]。既往研究表明MAP-MRI能有效地区分胶质瘤的不同级别[6,10-11]。然而目前采用MAP-MRI从CNS4R较低级别胶质瘤中鉴别CNS5下GBM的研究却未见报道。
本研究结果表明,与非GBM组相比,GBM组肿瘤实体区MD和QIV值显著降低,RTAP值则显著增高。这与既往研究中高级别胶质瘤的MD和QIV值较低,RTAP值较高的结论是类似的[6,10,12]。MD是DTI模型中的参数,代表水分子各个方向上扩散系数的平均值[13]。QIV则表示扩散信号几何均值的逆方差,在非高斯模型中,对扩散受限更为敏感,对组织成分的变化也更为敏感。QIV值越低表明水分子扩散受限的程度越大。RTAP代表水分子按时回归原点的概率(即RTOP)沿白质纤维束平行方向的标量,RTAP值较高表明水分子扩散受限从而更容易回到起点。但RTAP有显著差异而RTOP没有差异的情况可能与轴突直径、髓鞘的数量或研究样本量太少等原因有关[14-15]。本研究结果产生的原因可能是GBM的细胞增殖速度快,组织异质性高,成分复杂且更容易发生坏死和出血,因此水分子的扩散运动更容易受到限制。
另外,既往研究表明IDH突变型GBM的预后比IDH野生型更好,以及IDH野生型的低级别胶质瘤比突变型的低级别胶质瘤侵袭性更强,预后更差[16]。同时也有文献证实存在3个基因改变中的1个或多个(TERT启动子突变、EGFR基因扩增、+7/-10)就足以达到WHO Ⅳ级GBM的恶性程度[17]。因此CNS5新分类中GBM只包含IDH野生型一种类型,同时新增了以上基因型的诊断依据。因此,IDH等基因型的差异也可能是本研究中GBM组与非GBM组差异产生的原因之一。
本研究的局限性在于:①本研究为单中心研究,样本量相对较少,希望后续能纳入更多的中心和样本来验证本研究结果的可靠性;②由于本研究的ROI只包含肿瘤实质区,与病理检测组织并不完全一致,可能会导致一些误差;③本研究未排除复发胶质瘤患者,各种治疗引起的影像改变有可能会对结果判读造成一定干扰,但本研究两组中复发胶质瘤的占比并不存在显著差异。
综上所述,MAP-MRI在一定程度上具备从WHO CNS4R较低级别胶质瘤中鉴别CNS5胶质母细胞瘤的能力,其中QIV和RTAP的诊断效能最佳。MAP-MRI在CNS5新版分类下对胶质母细胞瘤的诊断以及临床治疗决策有一定的参考价值。
