基于网络药理学和分子对接探讨益气定眩饮治疗脑梗死的作用机制
2024-05-14伍昌总王思雨刘春华
伍昌总 王思雨 张 艺 张 启 刘春华
1.湖南中医药大学研究生院,湖南长沙 410208;2.湖南中医药大学第二附属医院,湖南长沙 410005
脑梗死(cerebral infarction,CI)又称缺血性脑卒中,主要病理改变是多种原因致使脑动脉血管狭窄进而脑组织出现局部缺氧、坏死[1],具有高致病率、致残率的特点,我国患者5年内CI复发率较高,大部分会失去自理和工作能力,给家庭和社会经济带来很大负担[2-3]。中医将其归于“缺血性脑中风”范畴,多以“肝肾不足,阴阳失调,气血逆乱,上犯于脑”为基本病机。益气定眩饮是国医大师刘祖贻在多年临床研究基础上以经典名方补阳还五汤为本,加“填精、化痰”之品优化组方而成[4-5],方中含黄芪30 g、葛根45 g、川芎6 g、红花10 g、赤芍10 g、地龙10 g、桃仁10 g等(因知识产权保护,暂不公布所有药物),该方虽在临床颇有成效,但作用机制尚未明确,故本研究运用网络药理学及分子对接技术,从生物信息学角度探讨其治疗CI的潜在作用机制,为临床运用提供新的思路和实验基础。
1 资料与方法
1.1 益气定眩饮的主要活性成分及潜在靶点获取
采用中药系统药理学数据库与分析平台筛选益气定眩饮的全部成分,在TCMSP、TCM-ID、SymMap数据库中收集益气定眩饮中各个活性成分对应的靶点蛋白及靶基因名,最后获取活性成分的预测靶点。
1.2 CI和益气定眩饮的相关靶点挖掘
以“cerebral infarction”为关键词在GeneCards数据库、DrugBank数据库检索与CI有关的基因,将益气定眩饮与CI的靶点取交集,并用R软件进行韦恩图绘制。
1.3 构建益气定眩饮和CI关键靶点网络
通过STRING数据库将益气定眩饮有效成分靶点与CI的交集基因相关联,利用Cytoscape 3.8.2内置工具分析有效成分及靶点的网络拓扑参数,构建益气定眩饮-CI靶点-信号通路网络图。
1.4 基因本体(gene ontology,GO)功能及京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析
将益气定眩饮-疾病核心基因进行GO及KEGG通路富集分析,从分子功能(microfilaments,MF)、细胞组分(cumulus cell,CC)和生物过程(base pair,BP)3个角度得出有关信号通路及生物进程并进行可视化分析。同时,将获得的关键通路和核心靶点进行联合分析,构建中药活性成分-靶点-疾病网络图。
1.5 “成分-靶点”分子对接验证
将上述获取的蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络图通过Cytoscape 3.8.2软件中的cytoNCA插件计算,再通过R软件筛选均超过三者中位值的靶点为核心靶点。通过核心靶点匹配益气定眩饮主要潜在活性成分,从RCSB PDB数据库中选择物种为Homo sapiens,搜索下载3D结构PDB格式文件,利用AUTODUCK软件对蛋白进行去水、加氢、计算电荷和能量最小化优化,与筛选的活性成分进行对接,选取结合能<-5.0 kJ/mol作为筛选活性成分的依据,对化合物和靶标蛋白进行分子对接分析。
2 结果
2.1 益气定眩饮有效活性成分筛选和靶点预测结果
TCMSP数据库收集到益气定眩饮的93个成分,以“OB≥30%”“DL≥0.18”为标准进行筛选,共得到益气定眩饮有效活性成分30个,其中葛根4种、红花4种、黄芪20种、熟地黄2种,见表1。
2.2 中药复方-疾病相关靶点获取
CI的致病基因共2872个,将CI相关靶点与益气定眩饮取交集,获得14个靶点,见图1。
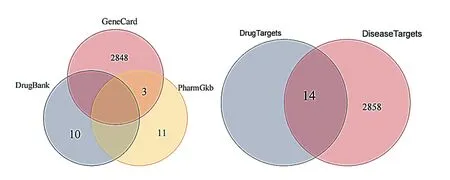
图1 CI疾病靶点整合及中药复方与CI疾病靶点交集图
2.3 益气定眩饮-CI交集靶点PPI网络构建及拓扑分析
中药-成分-靶点网络,共有113个节点和1039条边,见图2。木犀草素、β-豆甾醇度值最大,可以推测其是治疗CI的核心成分。利用Cytoscape 3.8.2软件构建PPI网络图,图中越接近紫色表明网络中节点越大,即degree值越大,得到ESR1、AKT1、MAPK1、TP53、CASP3、BCL2、TNF、IL-6这8个核心靶点(图3、表2),与其他靶点关联紧密,在整个PPI网络中起关键作用,说明本方活性成分作用于这些靶点治疗CI的可能性大。
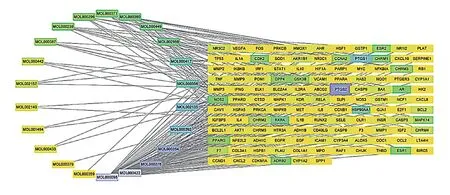
图2 “中药-成分-靶点”网络关系图

图3 PPI网络图

表2 核心靶点与其他靶点关联度
2.4 GO功能、KEGG通路富集分析注释结果
益气定眩饮-CI核心基因在R4.0.2上GO功能注释结果显示:BP分析得1097条通路、CC分析得16条通路、MF分析得110条通路,其中BP主要涉及对外来生物刺激的反应、对营养素水平的反应等;CC主要涉及薄膜筏、膜微区、囊泡内腔等;MF主要涉及DNA结合转录因子、RNA聚合酶Ⅱ特异性DNA结合转录等。益气定眩饮-CI核心基因在R4.0.2上KEGG前20条通路富集分析结果显示核心基因主要富集在PI3K-Akt信号通路、TNF信号通路、晚期糖基化(AGE-RAGE)信号通路、Toll受体信号通路等,见图4。

图4 GO功能分析气泡图、KEGG富集分析通路柱状图
2.5 分子对接验证
将度值较高的关键靶点CASP3、IL-6作为受体,与核心活性成分槲皮素、木犀草素等配体进行分子对接验证。一般认为,结合能<-5.0 kJ/mol表示有较好的结合活性。木犀草素与TP53结合力为-7.8 kJ/mol,豆甾醇与CASP3的结合力为-7.0 kJ/mol。见图5。
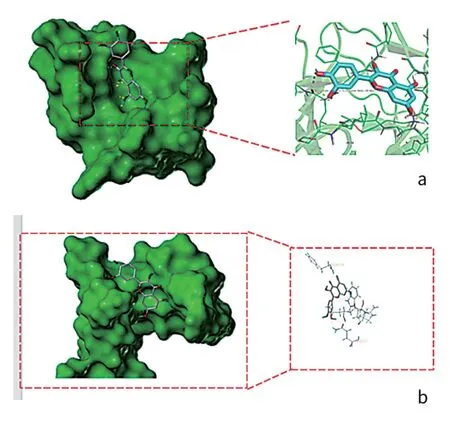
图5 木犀草素与TP53(a)分子对接图、豆甾醇与CASP3(b)分子对接图
3 讨论
中医学将CI归于“缺血性中风”范畴,本质属于本虚标实。有研究表明[6],“滋肾养肝、化痰消瘀”之法可改善CI神经功能评分,促进血管新生,益气活血法则可改善缺氧细胞、脂质代谢[7]。彭冬等[8]研究发现益气活血组方可促进脑缺血后血管新生,有充分实验研究表明补中益气汤方有促进脑缺血区周围血管新生的作用。经过数十年临床及实验研究验证,益气定眩饮对大鼠脑缺血损伤后的神经功能、局部神经元细胞形态均具有明显改善作用,随时间延长而效果更显著,这与上调VEGF、BDNF、TrkB蛋白表达及调节Akt/mTOR信号通路促进血管新生有关,从而达到改善脑组织供血供氧的目的,在临床上取到较好疗效[9]。
本研究通过网络药理学构建活性成分-靶点拓扑图,分析结果显示益气定眩饮治疗CI的核心成分是槲皮素、木犀草素,关键成分是β-豆甾醇、黄芩苷等。木犀草素为食源性黄酮类化合物,具有保护心脑血管、抗肿瘤、抗氧化及调节免疫等多种药理作用,木犀草素可以通过增强神经元细胞膜上的泵活性减轻缺血再灌注所致的神经元损伤[10-11]。β-豆甾醇可抑制细胞凋亡以及调节Caspase-3、Bcl-X1表达,从而降低氧化应激和炎症,脊柱甾醇保护大脑免受脑I/R损伤。黄芩苷可达到抑制脑NF-κB/CCL2/CCR2通路,激活多个目标的效果[12-13]。
富集分析及分子对接结果显示,益气定眩饮治疗CI的靶点主要集中在IL-6、TP53、CASP3等。IL-6炎症诱导导致星形胶质细胞凋亡,影响脑梗死区域的体积[14]。TP53通过影响一氧化氮生物合成及信号转导、内皮细胞凋亡负调控等生物过程来发挥治疗CI的作用[15]。CASP3减少Bcl-2水平增加损伤及脑神经细胞损伤,会加重脑缺血[16-17]。
KEGG富集分析结果显示核心靶点主要有AGE-RAGE、PI3K-Akt、Toll样受体等信号通路,说明本方活性成分可能通过以上途径对疾病进程进行干预。AGE-RAGE通路抑制衰老信号来延缓动脉粥样硬化的发展,从而改善动脉粥样硬化,减少斑块面积[18]。PI3K-Akt通路抑制神经元凋亡以挽救或延迟尚存缺血性半影中的梗死并调节抗氧化蛋白水平,从而保护神经元免受氧化应激损伤[19-20]。Toll样受体是一种天然免疫受体,作为免疫反应的一个重要中介在动脉粥样硬化的发生和进展中扮演着重要的角色[21-22]。
本研究通过生物信息学技术,表明益气定眩饮的有效活性成分可以通过多个靶点及通路作用于CI,其核心成分槲皮素能够作用于关键成分β-豆甾醇及关键靶点IL-6,通过靶点CASP3治疗CI,拓展了益气定眩饮治疗CI的新思路,为临床应用本方提供了理论依据,但本研究还存在一定局限性,需要进一步实验验证相关核心靶点,探讨具体机制。
