肠内营养支持在重症监护病房患者肠内营养中的应用
2024-05-13唐礼霞黄逸佳
唐礼霞 陈 阳 黄逸佳
上海大学附属南通医院 南通市第六人民医院重症医学科,江苏南通 226600
危重症患者常存在意识及吞咽功能障碍、急性应激反应、激素分泌等导致的身体代谢紊乱,其营养不良发生率为30%~50%[1]。为此改善重症患者营养水平十分重要,而重症监护室患者常通过肠内营养进行营养输注,但由于置管操作耐受性问题,肠内营养输注引起临床广泛重视[2]。重症患者在遭受严重创伤、感染、重大手术事件时处于急性应激状态,在急性应激状态下,体内释放大量儿茶酚胺、甲状腺激素、皮质醇等相关应激激素,这类激素可加速身体代谢率,细胞及组织需要更多能力应对应激状态,高代谢状态导致体内能量消耗增加[3]。机体为满足高能耗需要会加速脂肪、糖原及蛋白质的分解过程,以获取更多能量,出现高分解状态[4]。同时机体提供氨基酸用于能量代谢合成的蛋白质加速分解白细胞、抗体等蛋白质出现负氮平衡状态[5]。这些改变可能导致患者出现严重营养不良及免疫功能下降,免疫细胞通过产生促炎性细胞因子、抗炎细胞因子等不同种类的细胞因子调节免疫反应,营养不良可能导致促炎性细胞因子的过度激活,抗炎细胞因子产生减少,免疫系统异常激活[6-7]。患者在营养不良状态下,蛋白质不足、胶原蛋白合成受损,组织修复及伤口愈合必需的蛋白质供应不足,影响伤口结构支持及组织重建,延缓伤口愈合[8]。此外,营养不良可能导致体内某些药物代谢酶的活性降低,药物代谢率减慢,药物在体内停留时间过长,增加药物毒性降低药物疗效。本研究旨在观察强化肠内外营养支持对重症监护病房患者改善效果进行评价。
1 对象与方法
1.1 研究对象
以便利抽样法选取江苏省南通市第六人民医院2020 年1 月至2022 年12 月收治的82 例患者为研究对象,依据Kendall 原则选取样本量,公式为,其中概率值P=0.5,误差值α=0.05,统计量Z=1.96,总量e=103,考虑20%失访率,确定样本量n=82[5]。纳入标准:①重症监护病房收治患者;②年龄>18 岁;③行机械通气;④为首次入住重症监护室(intensive care unit,ICU);⑤患者知情同意本研究。排除标准:①处于哺乳期;②合并低磷血症等危险因素,如血液透析;③已完成高磷血症的治疗;④近3 个月内有甲状旁腺切除术史;⑤伴有先天性营养不良或营养代谢性疾病;⑥入ICU 前有接受肠内或肠外营养。剔除资料不完整或中途退出,以随机数字表法将其分为对照组和观察组,各41 例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。本研究经江苏省南通市第六人民医院医学伦理委员会经批准(NTLyLy2019025)。

表1 两组一般资料比较
1.2 研究方法
两组均接受氮等热量营养支持,营养液中蛋白质、脂肪、糖供给范围分别为10%~20%、50%~60%、30%~40%,含热量为125.5 kJ/(kg·d),氮与非蛋白质热量比为1∶150。
1.2.1 对照组 常规肠外营养支持。通过中心静脉或外周静脉中心静脉置管途径给予肠外营养,将葡萄糖、氨基酸、脂肪乳、脂溶性及水溶性维生素、胰岛素及电解质等按比例配置,加入肠外营养袋。入院24~48 h遵医嘱给予患者肠外营养支持,营养支持前确定输入导管位置,24 h 均匀输注营养液,0~24 h 给予全量的40%,每隔24 h 增加30%,直至全量。准确记录患者24 h 出入液量,定时检测血糖、电解质及肝肾功能。导管位置妥善固定,每日以穿刺点为中心碘伏消毒,肝素帽每周更换,三通接头每日更换。
1.2.2 观察组 行肠内营养支持。通过鼻肠管或鼻胃管途径给予肠内营养,肠内营养液为500 ml 瑞素肠内营养液(生产厂家:华瑞制药有限公司;国药准字号:J20 140075;规格:500 ml),该营养液包含蛋白质、脂肪、碳水化合物、水、维生素A、维生素D3、维生素E、维生素B1、维生素B6、维生素B12、维生素B2、维生素C、钼、硒、钠、钾、铜、叶酸、胆碱、锌等。4~6次/d,开始肠内营养时胃管输注速度为40~60 ml/h,肠管输注速度为20~25 ml/h。往后每日增加25 ml/h,最大速度为125~150 ml/h。肠内营养支持前评估肠内营养液适合途径,喂养前检查患者胃潴留量,肠内输注时取半卧位、坐位或头高(抬高30°~45°)卧位,肠内营养输注结束,维持支持体位30 min。准确记录患者出入液量,建立人工气道的患者,鼻饲时将气囊充气,避免食物反流误吸,加强对患者排出痰液的观察,观察有无营养液成分。
1.2.3 质量控制①为避免组间沾染,本研究将两组患者安排在不同病房,且要求患者及其家属禁止探讨研究有关事项;②护士长全程监控护理开展情况,对于未依照相关标准进行护理的护理人员,予以严重批评。
1.3 观察指标及评价标准
1.3.1 营养指标 于住院次日(护理前)、住院15 d 后(护理后),收集患者空腹静脉血5 ml,使用酶联免疫吸附试剂盒(生产厂家:北京键平九星生物医药科技有限公司)对前白蛋白(prealbumin,PA)正常值:280~350 mg/L、视黄醇结合蛋白(retinol-binding protein,RBP)正常值:26.7~57.9 mg/L、转铁蛋白(transferrin,TRF)正常值:2.2~4.0 μg/L 含量进行检测。
1.3.2 康复情况比较 比较住院天数、肠内营养并发症发生情况和肠内营养丢弃等情况。
1.4 统计学方法
采用SPSS 26.0 统计学软件进行数据分析。计量资料采用均数±标准差()表示,比较采用t 检验;计数资料采用例数和百分率表示,组间比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组护理前后营养学指标比较
护理前,观察组PA、RBP、TRF 水平比较,差异无统计学意义(P>0.05);护理后,两组PA、RBP、TRF均高于护理前,且观察组高于对照组(P<0.05)。见表2。
表2 两组护理前后营养学指标比较()
注t1、P1 为两组护理前比较;t2、P2 为两组护理后比较。PA:前白蛋白;RBP:视黄醇结合蛋白;TRF:转铁蛋白。
2.2 两组住院天数、肠内营养并发症发生情况和肠内营养弃去情况比较
观察组住院天数短于对照组(P<0.05);两组肠内营养并发症比较,差异无统计学意义(P>0.05);观察组肠内营养丢弃率低于对照组,差异有统计学意义(P<0.05)。见表3。
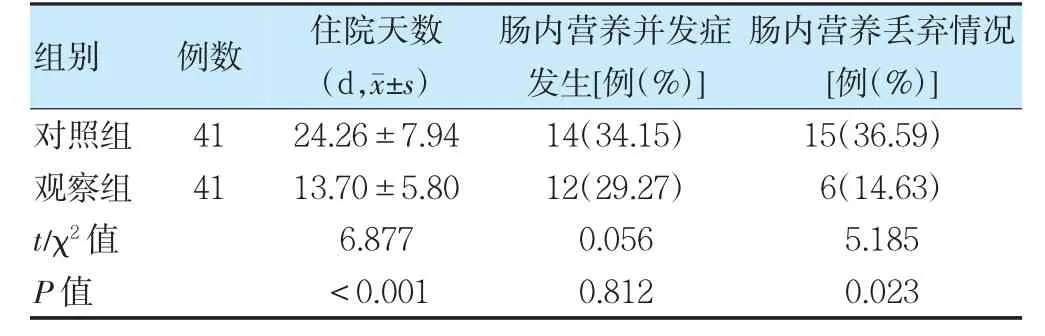
表3 两组住院天数、肠内营养并发症发生情况和肠内营养弃去情况比较
3 讨论
因重症监护病房患者病情危急,需要采取急救措施,并采取相应的护理措施。近年来,报道显示在ICU患者中运用循证护理,可以有效地改善患者的营养状况[9]。但传统护理干预并不完全适用于重症监护患者。部分重症患者术后仍然存在消化道损伤,胰腺损伤、手术应激反应等危险,均会增加患者腹泻、腹胀、胃潴留、电解质紊乱等风险[10]。重症患者对肠内营养制剂的依赖度较低,一旦出现胃肠反应,就需要弃去肠内营养制剂[11-13]。本研究结果显示,观察组肠内营养丢弃率低于对照组,提示阶梯决策辅助性护理可改善重症患者对肠道营养药物的依从性[14-16]。部分研究报道显示,肠内营养的使用可缩短肠内营养时间,从而降低患者的住院时间,减少住院负担[17-19]。本研究显示,强化肠内营养支持对重症患者具有促进肠道蠕动,减轻腹部胀气,使患者尽早通过口腔进食。若是肠道营养制剂引起的腹泻,可以适当地减少肠道营养制剂的浓度,同时还可通过药物来减少腹泻的并发症[20-21]。但仍有少数患者对腹泻不耐受,是由于外科手术应激等原因放弃了肠道营养,而强化肠内营养支持护理有助于降低因腹泻引起的丢弃营养剂行为。
本研究结果显示,观察组PA、RBP、TRF 高于对照组,提示强化肠内营养支持可提高重症监护患者营养水平,与郑伟等[22]报道相似。这是因为重症患者接受手术后生理和代谢上的改变,导致患者术后出现严重的营养不良,术后肠道营养会出现腹胀、腹泻等症状,稀释后可缓解腹泻。彭凌云等[23]报道显示,接受外科手术的重症患者可能出现腹泻、腹胀等,可指导患者经口服用安素,以耐受性为主,混在食物中,能减轻对胃肠的不耐受。调查研究中发现腹泻、呕吐、腹胀、血糖增高是导致重症患者术后放弃肠内营养制剂的主要影响因素[24-25]。而本研究在采取强化肠内营养支持,患者肠道蠕动明显加快,因腹胀而放弃肠道营养素的状况有所改善,同时解决了患者的血糖不稳定问题,重症患者术后的肠道营养支持度明显增加,患者营养水平得到了有效提高。
综上所述,强化肠内营养支持护理具有改善患者对肠内营养丢弃情况,促进其营养水平提高。但本研究样本受限于样本量大小、资金、人群地区分布等因素影响存在数据偏差,期望日后加以深入分析。
利益冲突声明:本文所有作者均声明不存在利益冲突。
