利妥昔单抗联合GDP 化疗方案在非霍奇金淋巴瘤中的应用
2024-05-10张丽
张丽
(河南省郑州市第三人民医院 郑州 450000)
作为血液系统常见的恶性肿瘤之一,淋巴瘤可发生于身体的任何部位,患者常伴有发热、消瘦、盗汗等全身症状,严重降低生活质量[1~2]。淋巴瘤分为霍奇金淋巴瘤和非霍奇金淋巴瘤,其中非霍奇金淋巴瘤是淋巴瘤常见类型之一,非霍奇金淋巴瘤65%~70%原发于淋巴结,30%~35%原发于淋巴结外[3]。目前,临床上针对非霍奇金淋巴瘤患者的治疗以化疗为主,其中GDP 化疗方案较常见,虽可有效抑制病情进展,但疗效仍存在较大提升空间[4]。近年来,利妥昔单抗被逐步应用于多种恶性肿瘤的临床治疗中,显示出良好的应用前景[5]。利妥昔单抗是一个CD20 的一个单克隆抗体,能够控制淋巴瘤。鉴于此,本研究探讨联合方案对患者免疫功能及生活质量等方面的影响。现报道如下:
1 资料与方法
1.1 一般资料 选取2021 年7 月至2022 年7 月医院收治的104 例非霍奇金淋巴瘤患者,按随机对照原则分为对照组和研究组,各52 例。对照组男27 例,女25 例;年龄45~70 岁,平均年龄(57.51±3.51)岁;体质量指数(BMI)16~33 kg/m2,平均BMI(22.92±2.40)kg/m2;病程3~8 个月,平均(5.12±1.23)个月;临床分期:Ⅱ期23 例,Ⅲ期20 例,Ⅳ期9 例。研究组男26 例,女26 例;年龄40~68 岁,平均年龄(54.13±2.89) 岁;BMI 17~32 kg/m2,平均BMI(22.71±2.33)kg/m2;病程2~10 个月,平均(5.25±1.67)个月;临床分期:Ⅱ期25 例,Ⅲ期15 例,Ⅳ期12 例。两组一般资料比较均衡性良好(P>0.05)。本研究经医院医学伦理委员会批准(伦理号:2021000217)。
1.2 入选标准 纳入标准:(1)符合《非霍奇金淋巴瘤临床实践指南(中国版)》相关诊断标准[6],同时经细胞学或病理学检查证实;(2)年龄40~70 岁;(3)患者及其家属对本研究实施意义、方法及实施中的义务和权利均有了解且签署知情同意书。排除标准:(1)患有严重的精神疾病者;(2)肺、肾等脏器严重损伤者;(3)患有严重呼吸系统疾病或免疫功能障碍者;(4)预计生存时间不足6 个月者;(5)对本研究所使用的药物存在过敏反应者;(6)妊娠或哺乳期妇女。
1.3 治疗方法
1.3.1 对照组 给予GDP 化疗方案进行治疗。具体措施:第1~8 天静脉滴注0.5 h 给予注射用盐酸吉西他滨(国药准字H20103523)1 000 mg/m2;第1~3 天静脉滴注2.5 h 注射用顺铂(国药准字H20073653)25 mg/m2;第1~4 天静脉滴注0.5 h 地塞米松磷酸钠注射液(国药准字H37021969)40 mg/m2。一个化疗周期为21 d,治疗6 个周期。
1.3.2 研究组 在上述基础上联合利妥昔单抗治疗,静脉滴注利妥昔单抗注射液(国药准字S20200022)375 mg/m2。
1.4 观察指标 (1)临床疗效。缓解:经CT 扫描病灶区减小面积≥80%,无可触及的淋巴结,且细针穿刺活检结果为阴性;部分缓解:经CT 扫描病灶区减小面积50%~80%;病情稳定:经CT 扫描病灶区减小面积为原来的一半;病情进展:经CT 扫描病灶区增大30%。总有效率为部分缓解率与缓解率之和。(2)生活质量。采取生活质量综合评定问卷调查表(GQOLI-74)评价治疗前、治疗后8 周改善情况,评价内容包括:认知、情绪、角色、社会及躯体功能,每项总分100 分,生活质量与评分具有正相关性。(3)免疫功能。采用流式细胞仪检测患者淋巴细胞亚群,并密切观察治疗前后免疫球蛋白A(IgA)、免疫球蛋白M(IgM)、免疫球蛋白G(IgG)指标及补体C3、C4水平。(4)不良反应。包括脱发、呕吐、白细胞减少、贫血、骨髓抑制等不良反应发生情况。(5)肿瘤标志物。在患者空腹状态下,采集患者肘静脉血3 mL,以3 000 r/min 离心8 min,采用酶联免疫吸附法对患者血管内皮生长因子(VEGF)、细胞质胸苷激酶1(TK-1)水平进行检测。
1.5 统计学方法 采用SPSS22.0 软件处理数据,计量资料以()表示,采用t检验;计数资料以%表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组疗效对比 对比两组临床疗效,研究组总有效率(59.62%)较对照组总有效率(36.54%)高(P<0.05)。见表1。
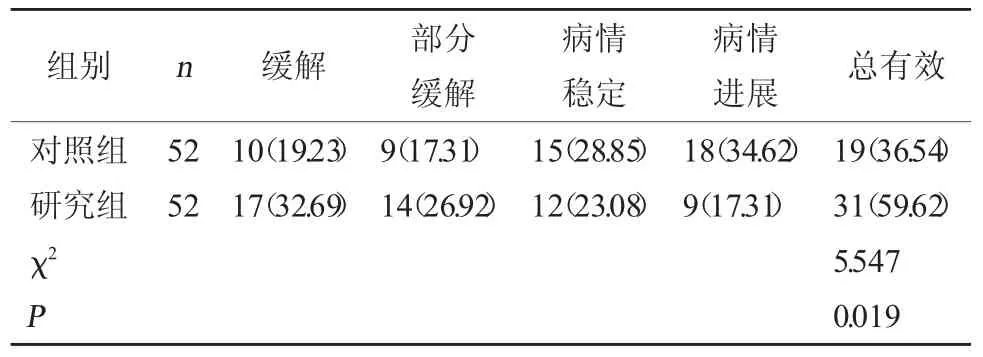
表1 两组疗效对比[例(%)]
2.2 两组肿瘤标志物对比 研究组治疗后TK-1、VEGF 水平均低于对照组(P<0.05)。见表2。
表2 两组治疗前后肿瘤标志物对比(pg/mL,)
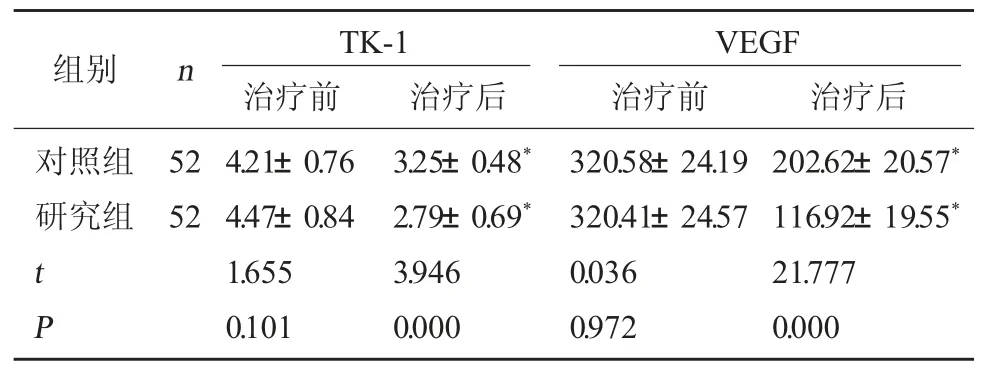
表2 两组治疗前后肿瘤标志物对比(pg/mL,)
注:与本组治疗前相比,*P<0.05。
VEGF治疗前治疗后对照组研究组组别nTK-1治疗前治疗后52 52 tP 4.21±0.76 4.47±0.84 1.655 0.101 3.25±0.48*2.79±0.69*3.946 0.000 320.58±24.19 320.41±24.57 0.036 0.972 202.62±20.57*116.92±19.55*21.777 0.000
2.3 两组生活质量评分对比 两组患者治疗后认知、情绪、角色、社会及躯体功能评分均高于治疗前,且研究组高于对照组(P<0.05)。见表3。
表3 两组生活质量评分对比(分,)

表3 两组生活质量评分对比(分,)
注:与本组治疗前相比,*P<0.05。
社会功能治疗前治疗后对照组研究组组别n躯体功能治疗前治疗后情绪功能治疗前治疗后52 52 tP 46.32±5.12 46.37±5.24 0.049 0.961 49.56±5.24*55.67±6.23*5.412 0.000 51.26±5.03 51.67±5.34 0.403 0.688 55.36±6.32*59.49±6.29*3.340 0.001 52.35±6.03 52.47±6.33 0.099 0.921 57.26±6.13*63.97±7.67*4.928 0.000角色功能治疗前治疗后对照组研究组组别n认知功能治疗前治疗后52 52 tP 53.26±6.12 53.67±6.25 0.338 0.736 56.19±6.35*65.59±7.26*7.028 0.000 53.45±5.12 53.24±6.12 0.190 0.850 59.24±6.25*65.58±7.27*4.769 0.000
2.4 两组免疫功能指标对比 两组治疗后IgA、IgM、IgG 及补体C3、C4 均比治疗前降低,组间相比,研究组IgA、IgM、IgG 与对照组相当(P>0.05),但研究组补体C3、C4 较对照组低(P<0.05)。见表4。
表4 两组免疫功能指标对比(g/L,)

表4 两组免疫功能指标对比(g/L,)
注:与本组治疗前相比,*P<0.05。
IgG治疗前治疗后对照组研究组组别nIgA治疗前治疗后IgM治疗前治疗后52 52 tP 3.85±1.57 3.72±1.45 0.439 0.662 2.89±0.98*2.72±0.53*1.012 0.314 2.99±1.57 2.78±1.34 0.734 0.465 2.13±0.78*2.22±0.67*0.581 0.563 19.24±3.12 19.35±3.46 0.170 0.865 18.24±2.67*18.26±2.14*0.039 0.969 C4治疗前治疗后对照组研究组组别nC3治疗前治疗后52 52 tP 1.89±0.67 1.82±0.71 0.517 0.606 1.21±0.34*0.97±0.30*3.817 0.000 0.98±0.37 0.88±0.42 1.288 0.201 0.45±0.27*0.31±0.12*3.417 0.000
2.5 两组不良反应情况对比 研究组不良反应发生率(48.08%)与对照组(55.77%)相比,差异无统计学意义(P>0.05)。见表5。
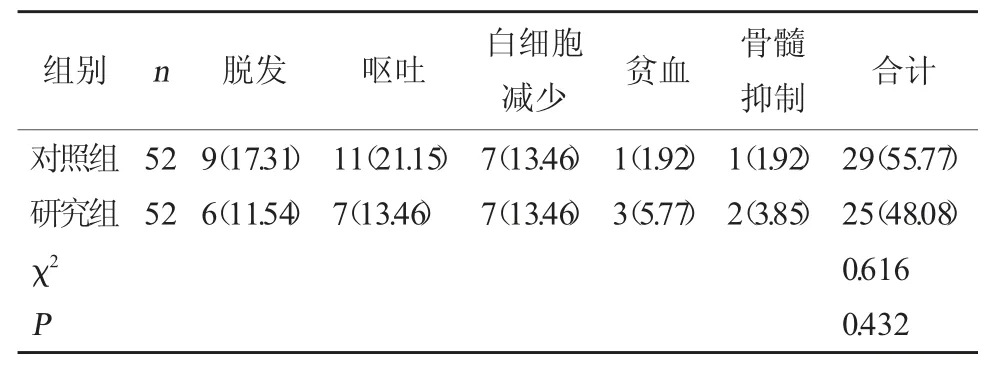
表5 两组不良反应情况对比[例(%)]
3 讨论
非霍奇金淋巴瘤的发病机制较为复杂,部分研究认为与遗传、免疫功能低下、病毒感染、化学致癌物等因素有关[7~8]。近年来,我国该病患者人数不断增多,且有向年轻化发展的趋势,给患者家庭及社会带来沉重的负担[9]。非霍奇金淋巴瘤区别于其他类型的恶性肿瘤,由于淋巴组织相对特殊,如果患者发病,就会伴随着其他部位病变。因此,在发病初期常常通过化疗来进行治疗。
目前,临床上治疗非霍奇金淋巴瘤患者多采用GDP 化疗方案进行治疗,GDP 化疗通过使用抗癌药物杀死癌细胞或抑制其生长[10]。该方案由吉西他滨、顺铂和地塞米松3 种药物组成,尽管该方案可以有效地帮助患者对抗癌症,但也存在一定的副作用,包括呕吐、贫血、白细胞减少、脱发、骨髓抑制等,且部分患者预后不理想[11]。因此,需要联合其他药物进行治疗。利妥昔单抗注射液一种靶向于CD20 的单克隆抗体,其与表达在B 淋巴细胞表面的CD20 分子结合,通过抗体依赖的细胞毒作用(ADCC)和补体依赖的细胞毒作用(CDC)杀伤肿瘤B 细胞。本研究在化疗的基础上增加利妥昔单抗对非霍奇金淋巴瘤患者进行治疗,结果显示,研究组总有效率(59.62%)高于对照组总有效率(36.54%),说明利妥昔单抗联合GDP 化疗治疗非霍奇金淋巴瘤疗效确切。其原因可能在于:CD20 是一种B 细胞表面的糖蛋白抗原,位于B 细胞上游复制和分化的关键点。利妥昔单抗通过与CD20 抗原结合,不仅可以直接引发B 细胞的细胞毒作用,还可以通过免疫细胞介导的细胞毒作用进一步增强对B 细胞的杀伤效果[12]。同时,体外研究证明,利妥昔单抗可使药物抵抗性的人体淋巴细胞对一些化疗药物的细胞毒性敏感,进一步提高治疗效果[13]。
临床发现,非霍奇金淋巴瘤患者免疫功能呈不同程度下降状态[14]。补体C3、C4 在肿瘤的生理发展过程中起着重要作用,当患者免疫功能下降,体液免疫上升,导致补体C3、C4 水平上升,而利妥昔单抗可通过补体依赖性发挥作用,进而使补体C3、C4 水平下降[15~16]。本研究结果显示,两组治疗后各项免疫功能指标均比治疗前降低,研究组治疗后IgA、IgM、IgG 与对照组相当,但补体C3、C4 较对照组低,GQOLI-74 各项评分均较对照组高(P<0.05),说明利妥昔单抗联合GDP 化疗方案可促进患者免疫功能改善,对延长患者生命有一定积极作用,且提高患者生活质量。本研究中,研究组TK-1、VEGF 水平均低于对照组(P<0.05),可见利妥昔单抗联合GDP化疗治疗非霍奇金淋巴瘤可抑制肿瘤的生长,降低血清肿瘤标志物水平。究其原因可能在于:TK-1 是细胞质胸苷激酶或者胸苷激酶1 检查,与癌细胞的DNA 合成密切相关,是细胞增殖活性检查的标志物。VEGF 是一种促进血管内皮细胞增殖和新生血管形成的重要生长因子, 在很多疾病的治疗中起着重要的作用。同时,VEGF 可作用于淋巴血管的形成,该因子还是内皮细胞特异的撕裂素,可降解纤维蛋白和基底膜。而利妥昔单抗联合GDP 化疗方案可快速减缓TK-1、VEGF 高表达,阻止肿瘤细胞增殖,抑制肿瘤新生血管生成,从而有效地减缓肿瘤生长和转移,最大限度地控制和杀灭肿瘤。另外,本研究对两组用药安全性进行比较,结果显示,不良反应率相比(48.08% vs 55.77%),两组相当(P>0.05),说明该治疗方案安全性良好,容易被患者所接受。
综上所述,给予非霍奇金淋巴瘤患者实施利妥昔单抗联合GDP 化疗方案进行治疗,疗效确切,可促进免疫功能、生活质量提升,抑制肿瘤标志物水平表达,且安全性良好,优势较为明显,进一步推广和使用价值较高。
