冰冻肺门影响胸腔镜肺叶切除术中转开胸的分析
2024-05-06张兴树余明阳程学超瞿文栋宋永祥
张兴树,余明阳,程学超,罗 倩,龚 明,瞿文栋,宋永祥
(遵义医科大学附属医院 胸外科,贵州 遵义 563000)
随着近年贵州地区胸部结核等慢性传染及感染性疾病发病率的回升,在全胸腔镜肺叶切除术中常常遇到肺门或纵隔区域的钙化、固定淋巴结或瘢痕肺门,导致胸腔镜手术不能顺利进行,中转开胸手术比例居高不下,同时也增加手术操作难度以及围术期风险。本文总结了遵义医科大学附属医院胸外科2018年1月至2021年12月733例接受肺叶切除手术的患者资料。733例患者顺利完成手术,术后死亡3例。其中522例(71.21%)在胸腔镜手术下完成了肺叶切除手术,211例(28.79%)患者因“冰冻肺门”影响中转开胸后完成手术。在中转开胸患者的统计中,包括主动中转开胸157例(74.41%),被动中转开胸54例(25.59%)。现分析“冰冻肺门”导致中转开胸的并发症和处理经验,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析纳入我院自2018年1月至2021年12月接受胸腔镜肺叶切除术患者的临床资料。纳入标准:行胸腔镜肺叶切除术的患者。排除标准:术中全胸膜腔闭锁、单肺通气不能维持、肿瘤太大、切割缝合器械故障。共纳入733例,其中男性366例,女性367例,年龄15~79岁,中位64岁。吸烟患者280例,非吸烟患者453例,既往肺结核或胸膜炎病史124例。恶性肿瘤512例,良性疾病221例。其中恶性肿瘤分期情况为:Ⅰ期347例,Ⅱ期79例,ⅢA期60例,ⅢB期14例,Ⅳ期4例(颅脑或者骨骼寡转移2例;术中探查发现胸膜以及膈肌侵犯2例,病变位置较深,无法行姑息性切除遂行肺叶切除),转移瘤5例,术后残端复发1例,原位腺癌2例。良性疾病包括:肺囊肿15例、结核性肺脓肿8例、支气管扩张24例、炎性假瘤38例、结核球(瘤)39例、肺错构瘤15例、肺隔离症13例、中叶综合征4例、硬化性肺血管瘤10例、肺曲菌球25例、动静脉瘘3例、IgG4相关性肺疾病1例、非典型腺瘤样增生4例、巨型肺大泡1例、肺硅结节1例、机化性肺炎2例、结核性毁损肺11例、周围神经鞘膜瘤1例、肺子宫内膜异位症1例、淋巴瘤样肉芽肿病1例、肺梭形细胞瘤4例。行左上肺叶切除术124例(16.92%),左下肺叶切除术148例(20.19%),右上肺叶切除术206例(28.10%),右中肺叶切除术70例(9.55%),右下肺叶切除术138例(18.83%),右上中肺叶切除术1例(0.14%),右中下肺叶切除术15例(2.04%),复合肺叶切除术(肺叶切除+楔形切除或肺段切除)15例(2.04%),全肺切除术10例(1.36%),袖式肺叶切除6例(0.82%)。本研究获得遵义医科大学附属医院伦理委员会批准(KLL-2023-568)。
1.2 方法
1.2.1 手术方法 采用双腔气管插管复合麻醉方式,术中单肺通气维持。手术主要以“两孔法”完成,取腋中线第7肋间做一长约1.0 cm切口作为腔镜观察孔,腋前线第4肋或第5肋间做一长约3.0 cm切口为手术操作口。部分手术采用全程“单孔法”完成,其中单孔胸腔镜切口取腋前线与腋中线第4肋或第5肋间长3.0~4.0 cm切口作为操作口及观察口。如镜下操作遇到“冰冻肺门”、血管损伤出血等特殊或危急情况时,延长操作口约10 cm并在胸腔镜下辅助小切口完成手术即为中转开胸。术后于观察孔或者操作孔放置胸腔闭式引流管引流积液。
1.2.2 观察指标 根据是否因“冰冻肺门”而中转开胸分为中转开胸手术组与全胸腔镜手术组,中转开胸手术组因术中是否出现因解剖肺门结构出现血管损伤出血、支气管撕裂等急迫或术中严重并发症,威胁患者生命,不得不放弃镜下操作,分为主动中转开胸组和被动中转开胸组。记录患者的手术时长、术中失血量、术后胸腔闭式引流管留置时长、术后住院时长、围术期死亡、是否非计划再次手术等,并比较两组患者肺部感染、切口感染、肺不张、皮下气肿、心律失常、下肢静脉血栓、乳糜胸、持续漏气、支气管胸膜瘘、重新置管、术后72 h内痛觉评分以及输血等术后并发症的发生情况。
2 结果
2.1 两组患者一般资料比较 两组患者在性别差异、吸烟史、胸部结核或胸膜炎病史发生情况经检验结果显示差异有统计学意义(P<0.05),因此,中转开胸手术组的男性比例明显高于女性,中转开胸组患者吸烟情况、胸部结核或胸膜炎病史发生情况均大于全胸腔镜组;两组患者年龄经检验结果显示差异无统计学意义(P>0.05,表1)。
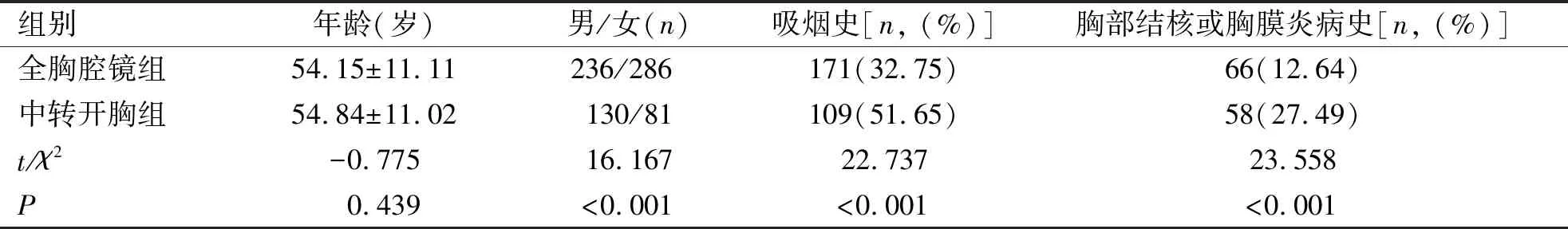
表1 两组患者的一般资料比较
2.2 两组患者手术相关资料比较 两组患者手术操作时长、术中失血量、术后胸腔闭式引流管留置时长、术后住院天数、非计划再次手术,结果显示差异具有统计学意义(P<0.05)。因此,中转开胸手术组患者的手术操作时长、术中失血量、术后胸腔闭式引流管留置时长、术后住院时长、非计划再次手术均高于全胸腔镜手术组。另外,两组患者发生围术期死亡共3例(全胸腔镜组1例、中转开胸组2例),结果显示差异无统计学意义(P>0.05,表2)。

表2 两组患者手术相关资料比较
2.3 两组患者术后并发症发生情况比较 两组患者术后发生皮下气肿、重新置管、切口感染、肺部感染、肺不张、术中或术后输血、持续漏气、术后72 h内疼痛评分结果显示差异有统计学意义(P<0.05)。因此,中转开胸手术组的皮下气肿、重新置管、切口感染、肺部感染、肺不张、术中或术后输血、持续漏气、术后72 h内疼痛评分发生率高于全胸腔镜手术组。两组患者心律失常、下肢静脉血栓、乳糜胸、支气管胸膜瘘发生情况结果显示差异无统计学意义(P>0.05,表3)。

表3 两组患者术后并发症比较(例)
2.4 主动中转与被动中转患者的手术资料和术后并发症发生情况比较 两组患者手术操作时长、术中失血量、术后住院天数经检验结果显示差异有统计学意义(P<0.05)。因此,被动中转组的手术操作时长、术中失血量、术后住院天数均高于主动中转组。在术后胸腔闭式引流管留置时长、非计划再次手术比较,差异无统计学意义(P>0.05,表4)。主动中转开胸手术组与被动中转开胸手术组患者术后并发症发生情况比较,结果显示差异均无统计学意义(P>0.05,表5)。
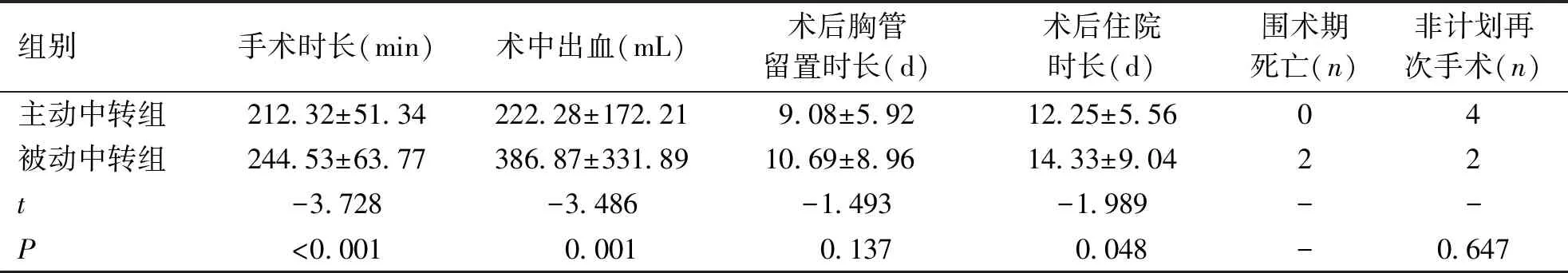
表4 主动中转组与被动中转组患者手术资料比较
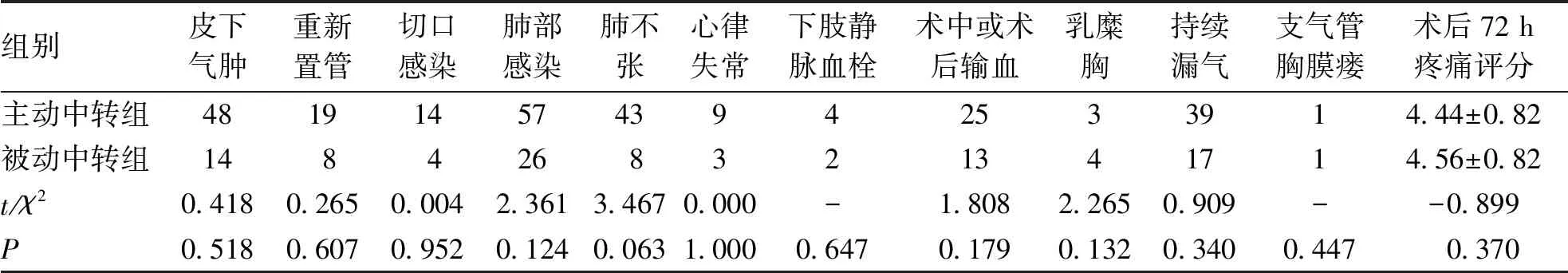
表5 主动中转组与被动中转组术后并发症发生情况比较(例)
3 讨论
胸腔镜微创手术经过20余年的发展其优点已得到充分证实[1],但胸腔镜术中难免会出现胸膜腔粘连、巨大肿瘤、术中血管或支气管损伤等导致中转开胸。目前,已往文献报道的全胸腔镜手术平均中转开胸率2%~23%[2-4],大多数研究者认为术中转开胸与患者年龄、肿瘤大小、钙化淋巴结等有关,单独对困难肺门导致中转开胸的研究尚少。丁超等[5]报道在肺结核微创胸腔镜治疗中肺门淋巴结粘连及胸腔粘连解剖困难是中转开胸的主要原因,中转开胸率22.2%(14/63),因淋巴结因素导致中转率为28.6%(4/14)。苏鹏等[6]对接受胸腔镜下肺叶切除术1 350例患者中对中转开胸83例的中转原因分析,结果显示有21例(25.30%)因淋巴结嵌顿而中转开胸。
近年因肺部慢性感染性疾病发展呈上升趋势[5, 7-8],特别是在贵州地区,部分病人出现肺门及纵隔区域淋巴结钙化、融合或肺门软组织瘢痕形成等影响全胸腔镜手术进程,或因解剖肺门、游离困难淋巴结等情况出现肺血管撕裂出血等情况,威胁患者生命安全,不得不中止全胸腔镜手术,选择在胸腔镜辅助小切口完成手术。为了便于研究,将此类肺门情况定义为“冰冻肺门”,由于长期慢性炎症刺激,肺门组织水肿瘢痕化与肺血管、支气管粘连致密或者困难淋巴结,就如同李运等[9]定义门钉淋巴结一样,在解剖血管时无法打开血管鞘,即使部分打开也无法完全游离血管,特别是肺动脉壁与支气管融合在一起,即使用组织剪锐性分离法,就如同冰块与冰柜壁一样紧贴,无法轻易分离,甚至出现血管撕裂,此类肺门条件被形象地称之为“冰冻肺门”。
在本研究中,排除了单纯因胸膜腔粘连导致中转开胸的患者资料,发现有733例患者中有211例(28.79%)患者因“冰冻肺门”干扰导致中转开胸,高于既往研究报道。由于贵州地区呼吸道慢性感染性疾病如肺结核、胸膜炎等疾病发生率高,这部分患者中出现胸膜腔粘连、肺门钙化、肺门瘢痕化等情况高于一般人群,同时也有研究者[6]认为由于肺部或胸膜长期慢性感染导致脏层胸膜与壁层胸膜紧密粘连或闭锁、气管及支气管壁、血管壁与周围组织结构分界不明,出现“门钉淋巴结”、“肺门瘢痕”等变化,因此,手术难度和中转开胸风险从而增加,这与本研究患者基线资料比较与手术中表现一致。
在手术方面,本研究结果显示,中转开胸手术组的手术操作时长、术中失血量、术后胸腔闭式引流管留置时间、术后住院天数均高于全胸腔镜手术组,差异具有统计学意义(P<0.05),其原因是肺门冰冻与肺血管、支气管壁紧密粘连,操作空间狭小甚至无操作空间,导致分离解剖困难,进而增加手术难度,延长手术时间,此类情况通常是由于肺部或胸膜长期慢性感染性疾病造成。因此,在实际操作中发现211例“冰冻肺门”情况患者无法继续腔镜手术,选择中转开胸,通过组织剪锐性和腔镜吸引器顿性结合的方法缓慢剔除碳化淋巴结,充分暴露肺动脉,若出现累及血管鞘,可打开血管鞘进行操作;当淋巴结无法充分分离,可穿过淋巴结缝合,然后结扎动脉分支,结扎动脉后,用剪刀将血管与淋巴结沿着从支气管中分离出来,尽可能地将困难淋巴结向远端游离,然后可将血管、支气管一并离断。在处理部分肿大或者钙化淋巴结与肺动脉呈环状生长,特别是左肺基底干动脉,可对肺动脉主干做预处理,游离出同侧肺动脉主干,采用肺动脉主干套带技术,操作完毕后松开套带[10-12]。当然在面对严重的肺门瘢痕或冰冻,周围组织水肿,界限不清,经腔镜下游离困难时,无法找到更好的处理办法;如果一旦强行分离,导致血管损伤,出血速度迅猛,很难精准地在腔镜下控制出血,形成被动局面,往往会主动中转开胸进行手术,但也相应增加了术中风险,延长手术时间,增加出血,甚至延长术后住院时间。本研究中被动开胸手术组在手术时长和术中出血相比主动中转组差异具有统计学意义(P<0.05),主要原因是这54例中,因冰冻肺门干扰游离周围组织结构时腔镜尝试分离过程中不同程度撕裂肺血管导致出血,腔镜下处理困难,导致术中失血,紧急被动中转开胸。可见冰冻肺门的影响是腔镜手术中转开胸的重要因素,这与相关报道也是一致的[13-14]。
本研究进一步分析了术后并发症两组发生情况,结果显示,中转开胸组的皮下气肿、重新置管、切口感染、肺部感染、肺不张、术中或术后输血、持续漏气、术后72 h内疼痛评分发生率均高于全胸腔镜组,差异具有统计学意义(P<0.05)。其中,皮下气肿、肺部感染、肺不张发生率位列前三。分析认为,皮下气肿的发生与肺部持续漏气、胸膜腔压力增大、术后引流管不通畅、切口(特别是开胸手术切口)或引流管处胸膜、肌肉缝合不紧等有关,当出现严重皮下气肿,导致患者呼吸功能受阻,排除支气管胸膜瘘等情况后必要时可予以负压抽吸或皮肤或皮下切开排气以改善呼吸和症状[15]。其中,肺部感染与肺不张是肺手术后主要并发症,发生率高,分析认为可能与既往长期慢性肺部疾病、吸烟及术后疼痛导致咳嗽排痰能力差等有关,尤其是中转开胸手术患者,创伤大,肺功能恢复慢,更易出现肺部感染、肺不张等并发症,与相关报道一致[16-17]。需要特别注意的是,本研究中,中转开胸组和全胸腔镜组均发生2例支气管胸膜瘘,且该4名患者均为慢性感染性肺部病变。现有研究者认为,支气管胸膜瘘是肺手术后最为严重的并发症之一,处理困难且病死率高[18-19]。本研究中2例患者经保守治疗无效后行支气管胸膜瘘修补加带蒂大网膜覆盖,1例患者行带蒂心包脂肪垫覆盖术,术后恢复可,顺利拔除引流管。1例经保守治疗有效,术后32 d拔除引流管。
“冰冻肺门”增加了肺叶切除术的难度,尤其是胸腔镜手术的难度和并发症发生率, 因此在遇到此类肺门情况的患者时应充分做好术前准备,详细询问患者病史以及判读术前影像学资料,综合评估后再选择合适术式,应谨慎选择腔镜微创手术,减少不必要的中转开胸,增加患者围术期风险。同时,术中遇到此类肺门条件时操作需轻柔,避免解剖过程中损伤肺血管。随着术者对“冰冻肺门”的学习和总结手术经验,部分“冰冻肺门”条件,如少数门钉淋巴结是可以完整切除的,当然,在遇到难以分离的肺门致密粘连,术中充分评估后无法完整分离,继续分离会导致血管损伤大出血,术者需果断做出决定不应继续强行分离,此外术中也可根据情况适当调整术式,比如做肺动脉成形及袖式肺叶切除术,并不会因分离“冰冻肺门”增加出血风险。
因此,本研究认为,在胸腔镜肺叶切除手术过程中,出现“冰冻肺门”干扰情况是中转开胸的首要原因,延长了手术操作时间、住院天数,增加患者围手术期风险及术后并发症发生率。若术前通过胸部薄层CT平扫或增强,亦或者EBUS检查来对“冰冻肺门”进行评估,做好中转开胸预案,以保障患者围手术期安全为前提进行手术。
