基于非靶向脂质组学分析脂蛋白Rv1411c对结核分枝杆菌脂质代谢的影响
2024-04-30孙玉亭全舒婷孙柏旭田雪綦辉焦伟伟申阿东孙琳
孙玉亭 全舒婷 孙柏旭 田雪 綦辉 焦伟伟 申阿东 孙琳
结核分枝杆菌(Mycobacteriumtuberculosis,MTB)的细胞壁由分枝菌酸及嵌于其中的其他糖脂和游离脂类组成[1-2],脂蛋白作为组成MTB细胞壁及细胞膜的重要成分,与MTB的毒力及免疫逃逸能力密切相关[3-4]。目前,MTB基因组可编码约100个脂蛋白[5],这些脂蛋白可以通过抑制主要组织相容性复合体(major histocompatibility complex,MHC)Ⅱ类分子表达及干扰巨噬细胞中细胞因子的产生来促进MTB的免疫逃逸[6-7]。部分脂蛋白参与脂质转运并协助脂质定位进而发挥功能。如脂蛋白LprN参与组成转运蛋白,与MTB摄取利用胆固醇作为碳源的能力相关[8-9]。脂蛋白LppX也通过结合和运输结核分枝杆菌硫蜡醇(phthiocerol dimycocerosates,PDIM)参与细胞壁的生物合成[10]。而Rv1411c作为一种分泌型表面糖脂蛋白,即脂蛋白LprG,也被认为是MTB的毒力蛋白之一,在敲除Rv1411c基因后可导致MTB毒力减弱[11];还可以结合脂阿拉伯甘露聚糖(lipoarabinomannan,LAM)和磷脂酰肌醇甘露糖苷(phosphatidylinositol mannoside,PIM)等糖脂成分并参与两者的膜表面转运过程,与细菌细胞壁的生物合成、免疫识别和免疫逃逸均相关[12-15]。同时,Rv1411c与Rv1410还可共同组成操纵子参与到甘油三酯(triacylglycerol,TAG)由细胞质转运至细胞壁的过程中,而敲除该操纵子或单独敲除Rv1410均可见MTB内部TAG脂质的积累,说明脂蛋白Rv1411c可作为下游分子参与到TAG转运,协同Rv1410维持细菌内部的脂质代谢稳态,并促进细菌在宿主体内的长期存活[16],提示脂蛋白Rv1411c可能通过参与调节MTB自身的脂质代谢来协助MTB在宿主体内的存活,但其具体调控机制,以及是否通过参与其他脂质的转运过程来影响MTB的脂质代谢仍未可知。
脂质组学作为一种高效准确的高通量检测方法,能够精确地获取不同生物体间的脂质组成及成分差异,其中非靶向脂质组学分析能够实现对样本脂质成分的无偏向系统解析,最大程度地反映样品中脂质的变化规律,从而发现差异代谢物[17]。为进一步探索脂蛋白Rv1411c对MTB生长过程中脂质代谢的影响,深入研究MTB以脂质为核心的宿主体内生存策略,本研究应用液相色谱-质谱(LC-MS)联用技术及非靶向脂质组学分析技术检测敲除Rv1411c基因的MTB(ΔRv1411c)菌株及MTB标准株H37Rv培养上清的脂质谱,为后续寻找治疗MTB感染的新靶点和探索MTB在体内的长期持留机制提供线索和指导。
材料和方法
一、实验材料与仪器
1.实验材料:MTB标准株H37Rv购自美国细胞培养协会(ATCC)细胞库,由首都医科大学附属北京胸科医院国家结核病临床实验室赠予。7H9液体培养基(货号:271310)、Middlebrook OADS增菌液(货号:212351)和7H10固体培养基(货号:262710)均购自美国BD公司;吐温80(货号:P8074-500ML)购自美国Sigma-Aldrich公司;胰蛋白胨(货号:T8490-500G)、酵母提取物(货号:Y8020-500G)和琼脂粉(货号:A8190-1KG)均购自北京索莱宝科技有限公司。
2.主要试剂:氯化钠(货号:A100241-0500)和甘油(货号:A600232-0500)均购自生工生物工程(上海)股份有限公司;磷酸盐(PBS)缓冲液干粉(货号:P10003)购自北京索莱宝科技有限公司;高纯度低电渗琼脂糖(货号:TSJ001)购自北京擎科生物科技股份有限公司;Trans2K®Plus Ⅱ DNA Marker(货号:BM121-01)和Trans15K DNA Marker(货号:BM161-01)均购自北京全式金生物技术股份有限公司;T4 DNA 连接酶(货号:M0202S)、FastDigest Van91I(货号:FD0714)、Thermo ScientificTMPacI(货号:ER2202)和Phusion High-Fidelity DNA Polymerase(货号:F530L)均购自美国赛默飞世尔科技公司;氨苄青霉素钠(货号:0339-25G)购自美国Amresco公司;潮霉素B(货号:H7772)购自美国Sigma-Aldrich公司;包装试剂盒(货号:MP5120)购自美国Epicentre公司;质粒提取试剂盒(货号:DP105)购自天根生化科技(北京)有限公司;胶回收试剂盒(货号:D2500-02)和细菌基因组提取试剂盒(货号:D3350-02)均购自美国Omega公司;分枝杆菌药敏检测试剂盒(货号:F1004)购自珠海市银科医学工程股份有限公司。
3.主要仪器及软件:液相色谱仪(ExionLC AD)、高分辨质谱仪(TripleTOF 5600+)、数据采集软件(Analyst TF 1.7.1)均来自美国AB SCIEX公司;MS-Dial(ver.3.70, April 17, 2019)内置Lipidomics数据库和MetaboAnalyst 4.0分析鉴定及作图软件均来自美国。
二、研究方法
1.噬菌体介导的ΔRv1411c菌株构建:以H37Rv基因组DNA为模板,根据待敲除基因Rv1411c上下游基因片段序列设计左臂上/下游引物(LFP/LRP)和右臂上/下游引物(RFP/RRP),其中,引物LRP和RFP分别包含Rv1411c基因左、右端部分DNA序列;使用引物LFP/LRP及RFP/RRP高保真扩增获得Rv1411c基因左臂和右臂PCR产物(940 bp和698 bp),并使用Van91I酶切PCR产物与质粒p0004s连接并转化入DH5α大肠杆菌菌体蛋白(E.coliDH5α)感受态细胞,筛选成功后转入敲除Rv1411c基因的E.coliDH5α阳性克隆子并提取质粒测序;进一步使用限制性内切酶PacI酶切质粒p0004s-ΔRv1411c后,与同样经PacI酶切后的质粒phAE159连接、包装并转化入E.coliB101细胞中,筛选获得阳性噬菌粒phAE159-ΔRv1411c并电转化入感受态mc2155细胞中,涂板培养2~3 d后筛选噬菌斑并扩增制备高滴度噬菌体;感染H37Rv并涂布7H10固体平板,37 ℃培养4~5周后,挑取单克隆接种于7H9液体培养基中,37 ℃培养4~5周后,分别设计左/右臂上/下游敲除验证引物LYZFP/LYZRP和RYZFP/RYZRP,在LFP引物匹配序列上游100~200 bp处设计上游验证引物LYZFP,在RRP引物匹配序列下游100~200 bp处设计下游验证引物RYZRP,LYZRP引物设计于sacB基因,RYZFP引物设计于hyg基因,使用敲除验证引物LYZFP/LYZRP和RYZFP/RYZRP,以及左、右臂引物LFP/LRP和RFP/RRP对H37Rv菌株基因组DNA进行扩增及PCR验证,获得Rv1411c基因敲除的ΔRv1411c菌株,并排除样本问题导致的阴性结果。PCR引物设计部位及验证原理见图1,扩增及验证引物序列见表1。

表1 构建及验证引物序列

图1 两片段法PCR引物设计部位及验证原理
2. PCR扩增和凝胶电泳:提取待检测菌株基因组DNA作为PCR扩增模板,使用特异性引物对模板进行扩增,扩增体系为:10 ng DNA模板、正向引物和反向引物各1 μl(浓度约为10 pmol/μl)、脱氧核糖核苷酸三磷酸(dNTPs)混合液2.5 μl、10×PCR缓冲液2.5 μl及Taq DNA聚合酶1 U,补足至总体积25 μl的灭菌去离子水;PCR循环条件为:95 ℃,5 min;94 ℃,30 s;55 ℃,30 s;72 ℃,1 min;72 ℃,5 min;30个循环,4 ℃保存以终止反应。制备
含有1%(w/v)琼脂糖、适量的电泳缓冲液及核酸染料的溶液,加热溶解并在恒温条件下冷却至凝固形成凝胶板,将处理后的PCR产物和相应的分子量标准品(DNA ladder)均匀地加入到琼脂糖凝胶的加样孔内,在恒定电压下运行电泳,电泳结束后,使用紫外透射仪观察并记录凝胶图像,通过对比DNA ladder 确定PCR产物大小。
3. H37Rv及ΔRv1411c菌株的复苏与培养:取H37Rv和ΔRv1411c菌株冻存菌液各100 μl置于罗氏培养基上,培养3~4周时刮取少量菌,研磨后转接到7H9培养基(含有10% OADC添加剂+0.5%甘油+0.05% 吐温80)培养至对数生长期,按照1∶10进行传代,置于37 ℃培养箱内静置培养3~4周,待菌液的浓度增长至对数生长期A600值≈0.6~1.0时进行后续实验。A600值为在600 nm波长下测定的菌液吸光度值。
4.绘制菌株生长曲线:将对数生长期的H37Rv和ΔRv1411c菌株接种于7H9液体培养基中,调整菌液起始A600值约为0.1并将其分装至3只管中,每管10 ml,以保证起始浓度一致,再将其放置于37 ℃ 恒温培养箱中培养,分别在培养第0、3、6、9、12、15、18、21、24、27天时检测菌株A600值,并通过计算A600值均值绘制H37Rv与ΔRv1411c菌株在不同时间点的生长曲线。
5.脂质组学样品的收集及处理:将处于对数生长期的H37Rv和ΔRv1411c菌液加入到7H9培养基,调整菌液起始A600值约为0.1并将其分装至6只管中,每管5 ml,待菌株生长至A600值约为1.0时,离心收取菌液上清并过滤,每管取上清样本500 μl,冻存于-80 ℃待后续进行脂质组检测。考虑样品在进行脂质提取过程中的损失及结合脂质组学的样本量需求,研究选择了6份平行样品进行实验,以保证结果的准确性与可靠性。
6.液相色谱-质谱联用技术及非靶向脂质组学检测:每管菌液上清样品加入588.2 μl甲基叔丁基醚(MTBE)、117.6 μl甲醇(MeOH)和294.1 μl水(H2O),MTBE∶MeOH∶H2O=10∶2∶5(v/v),涡旋吹打混匀后超声10 min,3000 r/min离心15 min分离有机相与水相,取上层的MTBE层100 μl冷冻干燥。使用AB SCIEX TripleTOF 5600+质谱仪和AB SCIEX ExionLC AD液相色谱仪对脂质样品进行分析。流动相A相为50%水+50%乙腈(ACN)+10 mM羧基氢氧化铵(NH4COOH);流动相B相为10%硝酸铈铵(CAN)+90%异丙醇(IPA)+10 mM NH4COOH。液相色谱洗脱梯度为:0~0.5 min,10% B相;0.5~17 min,100% B相;17~20 min,10% B相。使用电喷雾电离源(ESI)的正负离子电离模式进行电离,ESI质谱条件为雾化电压5.5 kV(正离子模式)和4.5 kV(负离子模式),离子源温度为550 ℃,去簇电压为80 V,碰撞能量为TOF-MS:80 V;TOF-MS/MS:(35±15) V。在质量-电荷比(m/z)为50~1500范围内采集全扫描光谱。
三、脂质组数据处理与分析
使用MS-Dial(ver.3.70)软件对质谱原始数据进行峰识别、峰过滤和峰对齐等处理,进一步通过质量测定与结构表征分析,将代谢物与软件内置的Lipidomics数据库进行匹配,实现对代谢物的鉴定。利用MetaboAnalyst 4.0平台对样本进行归一化处理。使用单变量统计分析、多元变量统计分析、差异分析等方法对MS-Dial提取得到的数据进行分析。单变量统计分析采用t检验和变异倍数(FC)分析,多元变量统计分析采用有监督的偏最小二乘法判别分析方法(PLS-DA),使用模型决定系数R2及预测能力得分Q2评估PLS-DA模型的拟合效果和预测效果,一般R2、Q2值越接近于1说明模型越好,越低说明模型的拟合准确性越差,当R2为0.7或0.8时可表示模型解释能力较好,Q2>0.5也可表示预测能力较好,并且R2与Q2的值应该比较接近。在PLS-DA法中,变量权重(variable importance in projection,VIP)值被用来评估变量在模型中的重要性,VIP值>1被公认为是一个有效的阈值,用于识别在PLS-DA回归等多元统计分析方法中具有显著预测能力的变量或生物标志物,一般认为该变量在区分不同组别中有显著的重要性,故在研究中以VIP值>1、FC>1.5或<0.67且P<0.05为筛选标准筛选差异代谢物,以确保结果的可靠性和可比性。使用京都基因和基因组百科全书(KEGG)富集分析和拓扑分析方法分析差异脂质代谢物相关的代谢通路。
四、统计学处理
结 果
一、H37Rv菌株基因Rv1411c敲除与鉴定
对H37Rv菌株Rv1411c基因进行敲除,并进行PCR扩增和凝胶电泳检测以验证Rv1411c基因敲除是否成功。如图2所示,使用引物LYZFP/LYZRP和RYZFP/RYZRP对ΔRv1411c菌株基因组DNA扩增,分别得到长度为1160 bp和1225 bp的片段(泳道1和3);使用上述引物对H37Rv菌株基因组DNA扩增,未能得到扩增片段(泳道2和4);使用引物LFP/LRP和RFP/RRP对H37Rv菌株基因组DNA进行扩增,得到长度为940 bp和698 bp的扩增片段(图3),验证基因成功敲除,成功获得ΔRv1411c菌株。

注 泳道M为菌株DNA Marker梯段标志;泳道1和2分别为以ΔRv1411c菌株和H37Rv菌株DNA为模板使用引物LYZFP/LYZRP进行PCR扩增的结果;泳道3和4分别为以ΔRv1411c菌株和H37Rv菌株DNA为模板使用引物RYZFP/RYZRP进行PCR扩增的结果

注 泳道M为菌株DNA Marker梯段标志;泳道1和2分别为以H37Rv菌株DNA为模板使用引物LFP/LRP和RFP/RRP进行PCR扩增的结果
二、Rv1411c蛋白对MTB体外生长的影响
测定H37Rv与ΔRv1411c菌液在培养不同时间点的A600值,结果显示,H37Rv和ΔRv1411c菌株在培养的第0、3、6、9、12、15、18、21、24、27天的A600值差异均无统计学意义(表2,图4)。
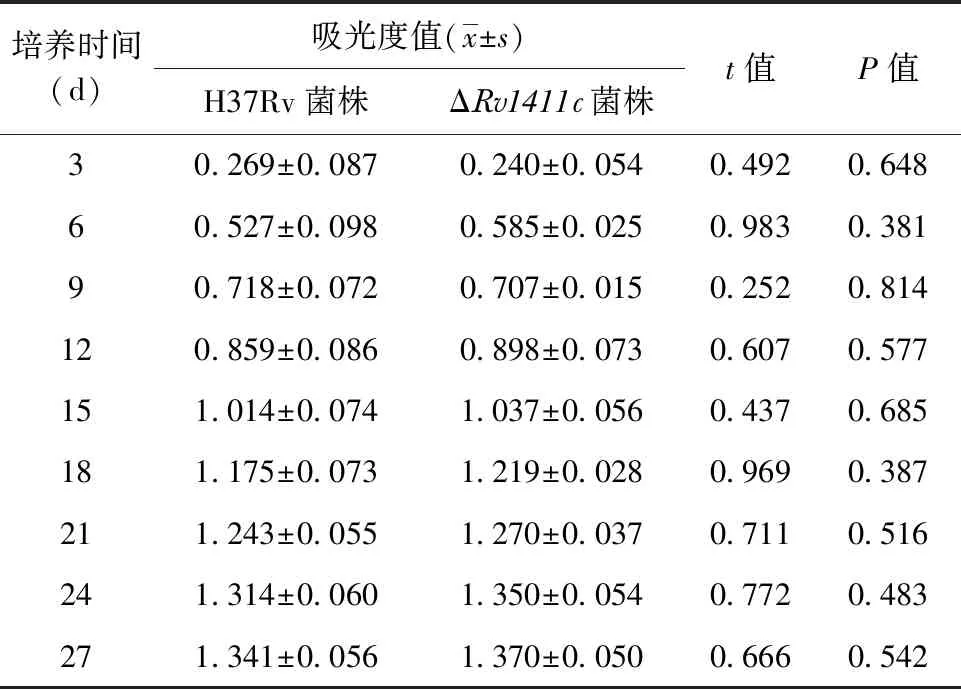
表2 培养不同时间点H37Rv和ΔRv1411c菌株的吸光度值检测结果
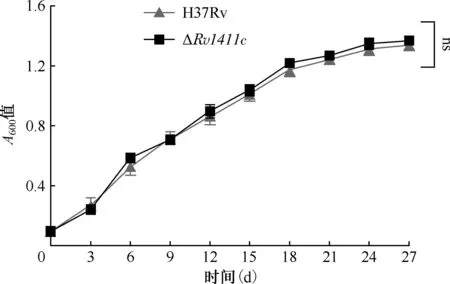
注 A600值为波长600 nm下测定的菌液吸光度值
三、Rv1411c蛋白对MTB脂质代谢的影响
1. H37Rv与ΔRv1411c菌液培养上清脂质代谢谱差异分析:采用PLS-DA法对H37Rv和ΔRv1411c菌株的脂质代谢进行分析,结果显示,H37Rv及ΔRv1411c菌液上清的脂质代谢成分具有良好的区分度,模型决定系数R2接近于1,预测能力得分Q2>0.34,说明PLS-DA模型拟合效果较好,模型具有一定预测能力且预测结果准确度较高(图5,表3)。样品通过色谱分离及质谱的精确质量测定与结构表征分析,成功鉴定出28种脂质亚类及460个不同的脂质分子,进一步通过PLS-DA模型分析获得17种脂质亚类的158个差异脂质分子(VIP值>1),部分VIP值>1.8的脂质分子见图6。
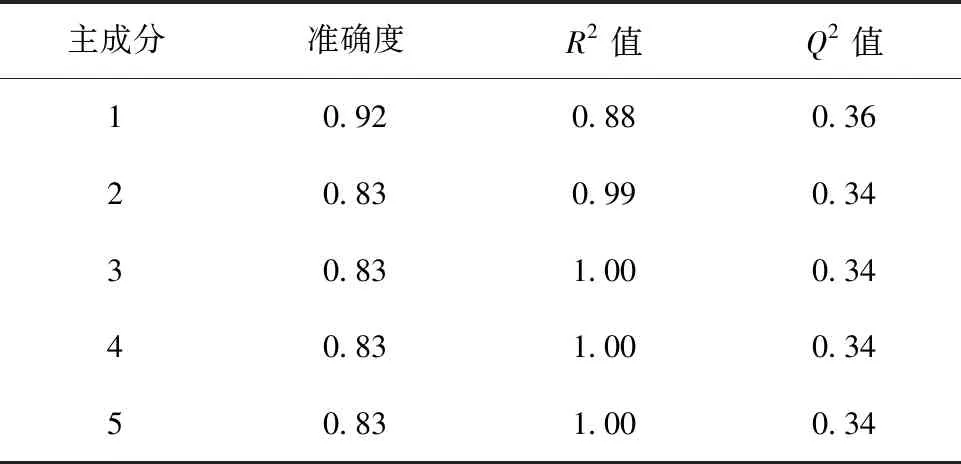
表3 PLS-DA模型性能评估结果
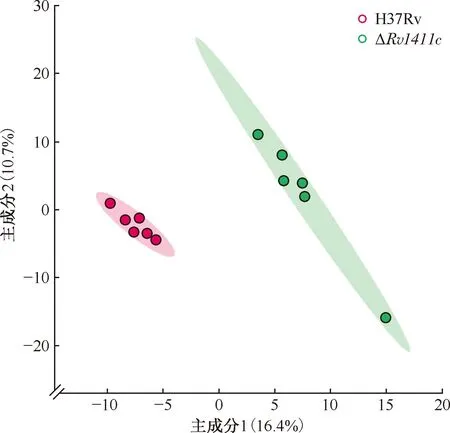
图5 H37Rv与ΔRv1411c菌株经偏最小二乘法判别分析法获得脂质代谢成分得分图 (n=6)
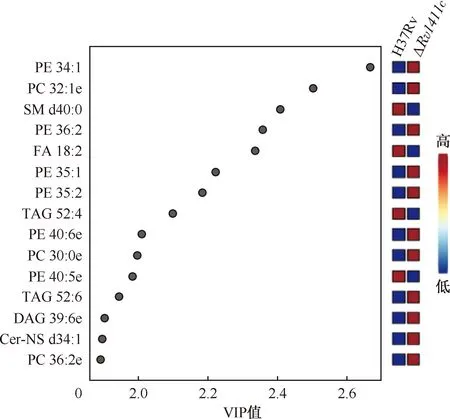
注 纵坐标代表脂质分子的质荷比分子量信息,其中,PE:磷脂酰乙醇胺,PC:磷脂酰胆碱,SM:鞘磷脂,FA:脂肪酸,TAG:甘油三脂,DAG:甘油二酯,Cer-NS:神经酰胺-NS;横坐标为各脂质分子的变量权重(VIP)值,介于1.8~2.8;右侧红紫色方块代表脂质分子在两组中表达量的高低
2. H37Rv与ΔRv1411c菌株中差异脂质分子的筛选:正、负离子模式下,进一步结合单变量统计学方法,在VIP值>1的基础上以FC>1.5或<0.67且P<0.05为筛选标准,从158个差异脂质分子中筛选H37Rv与ΔRv1411c菌株上清的差异脂质代谢物,共获得36个具有显著差异的脂质分子。与H37Rv相比,ΔRv1411c培养上清中有12个脂质分子上调,24个脂质分子下调(图7,表4)。差异脂质归属为11个亚类,分别为磷脂酰乙醇胺(phosphatidyl ethanolamine, PE)、磷脂酰胆碱(phosphotidylcholine, PC)、鞘磷脂(sphingomyelin, SM)、甘油二酯(diglyceride, DAG)、脂肪酸(fatty acid, FA)、TAG、神经节苷脂(ganglioside, GM)、溶血磷脂酰胆碱(lysophosphatidylcholine, LPC)、溶血磷脂酰乙醇胺(lysophosphatidyl ethanolamine, LPE)、磷脂酰肌醇(phosphatidylinositol, PI)和磷酯酰丝氨酸(phosphatidylserine, PS),以前三者脂质亚类为主(图8)。
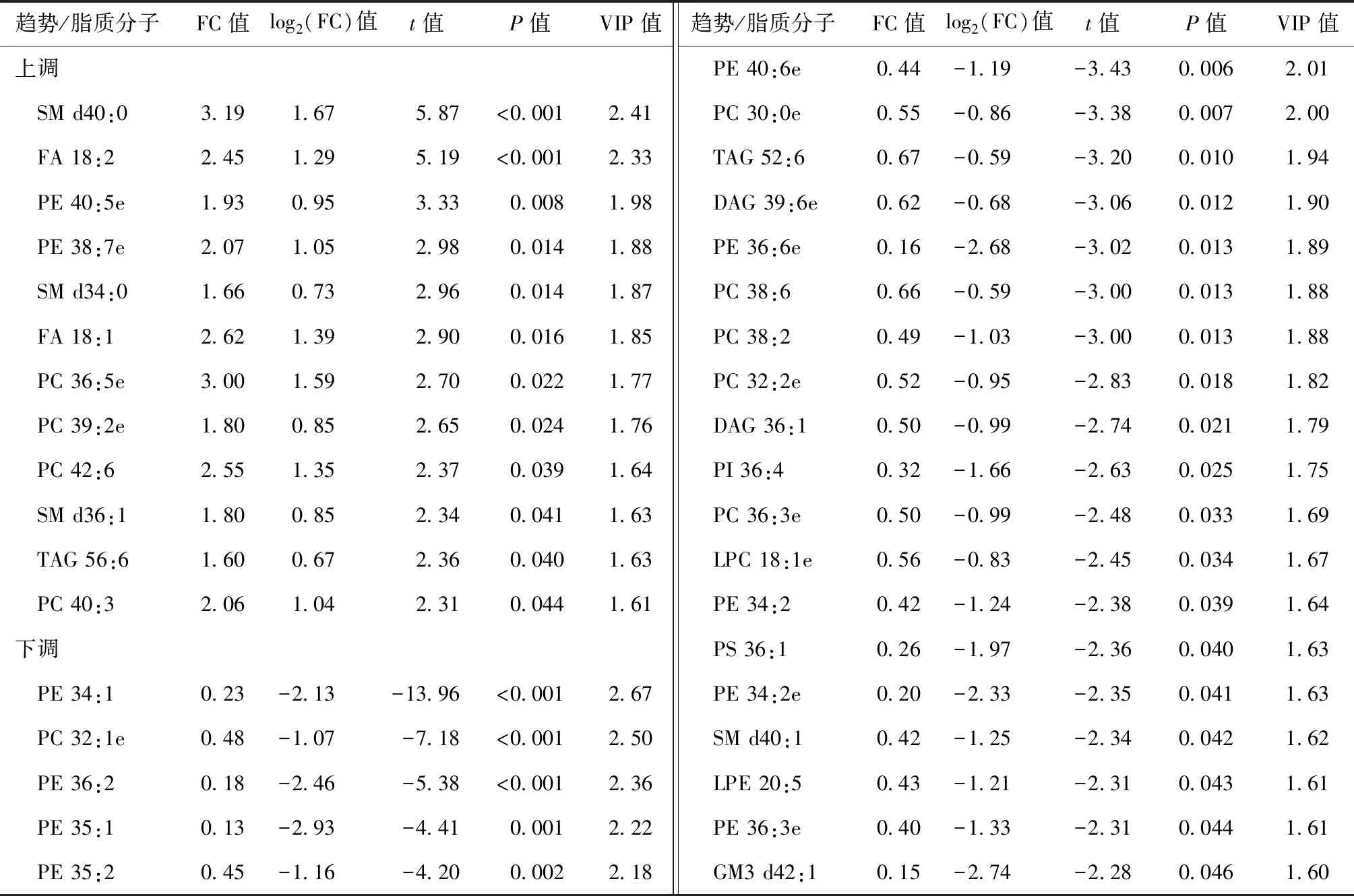
表4 H37Rv与ΔRv1411c菌株差异脂质成分分析结果
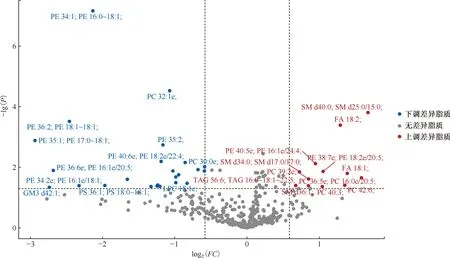
注 横坐标为log2转换后的差异表达倍数(FC)值,纵坐标为log10转换后的P值,-lg(P)是确保当P值减小时,对应的-y轴坐标值增大,即纵坐标越往上代表统计学的显著性越高。红点及蓝点分别代表符合筛选标准的上调及下调的差异脂质
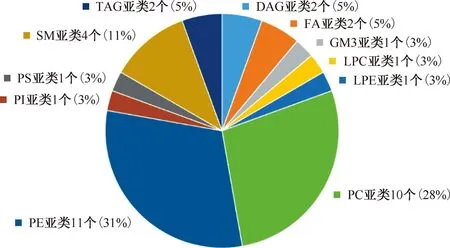
注 DAG:甘油二酯,FA:脂肪酸,GM:神经节苷脂,LPC:溶血磷脂酰胆碱,LPE:溶血磷脂酰乙醇胺,PC:磷脂酰胆碱,PE:磷脂酰乙醇胺,PI:磷脂酰肌醇,PS:磷酯酰丝氨酸,SM:鞘磷脂,TAG:甘油三脂
3.差异脂质分子代谢通路的富集分析和拓扑分析:利用MetaboAnalyst 4.0平台,对筛选出的36个显著差异的脂质分子进行KEGG代谢通路分析。结果显示,差异脂质代谢产物主要富集于以下8条通路,即:甘油磷脂代谢、亚麻酸代谢、α-亚麻酸代谢、糖基磷脂酰肌醇(GPI)-锚的生物合成、甘油脂代谢、鞘脂代谢、花生四烯酸代谢及不饱和脂肪酸的生物合成通路。根据拓扑分析影响因子数值进行分析及筛选,敲除Rv1411c造成的菌株间差异脂质与甘油磷脂代谢通路密切相关,其次为甘油脂代谢及糖基磷脂酰肌醇(GPI)-锚的生物合成通路(图9)。甘油磷脂代谢通路中有PE(C00350)、PC(C00157)和LPC(C04230)类所在的3个位点被映射(图10),其中,PE类映射的脂质分子包含PE 34:1、PE 34:2、PE 35:1、PE 35:2,在敲除菌株中表现为普遍的下调;PC类映射的脂质分子包含PC 30:0e、PC 36:5e、PC 38:2和PC 42:6,在敲除菌株中存在上调或下调的差异表达(图11);LPC类映射的脂质分子包含LPC 18:1e,在敲除菌株中表现为下调。
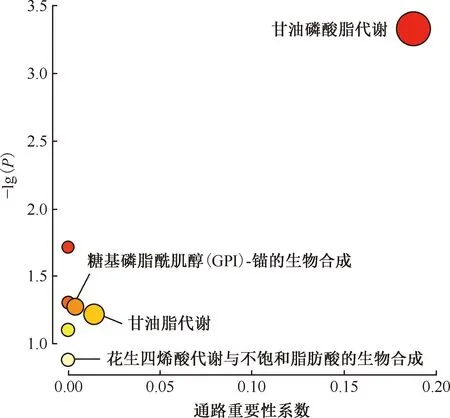
注 图中每个气泡代表1条代谢途径;纵坐标和气泡颜色深浅代表富集分析的P值[lg(P)],颜色深的代谢途径富集程度较高;横坐标及气泡面积则共同表示拓扑分析中该路径影响因素的大小

注 图中方框内字母和数字表示MetaboAnalyst 4.0平台对接的KEGG中的化合物代号,红色方框为处于代谢通路中重要节点的脂质分子
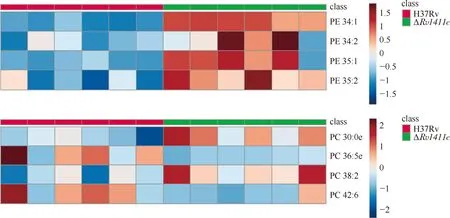
注 横坐标为红色和绿色代表的两种菌株,每种菌株均包含6个平行样品;纵坐标表示不同的脂质分子,颜色强度表示各脂质分子表达量的高低,由蓝色(下调)至红色(上调)变化
讨 论
MTB感染宿主后,机体可产生以巨噬细胞为核心的一系列复杂的免疫反应;同时,MTB也进化出不同的免疫逃逸机制来应对机体免疫细胞的杀伤[18]。脂质在MTB与宿主之间的免疫博弈中扮演着复杂的角色,一方面,MTB可以通过释放自身脂质成分参与宿主免疫的激活;另一方面,组成MTB包膜的糖脂成分参与协助入侵巨噬细胞及免疫逃逸[19-22]。除此之外,脂质也是MTB在宿主细胞中可利用的主要碳源[8]。研究发现,MTB可通过释放自身代谢产物,影响宿主的免疫反应及脂质代谢,维持自身在宿主体内的生存[23]。由此可见,MTB释放的脂质代谢成分与其致病机制密切相关。
本研究利用噬菌体介导的MTB基因敲除技术构建了Rv1411c敲除的菌株ΔRv1411c,发现体外生长的ΔRv1411c显示出与H37Rv菌株相似的倍增时间和生长特性,提示Rv1411c敲除并不影响标准培养基培养条件下的菌株生长,与Bigi等[11]研究结果一致。本研究通过非靶向脂质组学分析,发现敲除Rv1411c可显著影响MTB的脂质代谢,与H37Rv相比,ΔRv1411c上清中下调的差异脂质分子占总差异脂质的2/3,且下调的脂质分子涉及多种脂质亚类。基于此,笔者推测脂蛋白Rv1411c可能参与协助多种脂质从胞内向胞外转运的过程,进而有助于维持MTB内部的脂质代谢稳态。但目前的研究仅证明了脂蛋白Rv1411c具有对TAG、LAM、PIM等三酰化脂质的结合及转运功能,而对其他亚类脂质转运过程中发挥作用的机制还有待进一步研究和探索[13-14, 16]。因此,本研究为进一步探索MTB脂蛋白对于细菌脂质和能量运输中的作用机制提供了线索,也为今后探索其与细菌毒力的关系提供了思路。
MTB作为一种胞内寄生菌,可通过能量代谢的调节适应宿主微环境[24]。有研究发现,某些脂类代谢物与MTB在宿主体内的长期持留有关,在感染宿主期间MTB利用FA作为主要碳源,通过诱导巨噬细胞内FA等脂质的积聚来作为自身碳和能量的来源[25-27]。FA脂类有助于PDIM等MTB毒力分子的生成,可被直接同化成细胞膜磷脂,与细胞膜的完整性相关[28-29]。据此,笔者通过分析这些可能被分泌到胞外的脂质的变化和功能,间接揭示出它们在整体脂质代谢网络中的动态角色和潜在的生物学意义。本研究发现,ΔRv1411c上清中的FA亚类脂质成分发生明显变化,相较于H37Rv明显上调,提示敲除Rv1411c可能通过促进FA亚类脂质在转运过程中的外排或减弱FA亚类脂质在细胞壁上的锚定发挥作用,与MTB的毒力及胞内存活能力相关。以上说明MTB FA亚类的脂质与MTB的毒力及胞内存活能力密切相关,FA亚类脂质代谢对于MTB具有重要意义。对于其他差异脂质亚类的研究目前尚存不足。
通过对差异脂质的代谢通路分析,我们发现差异脂质代谢产物主要富集于以下8条通路,即:甘油磷脂代谢、亚麻酸代谢、α-亚麻酸代谢、糖基磷脂酰肌醇(GPI)-锚的生物合成、甘油脂代谢、鞘脂代谢、花生四烯酸代谢及不饱和脂肪酸的生物合成通路。经拓扑分析发现,与菌株间差异脂质最相关的代谢通路为甘油磷脂代谢,其次是甘油脂代谢和糖基磷脂酰肌醇(GPI)-锚的生物合成通路。甘油磷脂包括PE、PC、PI和PS等多种亚类,敲除Rv1411c后PE和PC类脂质相较于H37Rv发生了较明显的变化,24个下调的脂质分子中有17个集中分布于PE和PC类脂质,提示脂蛋白Rv1411c与上述脂质向胞外运输有关。研究发现,甘油磷脂(特别是PE)与PIM和LAM等脂质成分存在于MTB胞膜的最外层,是MTB与宿主之间相互作用的重要成分[30]。MTB可将PE和PI等脂质分子释放到宿主体内,以促进MTB在宿主体内的持久感染[31]。由此可见,脂蛋白Rv1411c可能是甘油磷脂从胞内向胞外转运的重要载体,间接介导了MTB与宿主之间的相互作用。有研究发现敲除Rv1411c可显著影响MTB在小鼠体内的生存,推测与敲除Rv1411c所导致的毒力衰减相关[11, 16]。我们的结果也进一步佐证了该研究的假说,即脂蛋白Rv1411c有可能通过协助PE和PI等脂质分子向宿主细胞的释放发挥毒力作用。考虑本文主要集中于菌株的脂质代谢,故将在未来对后两者通路脂质代谢的变化规律及可能的分子机制研究详细解析,以提供新的科学发现和理论支持。
总之,本研究构建了Rv1411c敲除的MTB菌株ΔRv1411c,考虑到脂蛋白Rv1411c在前期研究中主要参与脂质从包膜内到包膜外的转运,且部分脂质可脱离至菌体外,故研究聚焦于上清中菌株外排的分泌型脂质组学代谢差异,发现敲除Rv1411c后,菌株培养上清的脂质代谢谱发生明显差异,且以脂质下调为主。差异脂质代谢产物主要富集于甘油磷脂代谢通路,提示脂蛋白Rv1411c参与多种甘油磷脂类代谢产物由胞内向胞外的转运过程。本研究也存在一定局限性,如未结合菌株内部的脂质代谢情况进行分析,后续研究有必要从MTB调控自身整体脂质代谢的改变入手,进一步探索脂质代谢与MTB的毒力、致病力和胞内生存的关系,以及通过脂质层面调控清除宿主体内结核分枝杆菌潜伏感染的机制,这对于进一步揭示MTB与脂质相关的致病机制及开发新的抗结核药物和减毒疫苗均具有重要意义。
利益冲突所有作者均声明不存在利益冲突
作者贡献孙玉亭:实验设计、开展实验研究、采集和分析数据、撰写文章;全舒婷、孙柏旭和田雪:参与实验实施、收集分析和解释数据;綦辉、焦伟伟、申阿东和孙琳:实验设计、对文章的知识性内容作批评性审阅/指导,提供技术、材料和经费支持
