D-二聚体水平升高与继发性新生儿持续性肺动脉高压的关系探讨
2024-04-30白波陈波李广洪罗惠玲黄学良李菲
白波 陈波 李广洪 罗惠玲 黄学良 李菲
广州市花都区人民医院新生儿科,广州 510800
新生儿持续性肺动脉高压(persistent pulmonary hypertension of the newborn,PPHN)是指出生后肺血管阻力持续性增高,使胎儿型循环过渡至正常成人型循环发生障碍,而引起的心房和/或动脉导管水平血液的右向左分流,临床出现严重低氧血症等症状。Nakwan等[1]报道其病死率高达20.6%,其中新生儿肺血管适应不良,即因围产期窒息、肺实质性疾病、败血症等原因导致新生儿肺血管不能适应出生后的环境而舒张,肺动脉压力不能下降,被认为是继发性PPHN 的主要原因[2]。随着新生儿科以目标为导向的床边B 超技术的开展,能实时动态地监测新生儿肺动脉压力,部分肺动脉高压(pulmonary hypertension,PH)新生儿的肺动脉压并非是出生后持续不降,而是降而复升,一部分还出现PPHN的血液动力学改变[2],其中D-二聚体水平异常升高可能与此有关,为此笔者进行了相关研究,现报道如下。
资料与方法
1.一般资料
选择2020年6月1日至2023年5月31日于广州市花都区人民医院新生儿科近6 000人次住院患儿中符合《新生儿肺动脉高压诊治专家共识》[2]诊断标准的100例新生儿为研究对象。根据纳入标准分为PPHN 组33 例和PH 组67 例。(1)纳入标准:①孕周32~42 周适于胎龄儿;②需呼吸机辅助呼吸才能改善缺氧症状和体征;③入组前床边彩色多普勒超声检查肺动脉收缩压(pulmonary arterial systolic pressure,PASP)≤35 mmHg(1 mmHg=0.133 kPa);④入组时床边彩色多普勒超声检查PASP>35 mmHg;⑤床边彩色多普勒超声检查显示心房和/或动脉导管水平存在右向左或双向分流,或室间隔向左室凸起。(2)排除标准:①合并膈疝、复杂型先天性心脏病及母亲产前使用过非甾体类抗炎药;②家长明确拒绝受试儿的血液标本被用于科研。满足纳入标准①~⑤者纳入PPHN 组,仅满足纳入标准①~④者纳入PH组。
本研究经广州市花都区人民医院医学伦理委员会审批通过(批号:2022005)。
2.方法
所有受试儿均参照《实用新生儿学(第5 版)》[3]相关疾病及《新生儿肺动脉高压诊治专家共识》[2]进行综合管理和治疗,并根据缺氧症状与体征、经皮动脉血氧饱和度(transcutaneous oxygen saturation,SpO2)及血气分析结果按《新生儿机械通气常规》[4]予以相应的辅助呼吸支持,调节相关参数以保持SpO2≥90%,动脉血氧分压(percutaneous arterial oxygen saturation,PaO2)≥60 mmHg,动脉血二氧化碳分压(partial pressure of carbon dioxide,PaCO2)为30~50 mmHg,pH 值为7.25~7.45。除在入组时即刻进行血气分析、血乳酸及血浆D-二聚体检测或复测,并记录下连续常规监护仪监测的体温、脉搏、呼吸、SpO2、血压等参数外,入组后每6~12 h在常规1次床边B超检测PASP基础上,同时监测右上肢及下肢末端SpO2;当右上肢SpO2有明显波动或与下肢SpO2差值>5%时,即刻复测PASP。
3.PASP测定
采用彩色多普勒超声心动图仪(购自美国Philip 公司,型号:CX-30),探头频率为3.75~7.00 MHz,参照文献[5]的方法,测定所有受试儿最大三尖瓣反流压差及反流程度等,根据简化Bernoulli方程计算PASP。
4.D-二聚体检测
所有新生儿入组时采集静脉血2 ml,置于9∶1柠檬酸钠真空采血管中,送本院检验中心,采用酶联免疫荧光法检测血浆D-二聚体浓度(采用美国Instrumentation Laboratory Company 生产的 D-Dimer 试剂盒,产品编号:HD138-00014),正常值范围:10~500 µg/L,相关实验操作严格按照试剂盒说明书进行。
5.统计学方法
本研究数据采用SPSS 20.0 软件包进行数据处理和统计学分析。对于呈近似正态分布、方差齐的计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验;非正态分布的计量资料以中位数(四分位数)[M(P25,P75)]表示,组间比较采用Mann-WhitneyU检验;计数资料以例(%)表示,采用χ2检验,等级资料采用秩和检验;相关性分析采用Pearson 相关性分析;利用受试者操作特征曲线(receiver operating characteristic curve,ROC)分析血浆D-二聚体水平预测PPHN 的价值;对PPHN 的影响因素分析采用多因素logistic逐步回归分析,以P<0.05表示差异有统计学意义。
结果
1.PPHN组与PH组患儿临床资料比较(表1)

表1 PPHN组与PH组患儿临床资料比较
PPHN 组患儿的PASP、D-二聚体水平均高于PH 组,差异均有统计学意义(均P<0.001);高乳酸血症(血乳酸>3 mmol/L)、休克评分[3]≥4 分、酸中毒失代偿(pH≤7.2)、低氧血症(PaO2≤60 mmHg)及低碳酸氢盐(HCO3-≤18 mmol/L)患儿占比均高于PH 组,差异均有统计学意义(均P<0.05);两组患儿的孕周、性别、出生体质量、分娩方式、入组日龄、原发疾病、高碳酸血症(PaCO2>50 mmHg)比较,差异均无统计学意义(均P>0.05)。
2.血浆D-二聚体水平与PASP的相关性分析(图1)

图1 100 例肺动脉高压新生儿血浆D-二聚体水平与肺动脉收缩压(PASP)的相关性分析
Pearson相关性分析结果显示:所有患儿的血浆D-二聚体水平与其PASP水平呈正相关(r=0.671,P<0.001)。
3.血浆D-二聚体水平预测PH 新生儿发生PPHN 的ROC分析(图2)
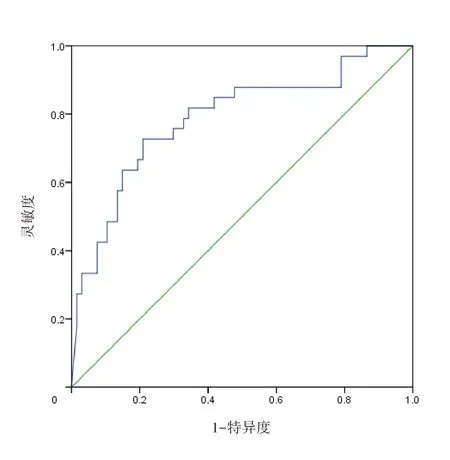
图2 D-二聚体水平预测100例肺动脉高压新生儿发生PPHN的ROC
血浆D-二聚体水平曲线下面积为0.788[P<0.001,95%置信区间(CI)为0.688~0.888)],当约登指数最大为0.518时,血浆D-二聚体水平的截断值为3 770.265 µg/L,其预测PPHN发生的灵敏度为0.727,特异度为0.791。
4.影响PPHN发生的多因素logistic回归分析(表2)
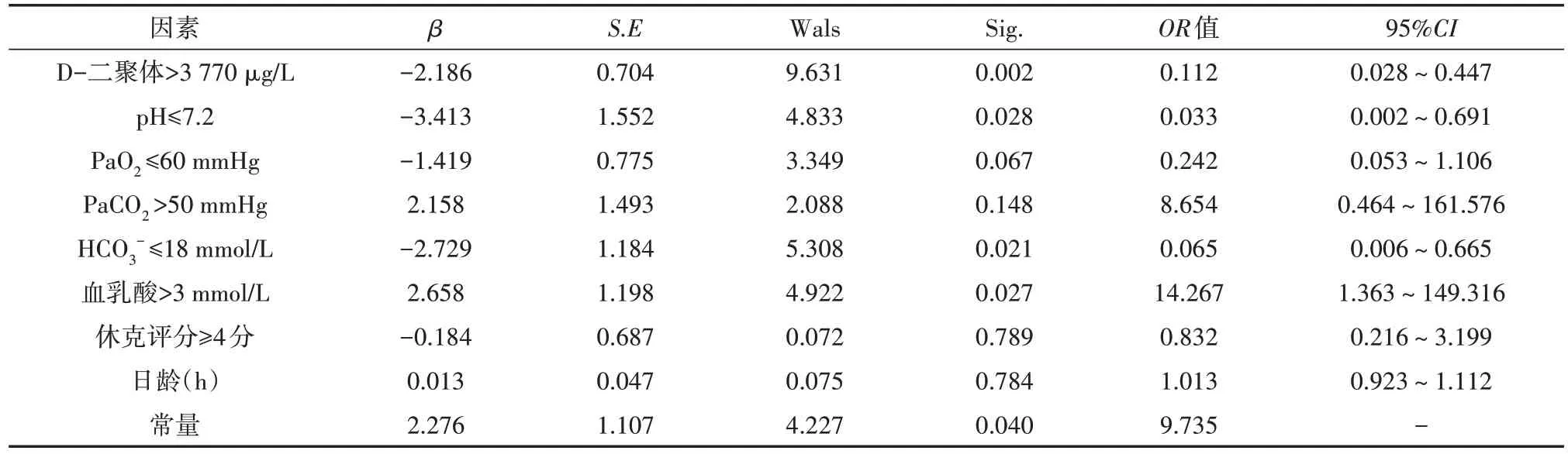
表2 100例肺动脉高压新生儿发展为PPHN的多因素logistic回归分析
以是否发生PPHN为因变量(赋值:发生=1,未发生=0),将血乳酸(赋值:>3 mmol/L=1,≤3 mmol/L=0)、D-二聚体(赋值:>3 770 µg/L=1,≤3 770 µg/L=0)、pH 值(赋值:≤7.2=1,>7.2=0)、PaO2(赋值:≤60 mmHg=1,>60 mmHg=0)、PaCO2(赋值:>50 mmHg=1,≤50 mmHg=0)、HCO3(-赋值:≤18 mmol/L=1,>18 mmol/L=0)及休克评分(赋值:≥4 分=1,<4 分=0)及入组日龄实际数值作为自变量纳入logistic 逐步回归分析,结果显示,D-二聚体、pH、HCO3-、血乳酸水平均是PH 患儿是否发展为PPHN 的影响因素(OR=0.112、0.033、0.065、14.267,均P<0.05)。
讨论
继发性PPHN 是新生儿期的一种严重疾病,常继发于窒息、吸入胎粪及呼吸窘迫综合征、严重感染等,吸入一氧化氮是治疗PPHN 的标准手段,但Pedersen 等[6]报道仍有30%以上的患儿因治疗效果不佳而生命受到威胁,提示继发性PPHN 的发生除与血管适应不良有关外,可能还有或伴有其他因素。赵松林和聂秀红[7]研究发现,血液高凝状态及肺血栓形成引起的血管内梗阻与成人慢性阻塞性肺疾病急性加重期合并PH 的发生有重要关系;Sharma 等[8]、Gijtenbeek 等[9]都发现,部分新生儿红细胞增多症患儿也可发生PPHN;Sergi 等[10]、Avasiloaiei 等[11]报道,在部分死亡的PPHN 患儿肺血管中发现大量血栓。这些研究都提示高凝状态或血栓形成引起的血管内梗阻可能也是新生儿PH 发生的重要原因。
D-二聚体是由纤维蛋白原经凝血酶、活化的Ⅷ因子作用下聚合、交联,再经纤溶酶降解后形成的包含2 个共价结合的D 结构的一种可溶性纤维蛋白降解产物。Park 等[12]发现,D-二聚体在正常人血液中的浓度很低,只有凝血发生后,交联纤维蛋白形成和降解的D-二聚体才能被激活。D-二聚体对高凝状态和血栓形成有很高的灵敏度,是特异性反映体内高凝状态和继发性纤溶亢进的分子标志物之一[13-14]。研究表明,缺氧、酸中毒、感染、炎症介质等因素均可导致肺血管内皮功能损伤,内皮细胞发生变性、坏死脱落,内皮下胶原纤维裸露,凝血级联反应易被激活,可导致患者血液处于高凝状态,甚至形成微血栓,使肺血管阻力增加,肺动脉压升高[15-16]。高凝状态或血栓形成反过来又可刺激血管内皮细胞、单核-巨噬细胞等炎症细胞,合成释放肿瘤坏死因子α、白细胞介素6(IL-6)、IL-10、IL-1β、内皮素1 等炎症介质,通过“炎症-内皮细胞-凝血”网络,导致炎症不断扩大,形成恶性循环从而加重PH[17-18]。已有研究证明,D-二聚体水平升高不仅与肺动脉血栓负荷显著升高有关,还与肺动脉压升高的程度及与急性肺栓塞患者危险分级呈正相关[7,19-21]。因而,D-二聚体已成为一项重要的辅助检查,被推荐用于诊断与排除诊断成人肺栓塞,但是否适用于儿童尚无一致意见[22]。
本研究发现,PPHN 组患儿血清D-二聚体水平显著高于PH 组(P<0.001),且D-二聚体水平与PASP 水平呈正相关(P<0.001);用D-二聚体水平预测PH新生儿发生PPHN的ROC 曲线下面积为0.788(P<0.001),当约登指数最大为0.518 时,D-二聚体水平截断值为3 770.265 µg/L,其预测PPHN 发生的灵敏度为0.727,特异度为0.791;多因素logistic 回归分析发现,D-二聚体水平>3 770 µg/L、pH≤7.2、HCO3-≤18 mmol/L 及血乳酸>3 mmol/L 均是PPHN 发生的独立危险因素(均P<0.05)。据此,笔者认为,新生儿PH 与D-二聚体水平异常升高有关,且D-二聚体水平越高,高凝状态可能越重,血栓形成的可能性更大,从而导致血管阻力更大、PASP 更高及组织供血更少;当动脉导管水平及/或心房水平发生右向左或双向分流时,则发展为PPHN 而出现严重的低氧血症。
本研究结果还提示,继发性PPHN 的发生并非都是因为血管适应不良而导致PASP持续不降,部分可能是降而复升,其原因可能与多数医院新生儿科尚未开展以目标为导向的床边B 超检查技术,较难实现实时动态监测PASP 有关[20]。本研究笔者认为,部分PPHN 的发生可能是一个渐进的过程,在这过程中,高凝状态、微血栓形成可能是PPHN发生或进一步恶化的重要原因,既可能是缺氧、酸中毒、感染等因素损伤肺血管的结果,也可能是炎症介质引起肺血管再损伤的始动因素。因而认为,在临床实践中,对有缺氧、酸中毒、感染等疾病的新生儿除尽可能实时动态监测PASP外,还需动态监测D-二聚体水平,当PASP>35 mmHg且需呼吸机辅助呼吸方能改善缺氧症状者,若其D-二聚体水平异常增高,应高度警惕PH 是否与高凝状态或微血栓形成有关,及时辅以抗凝、抗血栓、抗炎症反应可能会让患儿获益更多。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明白波、李菲:酝酿和设计试验,实施研究,采集数据,分析/解释数据,起草文章,统计分析;陈波:酝酿和设计试验,实施研究,采集数据,分析/解释数据,对文章的知识性内容作批评性审阅,统计分析,获取研究经费,行政、技术或材料支持,指导;李广洪:酝酿和设计试验,实施研究,采集数据,分析/解释数据,对文章的知识性内容作批评性审阅,统计分析;罗惠玲、黄学良:实施研究,采集数据,分析/解释数据,对文章的知识性内容作批评性审阅,统计分析
