伴甲状腺炎的抗GAD65抗体阳性自身免疫性脑炎1例
2024-04-25杨秋蓉郑昭时韩雪梅
于 乐,安 晶,杨秋蓉,郑昭时,韩雪梅
(吉林大学中日联谊医院 神经内一科,吉林 长春130033)
1 临床资料
患者,女性,54岁,因“行走不稳、言语笨拙1周”于2022年6月来本院就诊。1周前无明显诱因出现行走不稳、言语笨拙,一过性眩晕,可在他人搀扶下行走,言语笨拙类似吟诗样。既往否认饮酒史、特殊药物及毒物服用史;家族中无类似疾病病史。神经系统查体:意识水平及意识内容正常,无失语,小脑性语言,概测视野正常,双侧水平眼震,四肢肌力正常、肌张力略降低,共济失调步态,双侧指鼻试验不稳准,双侧快速轮替试验笨拙,双侧跟膝胫试验欠稳准,昂白氏征睁眼及闭眼均不稳准,左侧病理征阳性可疑,余体格检查未见明显异常。改良Rankin量表(mRS)4分,国际合作共济失调量表(ICARS)37分,共济失调等级量表(SARA)13分。以“小脑共济失调”收入院。实验室检查结果:游离三碘甲状腺原氨酸(FT3)2.37 pmol/L(参考值3.1~6.8 pmol/L)、总三碘甲状腺原氨酸(T3)0.74 nmol/L(参考值1.35~3.15 nmol/L)、总甲状腺素(T4)54.2 nmol/L(参考值70~156 nmol/L)、促甲状腺激素(TSH)0.456 mIU/L(参考值0.372~4.94 mIU/L)、抗甲状腺球蛋白抗体(TgAb)53.7%(参考值0~35%)、抗甲状腺微粒体抗体(ATM)51.6%(参考值0~35%)、抗甲状腺过氧化物酶抗体(TPOAb)155.2 IU/ml(参考值0~34 IU/ml)、甲状旁腺激素(PTH)82.23 pg/ml(参考值15~65 pg/ml)。人附睾蛋白4(HE4)91.89 pmol/L(参考值<140 pmol/L)、糖类抗原242(CA242)20.94 U/ml(参考值<20 U/ml)。糖化血红蛋白4.7%(参考值4.6~6.0%)。甲状腺超声:甲状腺双叶结节(ACR-TIRADS:1、2及3类)。头颅MRI平扫(图1):双侧小脑半球、右侧基底节区、半卵圆中心、放射冠区及左侧额叶腔隙性脑梗死及软化灶;DWI像未见异常。脑电图正常。肌电图:双下肢深感觉径路传到皮层段波幅下降。胸部CT未见明显异常。脑脊液常规生化检查:葡萄糖4.5 mmol/L(参考值2.2~3.9 mmol/L),其余正常。脑脊液及血清行自身免疫性脑炎、中枢神经系统脱髓鞘病及副瘤综合征抗体检测:抗GAD65抗体IgG阳性(1∶100,CBA法)。FDG-PET(图2):双侧顶叶、额叶、Broca区、前扣带回、后扣带回、左侧顶颞叶糖代谢降低,双侧尾状核、双侧小脑、丘脑、脑桥、中脑、右侧颞叶外侧、双侧颞中回糖代谢增高,脑实质内见斑片状低密度影,不伴糖代谢异常。全身FDG-PET未见恶性肿瘤表现。诊治过程:结合患者临床资料及相关辅助检查,诊断为伴甲状腺炎的抗GAD65抗体阳性自身免疫性脑炎,给予人类免疫球蛋白及大剂量激素冲击治疗,激素减量,后长期口服小剂量激素维持治疗,共济失调症状明显好转,mRS评分1分,ICARS评分22分,SARA评分9分。2022年8月首次复诊:患者病情平稳,为强化免疫治疗,给予环磷酰胺每月1次静点。复查头颅MRI较前未见明显变化,甲状腺功能各项指标均恢复正常,血清抗GAD65抗体滴度为1∶10,后患者由于疫情无法复诊,导致共济失调症状加重,需他人搀扶才可行走数米。于2023年4月来院行环磷酰胺治疗后,症状再次好转,可独立行走数百米。2023年8月复查,环磷酰胺累积剂量达8 g,患者症状稳定。
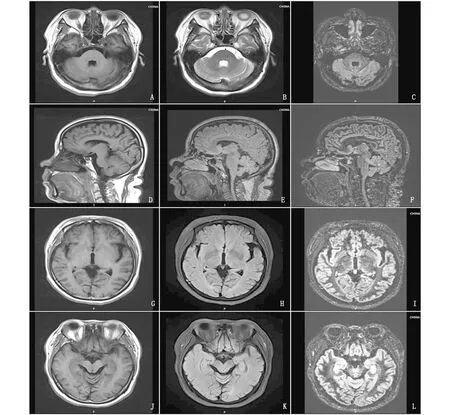
图1 头颅MRI检查结果 [A.小脑横断面MRI(T1未见小脑萎缩);B.小脑横断面MRI(T2未见小脑萎缩);C.双反转序列图像横断面(小脑蚓部高信号);D.小脑矢状面MRI(T1未见异常);E.小脑矢状面MRI(T2未见异常);F.双反转序列图像矢状面(小脑蚓部高信号);G.幕上横断面MRI(T1未见异常);H.幕上横断面MRI(T2未见异常);I.双反转序列图像横断面(幕上未见异常);J.海马横断面MRI(T1未见异常);K.海马横断面MRI(T2未见异常);L.双反转序列图像横断面(海马未见异常)]
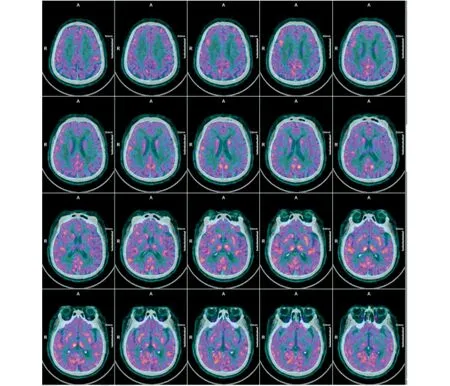
图2 FDG-PET检查结果 (双侧顶叶、额叶、Broca区、前扣带回、后扣带回、左侧顶颞叶糖代谢降低,双侧尾状核、双侧小脑、丘脑、脑桥、中脑、右侧颞叶外侧、双侧颞中回糖代谢增高,脑实质内见斑片状低密度影,不伴糖代谢异常)
2 讨论
自身免疫性脑炎(autoimmune encephalitis,AE)是由抗神经元抗体介导的中枢神经系统炎症性疾病,可出现多种神经及精神症状,抗谷氨酸脱羧酶(glutamic acid decarboxylase,GAD)65抗体阳性AE为其亚型之一。AE是非感染性脑炎最常见的原因之一,介导AE发病的抗体大致分为三类:第一类为抗细胞表面抗原抗体,包括抗N-甲基-D-天冬氨酸受体(NMDAR)抗体、抗富亮氨酸胶质瘤失活蛋白1(LGI1)抗体、抗γ-氨基丁酸B型受体(GAB-ABR)抗体等;第二类为抗细胞内突触抗原抗体,包括抗GAD抗体、抗两性蛋白抗体等;第三类为抗细胞内抗原抗体,包括抗Hu抗体、抗Ma2抗体、抗CV2抗体等[1]。抗细胞内抗原抗体多与小细胞肺癌、乳腺癌、胸腺瘤等肿瘤伴行,若同时检测到抗细胞内抗原抗体与抗细胞表面抗原抗体,患者患隐匿性肿瘤的风险更高,且对免疫治疗的反应性更差,这与神经元不可逆损伤有关,但抗GAD65抗体与肿瘤相关性较小,进展较慢,对免疫治疗反应较好[2]。
GAD是介导兴奋性神经递质L-谷氨酸经脱羧转化为抑制性神经递质GABA的限速酶,在小脑、海马、基底神经节、脑干和脊髓灰质等富含GABA能神经元处高表达,在突触前末端合成的GABA被包裹在突触囊泡中后通过胞吐释放到突触间隙,与突触后膜上GABAR结合,导致突触后神经元超极化,产生抑制信号,参与突触的神经传递[3]。抗GAD65抗体是一种具有表位特异性的致病性自身抗体,阻碍囊泡穿梭到释放位点,可逆地减少GABA的合成及胞吐,减弱GABA对邻近谷氨酸释放的突触前抑制,导致GABA与谷氨酸失衡,产生神经系统的兴奋毒性作用,抗体也可使小脑浦肯野纤维不可逆地损伤。GAD作为胞内酶,无法直接与抗GAD65抗体结合,但通过与细胞内蛋白形成复合物锚定在突触囊泡膜上,使其在胞吐过程中短暂暴露于细胞表面,当突触囊泡膜与突触前膜融合时,GAD被抗体识别。抗GAD65抗体也可通过在血管外膜的成纤维细胞中内化,使其能穿透神经元,从而导致GAD功能受损,损害GABA能传递[4]。
抗GAD65抗体由于选择性抑制不同的GAD酶活性,而GAD免疫识别的差异即表位特异性,使GABA能通路受到选择性抑制,导致表型多样性。因此抗GAD65抗体可以表现为多种临床综合征,如僵人综合征、AE、1型糖尿病、成人隐匿性自身免疫性糖尿病[5]、甲状腺炎等。上述临床综合征可单独或合并出现[6]。本例患者同时合并AE、成人隐匿性自身免疫性糖尿病及甲状腺炎,血清及脑脊液中均检测到抗GAD65抗体。
抗GAD65抗体阳性AE多见于60岁以下女性,多以亚急性或慢性起病,步态共济失调为最常见症状,临床症状具有高度异质性[7]。30%患者在出现共济失调前可发生脑干短暂性功能障碍,表现为阵发性眩晕及波动性复视,可持续存在整个病程,称“脑干发作”。该患者在病程初期一过性眩晕症状考虑存在“脑干发作”。因此对于病因不明的短暂神经症状,特别是存在免疫共病患者,需考虑到该病的可能,但是需要与椎基底动脉系统的短暂性脑缺血发作相鉴别[8]。抗GAD65抗体阳性AE患者脑脊液中蛋白水平和细胞计数通常正常,有时可检测到特异性寡克隆区带。脑脊液抗GAD65抗体滴度通常低于血清,也可表现为阴性,但脑脊液抗GAD65抗体更能预测神经系统疾病。因此可对不明原因AE患者于初诊时行血清及脑脊液抗体联合检测,于复诊时可仅检测血清中抗体,以方便监测患者对免疫治疗的反应[9-10]。抗体检测时需注意抗体假阳性的可能,URRIOLA N等[11]报道过1例因抗体假阳性被误诊为AE,尸检证实为克-雅病。除克-雅病等神经系统退行性疾病外,抗GAD65抗体阳性也可见于COVID-19感染[12]、COVID-19疫苗的接种[13]、他克莫司的毒性作用、免疫缺陷病、移植物抗宿主病及免疫检查点抑制剂[11]等,提示上述情况可引发自身免疫。
抗GAD65抗体阳性AE不同的起病形式,其头部MRI及FDG-PET的影像学表现不尽相同。头颅MRI有助于区分起病形式,如急性起病患者的头颅MRI上极少出现小脑萎缩,慢性起病患者头颅MRI可表现为不对称小脑萎缩,尤其小脑蚓部萎缩[14]。FDG-PET葡萄糖代谢异常早于组织结构改变,在临床症状出现前或头颅MRI阴性者,可以通过FDG-PET检测到异常的葡萄糖代谢,提高诊断该病的敏感性。目前认为糖代谢变化与AE的抗体类型及疾病活动性显著相关,且代谢梯度的变化程度与病情严重程度呈正相关。如GABABR脑炎颞叶内侧、海马高代谢[15]。NMDAR脑炎急性期从额颞部至枕部代谢梯度递减[16];LGI1脑炎在全脑普遍低代谢背景下壳核、基底节区及海马高代谢。有关抗GAD65抗体脑炎FDG-PET葡萄糖代谢文献报道较少。部分抗GAD65抗体阳性AE患者单侧小脑半球灌注及葡萄糖代谢减少,在顶叶、额叶、枕叶、颞叶和海马等皮质区域出现低代谢[14]。而本例患者双侧顶叶、额叶、Broca区、前扣带回、后扣带回、左侧顶颞叶糖代谢降低,双侧尾状核、双侧小脑、丘脑、脑桥、中脑、右侧颞叶外侧、双侧颞中回糖代谢增高,推测这与该病导致广泛性脑网络连接损害,机体的补偿机制使脑默认网络连接增加有关[14]。在疾病不同阶段,糖代谢表现出由增高到降低的动态规律。在急性期呈高代谢,恢复期及复发时呈低代谢。症状好转后,糖代谢可恢复正常。本例患者头部MRI显示小脑无萎缩,未见异常信号表现,而FDG-PET提示皮层广泛糖代谢减低背景下,双侧尾状核、双侧小脑、丘脑、脑桥、中脑糖代谢增高,结合患者发病特点,考虑与患者急性起病,病程较短,尚处在炎症活动急性期有关,需要在将来的随访中观察影像学动态变化。有文献报道抗GAD65抗体阳性AE还可快速进展为额颞叶痴呆[17],本例患者FDG-PET上已经显示与认知相关脑区代谢异常,应警惕未来发生认知障碍。
本例患者合并甲状腺炎,抗GAD65抗体相关文献中患者极少合并甲状腺炎,且机制尚未完全明了,对抗GAD65抗体与甲状腺抗体的相关性缺乏大样本分析。ZHU F等[18]认为,由于GAD在中枢神经系统抑制性神经元、胰腺β细胞及甲状腺中广泛存在,除影响神经系统外,还可导致甲状腺功能异常及甲状腺相关抗体阳性,抗GAD65抗体阳性为甲状腺相关抗体阳性的危险因素,且甲状腺的损害程度及病程均可能对抗GAD65抗体滴度产生影响,因此对抗GAD65抗体阳性患者有必要筛查甲状腺相关抗体。本例患者经激素冲击及免疫治疗后,甲状腺功能恢复至正常,考虑甲状腺功能异常与抗GAD65抗体有关。
早期治疗对该病预后具有极大价值。指南推荐免疫治疗、对症治疗、支持治疗及康复治疗[1]。免疫治疗包括一线治疗(类固醇、人类免疫球蛋白、血浆置换)及二线治疗(利妥昔单抗、硫唑嘌呤、环磷酰胺、霉酚酸酯等)[19-20]。其中血浆置换是降低外周抗体滴度最有效方法,但对鞘内合成的抗体无效。近年来,除上述药物外,新型单抗类药物如托珠单抗和硼替佐米的作用也被证实。除免疫治疗外,还应该对合并精神疾病、癫痫、肌肉痉挛、僵硬等患者行对症治疗,以及对可能合并的肿瘤及其他免疫共病进行诊治。在使用免疫抑制剂前后,尤其是亚急性起病、年龄大于50岁、男性、合并抗细胞表面抗原抗体如抗GABABR抗体等潜在恶性肿瘤危险因素的患者,应定期筛查隐匿性恶性肿瘤。环磷酰胺作为细胞毒性药物,对合并肿瘤危险因素患者获益更大。本例患者脑脊液中抗体滴度较高,在治疗上,故未选择血浆置换治疗,而选用可通过血脑屏障的免疫抑制剂环磷酰胺强化免疫治疗,从而抑制鞘内抗体产生,削弱细胞毒性T细胞介导的免疫反应[21]。
对于无明显危险因素的共济失调或不明原因脑干功能障碍等症状时,且神经症状和影像学无特异性表现的患者,无论是否合并自身免疫疾病,均应考虑抗GAD65抗体阳性AE导致小脑性共济失调的可能性,并及时进行抗体检测,同时启动免疫调节治疗,阻止疾病进展[22-23]。该病一旦确诊,需要长期随访筛查肿瘤及抗体滴度以评估患者对治疗的反应,并监测血糖。当抗GAD65抗体滴度升高时,警惕疾病复发或合并另一抗GAD65抗体综合征[24-25],如僵人综合征等。
综上,本文回顾性分析了1例以步态不稳、言语笨拙起病的伴甲状腺炎的抗GAD65抗体阳性AE,并通过FDG-PET行功能性神经成像,旨在提高临床医生对该病临床及影像学的认识,改善患者预后。
