清热解毒方治疗非急性期热毒伤肺型放射性肺炎临床研究*
2024-04-23李增云马庆彤
李增云,马庆彤
济南市中西医结合医院,山东 济南 271100
放射性肺炎属于放射性肺损伤的一部分,在胸部肿瘤放疗相关并发症中较为多见。胸部肿瘤放疗致肺组织损伤后,诸多细胞因子及分子生物将启动损伤的修复功能,进而引发比射线本身更为严重的肺损伤,给肿瘤患者的后续治疗及预后带来一定的影响[1]。放射性肺炎为肿瘤患者非手术综合治疗的主要限制因素,该并发症的出现不仅会使治疗实施受限,同时也会影响患者的生存质量,不利于临床后续治疗的开展[2]。当前,糖皮质激素治疗为临床放射性肺炎患者的首选方案,辅助以相应的处置以改善症状,但激素的使用仍旧无法避免剂量大、周期长以及免疫抑制等诸多不足,使得患者对于该疗法的效果存疑[3-4]。激素治疗的目的是使患者度过急性期,然而大剂量激素冲击疗法易导致激素过量或患者因害怕不良反应减量过早而造成放射性肺炎反复发生,进而影响治疗的效果。有学者通过临床研究发现,中药能通过调节多种细胞因子防治放射性肺炎,在临床中具有较高的实用性[5]。放射性肺炎属中医学“肺萎”“燥咳”等范畴,肺乃娇脏,具有喜润而恶燥的特征,长期的放射治疗不仅容易伤及阴气,同时还易造成热毒内侵,进而灼伤肺络,许多临床工作者则以清热与解毒并重,辨证论治。笔者采用清热解毒方治疗非急性期热毒伤肺型放射性肺炎,现报道如下。
1 资料与方法
1.1 一般资料选取2021年10月至2022年7月济南市中西医结合医院收治的非急性期放射性肺炎患者60例,按照随机数字表法分为对照组和观察组,每组各30例。对照组男18例,女12例;年龄55~75(57.82±6.47)岁;病程30~90(63.18±6.45) d;腺癌20例,鳞癌10例。观察组男20例,女10例;年龄55~75(57.60±6.80)岁;病程32~90(63.51±6.23) d;腺癌21例,鳞癌9例。两组患者一般资料经统计学处理,差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准
1.2.1 西医诊断标准符合《放射性肺炎的诊断与治疗》[6]的诊断标准:有胸部恶性肿瘤放射治疗史,总照射剂量超过8 Gy;出现在放射治疗后的6个月内;临床表现为呼吸困难、咳嗽、胸痛胸闷等;影像学检查发现照射局部出现斑片状模糊影或磨玻璃样变;肺功能检查可出现肺顺应性及弥散功能降低。
1.2.2 中医诊断标准符合《中医内科学》[7]中热毒伤肺型的诊断标准,咳声低微,神疲乏力,消瘦,胸闷,苔白干燥或无苔,脉细。
1.3 病例纳入标准符合上述诊断标准;预计生存期>3个月;患者及家属均知情同意。
1.4 病例排除标准放射性肺炎急性期;同时接受化疗、靶向治疗及免疫治疗;发生时间为放射治疗3个月内;已进入晚期肺纤维化阶段。
1.5 治疗方法对照组予以吸氧、雾化、止咳及化痰处置,注射用甲泼尼龙琥珀酸钠(国药集团容生制药有限公司,批号:国药准字H20010098),每次80 mg,静脉滴注,每日1次,连续3 d后改为每次 40 mg,静脉滴注,连续3 d,停药后改为口服醋酸泼尼松片(浙江仙琚制药股份有限公司,批号:国药准字H33021207),每次20 mg,每天1次,连续服用3 d后减剂量至5 mg,直至停药。治疗期间同时予以注射用奥美拉唑抑酸保护胃黏膜,并予以头孢类抗生素预防感染或根据药敏结果合理选用抗菌药物。观察组在对照组治疗的基础上加用清热解毒方,具体药物组成:白花蛇舌草、蒲公英、鱼腥草各30 g,瓜蒌、桑白皮各20 g,连翘15 g,金银花15 g,黄芩、柴胡各12 g,苦杏仁、麦冬、生地黄、葶苈子各10 g,甘草6 g。每日1剂,水煎300 mL,早中晚各1次。
1.6 观察指标
1.6.1 中医证候积分对两组患者治疗前后咳嗽咳痰、胸闷气短、神疲乏力、五心烦热、口干咽燥及食欲不振等症状按照无、轻度、中度、重度进行评定,分别计0~3分,分值越高,症状越重。
1.6.2 病情分级依据美国肿瘤放射治疗协作组分级[8]对两组患者病情程度进行分级,0级:无症状;1级:轻度干咳;2级:持续咳嗽、需麻醉性止咳药;3级:重度咳嗽,对麻醉性止咳无效;4级:持续吸氧或辅助通气治疗。
1.6.3 肺功能测定两组患者治疗前后肺总量及肺弥散功能。
1.6.4 细胞炎症因子采集两组患者治疗前后清晨空腹静脉血5 mL,使用ELISA法测定白细胞介素-6(interleukin-6,IL-6)、转化生长因子-β1(transforming growth factor-β1,TGF-β1)及肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平。
1.6.5 不良反应发生情况记录两组患者恶心呕吐、皮疹、头晕头痛等不良反应出现例数,并计算不良反应发生率。
1.7 疗效判定标准参照《疾病临床诊断和疗效标准:医政规范之五》[9]制定。显效:心率、呼吸频率、体温、血氧饱和度等均复常;有效:体温、血压、心率及呼吸频率均有所降低,血氧饱和度明显上升,但尚未达到正常标准;无效:临床症状无明显变化甚至恶化。
有效率=(显效+有效)/n×100%
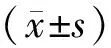
2 结果
2.1 两组放射性肺炎患者治疗前后中医证候积分比较两组患者治疗后各项中医证候积分低于本组治疗前,且治疗后观察组低于对照组(P<0.05),见表1。
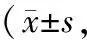
表1 两组放射性肺炎患者治疗前后中医证候积分比较 分)
2.2 两组放射性肺炎患者临床疗效比较观察组有效率为83.33%,对照组有效率为73.33%,观察组有效率高于对照组(P<0.05),见表2。

表2 两组放射性肺炎患者 临床疗效比较 例(%)
2.3 两组放射性肺炎患者治疗前后病情分级比较两组患者治疗后0级、1级、2级占比高于本组治疗前,3级、4级占比低于本组治疗前,且治疗后组间比较,差异具有统计学意义(P<0.05),见表3。

表3 两组放射性肺炎患者治疗前后病情分级比较 例(%)
2.4 两组放射性肺炎患者治疗前后肺功能比较两组患者治疗后肺总量及肺弥散功能高于本组治疗前,且治疗后,且治疗后观察组高于对照组(P<0.05),见表4。
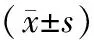
表4 两组放射性肺炎患者治疗前后 肺功能比较
2.5 两组放射性肺炎患者治疗前后细胞炎症因子水平比较两组患者治疗后IL-6、TGF-β1及TNF-α水低于本组治疗前,且治疗后观察组低于对照组(P<0.05),见表5。
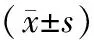
表5 两组放射性肺炎患者治疗前后 细胞炎症因子水平比较
2.6 两组放射性肺炎患者不良反应发生率比较两组患者不良反应发生率比较,差异无统计学意义(P>0.05),见表6。

表6 两组放射性肺炎患者不良反应 发生率比较 例(%)
3 讨论
在胸部肿瘤放疗群体中,放射性肺损伤早期表现为放射性肺炎,晚期则为放射性肺纤维化[10]。据统计,在行胸部放疗患者群体中出现放射性肺炎者约为10%~20%[11]。国内外学者均将激素及抗生素作为放射性肺炎的治疗手段,但患者使用后会出现依赖性,且不良反应发生率较高[12-13]。放射性肺炎轻者无明显症状,严重者可导致呼吸功能障碍,肺广泛纤维化,甚至引发呼吸衰竭[14]。此外,放射性肺炎的发病也限制了肿瘤的放疗剂量,很大程度上降低了放疗效果[15]。因此,寻找有效且安全的手段防治放射性肺炎,对于肿瘤患者而言至关重要。
消化系统、呼吸系统等多部位的肿瘤均易通过多种途径而发生肺转移。因此,在临床放射治疗过程中往往会适当扩大放射范围而累及肺部。中医学中并无放射性肺炎的病名,就症状而言,该疾患与“肺萎”“喘症”相类似,大体的体征均为呼吸障碍、咳嗽咳痰、发热与胸痛等,主要病机为热毒瘀堵于肺,阴血耗损引发瘀血,进而造成肺脉络的失养。从结果方面讨论,放射性肺炎是一种热毒之邪,肿瘤患者本身即体虚,而作为热毒之邪的射线入侵后则易引发气随津脱,毒热灼阴,肺热津伤后其宣发肃降功能失职,长此以往,则为肺萎;从根本方面而言,放射性肺炎的病机则为气血阴阳俱虚,随着病情的推进,逐渐形成热毒、瘀血聚集在肺,加重肺损伤。
综上,放射性肺炎的病位在肺,病机为热毒壅肺,肺失宣降,脉络不通,最终导致肺部损伤,痰、热、毒壅于肺中,治疗应以清热解毒为主。考虑到放射性肺炎患者原发肿瘤与肺部炎症相互交织,体质虚弱尤为严重,临证时应多给予中药治疗。清热解毒方为本院治疗放射性肺炎的经验方,方中白花蛇舌草、蒲公英、鱼腥草为君药,三者皆能清热解毒,白花蛇舌草利湿消痈,蒲公英消痈散结,鱼腥草消痈排脓;金银花、连翘共为臣药,强化君药清热解毒的功效;瓜蒌清热化痰,桑白皮泻肺平喘,黄芩清热燥湿,柴胡疏肝退热、升提中气,苦杏仁降气止咳,麦冬清肺润燥,清心除烦,生地黄清热凉血,葶苈子泻肺平喘,上药共为佐药;甘草为使药,发挥调和诸药的作用。诸药合用,共行清热解毒之功。
本研究结果显示,观察组有效率高于对照组,治疗后各项中医证候积分低于对照组,病情分级改善情况优于对照组,差异均有统计学意义(P<0.05),说明清热解毒方的应用能缓解放射性肺炎患者临床症状,延缓病情进展。放射性肺炎的主要特征为纤维基质合成、纤维母细胞增殖、炎性因子异常表达、内皮细胞损伤以及肺泡上皮细胞损伤[16]。其中炎性因子持续升高,可造成肺组织持续急性或延迟性损伤[17],作为炎症因子代表的IL-6、TGF-β1及TNF-α等皆被认为在放射性肺炎的进程中具有突出的作用[18-19]。IL-6在肺实质中主要由肺泡巨噬细胞等诸多细胞合成,具有多种生物学活性,测定IL-6水平则能够判断肺组织的炎性状态[20]。放疗、化疗过程中的电离辐射会导致DNA损伤和活性氧的生成,活性氧则会促进TGF-β1的产生与激活,TGF-β1刺激成纤维细胞过度产生细胞外基质,进而促进肺纤维化[21]。研究表明,急性放射性肺损伤大鼠肺组织中IL-6、TGF-β1及TNF-α的表达水平显著升高,下调IL-6、TGF-β1及 TNF-α 的表达则可以减轻放射性肺损伤的发生,且能够逆转照射引起的肺纤维化。因此,在放射性肺炎的治疗中控制患者炎性因子水平对于疾患的治疗以及患者的预后均至关重要。
现代药理学研究证实,白花蛇舌草乙酸乙酰部位可通过抑制Nur77/JNK信号通路发挥抗肿瘤作用[22];蒲公英叶提取物具有抗炎活性[23-24];动物实验中发现,鱼腥草多糖可通过减少炎症细胞释放、改善肺水肿等病理形态以及减少相关炎症因子分泌来保护大鼠慢性炎症肺损伤[25];瓜蒌皮水提物灌胃给药能提高免疫能力,同时瓜蒌水煎剂可镇咳祛痰[26];桑白皮水提物能够通过提高T淋巴细胞亚群CD4+、CD25+、Foxp3+的比例,降低Th2相关炎性反应因子的表达进而发挥平喘的功效[27];葶苈子水煎液可通过抑制气道炎症细胞的浸润以及嗜酸性粒细胞的激活,进而降低炎症因子的释放,同时其抗肿瘤活性可能与抑制肿瘤慢性炎症相关[28-29]。本研究中,治疗后观察组IL-6、TGF-β1及TNF-α水平低于对照组(P<0.05),提示清热解毒方可降低炎症细胞因子的表达,抑制炎症因子的表达,这可能与方中诸多中药协同抗炎的药理作用有关。另外,本研究还发现,治疗后观察组肺总量及肺弥散功能等肺功能指标高于对照组(P<0.05)。
综上所述,清热解毒方治疗非急性期热毒伤肺型放射性肺炎,可有效缓解患者的临床症状,改善其肺功能,其作用机制可能是通过降低IL-6、TGF-β1 以及TNF-α等细胞炎症因子水平而实现的,但对于研究涉及的清热解毒方下调细胞因子表达水平的具体机制需要后续的深入研究与探析。
