蒽环类药物心脏毒副作用机制及中医药治疗研究进展
2024-04-10赵雪娜张馨蕾
赵雪娜 张馨蕾 舒 政 张 梅
1.山东第一医科大学(山东省医学科学院)研究生部, 山东 济南 250117;2.山东第一医科大学第一附属医院乳腺外科,山东 济南 250014
恶性肿瘤是人类史上最严重的致死性疾病之一,在全国中青年的致残率与死亡率的病因统计中居于首要因素[1]。由于恶性肿瘤整体防治计划的实施、诊断和外科技术的不断进步,患者的存活期限明显延长。在恶性肿瘤综合治疗迅速发展的今天,又产生了许多新的健康问题,其中与恶性肿瘤治疗相关的心脏毒性已成为了最严重的并发症之一。化疗药物与心脏毒性流行病学研究表明,心血管疾病是老年恶性肿瘤患者中最主要的死亡因素,甚至高于其原发病和复发引起的死亡,在我国老年乳腺癌患者十年内发生的心力衰竭累计死亡率中,蒽环类化疗者为38%,非蒽环类化疗者为32.5%,未接受过化疗药物者为29%[2-3]。蒽环类药物在临床恶性肿瘤化疗方案中较为常用,包括表柔比星、多柔比星、伊达比星、戊柔比星等,其中多柔比星,也称阿霉素(doxorubicin,DOX),是目前最常见的抑制恶性肿瘤药物之一。蒽环类用药引起的心肌毒性通常具有进展性和不可逆性,初次应用蒽环类药品时可能引起严重心肌损害,其致心脏毒性的机制包括氧化应激和生成ROS、拓扑异构酶II 的抑制和双链DNA断裂导致的转录基因改变与细胞凋亡、线粒体的功能损伤等[4]。肿瘤治疗过程中化疗药物引起的轻度心肌损害可能会慢慢恢复,重度损害则会导致治疗终止,甚至造成不可逆性损害。因此,在肿瘤治疗过程中,防止心脏损害、关注患者心功能状态尤为重要。药物治疗性心肌中毒的主要症状是胸闷、呼吸困难、心慌、心电图失常、左心射血分数(left ventricular ejection fraction,LVEF)降低和心肌酶谱的改变,甚至引起心力衰竭。目前,临床治疗上多是采用临床体征、心肌酶谱结果和心电图、超声心动图等无创性方法检测心功能。
1 蒽环类药物心脏毒性相关机制
1.1 氧化应激:活性氧(reactive oxygen species,ROS)的生成
蒽环类药物产生ROS水平通常和下列3个方面相关:(1)DOX 与心肌细胞的亲和力显著大于其他物质,心肌细胞中大量聚集DOX,以致心肌细胞极易遭受破坏。心肌细胞接触到DOX后,通过与还原型 辅 酶 Ⅱ(nicotinamide adenine dinucleotide phosphate,NADPH)、黄嘌呤氧化酶和细胞色素P450酶等的相互作用,DOX醌基被细胞氧化还原分解转变成与其相互作用的半醌自由基,半醌自由基和O2反应后又重新产生了醌基,此过程不断地氧化分解产生超氧阴离子(O2-),这也是DOX 在缺氧坏死时形成ROS 的最主要过程[5-6]。(2)在游离铁存在下,蒽环类药物能够触发机体自由基氧化生成电子的循环反应(氧化还原循环),即蒽环类药物可通过一个适当剂量的叶黄素蛋白从氧化还原态下的叶黄烷酶上得到一个电子,被氧化还原生成1 个半醌自由基。半醌自由基与铁形成1个“药物-Fe2+-自由基”的复合体,这种复合体氧化还原成为ROS,并再次成为原形药剂,ROS本身也可以歧化并转化成羟自由基(·OH)和O2-,并且可以产生化学性质相对更稳定的、生物毒性更高的醛类药物(如MDA),造成了“蒽环类药物-ROS”损伤复合物的大量出现[7].(图1)。(3)一氧化氮合酶(nitric oxide synthase,NOS)是产生ROS 的主要原料之一,蒽环类物质可直接结合于细胞内皮中的一氧化氮合酶还原酶结构域,首先夺取NADPH的一个电子,生成一个半醌基结构,最后再将电子转移至O2生成O2-,从而对心肌产生毒性[8]。

图1 ROS生成机制图
1.2 线粒体损伤
DOX 和线粒体内膜中的心磷脂结合,产生DOX-心磷脂的不可逆复合体,当心磷脂在遭到ROS的攻击时,导致细胞色素C从线粒体内膜中分离出来,还能够解开Ⅰ、Ⅲ、Ⅳ线粒体呼吸链复合体,形成线粒体渗透过渡孔(mitochondrial permeation transition pores,mPTP)[9-10]。mPTP 与B 淋巴细胞瘤-2(b-cell lymphoma-2,Bcl-2)家族蛋白相关,导致三磷酸腺苷(adenosine triphosphate,ATP)使用减少,引起线粒体和细胞质肿胀(图2)。DOX通过铁调节蛋白1(iron regulatory protein 1,IRP-1)和铁调节蛋白2(iron regulatory protein 2,IRP-2)的RNA结合活性来调节细胞内铁稳态,此外,DOX 还可影响细胞铁定位,使铁在线粒体中积累,铁在线粒体中增加能提高DOX 对心脏的敏感性,从而对心脏产生毒性[11]。DOX还会降低DNA甲基转移酶I的表达,导致线粒体DNA(mitochondria DNA,mtDNA)低甲基化和心脏线粒体细胞破坏[12]。此外,蒽环类药物进入细胞后通过一系列氧化还原反应,产生的自由基也可导致线粒体功能受损。
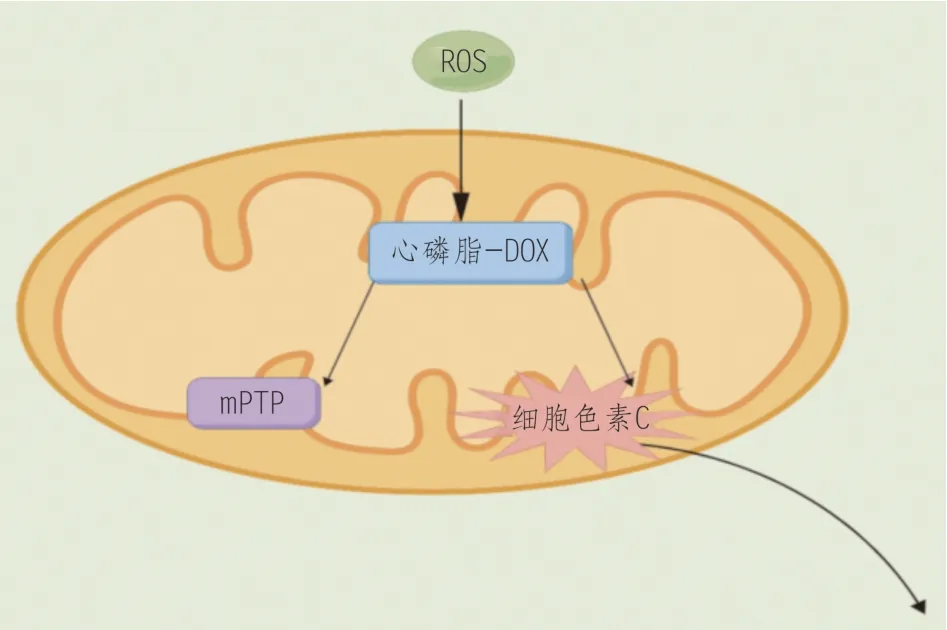
图2 线粒体损伤机制图
1.3 抑制拓扑异构酶Ⅱ
DOX 可以抑制拓扑异构酶2(topoisomerase-2,Top2),哺乳动物细胞中有2 种Top2 同工酶,Top2α和Top2β,Top2α在终末分化的心肌细胞中不表达,Top2β 存在于所有细胞中,DOX 通过Top2β 插入心肌细胞DNA 并产生毒性,通过形成一个共价的Top2 -DNA 复合物(裂解复合体)导致双链DNA断裂[13]。
1.4 钙超载
DOX 可导致细胞质空泡化和心脏肌原纤维的紊乱,破坏亚细胞器的结构。DOX导致肌浆网严重扩张,从而能使Ca2+紊乱[14]。蒽环类制剂一方面可增加细胞内贮存的Ca2+的释放,另一方面又可通过降低肌浆网中Ca2+-ATP 酶的表达,从而使得机体内游离Ca2+的水平明显升高,从而引发机体内钙超载,反之Ca2+增加也可以导致ROS的产生。钙超载也可通过干扰患者心肌细胞的电活动而引发严重心律失常,还可以同时造成大量ATP 酶合成代谢障碍,导致心肌毒性[15]。
1.5 细胞凋亡
DOX通过增加凋亡基因Bax和细胞色素C的表达以及凋亡素(Caspase-3)的活性,同时降低Bcl-2的表达来诱导组织凋亡[16]。Ⅱ型拓扑异构酶促进DNA双链的解链和解开链的连接,蒽环类药物可以阻止断裂DNA双链的连接,这种效应的积累会导致细胞凋亡[17]。蒽环类药物通过嵌入DNA发挥作用,当与Top2α 结合时,复合物可抑制DNA 的复制,将细胞周期阻滞在G1/G2期,并诱导其凋亡[18]。
2 中医药治疗肿瘤心脏毒性相关机制
2.1 西红花苷
西红花苷是西红花的主要活性成分之一,又被称为西红花素、藏红花素等,现已被证实是唯一存在的水溶性类胡萝卜素。西红花苷又可分为2 种,即西红花苷-1、西红花苷-2 等,均名为西红花酸[19]。临床研究显示,西红花苷具有极为显著的抗心血管疾病活性、神经药理活性、抗炎、治疗各种皮肤软组织炎症性损伤、保肝利胆、抗肿瘤等多重药理功效,目前在临床上主要用于防护动脉血管内皮细胞损伤、降压、抗动脉粥样硬化和治疗心血管疾病等[20]。药理学研究表明,西红花苷的抗心血管疾病机理主要涉及降血脂、降血压和心肌保护功能等[21]。另外,基础研究也表明,西红花苷在不影响多柔比星体外抑制肿瘤细胞活性的条件下,对多柔比星诱发的心肌细胞损伤和组织结构变化有明显的效果。不同治疗剂量西红花苷对防止缺血缺氧性心肌损伤具有明显的保护作用,且具有剂量依赖性[22-23]。
在心脏保护方面,西红花苷能明显降低细胞膜的脂质过氧化性及破坏作用,明显增强肥大心肌细胞中谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)及SOD(superoxide dismutase,SOD)的活性,表明西红花酸对心肌具有一定的保护作用,并与内源抗氧化酶活力调控密切相关[24-25]。在心肌缺血方面,西红花酸预防给药能够明显地减少大鼠血清中肌酸激酶、乳酸脱氢酶、血清肌钙蛋白I 的产生,并明显降低血清和心肌血浆中丙二醛(malonaldehyde, MDA)的浓度,对减轻心肌水肿也有明确的作用[26-27]。心肌缺血再灌注损伤可导致继发性心脏功能严重紊乱、心肌组织损伤及组织代谢机制改变,西红花苷可预防或治愈严重心脏功能紊乱综合征和其他缺血性心脏病,改善心肌急性缺血再灌注所致心律失常。此外,西红花苷对心肌肥厚也有一定的改善作用[28-31]。
西红花苷是西红花的主要活性成份,有着丰富的药理功效,其对心血管疾病也有较好的效果,但是由于目前关于西红花苷的药效研究主要集中于植物细胞和动物方面,因此临床资料还比较欠缺,必须进行大量临床试验来明确西红花苷在人体内的药效活性。随着研究的深入开展,西红花苷的功效会得到进一步的证实,也会为化疗患者带来更多益处。
2.2 人参皂苷
人参皂苷是人参的主要成分,对心血管系统具有良好的保护功效,同时还能阻止心肌纤维化和心房重建,并阻止心肌细胞的坏死,此外,还可调节或増强免疫功能、造血功能,并具有多种抗肿瘤功效。研究表明,人参皂苷Rg3 可通过逆转对小鼠细胞的免疫抑制,增强动物机体自身杀伤细胞活力、脾淋巴细胞增殖活性,上调血清γ 干扰素(interferon-γ,IFN-γ)、肿瘤坏死因子α(tumor necrosis factor,TNFα)、白介素-2(interleukin-2,IL-2)水平[32]。此外,使用含蒽环类药物治疗血液系统中恶性肿瘤的患者时,若在化疗时加服含有人参皂苷的中成药治疗,可适当减轻化疗期间药物对人心脏引起的毒副反应[31]。
在抑制心肌细胞氧化应激方面,人参皂甙作为一个抗氧化剂,可以保护心肌细胞免遭氧化破坏,其保护机制是清除H2O2和羟基自由基[33]。在改善心肌重塑方面,人参皂苷对家兔心室肥厚具有抑制作用[34-35]。此外,人参皂苷能够通过双向调节有关信号通路快速改善大鼠心功能不全,并可减轻右心室重构[36]。
人参皂苷是人参的重要功能成分之一,在抑制心肌细胞氧化应激、改善心肌重塑等方面具有重要的药理作用,对于人参皂苷的生物作用机制目前还需要进一步研究,以期为化疗患者带来更多益处。
2.3 当归
当归提取物具有明显的保护正常心肌细胞,减轻对心肌组织损伤,抑制血小板原粘附,清除氧自由基的作用。有研究表明,在大鼠每日给予当归后,联合每周给予氯化钠注射液或DOX,观察大鼠的一般行为和心脏功能与结构的改变,结果显示,当归可降低大鼠CK 和谷草转氨酶含量,并有效改善大鼠心电传导异常,提示当归对心脏有保护作用[37]。
在心脏保护方面,当归可使左心室收缩压、左心室内压最大上升速率等增高,血清肌酸激酶同工酶等浓度明显降低,从而证明了当归可以通过降低缺血再灌注大鼠的心肌梗死面积和组织损害,抑制了氧化应激和炎症反应,发挥对心肌损伤的保护功能[38-39],当归可以通过调控自噬相关蛋白的表达来降低缺氧/复氧情况,从而减少对心肌细胞的损伤[40]。
2.4 红景天
红景天有抗氧化、抗炎、抗癌、调节身体新陈代谢和保护中枢神经系统的作用,主要用于中枢神经退行性损害、心血管疾病、高血压、肿瘤以及其他多种疾病的预防[41]。红景天苷、酪醇、多糖等作为其独有的化学成分,可达到有效抑制急性心肌缺血-再灌注损伤、抗慢性心力衰竭、降血脂、抗血栓形成、抗缺血性心律失常、辅助诊断高血压以及明显改善高血糖的作用[42]。奚蕾等[43]研究结果显示,使用多疗程蒽环类药物化疗的患者,同时使用红景天时可对心肌细胞产生保护效果,且具有剂量依赖性。
在对抗心肌细胞损伤方面,红景天苷可缓解因高脂诱导的心肌细胞损害,并减轻氧化损害,从而降低细胞凋亡[44]。红景天苷可通过调节相关通路来保护缺氧/复氧损伤,从而减轻心肌细胞由ER 应激导致的细胞凋亡,可有效缓解因压力超负荷所导致的大鼠心肌肥厚,红景天还可通过降低左室心肌转化生长因子β(Transforming growth factor, TGF-β 1)的表达,影响TGF-β信号的转导[45-46]。
将智能化技术充分应用于电气工程及其自动化当中,可以在很大程度上提高处理相关数据信息的效率,有着较强的信息整合能力,可以为电气工程及其自动化的后续工作提供更加精确的信息数据。与此同时,电气工程及其自动化系统还有着明显的复杂性特点,且对于不同的处理对象,其变现出的特点也存在着一定的区别,即便是智能化技术也会在控制上存在不足之处。因此,就需要相关人员和智能化技术充分的结合在一起,相关工作人员要在全面掌握电气设备与电气工程相关知识的基础上,充分利用智能化技术不断改进电气工程及其自动化,提升企业整体的工作效率,以此使企业能够获取更高的效益。
2.5 黄芪
黄芪多糖、黄芪总黄酮、黄芪甲苷等是黄芪的主要有效成分,具有清热、消暑、燥湿、泻火、明目、解毒、补气、清热等重要作用[47]。研究表明,黄芪具有保护神经血管、调节自身免疫、抗肿瘤、抗氧化应激、改善细胞代谢等生物学作用[48]。有学者发现,黄芪注射液可保护小鼠损伤心脏的SOD活性,减少MDA 的生成,使体内氧自由基被有效清除,并阻止由氧自由基所致的级联反应,从而有效降低DOX所致的心脏毒性[49]。
在保护急性心脏衰竭方面,黄芪注射液能明显缓解大鼠心律失常的发生,对改善大鼠心脏功能、减轻心肌病理损伤具有十分重要的作用[50]。黄芪甲苷对心肌梗死后血管新生具有促进作用,而其影响机理与PTEN/PI3K/AKT 的途径密切相关[51]。临床数据表明,黄芪对儿童心肌缺血再灌注损伤的保护作用也十分显著[52]。在改善大鼠心肌重塑方面,使用黄芪甲苷可以明显改善大鼠心肌因主动脉径缩窄所致严重进行性心肌肥厚,其保护机制与黄芪甲苷激活自噬、减轻氧化应激相关[53-54]。
2.6 黄芩
中药黄芩中的有效成分之一为黄芩苷,是目前黄芩类药物中含量最高的一种黄酮类物质。现代医学的药理实验初步证实,黄芩苷具有广谱抗菌、抗病毒、保护脑功能、促进肝及组织再生、抗肿瘤、抗炎、抗氧化、降脂降糖的药理作用[55]。黄芩苷作为天然有效安全的抗氧化剂,可快速清除人体氧自由基,预防人体由氧自由基而引起的人体成骨纤维细胞等的严重损伤。研究发现,预先大量给予黄芩苷提取物可以明显保护DOX对心肌的损伤,使小鼠的SOD和谷胱甘肽过氧化酶活性被破坏,因而减低了MDA 的产生量,使内源性氧自由基消除能力提高,减缓自由基对心脏的伤害[56]。
在抑制心肌细胞凋亡方面,黄芩苷可以达到完全抑制内质网应激诱导的心肌细胞凋亡,通过CHOP/eNOS/NO信号通路来实现其抑制作用[57]。此外,黄芩苷能大大减轻由缺氧引起的心肌细胞活力急剧降低和诱导细胞快速凋亡,主要通过HIF1α/BNIP3信号通介导[58]。
黄芩苷在保护心肌方面具有十分显著的作用,但目前对于黄芩苷的研究大多基于细胞水平或者动物实验,临床数据较少,且有研究发现,黄芩苷具有水溶性差、口服极难吸收、成药性差等问题,不利于临床实验的开展[56]。因此,应对黄芩苷胶囊的微观结构模型进行全面改造,提高其微观药动学特点,使之更好的被临床应用。
2.7 复方苦参注射液
复方苦参注射液以提炼的苦参为主要成分,有凉血清热解毒、散结止痛的功能,其有效成分为苦参碱、氧化苦参碱等多种生物碱。苦参碱还能通过提高心脏中抗氧化酶的活力,阻止自由基过氧化,具有防止心脏缺血的作用。氧化苦参碱还能通过减少MDA 浓度增加SOD 活力,从而可以对慢性心肌缺血患者心肌组织起保护及恢复作用[59]。此外,有研究发现,复方苦参注射液可改善患者对蒽环类药多疗程化学治疗后心脏毒性的耐受性,对心脏具有显著的保护效果[60]。
在减轻心肌细胞凋亡方面,苦参碱还能直接使小鼠线粒体膜电位改变,进而提高小鼠的线粒体呼吸链复合物Ⅰ的活性,通过降低DOX所致的人体心肌细胞坏死程度,提高了细胞生存率[62]。此外,氧化苦参碱对细胞凋亡起抑制作用,其抑制作用主要是通过影响心肌细胞内的MAPK/ERK5等信号通路来实现的[63]。在改善心脏重塑方面,有研究通过用注射器在健康小鼠腹腔注射柯萨奇B3 病毒后构建了小鼠病毒性心肌炎模型,通过测定左室细胞游离脂肪酸、ATP、腺苷酸、乳酸、Ⅰ型胶原蛋白、Ⅲ型胶原蛋白的含量,结果显示,氧化苦参碱能通过线粒体产生保护作用,从而改善心肌能量代谢,减少心肌细胞凋亡,逆转心室重构[64]。
2.8 心脉隆注射液
心脉隆注射液是一种在蟑螂身上提炼后制成的多肽类药剂,中医学认为有补气养血、温阳利水的作用。心脉隆注射液还能够保护心肌细胞,提高心肌收缩能力,提高SOD 的生物活力,进而更高效地消除氧自由基,降低乳酸脱氢酶等心肌毒性标志物的含量[65]。研究人员使用心脉隆注射液防治蒽环类化疗药物过量所致的严重心脏毒性,并对比药物治疗前后心功能、心电图异常率的变化,结果表明,用心脉隆注射液能降低心电图异常率,对蒽环类药物化疗患者的心肌具有保护效果。心脉隆注射液可以改变因缺血性心肌再灌注损害所致的心功能改变,还可以提高心肌冠状动脉血流量,从而降低心肌梗死程度,并对心肌坏死有一定的抑制作用[67]。
2.9 炙甘草汤
炙甘草汤主要中药成分为炙甘草、生姜、桂枝、人参、生地黄、阿胶、麦门冬、麻仁、大枣。药理学分析结果表明,方中的人参、甘草等均可提高心肌细胞中ATP 的含量,提高每搏输出量,有利于维持正常心肌细胞功能,对化学治疗类药物所导致的急性心功能不全具有预防和保护作用[68]。
在对抗心肌纤维化方面,炙甘草汤可以提高由异丙肾上腺素所引起的心肌纤维化患者心功能,从而控制了患者心肌纤维化情况,其机理很可能与调节核因子κB(Nuclear factor kappa-B,NF-κB)的途径密切相关[69]。也有临床资料显示,加用炙甘草汤治疗扩张型心肌病比单用西药疗效更确切,且能抑制心肌的纤维化[70]。在治疗心律失常方面,用炙甘草汤配合胺碘酮片防治心律失常的患者比单用胺碘酮片疗效更佳,能改善临床症状,下调血清超敏C反应蛋白和单核细胞趋化蛋白-1的水平[71]。因此,临床上治疗因蒽环类药化疗后引起的心律失常除了常用药物外,加用炙甘草汤也可显著减轻患者的病情。
2.10 参麦注射液
参麦注射液的主要组成为人参、麦冬,2种成分都具有较强的抗心肌损伤作用。研究者将76 例乳腺癌、恶性淋巴瘤等化疗患者随机分为治疗组和对照组,治疗组为蒽环类药物加用参麦注射液,对照组为单纯蒽环类药物,研究两组前后心电图的改变、心功能分级,结果表明,合并使用参麦注射液可显著降低蒽环类药物引起的心肌毒性[72]。在治疗心肌梗死方面,参麦注射液能提高心肌梗死患者心肌血管再生,可能与调节PI3K/AKT 信息通路密切相关[73]。也有资料显示,参麦注射液联合替格雷罗可降低急性心肌梗死患者机体的炎症反应,从而提高心功能[74]。
2.11 中药汤剂养心汤
中药汤剂养心汤是由肉桂、山萸肉、补骨脂、黄芪、当归、丹参、川芎、元胡、甘草等构成,有通脉、通络、补肺、养气、活血的作用,还具备活血化瘀,畅通心脉的作用,能有效舒张冠状血管,降低冠状血管阻力,增强冠状动脉血流量和心排血量,从而对心肌产生保护作用。
在减轻心肌的缺氧及再灌注性损伤方面,有研究将慢性冠心病介入术后心肌缺血患者随机分成对照组和试验组,对照组患者服用盐酸曲美他嗪,试验组患者则在对照组基础上给予通脉养心汤,通过观察两组肌钙蛋白、肌酸激酶同工酶、缺血修饰白蛋白、SOD 及基质金属蛋白酶-9 水平的差异,结果表明,通脉养心汤配合曲美他嗪有助于减少术后心肌缺血再灌注损伤和炎性反应,提高患者心功能[75]。
4 结语与展望
综上所述,目前蒽环类化疗药物在一些恶性肿瘤疾病的辅助治疗中十分常见,但也对患者心血管系统产生了一定损伤,西红花、红景天、黄芪、黄芩苷等中药材在对抗蒽环类化疗药物引起的心脏损伤方面具有重要作用,但也存在以下问题,如对某些药物的研究多基于细胞水平或动物水平,临床资料较少;还有一部分药物存在成药性差,口服吸收难等问题,临床应用存在局限,未来可以改变中药的剂型或者运用相应技术改善药物动力特点等。蒽环类化疗药物心脏毒性具有可预见性,因此,中医药在预防肿瘤导致的心脏疾病方面可能会具有较大的应用前景和研究价值,也符合国家中医药“治未病”的理念。