葡萄球菌核酸酶样结构蛋白1/SLC7A11抑制铁死亡对骨肉瘤发生发展的影响
2024-04-10王胜涛徐淑娟贵鹏李欣咛隋玉涵李朝旭
王胜涛 徐淑娟 贵鹏 李欣咛 隋玉涵 李朝旭
基金项目:广西医疗卫生重点学科建设项目(桂卫教科发〔2022〕4号)和广西医疗卫生重点培育学科建设项目(桂卫教科发〔2022〕4号)
摘要:目的 探讨葡萄球菌核酸酶样结构蛋白1(SND1)对骨肉瘤细胞生物学功能的影响,及其通过SLC7A11调控骨肉瘤细胞铁死亡的作用机制。方法 检测人成骨细胞hFOB1.19以及骨肉瘤细胞系Saos-2、U2OS、HOS和143B中SND1的表达水平。采用小干扰RNA敲减骨肉瘤细胞HOS和143B中SND1的表达(si-SND1),采用CCK8法、细胞克隆形成实验、细胞迁移和侵袭实验探究SND1的表达对骨肉瘤细胞生物学功能的影响;调控骨肉瘤细胞中SND1以及SLC7A11基因的表达,探究SND1通过SLC7A1基因对骨肉瘤铁死亡介导的肿瘤细胞凋亡的影响。结果 骨肉瘤细胞Saos-2、U2OS、HOS和143B中SND1 mRNA和蛋白的表达水平显著高于人成骨细胞hFOB1.19(P均<0.01)。与对照组比较,si-SND1转染显著降低HOS和143B细胞中SND1的表达水平(P均<0.01),且细胞活性显著降低,克隆形成数量显著减少,细胞迁移和侵袭能力显著降低(P均<0.001)。铁死亡诱导剂Erastin促进骨肉瘤HOS和143B细胞凋亡,而抑制剂Ferrostatin-1刺激上调细胞活性(P均<0.001)。敲减SND-1后使用Erastin可进一步降低骨肉瘤HOS和143B细胞活性,而使用Ferrostatin-1刺激后可显著恢复细胞活性(P均<0.001);Erastin处理后,si-SND1组细胞中铁离子和丙二醛表达增高,谷胱甘肽表达降低(P均<0.001)。体内实验结果显示,敲减SND1可以明显抑制143B裸鼠移植瘤的瘤体质量(P<0.001)。敲减SND1后骨肉瘤HOS和143B细胞中SLC7A11的表达水平显著减少(P均<0.001),且铁死亡水平升高(P<0.001,P=0.020)。结论 骨肉瘤细胞中SND1表达显著增高,其可能通过上调SLC7A11的表达抑制铁死亡,进而促进骨肉瘤细胞活性。
關键词:骨肉瘤;葡萄球菌核酸酶样结构蛋白1;铁死亡
中图分类号: R738.1 文献标识码: A 文章编号:1000-503X(2024)01-0011-08
DOI:10.3881/j.issn.1000-503X.15746
Effect of Staphylococcal Nuclease and Tudor Domain Containing 1/SLC7A11 on the Occurrence and Development of Osteosarcoma by Inhibiting Ferroptosis
WANG Shengtao1,XU Shujuan2,GUI Peng3,LI Xinning4,SUI Yuhan4,LI Zhaoxu1
1Department of Joint Surgery and Sports Medicine,Nanxishan Hospital of Guangxi Zhuang Autonomous Region,Guilin,Guangxi 541002,China
2Department of Hematology,Affiliated Hospital of Guilin Medical University,Guilin,Guangxi 541001,China
3Department of Trauma and Hand Surgery,Nanxishan Hospital of Guangxi Zhuang Autonomous Region,Guilin,Guangxi 541002,China
4Graduate School,Guangxi University of Chinese Medicine,Nanning 530200,China
Corresponding author:LI Zhaoxu Tel:0773-3830680,E-mail:lzxpds@126.com
ABSTRACT:Objective To investigate the effect of staphylococcal nuclease and tudor domain containing 1(SND1) on the biological function of osteosarcoma cells and decipher the mechanism of SND1 in regulating ferroptosis in osteosarcoma cells via SLC7A11.Methods Human osteoblasts hFOB1.19 and osteosarcoma cell lines Saos-2,U2OS,HOS,and 143B were cultured,in which the expression level of SND1 was determined.Small interfering RNA was employed to knock down the expression of SND1(si-SND1) in the osteosarcoma cell line HOS and 143B.The CCK8 assay kit,colony formation assay,and Transwell assay were employed to examine the effect of SND1 expression on the biological function of osteosarcoma cells.Furthermore,we altered the expression of SND1 and SLC7A11 in osteosarcoma cells to investigate the effect of SND1 on osteosarcoma ferroptosis via SLC7A11.Results The mRNA and protein levels of SND1 in Saos-2,U2OS,HOS,and 143B cells were higher than those in hFOB1.19 cells(all P<0.01).Compared with the control group,transfection with si-SND1 down-regulated the expression level of SND1 in HOS and 143B cells(all P<0.01),decreased the viability of HOS and 143B cells,reduced the number of colony formation,and inhibited cell invasion and migration(all P<0.001).The ferroptosis inducer Erastin promoted the apoptosis of HOS and 143B cells,while the ferroptosis inhibitor Ferrostatin-1 improved the viability of HOS and 143B cells(all P<0.001).After SND-1 knockdown,Erastin reduced the viability of HOS and 143B cells,while Ferrostatin-1 restored the cell viability(all P<0.001).After treatment with Erastin in the si-SND1 group,the levels of iron and malondialdehyde were elevated,and the level of glutathione was lowered(all P<0.001).The results of in vivo experiments showed that SND1 knockdown inhibited the mass of the transplanted tumor in 143B tumor-bearing nude mice(P<0.001).Knocking down the expression of SND1 resulted in down-regulated SLC7A11 expression(all P<0.001) and increased ferroptosis in HOS and 143B cells(P<0.001,P=0.020).Conclusions SND1 presents up-regulated expression in osteosarcoma cells.It may inhibit ferroptosis by up-regulating the expression of SLC7A11,thereby improving the viability of osteosarcoma cells.
Key words:osteosarcoma;staphylococcal nuclease and tudor domain containing 1;ferroptosis
Acta Acad Med Sin,2024,46(1):11-18
骨肉瘤是起源于间充质细胞的恶性骨肿瘤,具有转移早、易耐药、致残率高、死亡率高等特点[1]。葡萄球菌核酸酶样结构蛋白1(staphylococcal nuclease and tudor domain containing 1,SND1)是进化上高度保守的蛋白质,广泛表达于人类、小鼠、大鼠等多种生物[2]。研究表明SND1与多种肿瘤的发生发展有关,能促进乳腺癌起始细胞的存活和致瘤性[3];还参与调控结直肠癌细胞的增殖、凋亡和侵袭[4]。但SND1对骨肉瘤的作用目前研究较少,机制尚不清楚。铁死亡是一种由铁依赖性脂质过氧化驱动的细胞死亡形式,以游离铁增加和脂质过氧化物累积为特征,促进细胞内活性氧的产生和氧化性细胞凋亡[5]。研究证实铁死亡能够抑制肿瘤细胞的生长。应用铁死亡诱导剂RSL3、Erastin和抑制剂Ferrostatin-1调节铁死亡相关通路能够有效增强化疗、靶向治疗甚至免疫治疗的效果[6]。因此诱导铁死亡可能成为一种新型的癌症治疗方法。現已有研究证实P53、RSL3、FSP1和SLC7A11等多个基因均参与癌细胞对铁死亡的敏感性调节[7]。其中,SLC7A11编码蛋白在多种癌症中均呈高表达,是向细胞内转运胱氨酸以进行谷胱甘肽(glutathione,GSH)合成的关键膜通道蛋白[8]。作为细胞内氧化还原反应的关键调节剂,抑制SLC7A11表达可能为抗肿瘤提供基于铁死亡的新策略。因此,本研究采用多种骨肉瘤细胞系和裸鼠异种移植瘤模型,观察SND1对骨肉瘤细胞活性、克隆形成、迁移、侵袭的影响,探讨SND1/SLC7A11对骨肉瘤细胞铁死亡的调控机制,旨在为骨肉瘤治疗靶点的选择提供全新视角。
1 材料和方法
1.1 细胞株与实验动物
人成骨细胞系hFOB1.19和骨肉瘤细胞系Saos-2、U2OS、HOS和143B均购自中国科学院细胞库。6周龄雄性BALB/c裸鼠购自上海斯莱克实验动物有限公司。
1.2 主要试剂与仪器
铁死亡诱导剂Erastin、抑制剂Ferrostatin-1购自美国MedChemExpress公司,DMEM/F-12和DMEM培养基购自美国Gibco公司,胎牛血清购自美国HyClone公司,ECL发光液、BCA蛋白定量试剂盒购自美国Thermo Fisher Scientific公司,PVDF膜购自美国Millipore公司,CCK-8购自上海碧云天生物技术有限公司,一次性细胞嵌入皿24孔(8 μm)购自广州洁特生物过滤股份有限公司,丙二醛含量检测试剂盒和还原型GSH含量检测试剂盒购自北京索莱宝科技有限公司,铁离子检测试剂盒、SND1和β-actin抗体购自美国Abcam公司,小干扰RNA(small interfering RNA,siRNA)转染SND1和对照序列购自上海吉玛制药技术有限公司。SpectraMax iD3多功能酶标仪购自美国Molecular Devices公司,CO2细胞培养箱购自美国Thermo Fisher Scientific公司,电泳系统和凝胶成像分析系统购自美国Bio-Rad公司。
1.3 细胞培养
人成骨细胞hFOB1.19使用含10%胎牛血清、2.5 mmol/L L-谷氨酰胺和0.3 mg/mL遗传霉素的DMEM/F-12培养基,置于37 ℃、5% CO2培养箱中培养。待细胞生长至80%时,胰蛋白酶消化并传代培养。骨肉瘤细胞Saos-2、U2OS、HOS和143B使用含10%胎牛血清、1%青霉素/链霉素的DMEM培养基,置于37 ℃、5% CO2培养箱中常规培养和传代。
1.4 细胞转染
将143B细胞接种于6孔板中培养,按照Lipofectamine 2000试剂盒说明书将靶向SND1的siRNA(si-SND1)以及阴性对照(si-NC)分别转染至细胞中。si-SND1基因序列:5-GGACAAGGCCGGCAACTTTAT-3,si-NC基因序列:5-GGAGATTCTAGTAGGAGAA-3。采用10 μmol/L Erastin或2 μmol/L Ferrostatin-1处理各组细胞48 h,以诱导或抑制细胞内铁死亡。
1.5 细胞活性检测
将HOS和143B细胞以5×103个/孔的密度接种于96孔板中,分别在0、24、48、72 h向每孔加入10 μL CCK-8溶液孵育2 h,采用酶标仪测定450 nm处各孔光密度值。
1.6 细胞克隆形成实验
将HOS和143B细胞以3×103个/孔的密度接种于6孔板中,轻摇使细胞分散均匀,置于培养箱培养14 d,PBS清洗细胞2次,室温甲醇固定15 min,1%结晶紫染色10 min,光学显微镜下观察克隆形成情况,统计细胞克隆数量。
1.7 细胞迁移和侵袭实验
将悬浮在无血清DMEM培养基中的HOS和143B细胞以4×104/mL的密度分别接种于无基质胶和涂有Matrigel基质胶的上室内,另将含10%胎牛血清的DMEM培养基加入下室,培养24 h后,4%多聚甲醛固定30 min,1%结晶紫溶液染色30 min,清洗小室并用干净的棉棒擦去小室内部的细胞,光学显微镜观察细胞迁移和侵袭情况,并统计迁移和侵袭细胞的数目。
1.8 活性氧、铁离子、GSH和丙二醛水平测定
分别使用活性氧(reactive oxygen species,ROS)流式检测试剂盒、铁离子测定试剂盒、还原型GSH检测试剂盒和丙二醛检测试剂检测细胞蛋白样品中铁离子、GSH和丙二醛的水平,按照试剂盒说明书进行操作。
1.9 Western blot检测
使用含有蛋白酶抑制剂的RIPA裂解液提取细胞总蛋白,BCA法测定蛋白浓度。向蛋白样品中加入5×上样缓冲液,100 ℃金属浴使蛋白变性。取30 μg蛋白样品经SDS-PAGE凝胶电泳分离(浓缩胶80 V、30 min,分离胶120 V、90 min),转膜至PVDF膜上,5%脱脂奶粉封闭1 h,加入一抗4 ℃孵育过夜,TBST洗膜3次,每次10 min,加入辣根过氧化物酶标记的二抗室温孵育2 h,ECL显影,凝胶成像系统拍照,采用Image J软件进行灰度分析。
1.10 实时定量PCR检测
收集各组细胞,使用TRIzol试剂提取细胞总RNA,采用分光光度计检测RNA浓度。按照逆转录试剂盒说明书将RNA逆转录为cDNA,并采用实时定量PCR(quantitative real-time PCR,qPCR)试剂盒进行扩增。以GAPDH为内参基因,采用2-△△Ct法计算相对表达量。引物序列:SND1正向引物:5-TGCAGCGGGGTAATCCTGA-3,反向引物:5-CCTCCGACACTTCGTCATCC-3;SLC7A11正向引物:5-GGTGGTGTGTTTGCTGTC-3,反向引物:5-GCTGGTAGAGGAGTGTGC-3;GAPDH正向引物:5-GGTCTCTGACTTCAACA-3,反向引物:5-GTGAGGG-TCTCTCTCTTCCT-3。
1.11 异种移植瘤模型建立
转染si-SND1或si-NC的143B细胞以1×106个/mL细胞密度经皮下注射到裸鼠体内。每4 d测量肿瘤体积1次,3周后处死裸鼠,收集异种移植肿瘤。肿瘤体积(mm3)=0.5×长径×宽径2。
1.12 统计学处理
采用GraphPad Prism 8.0统计软件,符合正态分布的连续性变量以均数±标准差表示,组间比较采用独立样本t检验,多组间比较采用单因素方差分析,并使用LSD检验进行两两比较;非连续变量以百分比表示,组间比较采用Mann-Whitney U检验,多组间比较采用Kruskal-Wallistest检验。所有实验均独立重复3次。P<0.05为差异有统计学意义。
2 结果
2.1 SND1在骨肉瘤细胞系中的表达水平
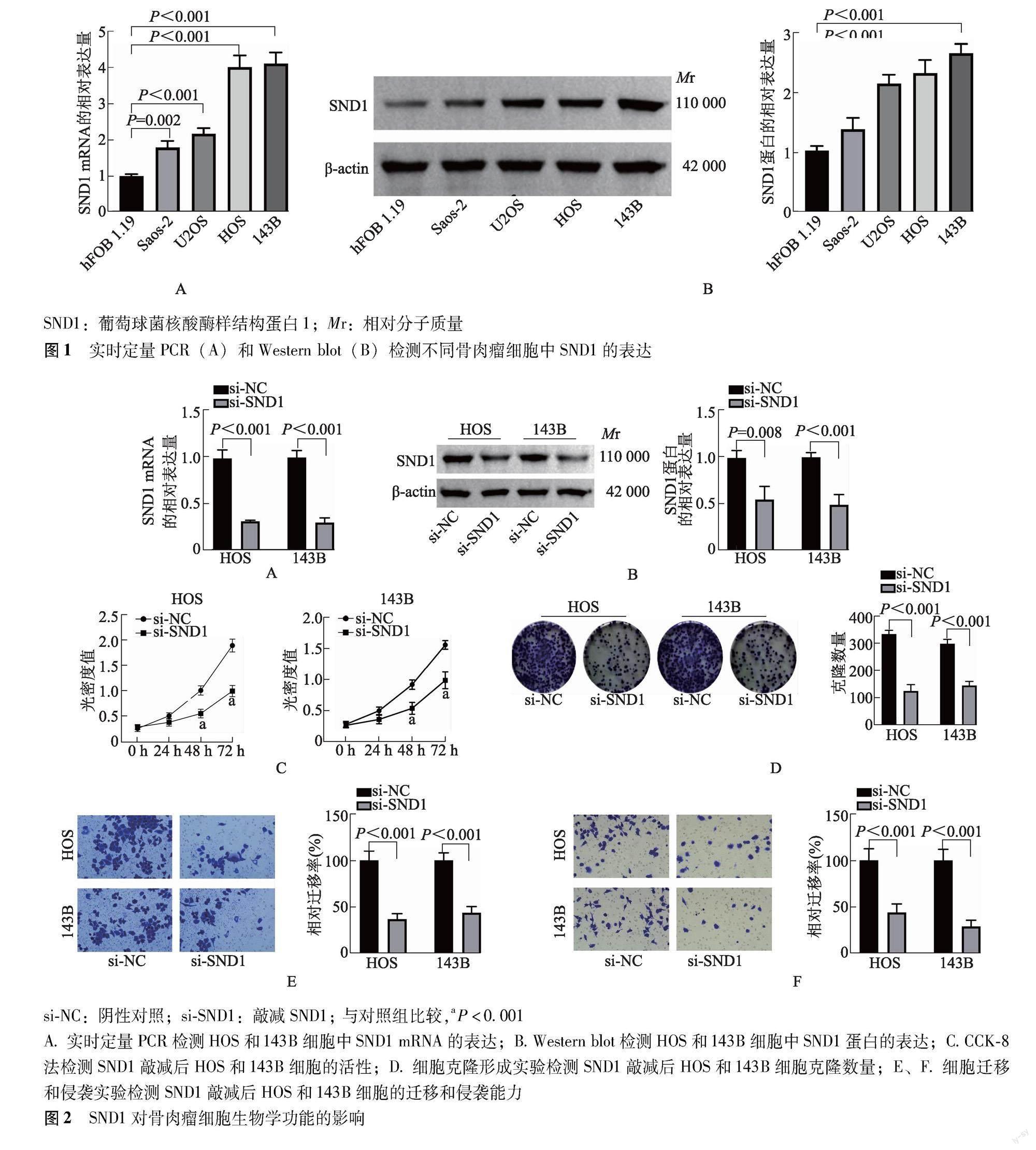
qPCR检测结果显示,骨肉瘤细胞Saos-2、U2OS、HOS和143B中SND1 mRNA的表达水平显著高于人成骨细胞hFOB1.19(P=0.002,P<0.001,P<0.001,P<0.001)(图1A);Western blot法检测结果显示,骨肉瘤细胞Saos-2、U2OS、HOS和143B中SND1蛋白的表达水平显著高于人成骨细胞hFOB1.19(P均<0.001)(图1B),选取SND1表达较高的HOS和143B细胞用于后续实验。
2.2 敲减SND1对骨肉瘤细胞活性、克隆形成、迁移和侵袭能力的影响
敲减SND1后,与si-NC组比较,si-SND1组HOS和143B細胞中SND1的mRNA(P均<0.001)及蛋白(P=0.008,P<0.001)表达水平显著减少;细胞的活性显著降低,细胞克隆形成数量显著减少,细胞迁移和侵袭能力显著降低(P均<0.001)(图2)。
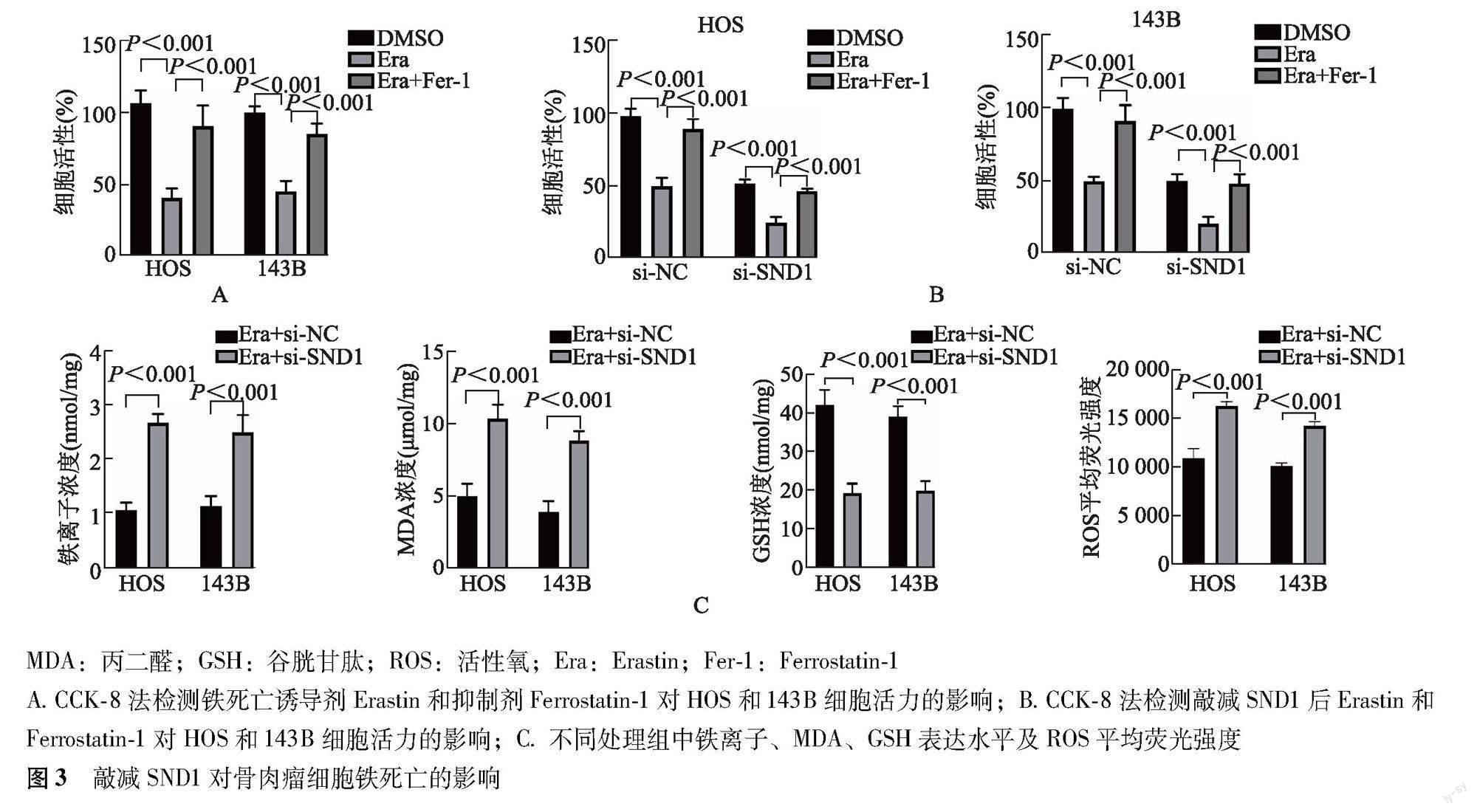
2.3 敲减SND1对骨肉瘤细胞铁死亡的影响
与DMSO对照比较,铁死亡诱导剂Erastin显著降低HOS和143B细胞活性,使用抑制剂Ferrostatin-1后HOS和143B细胞活性恢复升高(P均<0.001)(图3A)。敲减SND-1后使用铁死亡诱导剂Erastin可进一步降低骨肉瘤HOS和143B细胞活性,使用Ferrostatin-1刺激后细胞活性恢复升高(P均<0.001)(图3B)。此外,与Erastin+si-NC组比较,Erastin+si-SND1组细胞中铁离子、丙二醛以及ROS表达升高,GSH表达降低(P均<0.001)(图3C)。
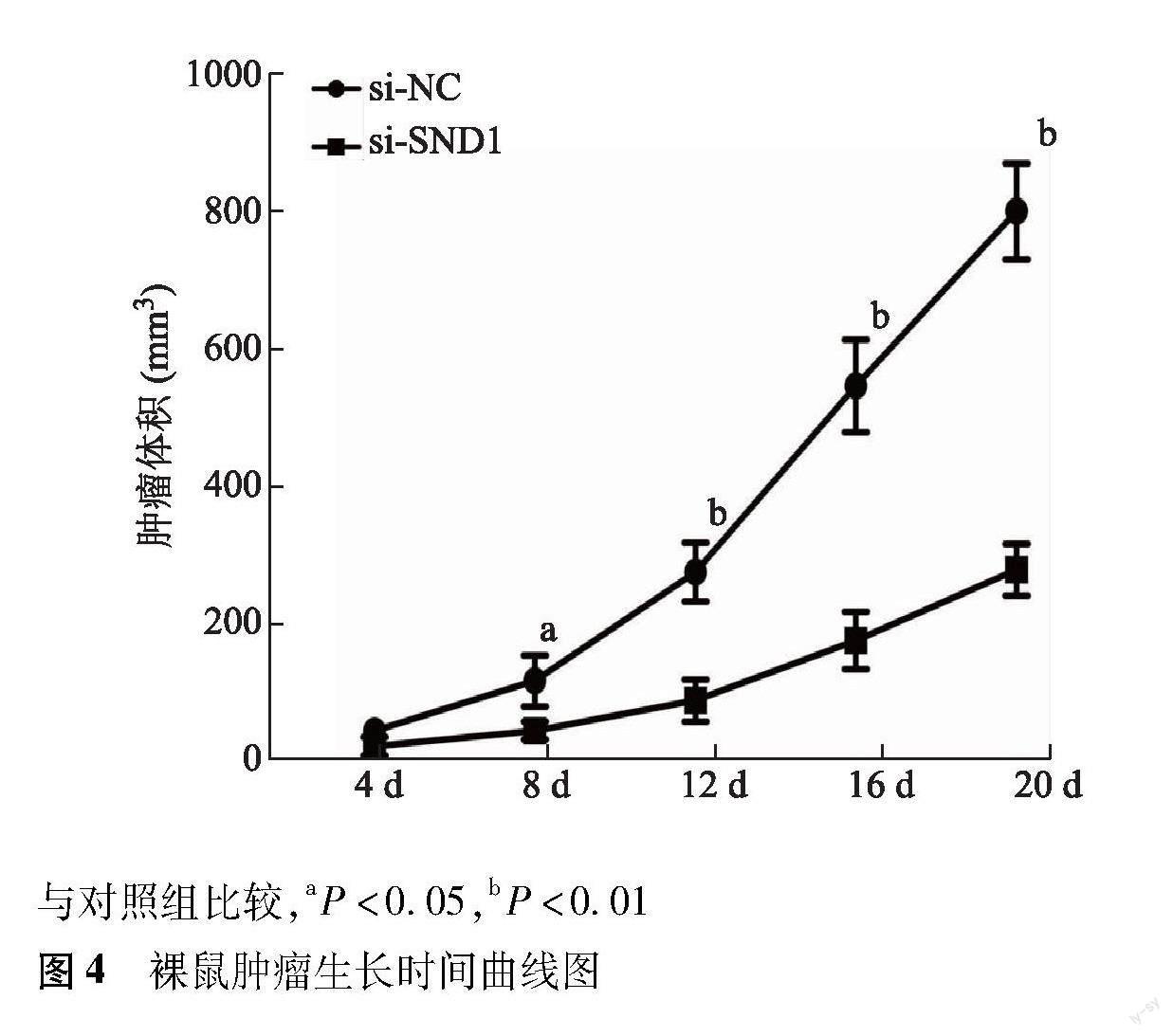
2.4 敲减SND1对裸鼠移植瘤体积和质量的影响
与对照组比较,敲减SND1后的143B细胞裸鼠移植瘤在8、12、16、20 d肿瘤体积均明显降低(P均<0.05)(图4)。第21天si-SND1组肿瘤质量小于si-NC组[(435.72±84.80)mg比(882.60±119.71)mg,P<0.001]。
2.5 SND1调控SLC7A11表达对铁死亡的抑制作用
qPCR和Western blot检测结果显示,骨肉瘤HOS和143B细胞中SLC7A11 mRNA和蛋白的表达水平均显著高于人成骨细胞hFOB1.19(P均<0.001)(图5A、5B)。敲减SND1或Erastin处理均能够抑制骨肉瘤HOS和143B细胞中SLC7A11的表达水平(P均<0.05)(图5C、5D)。敲减SND1后,细胞铁死亡标志物铁离子、MDA、ROS表达升高,GSH表达下降(P均<0.05)(图5E)。
3 讨论
骨肉瘤恶性程度高,预后较差,患者5年生存率相对较低。尽管尝试开发多种药物和新型治疗手段,但是效果并不理想。探明骨肉瘤的调控机制有助于临床开发新型治疗靶点药物。本研究关注SND1对骨肉瘤细胞生物学功能的影响,并强调了其对骨肉瘤细胞铁死亡过程的重要调节作用,这为揭示骨肉瘤的病理机制提供了更深层次的理论基础。
SND1是維持生物体正常发育的关键蛋白,主要表达在内质网膜上,并在33种肿瘤中具有潜在的致癌作用,其机制可能与主要组织相容复合体Ⅰ在内质网中的降解有关[9]。基于癌症基因组图谱和基因表达数
据库的数据集分析结果表明,SND1在结肠癌、黑色素瘤中调控CD8+ T细胞相关的免疫逃逸[10]。SND1可能通过靶向miRNA665促进骨肉瘤细胞的增殖。然而SND1对骨肉瘤的其他调节作用尚不清楚[11]。本研究以成骨细胞hFOB1.19为对照,检测了4种骨肉瘤细胞中SND1的表达,结果显示SND1表达水平显著升高。调减SND1表达后HOS和143B细胞的活性降低、克隆形成数量明显减少,迁移和侵袭能力下降,表明下调SND1可抑制骨肉瘤细胞的发生发展。
铁死亡作为一种新型的细胞死亡形式,在肿瘤的临床治疗中具有重要的研究和应用价值[12]。既往文献表明铁死亡能够促进包括骨肉瘤在内的多种肿瘤细胞的凋亡[13-14]。但是SND1对骨肉瘤细胞铁死亡的影响不明确。本研究采用铁死亡诱导剂Erastin和抑制剂Ferrostatin-1对骨肉瘤细胞的铁死亡过程进行细胞水平上的调控,结果表明诱导铁死亡后骨肉瘤细胞的活性显著下降,敲减骨肉瘤细胞中SND1的表达后肿瘤细胞活性进一步降低。当使用铁死亡抑制剂Ferrostatin-1抑制肿瘤细胞铁死亡后,si-SND1组骨肉瘤细胞的活性逐渐恢复,说明SND-1通过铁死亡调控骨肉瘤细胞的活性。同时,Erastin+si-SND1组铁死亡标志物铁、丙二醛表达量增加,GSH表达下降,说明敲减SND1可能通过促进铁死亡抑制肿瘤细胞的活性。既往研究表明,胱氨酸/谷氨酸反转运蛋白SLC7A11是抗氧化的关键蛋白,在肺癌[15]、卵巢癌[16]等多种癌症中过度表达,且通过抑制铁死亡促进肿瘤生长。SLC7A11在骨肉瘤中的研究较少,布比卡因、替拉扎明[17]等化疗药物被证实是通过SLC7A11介导的铁死亡过程抑制肿瘤生长。本研究探讨SND1是否通过SLC7A11途径调控骨肉瘤细胞的铁死亡,结果表明骨肉瘤细胞中SLC7A11的表达上调,抑制SND1或促进铁死亡都可以降低SLC7A11的表达水平。此外,SND1敲减还促进了Erastin介导的SLC7A11表达下调,并导致细胞铁死亡水平的升高;而过表达SLC7A11骨肉瘤细胞的铁死亡水平显著降低。因此,敲减SND1可能是通过下调SLC7A11的表达促进骨肉瘤细胞的铁死亡,进而抑制骨肉瘤。
本研究还通过异种移植瘤模型初步探索了干预SND1对骨肉瘤的影响,结果显示下调肿瘤细胞中SND1的表达能够减少裸鼠成瘤体积和质量,说明以SND1为靶点的治疗方式可能会延缓骨肉瘤的疾病进展。然而本研究尚存在不足,SND1通过SLC7A11调控骨肉瘤铁死亡的机制尚不明确,未来的研究应加以完善,以阐明SND1调控骨肉瘤的分子机制。
综上,本研究结果表明,SND1在骨肉瘤细胞中呈高表达,下调SND1表达可以抑制骨肉瘤细胞活性,降低骨肉瘤细胞克隆形成、迁移和侵袭能力,并抑制异种移植瘤的生长。SND1可能通过促进SLC7A11的表达抑制铁死亡进而促进骨肉瘤的发生发展。SND1及其靶向铁死亡的调控为骨肉瘤的临床治疗提供了潜在的新思路。
利益冲突 所有作者声明无利益冲突
作者贡献声明 王胜涛:设计实验研究、统计分析、撰写论文;徐淑娟:实验实施、统计分析;贵鹏、李欣咛、隋玉涵:收集数据、整理数据;李朝旭:指导研究、修改论文
参 考 文 献
[1]杨美菊,武壮壮,申振,等.调节骨肉瘤的微小RNA研究进展[J].中华实验外科杂志, 2021,38(7):1386-1391.DOI:10.3760/cma.j.cn421213-20201104-00807.
[2]Ochoa B,Chico Y,Martínez MJ.Insights into SND1 oncogene promoter regulation[J].Front Oncol,2018,8:606.DOI:10.3389/fonc.2018.00606.
[3]Shen M,Smith HA,Wei Y,et al.Pharmacological disruption of the MTDH-SND1 complex enhances tumor antigen presentation and synergizes with anti-PD-1 therapy in metastatic breast cancer[J].Nat Cancer,2022,3(1):60-74.DOI:10.1038/s43018-021-00280-y.
[4]Fu X,Duan Z,Lu X,et al.SND1 promotes radioresistance in cervical cancer cells by targeting the DNA damage response[J].Cancer Biother Radiopharm,2022.DOI:10.1089/cbr.2021.0371.
[5]Hirschhorn T,Stockwell BR.The development of the concept of ferroptosis[J].Free Radic Biol Med,2019,133:130-143.DOI:10.1016/j.freeradbiomed.2018.09.043.
[6]Lei G,Zhuang L,Gan B.Targeting ferroptosis as a vulnerability in cancer[J].Nat Rev Cancer,2022,22(7):381-396.DOI:10.1038/s41568-022-00459-0.
[7]Gao M,Fan K,Chen Y,et al.Understanding the mechanistic regulation of ferroptosis in cancer:gene matters[J].J Genet Genomics,2022,49(10):913-926.DOI:10.1016/j.jgg.2022.06.002.
[8]Koppula P,Zhuang L,Gan B.Cystine transporter SLC7A11/xCT in cancer:ferroptosis,nutrient dependency,and cancer therapy[J].Protein Cell,2021,12(8):599-620.DOI:10.1007/s13238-020-00789-5.
[9]Wang Y,Wang X,Cui X,et al.Oncoprotein SND1 hijacks nascent MHC-I heavy chain to ER-associated degradation,leading to impaired CD8+ T cell response in tumor[J].Sci Adv,2020,6(22):eaba5412.DOI:10.1126/sciadv.aba5412.
[10]Cui X,Zhang X,Liu M,et al.A pan-cancer analysis of the oncogenic role of staphylococcal nuclease domain-containing protein 1(SND1) in human tumors[J].Genomics,2020,112(6):3958-3967.DOI:10.1016/j.ygeno.2020.06.044.
[11]Jin XM,Xu B,Zhang Y,et al.LncRNA SND1-IT1 accelerates the proliferation and migration of osteosarcoma via sponging miRNA-665 to upregulate POU2F1[J].Eur Rev Med Pharmacol Sci,2019,23(22):9772-9780.DOI:10.26355/eurrev_201911_19540.
[12]Yan HF,Zou T,Tuo QZ,et al.Ferroptosis:mechanisms and links with diseases[J].Signal Transduct Target Ther,2021,6(1):49.DOI:10.1038/s41392-020-00428-9.
[13]Zhao J,Zhao Y,Ma X,et al.Targeting ferroptosis in osteosarcoma[J],J Bone Oncol,2021,30:100380.DOI:10.1016/j.jbo.2021.100380.
[14]Lei G,Zhang Y,Koppula P,et al.The role of ferroptosis in ionizing radiation-induced cell death and tumor suppression[J].Cell Res,2020,30(2):146-162.DOI:10.1038/s41422-019-0263-3.
[15]Zhang W,Sun Y,Bai L,et al.RBMS1 regulates lung cancer ferroptosis through translational control of SLC7A11[J].J Clin Invest,2021,131(22):e152067.DOI:10.1172/JCI152067.
[16]Hong T,Lei G,Chen X,et al.PARP inhibition promotes ferroptosis via repressing SLC7A11 and synergizes with ferroptosis inducers in BRCA-proficient ovarian cancer[J].Redox Biol,2021,42:101928.DOI:10.1016/j.redox.2021.101928.
[17]Luo Y,Gao X,Zou L,et al.Bavachin induces ferroptosis through the STAT3/P53/SLC7A11 axis in osteosarcoma Cells[J].Oxid Med Cell Longev,2021,2021:1783485.DOI:10.1155/2021/1783485.
(收稿日期:2023-06-28)
