抑制髓样细胞触发受体-1(TREM-1)减轻慢性间歇性低氧诱发的模型小鼠动脉粥样硬化
2024-03-22余晗俏余育斌冯丽娜盛晓生叶晓霞王林燕
余晗俏,李 超,余育斌,冯丽娜,盛晓生,叶晓霞,王林燕
1.金华市人民医院 心内一科,浙江 金华 321000;2.金华市金东区第二人民医院 全科医学科,浙江 金华 321000
阻塞性睡眠呼吸暂停(obstructive sleep apnea,OSA)是在睡眠期间反复出现呼吸暂停,并导致上呼吸道塌陷和间歇性低氧血症[1]。OSA与心血管疾病有关,其慢性间歇性低氧(chronic intermittent hypoxia,CIH)的特征会导致内皮功能障碍和动脉粥样硬化(atherosclerosis,AS)发生发展[2]。促炎性巨噬细胞与AS发生、预后发展密切相关,能够通过吞噬动脉血管内皮下脂蛋白形成泡沫细胞,导致AS发生发展,与AS斑块的不稳定性及AS不良预后密切相关[3-4]。髓样细胞触发受体-1(triggering receptor expressed on myeloid cells-1,TREM-1)是一种在成熟单核细胞、巨噬细胞上表达的蛋白质,参与炎性信号放大[5-6]。实验证明,TREM-1与促炎性巨噬细胞活化及AS发生发展相关[7],但是抑制TREM-1对AS作用尚不得知。本研究旨在探究抑制TREM-1对AS的作用及潜在机制。
1 材料与方法
1.1 材料
1.1.1 动物:雄性ApoE-/-小鼠购于北京维通利华公司。
1.1.2 试剂:TREM-1抑制剂LR12(MCE公司);TNF-α、IL-1β、IL-10 ELISA试剂盒(武汉伊莱瑞特生物科技股份有限公司);Trizol试剂、反转录试剂盒、SYBR Green PCR master mix(北京天根生化公司);油红O染液(上海碧云天生物技术公司);TREM-1抗体、CD68抗体、FITC标记二抗、Alex Flour 594标记二抗(Abcam公司);高脂饲料(北京华阜康生物科技公司)。
1.2 方法
1.2.1 小鼠的分组及处理:将ApoE-/-小鼠随机分为空白组(blank,小鼠饲养在正常氧气环境下,给予普通饲料喂养)、模型组(model,将小鼠置于6%氧气舱维持20 s,转入20%氧气舱,维持该浓度20 s,如此操作每天循环240次,连续12周,期间小鼠予以高脂饲料饲养)和实验组(experiment,小鼠高脂饲料饲养4周后,腹腔注射TREM-1抑制剂LR12,5 mg/kg,每天1次,连续干预8周,其他干预条件与模型组一致),每组8只。
1.2.2 ELISA检测血脂及血清炎性因子:饲养12周后,取小鼠外周血,离心,取血清。采用生化免疫分析系统检测血清TC、LDL、TG水平;采用TNF-α、IL-1β、IL-10 ELISA试剂盒检测血清TNF-α、IL-1β、IL-10水平,具体方法参照ELISA试剂盒说明书。
1.2.3 RT-qPCR检测mRNA:取小鼠主动脉,采用Trizol法提取组织中RNA,然后反转录获得cDNA,采用qPCR检测主动脉中TREM-1 mRNA表达水平。TREM-1引物:上游,5′-GATGTCGAGAGTCCC AATGA-3′,下游5′-GCTGGCATTCTGAGGCAAAA-3′;GAPDH引物:上游,5′-GATTAGCCGAGGTATAGCCA-3′,下游5′-ACTTGGAGCTTCGGACAAGA-3′。
1.2.4 HE染色及油红O染色检测主动脉根部或主动脉:将小鼠心脏及分离的主动脉放入含有4%多聚甲醛的离心管中固定。取小鼠心脏,然后用剪刀将心脏横切分为两部分,分离主动脉根部,使用optimal cutting temperature(OCT)包埋剂包埋主动脉根部切片,制备切片。同时取固定好的主动脉,纵向剖开,将其展开固定在蜡台上。将制备的主动脉根部切片进行HE染色,将制备的主动脉根部切片机展开的主动脉进行油红O染色。
1.2.5 免疫荧光(immunofluorescence,IF)染色检测TREM及巨噬细胞:取上述主动脉根部冰冻切片,山羊血清封闭,抗小鼠TREM-1抗体(1∶1 000)、抗小鼠CD68抗体(1∶1 000)孵育,之后使用FITC、Alex Flour 594标记抗兔及大鼠二抗体孵育,DAPI封片,在荧光显微镜下观察拍照。
1.3 统计学分析

2 结果
2.1 CIH诱发动脉粥样硬化小鼠主动脉斑块TREM-1表达水平
空白组主动脉上有少量斑块及炎性细胞浸润,模型组主动脉上有大量斑块沉积及炎性细胞浸润。模型组主动脉斑块TREM-1蛋白及mRNA及表达水平显著高于空白组(P<0.05)(图1,表1)。

表1 动脉粥样硬化模型小鼠主动脉斑块TREM-1表达水平

图1 动脉粥样硬化模型小鼠主动脉斑块TREM-1表达量检测Fig 1 Detection of TREM-1 expression in aortic plaque of atherosclerosis in satherosclerotic mouse model
2.2 阻断TREM-1减少CIH诱发的动脉粥样硬化斑块沉积
实验组主动脉及主动脉根部斑块面积显著少于模型组(P<0.05)(图2,表2)。

*P<0.01 compared with blank; #P<0.01 compared with model.
2.3 阻断TREM-1对CIH诱发的动脉粥样硬化模型小鼠血脂的影响
实验组小鼠血浆TC、TG、LDL水平显著低于模型组(P<0.05)(图3)。
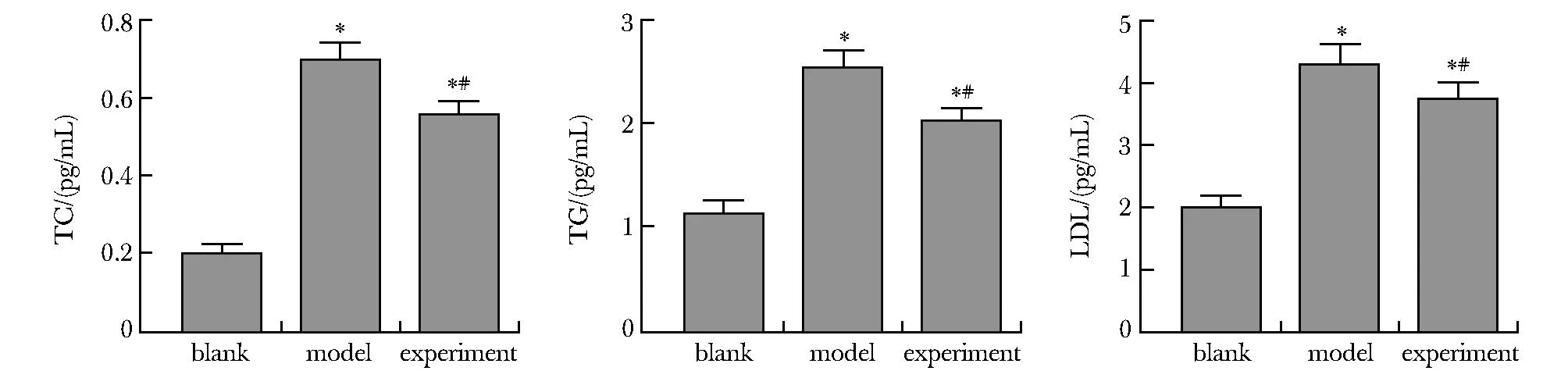
TC.total cholesterol; TG.triacylglycerol; LDL: low density lipoprotein; *P<0.01 compared with blank; #P<0.01 compared with model.
2.4 阻断TREM-1对CIH诱发的动脉粥样硬化模型小鼠炎性因子水平影响
实验组小鼠血浆TNF-α、IL-1β显著低于模型组,且IL-10水平显著高于模型组(P<0.05)(图4)。

*P<0.01 compared with blank; #P<0.01 compared with model.
2.5 阻断TREM-1对CIH诱发的动脉粥样硬化模型小鼠斑块巨噬细胞浸润的影响
实验组主动脉斑块巨噬细胞及TREM-1水平显著少于模型组(P<0.05),且斑块中TREM-1与巨噬细胞共定位(图5)。
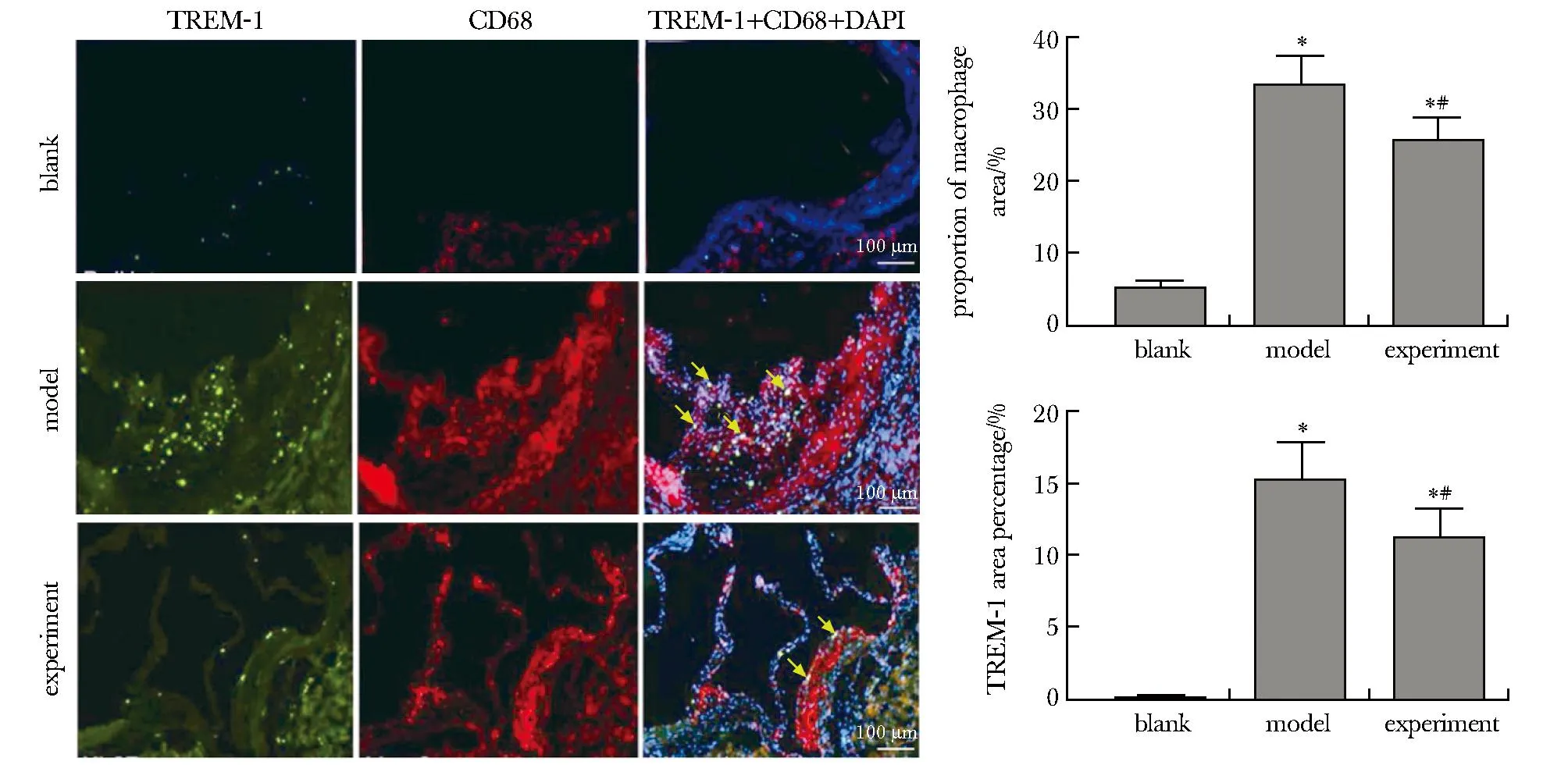
Green.TREM-1; Red.macrophages (CD68); Blue.nucleus (DAPI); *P<0.01 compared with blank; #P<0.01 compared with model.
3 讨论
OSA的特点是睡眠期间呼吸反复暂停,可导致上气道塌陷和CIH[8-9]。CIH是OSA的一个显著特征,其可产生多种炎性细胞因子,也是造成OSA患者AS损害的基础[4],但具体调控机制尚不明晰。研究表明TREM-1与AS发生发展有关[10]。TREM-1可通过影响机体脂质代谢,促使泡沫细胞生成,进而影响并促进AS进展研究指出血管平滑肌细胞(vascular smooth muscle cells,VSMCs)和树突状细胞的TREM-1表达可促进动脉斑块的不稳定性[7]。在临床比较有症状和无症状AS斑块的研究中,发现与无症状斑块相比,有症状斑块中TREM-1的表达显著上调;与来自无症状斑块的VSMCs相比,来自有症状斑块的血管平滑肌细胞与强效炎性细胞因子TNF-α的刺激诱导了TREM-1的更高表达[11]。本研究发现CIH诱导的动脉粥样硬化模型小鼠主动脉斑块中TREM-1 mRNA及蛋白表达水平显著升高。为进一步探究TREM-1在CIH诱导AS中作用,本研究采用TREM-1特异性拮抗剂LR12在CIH诱导AS发生过程进行干预,发现拮抗TREM-1能够显著的减少CIH诱导的ApoE-/-小鼠主动脉及主动脉根部斑块沉积,表明TREM-1在CIH诱导动脉粥样硬化中扮演重要角色。
在OSA导致AS的众多因素中,炎症和血脂异常是其中最重要的因素[8,12]。血浆中的LDL-C在内皮损伤或功能失常时附着血管壁,然后被进入内皮下的M1型巨噬细胞吞噬,使巨噬细胞泡沫化,促进AS的发生发展[12-13]。本研究发现,拮抗TREM-1组小鼠血浆TC、TG、LDL水平显著低于模型组小鼠,且血浆TNF-α、IL-1β显著低于模型组,IL-10水平显著高于模型组,表明拮抗TREM-1抑制AS发生发展可能是通过抑制血脂及炎性反应。研究显示,TNF-α、IL-1β、?劄?L-10在巨噬细胞激活过程扮演重要角色[14]。CIH可作为一种炎性刺激,诱导巨噬细胞向M1型极化,促进IL-6的表达[15]。巨噬细胞可分泌表达TREM-1,提示TREM-1可能通过调控巨噬细胞激活调控AS发生发展。进一步对AS斑块中M1型巨噬细胞进行染色发现,抑制TREM-1小鼠CIH诱导AS斑块M1型巨噬细胞及TREM-1表达显著低于模型组,且二者荧光信号共定位,提示可能巨噬细胞分泌的TREM-1通过调控巨噬细胞激活,继而调控AS发生发展。
综上所述,TREM-1参与CIH诱发的动脉粥样硬化发生发展,抑制TREM-1可以缓解CIH诱发的动脉粥样硬化,其机制与抑制巨噬细胞活化有关。
