3D打印补偿膜在乳腺癌即刻乳房重建术后放疗中的应用
2024-03-20王勇周玉玲周琼辉曾彪胡英
王勇 周玉玲 周琼辉 曾彪 胡英
作者单位:410000 长沙 湖南省肿瘤医院胸部放疗二科
乳腺癌是女性常见的恶性肿瘤,手术和放疗是其综合治疗的重要手段,但患者往往对形体完整和美观具有强烈愿望。目前,对于无法保乳的患者可通过即刻乳房重建术保持乳房完整和美观[1],其远期生存率与改良根治术并无明显差异[2-4]。在乳腺癌术后辅助放疗中常采用6 MV 高能X 射线,由于存在“建成效应”,即由空气(低密度)射入人体(高密度)时在皮肤表面形成低剂量区,因此高能X 射线在进入皮肤后,其最大剂量值不在皮肤表面,而是在皮下正常组织内[5]。基于高能X 射线这一特性,在临床上进行乳腺癌放疗时通常使用3~5 mm 厚度的组织补偿膜覆盖于皮肤上,以此提高表皮及皮下组织的受照剂量[6]。组织补偿膜一般要求紧贴乳房皮肤,目前市售补偿膜的规则、尺寸大小基本固定,但即刻重建术后的乳腺癌患者皮肤呈一定弧度,因此需要裁减才能较好地贴合于乳房;此外市售补偿膜在实际使用时常与皮肤存在一定的空气间隙,这可能致使乳房皮肤放疗剂量不足,从而影响放疗疗效,增加患者局部复发风险。3D打印可以根据患者的个体差异定制出与重建乳房形状完全匹配的补偿膜,有望解决这一问题。目前国内已有3D 打印补偿膜应用在乳腺癌改良根治术后患者中的报道[7-8],但尚未见应用于乳腺癌即刻乳房重建术后患者的报道。本研究旨在探讨3D 打印补偿膜在乳腺癌即刻乳房重建术后放疗中的应用效果,为其应用于临床治疗提供参考。
1 资料与方法
1.1 一般资料
选取2021年11月至2022年5月在湖南省肿瘤医院进行乳腺癌改良根治术后即刻重建乳房的11 例女性乳腺癌患者,年龄范围33~51 岁,中位年龄43 岁。11 例患者全部经病理证实为乳腺癌,其中5 例为右乳癌,6 例为左乳癌;术后分期均为ⅡA~ⅢB 期,同时完成了6~8 个周期的全身化疗。本研究经湖南省肿瘤医院伦理委员会批准(伦理号:KYJJ-2020-177)。依据2021 年乳腺癌的美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)和中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)指南,所有患者术后辅助放疗指征均明确,放疗前均签署放疗知情同意书。
1.2 方法
1.2.1 主要设备 恒温水箱KBT-802,Klarity 热塑膜及定位坐标板,苏州普能医疗3D体膜打印机,PHILIPS 16排大孔径CT 模拟定位机,LAP 激光灯系统,医科达Monaco放疗计划系统。
1.2.2 模拟定位 所有患者均取仰卧位平躺于Klarity定位坐标板上(患者体中线与Klarity 定位坐标板中线重合),双手抓头顶上方固定板杆,体表确定激光定位点,PHILIPS 16 排大孔径CT 模拟定位机在自由呼吸下行CT 定位扫描,从第一颈椎水平扫描至肝下缘水平,扫描层厚度5 mm。第1 次CT 定位扫描后把图像传送至Monaco 放疗计划系统以及普能PMT 3D 打印软件。待3D 打印补偿膜制作完成后,将3D 打印补偿膜及市售补偿膜覆盖于重建乳房表面,再用Klarity 热塑膜固定,采用同一序列进行第2 次和第3 次CT 定位扫描。
1.2.3 3D 打印补偿膜的制作 患者进行CT 定位扫描后,把图像传输到Monaco放疗计划系统中。在治疗计划系统(treatment planning system,TPS)中勾画靶区范围,然后勾画需要提高表面剂量的皮肤轮廓,确定补偿膜的外形及大小。再从TPS中将DICOM格式的补偿膜图像传输到普能PMT 3D打印软件中,平滑处理补偿膜三维模型后,再将每个患者定制的补偿膜数据以STL格式导入3D打印机中,采用聚乳酸(polylactic acid,PLA)材料进行打印。模具打印完成后检查是否完整无网眼,再配兑硅胶进行浇筑、脱模,获得实体组织补偿膜。
1.2.4 计划靶区(planning target volume,PTV)和危及器官勾画 由同一医师在CT 定位图像上勾画靶区和危及器官,靶区由同一高年资医师审核。靶区勾画标准同乳腺癌根治术后标准(参考RTOG)。临床靶区(clinical target volume,CTV)勾画范围:上界为环状软骨或锁骨头的下缘,下界为CT 图像上健侧乳腺消失水平,内界为患侧胸骨旁线(包括手术疤痕),外界为健侧乳腺外界水平,前界为皮肤,后界为肋骨前缘(胸大肌筋膜、胸肌间淋巴结和乳房下的胸壁淋巴引流区)。PTV 是在CTV 基础外扩5 mm(对超出肺内及皮肤外的修回)。勾画危及器官:肺、心脏、食管、臂丛、健侧乳腺、脊髓、患侧肱骨头等。勾画补偿膜与乳房贴合的空气间隙。
1.2.5 计划设计 PTV 处方剂量为50 Gy/25 Fx,采用医科达Monaco 放疗计划系统(Version 5.51),6 MV-X的7 野调强放疗(intensity modulated radiation therapy,IMRT),每次2 Gy,每日1次,每周5次,共5 周。每例患者由同一物理师分别制定计划A 和计划B 两组放疗计划,计划A是以覆盖3D打印补偿膜进行的第2次CT定位扫描图像,计划B 是以覆盖市售补偿膜进行的第3次CT 定位扫描图像。先设计3D 打印补偿膜覆盖的放疗计划,然后把该放疗计划复制到市售补偿膜的定位图像上,再进行优化,因此同一例患者的两个放疗计划的射野参数、优化参数、生物优化函数等均保持一致。每例患者的两个计划制作完成后,统计其在两组计划中的靶区最大剂量、靶区的均匀度和覆盖度以及危及器官受照射量。靶区剂量要求处方剂量包含95% PTV,55 Gy剂量所占靶区体积应小于5%,53.5 Gy剂量所占靶区体积应小于10%,同时靶区之外的剂量应低于53.5 Gy。
1.2.6 组织补偿膜贴合度评估 在定位CT 图像上勾画出覆盖靶区外补偿膜与皮肤之间的空气间隙,系统统计出每一个间隙的总体积数,空气间隙的总体积越小,说明贴合度越好,反之越差,理想值为0。
1.2.7 靶区及危及器官的剂量学评估 靶区剂量学评估指标为均匀性指数(homogeneity index,HI)和新适形度指数(new conformity index,nCI)。HI=(D1%-D98%)/DP,其中DP为处方剂量(cGy);HI理想值为0,HI值越小说明靶区剂量的均匀性越好,反之越差[9]。nCI=VPIV×VTV/V²TIV,其中VPIV为处方剂量线所包含的体积(cm3),VTV为靶区体积(cm3),VTIV为处方剂量线所包含的靶区体积(PIV 与TV 的交集,cm3);nCI值范围为0~1,越接近于1适形程度越高,反之越差[10]。危及器官患侧肺的剂量学指标为Dmean、V5、V20、V30,心脏的剂量学指标为V30,健侧乳腺的剂量学指标为Dmean。其中,Dmean 为危及器官的平均受照射剂量,V5、V20 和V30 为危及器官分别受5 Gy、20 Gy 和30 Gy照射的体积占危及器官体积的百分数。
1.3 统计学方法
采用SPSS 26.0 软件进行统计分析,符合正态分布的计量资料以均数±标准差()表示,两组比较采用配对t检验;不符合正态分布的计量资料用中位数和四分位间距[中位数(IQR)]描述,组间比较采用配对秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 组织补偿膜的贴合度情况
CT 图像显示,市售补偿膜与患者皮肤的空气间隙较大(图1A、图1C、图1E),3D打印补偿膜与皮肤贴合度较高(图1B、图1D、图1F),且3D打印补偿膜材料具有均匀性、适形性,表明3D 打印补偿膜可有效提高放疗剂量的准确性和稳定性。3D 打印补偿膜对应计划A 的空气间隙体积为(8.029±2.542)cm3,市售补偿膜对应计划B 的空气间隙体积为(20.048±4.372)cm3,3D 打印补偿膜的空气间隙体积明显小于市售补偿膜(t=-5.300,P<0.001)。
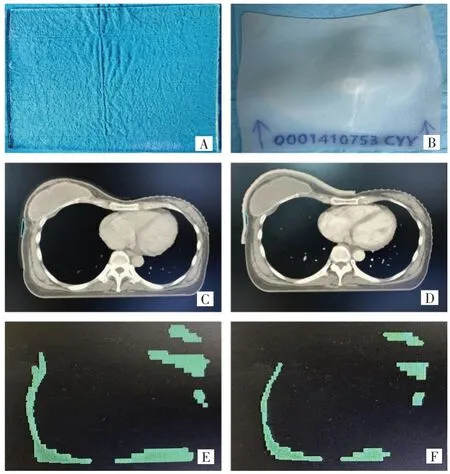
图1 3D打印补偿膜与市售补偿膜的空气间隙Fig.1 Air gap between 3D printing compensation film and commercial compensation film
2.2 靶区剂量学指标比较
在两组放疗计划的靶区剂量中,计划A的HI低于计划B(0.134%±0.008%vs0.161%±0.016%,t=-2.246,P=0.049),而nCI 则相反[0.79%(IQR:0.77%~0.83%)vs0.78%(IQR:0.75%~0.81%),Z=-2.316,P=0.021],表明3D 打印补偿膜在靶区均匀性及适形度上均优于市售补偿膜。
2.3 危及器官的剂量学比较
与计划B 相比,计划A 的健侧乳腺Dmean 和患侧肺V20 明显降低(均P<0.05),但心脏V30 和患侧肺Dmean、V5、V30 无明显变化(均P>0.05),提示3D打印补偿膜较市售补偿膜可降低危及器官受照射量。见表1。

表1 3D打印补偿膜与市售补偿膜的危及器官剂量学比较Tab.1 Comparison of organ at risk dosimetry between 3D printing compensation film and commercial compensation film
3 讨论
目前指南推荐有高危因素的乳腺癌患者进行术后辅助放疗[11]。既往研究显示,在乳腺癌放疗中需添加组织补偿膜以提高表皮剂量[12]。由于乳腺癌术后即刻乳房重建患者的乳房有一定弧度,且因术后留下瘢痕,目前的市售补偿膜与乳房往往不能完全贴合,导致形成一定的空气间隙,从而不能精确计算皮肤表面的实际照射剂量,致使靶区剂量分布与放疗计划实际不符,最终影响放疗效果。有研究报道,3D 打印补偿膜的剂量学参数等同于市售补偿膜,但其贴合度明显优于市售补偿膜[13]。还有研究报道,在物理计划评估中,3D 打印补偿膜和市售补偿膜的有效剂量覆盖等同,但3D 打印补偿膜的空气间隙明显减少,且改善了靶区的均匀性[14]。本研究在乳腺癌术后即刻乳房重建患者放疗中对比两者的应用效果,其中使用的市售补偿膜为28 mm×28 mm×5 mm 的方形体,形状大小固定统一,结果发现在使用时即使进行适当裁减,其贴合度仍然不佳,会存在一定的空气间隙。而既往文献报道,5 mm 的空气间隙就可使表面剂量下降10%左右,因此放疗时应尽可能将补偿膜完全覆盖于皮肤表面,以降低空气间隙对表皮剂量的影响[15-16]。而本研究使用的3D 打印补偿膜是基于每位患者体表曲度数据,使用质地均一、电子密度接近于水、制作时间短、易于成型的硅胶材料个体化定制的组织补偿物,具有硅胶材料的均匀性、适形性、生物等效性和可重复性,与市售补偿膜相比,能更完美地贴合乳房,空气间隙明显减小,且在靶区剂量的均匀度和适形度上优于市售补偿膜,表明3D 打印补偿膜能有效提高放疗剂量的准确性。
3D 打印技术已在多种肿瘤的放射治疗中得到应用并取得一定进展,如头颈部肿瘤、浅表肿瘤等[17-18]。盛成阳等[7]研究发现,3D 打印个体化补偿膜在HI、CI、心脏V30 和患侧肺受量(Dmean、V20、V30)方面优于市售补偿膜,在建成效应剂量上也优于市售补偿膜。闫昱萤等[8]研究也发现3D 打印组织补偿膜在空气间隙、CI、HI、患侧肺受量(V30、V20、Dmean)均优于常规组织补偿膜,但两者的患侧肺受量V5 无明显差异。此外,有研究报道补偿膜的应用可以保护患者的心功能[19]。本研究中3D 打印补偿膜靶区HI、nCI 及患侧肺V20 均优于市售补偿膜,提示3D 打印补偿膜对患侧肺具有更好的保护性以及更好的靶区覆盖。但本研究中3D 打印补偿膜的患侧肺(Dmean、V5、V30)、心脏V30 与市售补偿膜相比并无明显差异,这可能与本研究纳入的患者例数少以及物理师对放疗计划的把握度相关,另外两组放疗计划的心脏V30无明显差异也可能与收集的左侧乳腺癌患者较少有关。此外,本研究还发现3D 打印补偿膜对健侧乳腺具有更好的保护作用,提示3D 打印补偿膜可使放射剂量更聚集于放疗靶区上。
综上所述,在乳腺癌改良根治术后即刻乳房重建患者的放疗中,3D 打印补偿膜在对患侧肺、健侧乳腺的保护方面明显优于市售补偿膜,且具有更好的靶区均匀性及适形性。本研究结果说明,3D 打印补偿膜可能是该类患者的优势选择。但是本研究为单中心、小样本研究,因此研究结论还需开展多中心、大样本研究数据进行验证。
