芪地糖肾方调控NLRP3/Caspase-1/GSDMD通路介导高糖刺激肾小球内皮细胞焦亡的研究
2024-03-20董昭熙谢惠迪宿家铭郑毅成柳红芳
史 扬,董昭熙,周 盈,谢惠迪,郭 燕,宿家铭,郑毅成,柳红芳
(1. 北京中医药大学东直门医院,北京 100700;2. 北京市普仁医院,北京 100062;3. 解放军总医院第一医学中心肾脏病全国重点实验室,北京 100853)
糖尿病肾脏病(diabetic kidney disease,DKD)是导致全球终末期肾脏病(end stage renal disease,ESRD)的首位病因[1],由DKD进展至ESRD的群体较其他患者群体具有更高的病死率[2],且世界范围内的疾病负担调查显示,近30年来的DKD致死率均未见改善[3]。目前西医对DKD的治疗强调优化生活方式管理及血糖、血压控制,但研究显示严格控制血糖和血压的标准治疗仍无法阻止DKD进展至ESRD或降低DKD相关病死率[4-6]。蛋白尿作为DKD病情进展的独立危险因素,与病死率呈正相关[7],而肾小球内皮细胞功能障碍早于足细胞损伤且是早期微量蛋白尿的主要诱因,可多靶点作用推进DKD病程进展[8-9]。寻找早期影响肾小球内皮细胞功能的致病因素可能是DKD防治的关键。作为首层肾小球滤过屏障,肾小球内皮细胞对葡萄糖水平变化高度敏感,高血糖可从多个分子机制诱发其功能障碍,焦亡通路激活在其中起着关键作用,并导致进行性肾功能损害[10]。高糖刺激可诱导NOD样受体家族热蛋白结构域相关蛋白3(NLRP3)募集,并与半胱氨酸天冬氨酸蛋白酶-1前体(pro-Caspase-1)、凋亡相关斑点样蛋白(ASC)组装成多聚体蛋白复合物即NLRP3炎症小体[11];随后,NLRP3将pro-Caspase-1切割成其活性形式Caspase-1,进一步切割消皮素D蛋白(GSDMD),从而导致白细胞介素-1β(IL-1β)、白细胞介素-18(IL-18)等炎性因子分泌并伴随免疫细胞募集,触发细胞焦亡[12],加速肾小球硬化的病理进程。芪地糖肾方是北京中医药大学东直门医院柳红芳教授的经验方,可通过改善肾脏微炎症状态、减少尿蛋白以对抗糖尿病肾病进展[13-14],可减轻肾小球内毛细血管基底膜增厚,缓解包括肾小球内皮细胞在内的DKD肾脏病理改变[15],但其作用机制尚有待明确。本研究从细胞水平探讨了芪地糖肾方对高糖刺激的肾小球内皮细胞焦亡相关通路的调控作用,以期揭示其改善肾小球内皮细胞损伤、延缓DKD进展的作用机制,为该方的临床应用提供更多依据。
1 实验材料与方法
1.1实验细胞及药物 小鼠肾小球内皮细胞购于广州吉尼欧生物科技有限公司。 芪地糖肾方(由熟地黄、生黄芪、炒芡实、山萸肉、水蛭、熟大黄、白花蛇舌草组成)所含的中药饮片均购自北京中医药大学东直门医院中药房,将该方饮片浸泡于1~2 L双蒸水中15 min,按传统煎药方法将药物煎煮2次后混合均匀,并过滤及浓缩,获得中药水煎液约100 mL,使用冷冻干燥机冻干后迅速收集冻干粉,密封后于-20 ℃储存。使用完全培养基配置芪地糖肾方中药母液(10 mg/mL),用于细胞实验前以0.22 μm滤器过滤,现配现用。
1.2实验试剂 NLRP3抗体(ABclonal公司,货号:A21906),ASC抗体(Immunoway公司,货号:YT0365),Caspase-1抗体(proteintech公司,货号:22915-1-AP),GSDMD抗体(proteintech公司,货号:20770-1-AP),IL-1β抗体(CST公司,货号:12242),IL-18抗体(proteintech公司,货号:10663-1-AP),GAPDH 抗体 (proteintech公司,货号:60004-1-1g),β-actin抗体(proteintech公司,货号:81115-1-RR),HRP标记山羊抗兔 IgG(proteintech公司,SA00001-2),HRP标记山羊抗鼠IgG(proteintech公司,SA00001-1),鬼笔环肽(proteintech公司,PF00001),通用型抗体稀释液(苏州新赛美公司,WB500D),胎牛血清(FBS,Vivacell公司,C04001-500),0.25% Trypsin & 0.02%EDTA胰酶(Vivacell公司,C3530-0100),青链双抗(Vivacell公司,C3420-0100),PBS(Vivacell公司,C3580-0500),D-Glucose (北京兰博利德公司,G8270-1KG);24孔板专用细胞爬片剂(Solarbio公司,YA0350),防荧光淬灭封片剂(含DAPI)(Solarbio公司,ZLI-9557),一步法PAGE凝胶快速制备试剂盒10%(雅酶生物公司,PG212),BCA定量试剂盒(雅酶生物公司,ZJ102),特超敏ECL化学发光底物(Biosharp公司,BL520B),驴抗小鼠IgG(H+L) 高度交叉吸附二抗(Thermo Fisher公司,A21202),驴抗兔 IgG(H+L)高度交叉吸附二抗(Thermo Fisher公司,A21207),DMEM基础培养基(Thermo Fisher公司,10567-014)。
1.3实验仪器 37 ℃细胞恒温培养箱 (日本SANYO),电泳仪、垂直电泳槽及转印电泳槽 (北京龙方),Tanon 4600全自动化学发光图像分析系统(上海天能),细胞超净工作台(美国Theromo Fisher)。
1.4细胞培养方法 制备含有10%胎牛血清和1%双抗的糖浓度为5.5 mmol/L的DMEM完全培养基,细胞培养于37 ℃、5% CO2的恒温孵育箱内,隔天换液,细胞融合至80%左右进行传代及后续实验。
1.5检测指标及方法
1.5.1细胞中NLRP3表达和细胞骨架情况 采用免疫荧光染色法观察:提前将爬片置于24孔板中,将约5 000个肾小球内皮细胞接种在24孔板中,分为正常组、高糖组、芪地糖肾方组,细胞过夜贴壁后分别予完全培养基、30 mmol/L高糖培养基、30 mmol/L高糖培养基+芪地糖肾方(冻干粉)100 μg/mL培养48 h。弃去培养基,用无菌PBS洗3遍;4%多聚甲醛室温固定20 min,PBS洗3遍;0.1%Triton X-100透膜6 min,PBS洗3遍;5%驴血清室温封闭30 min,PBS洗3遍;一抗4 ℃慢摇床孵育过夜,PBS洗3遍;二抗室温慢摇床孵育1.5 h(避光),PBS洗3遍;用含DAPI封片剂封片(鬼笔环肽孵育后直接DAPI封片,无需孵育二抗)。
1.5.2细胞中焦亡通路相关蛋白表达情况 采用Western blot法检测:将约80万个肾小球内皮细胞接种在直径100 mm的培养皿中,分为正常组、高糖组、芪地糖肾方组,过夜贴壁后分别予完全培养基、30 mmol/L高糖培养基、30 mmol/L高糖培养基+芪地糖肾方(冻干粉)100 μg/mL培养48 h。弃去培养基,无菌PBS快速清洗细胞3次,加入蛋白裂解液,于冰上用细胞刮刀收集细胞,充分裂解后离心取上清,BCA定量测定蛋白浓度后配制蛋白样品,于-80 ℃冰箱保存备用。制备10%的PAGE凝胶,上样电泳、湿转法将蛋白印迹转移至NC膜上,5%脱脂牛奶封闭70 min,加入一抗(NLRP3抗体1∶1 000,ASC抗体1∶1 000、Caspase-1抗体1∶1 000,GSDMD抗体1∶1 000,IL-18抗体1∶800,IL-1β抗体1∶500,GAPDH抗体1∶10000,β-actin抗体1∶10000),4 ℃慢摇床孵育一抗过夜。次日用TBST洗膜6 min×3次,加入HRP标记山羊抗兔/鼠(1∶8 000)室温慢摇床孵育二抗50min,后用TBST洗膜6min×3次。1∶1配置超敏ECL发光液浸泡条带,全自动发光仪显影。使用Image J软件分析WB条带灰度值。
1.6统计学方法 采用SPSS 25.0软件进行数据分析。使用Shapiro-Wilk检验数据正态性,Levene检验数据方差齐性,若数据为正态分布且方差齐,采用单因素方差分析;若数据不是正态分布或方差不齐,采用非参数检验。P<0.05为差异有统计学意义。
2 结 果
2.1各组肾小球内皮细胞中NLRP3表达情况 与正常组比较,高糖组NLRP3荧光染色红色点状荧光信号显著增强;与高糖组比较,芪地糖肾方组NLRP3红色点状荧光表达信号减弱。见图1。
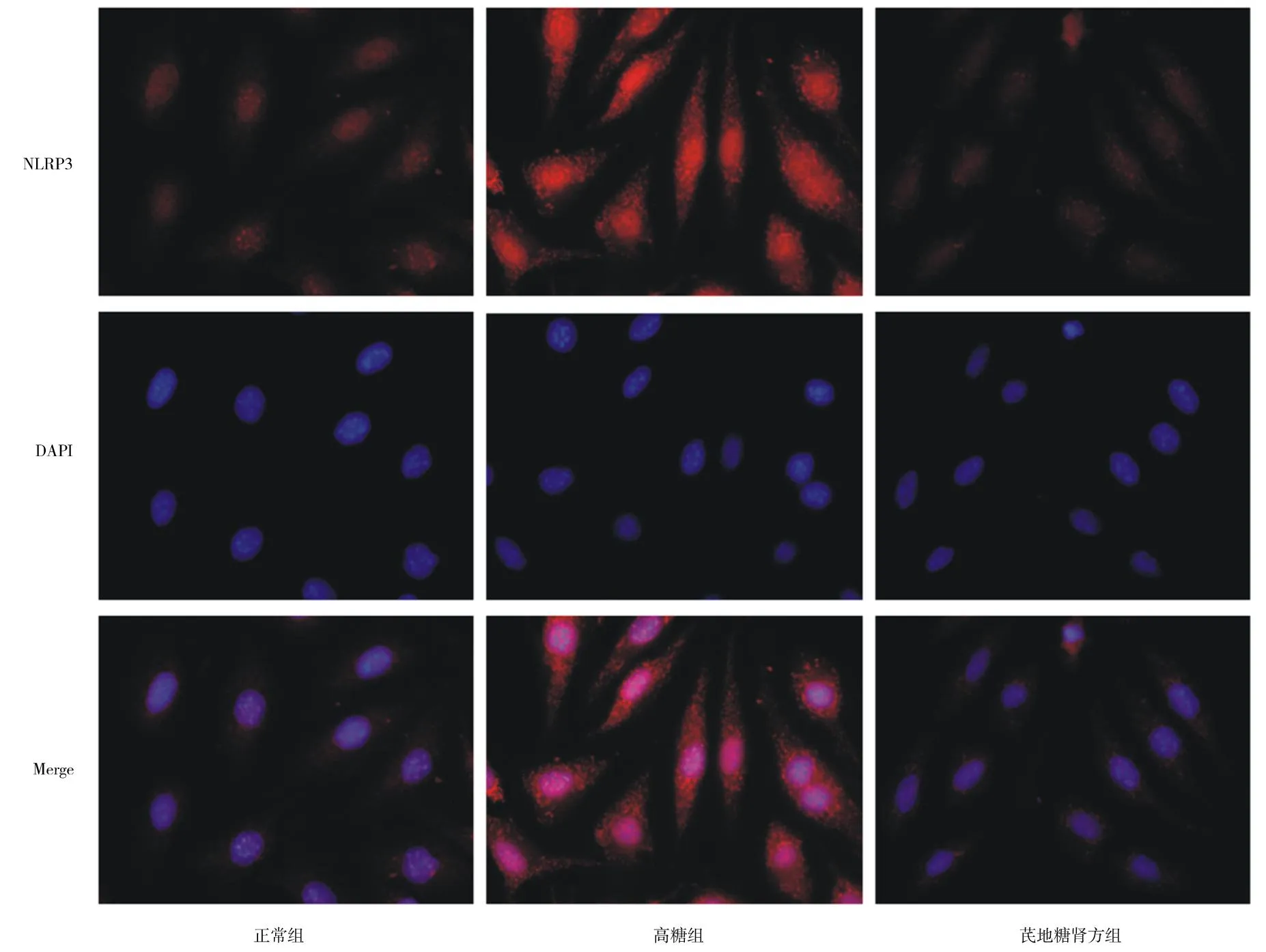
图1 正常组和高糖刺激各组肾小球内皮细胞中NLRP3表达情况(免疫荧光染色,×400)
2.2各组肾小球内皮细胞骨架情况 正常组细胞的绿色丝状荧光信号较强,清晰可见,数量可观,排列有序;与正常组比较,高糖组细胞中绿色丝状荧光强度显著减弱,且微丝数量减少,排列紊乱,骨架受损情况明显;与高糖组比较,芪地糖肾方组细胞的绿色丝状荧光信号增强,微丝数量增多,紊乱排列改善。见图2。
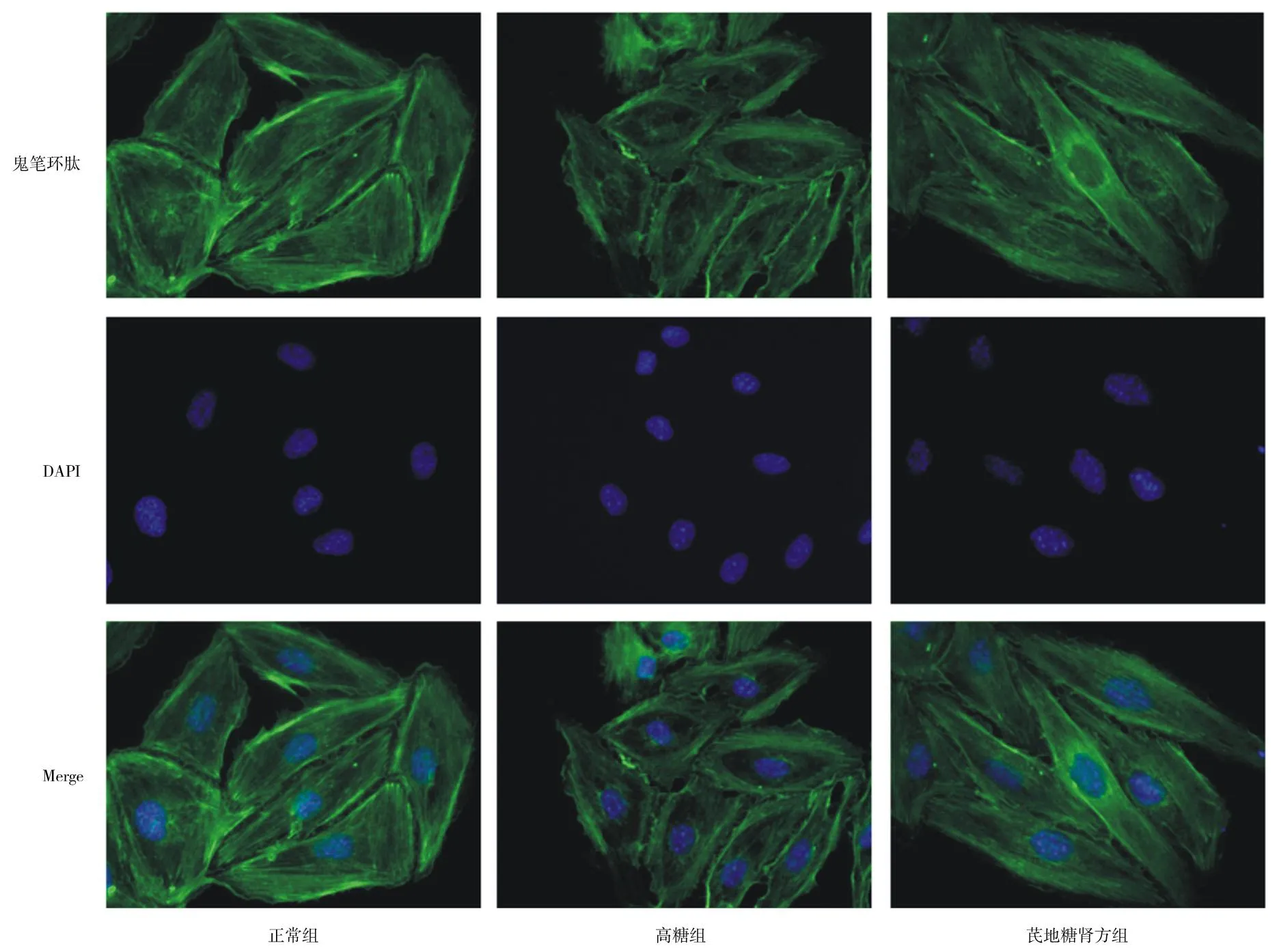
图2 正常组和高糖刺激各组肾小球内皮细胞骨架情况(免疫荧光染色,×400)
2.3各组肾小球内皮细胞焦亡通路相关蛋白表达情况 高糖组NLRP3、Caspase-1、GSDMD、ASC、IL-18、IL-1β蛋白相对表达量均明显高于正常组(P均<0.05),芪地糖肾方组NLRP3、Caspase-1、GSDMD、ASC、IL-18、IL-1β蛋白相对表达量均明显低于高糖组(P均<0.05)。见图3及表1。
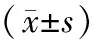
表1 正常组和高糖刺激各组肾小球内皮细胞中焦亡通路相关蛋白相对表达量比较
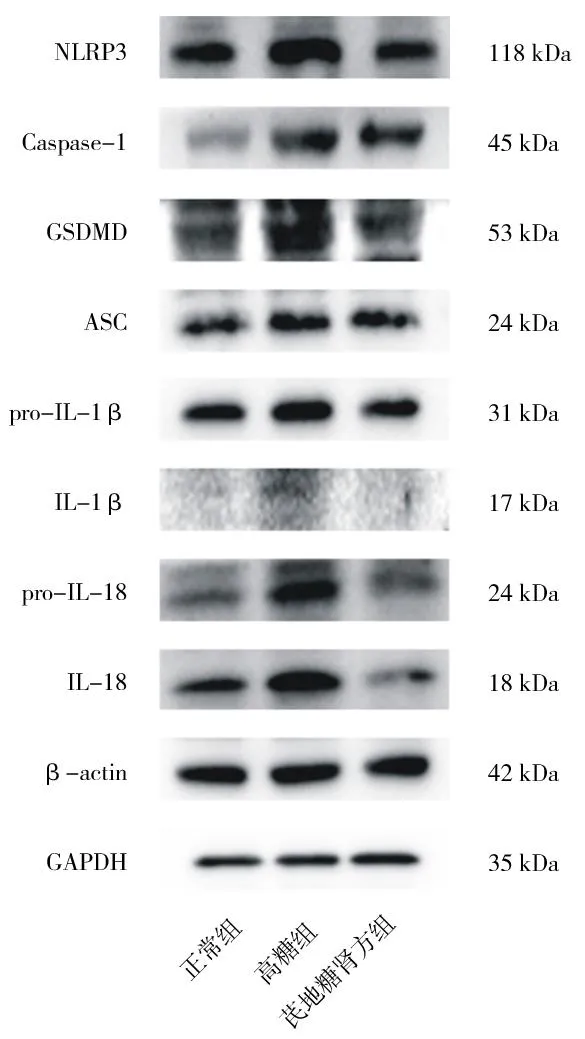
图3 正常组和高糖刺激各组肾小球内皮细胞中焦亡通路相关蛋白表达情况
3 讨 论
肾小球内皮细胞附着在肾小球毛细血管腔的内层表面,有独特的窗孔结构,其表面的糖萼层带有负电荷,二者构成内皮细胞的机械和电荷滤过屏障。肾小球内皮细胞通过肾小球基底膜与肾小球脏层上皮细胞(即足细胞)相连接,三者共同构成肾小球滤过屏障,是肾小球内执行滤过功能的第一道关卡,对维持肾小球滤过屏障的正常运作具有关键性作用[16-18]。高血糖首先引起肾小球内皮细胞损伤,窗孔结构破坏并伴随内皮糖萼层的减少,导致肾小球滤过屏障损伤,肾小球内皮细胞的通透性增加[19],且肾小球内皮细胞功能障碍可通过细胞间通讯作用进而导致肾小球基底膜及足细胞功能障碍,加速破坏肾小球滤过屏障,导致蛋白尿和肾功能损伤的持续加重[20]。另外高糖刺激能使肾小球内皮细胞内炎症小体激活,并触发Caspase-1主导的经典焦亡通路,从而加剧尿蛋白漏出及肾小球硬化的病理损伤[21]。焦亡是以细胞肿胀、质膜破裂及炎性因子释放为标志性特征的一种细胞死亡方式,NLRP3炎症小体是焦亡通路的重要启动子,向下可触发经典的Caspase-1依赖性级联反应,活化的Caspase-1进一步切割GSDMD蛋白及IL-1β、IL-18前体蛋白,导致IL-1β、IL-18等促炎因子的成熟及分泌,诱导细胞焦亡产生[22]。近年研究发现,肾小球内皮细胞损伤出现早于临床尿微量白蛋白的检出,其损伤是DKD的早期事件及有力的“幕后推手”,且焦亡通路激活是DKD早期常见的致病机制[23-25]。因此,针对肾小球内皮细胞的早期干预治疗可能是对抗DKD病程进展的有效手段。
柳红芳教授结合多年临证经验,受吕仁和教授“微型癥瘕”及仝小林教授“虚、瘀、浊”病机理论所启,提出DKD“精损络痹”的核心病机。“精损”即肾精亏虚,“络痹”即肾络痹阻[26]。精损与络痹互为因果,又相互影响,DKD时瘀热湿浊等邪可直接结聚,病久入脏,阻于肾络;肾精亏耗,肾气阴阳乏源亦可致痰瘀热浊等邪气滋生,兼之正虚无以抗邪,因虚致实,诸邪留滞胶结难去,郁闭络脉、阻截精窍,故成肾络痹阻之态。肾络痹阻则肾精之源布失其道,藏精之地充无所充,精愈亏而邪愈盛,形成愈实愈虚、愈虚愈实的恶性循环。肾络痹阻不仅直伤肾精,又劫生精之道,诸因互促加重肾精亏虚,由此见肾络痹阻是DKD的关键病机。基于DKD精损络痹的核心病机,柳红芳教授提出“填精通络”即填补肾精、祛邪通络的治疗原则,并据此法凝练出芪地糖肾方为代表方,该方临床效验明确且现已通过国家专利审批(专利号:ZL201711097315.2)。芪地糖肾方以熟地、生黄芪、山萸肉与炒芡实行填肾精、助肾用之功,扶正补虚,以补助通;以水蛭、熟大黄及白花蛇舌草共行泄热逐瘀、疏通肾络之功,祛邪安正,通络除痹;诸药并行,共奏填补肾精、通络除痹之效,使肾精充、正强以助除痹,使络痹通、邪祛以复精亏。
现代中医研究认为高糖刺激诱发细胞焦亡所引起的病理产物堆积与“络毒”学说具有高度一致性[27],DKD时肾小球内皮细胞中炎症因子累积与瘀热湿浊等邪结聚肾络,即与“络痹”的病理过程高度同步。本课题组前期研究显示,高糖刺激下足细胞内质网功能障碍,使原本应在足细胞内质网中加工合成的机体所需的精微物质生成障碍,被视作“精损”的病理过程[28]。现代研究发现,肾小球内皮细胞与足细胞存在密切的细胞间通讯机制,糖尿病阶段肾小球内皮细胞即出现病理性形态改变,DKD时肾小球内皮细胞损伤可进一步导致足细胞损伤的发生,而足细胞功能障碍又加剧肾小球内皮细胞损伤[29-30]。肾小球内皮细胞焦亡激活导致邪积络痹,不仅导致足细胞内精微物质生成障碍,直伤肾精;肾精亏耗,正虚难抗邪聚,因虚致实,足细胞功能障碍又加重肾小球内皮细胞损伤,正应精损与络痹互为因果又相互影响的过程。鬼笔环肽是从伞形毒蕈蘑菇中分离出来的毒素,可以特异性地与丝状肌动蛋白(F-actin)相结合,F-actin是细胞骨架的必备组分,可维持细胞的基本结构和生理功能。本实验通过鬼笔环肽染色观察芪地糖肾方对肾小球内皮细胞的保护作用,结果显示芪地糖肾方可明显改善高糖刺激后肾小球内皮细胞的细胞骨架受损状态,这与前期动物实验结果相一致[15]。焦亡通路相关蛋白表达情况显示,高糖诱导下肾小球内皮细胞焦亡通路被激活,而芪地糖肾方可通过抑制焦亡通路重要启动子,即NLRP3、ASC及Caspase-1前体蛋白组装成的炎症小体激活,进一步下调焦亡执行因子GSDMD蛋白表达水平,从而减少IL-1β、IL-18的成熟与分泌。提示逆转高糖影响下肾小球内皮细胞焦亡通路激活状态,可能是芪地糖肾方改善DKD肾小球内皮细胞损伤,对抗肾小球硬化病变的关键作用靶点。
综上所述,肾小球内皮细胞在高糖持续刺激下可触发NLRP3炎症小体并激活焦亡通路,促使炎症因子IL-1β、IL-18堆积,导致肾小球内皮细胞损伤,推进肾脏炎症、肾小球硬化进程;芪地糖肾方可通过抑制NLRP3/Caspase-1/GSDMD焦亡相关通路激活诱导的IL-1β、IL-18等促炎因子分泌,从而显著改善高糖刺激引起的肾小球内皮细胞损伤,进一步为芪地糖肾方的临床应用与推广提供了理论依据。但本研究仅从体外实验初步探讨验证相关结论,仍需深入研究以进一步完善其相关药理作用机制和靶点。
利益冲突:所有作者均声明不存在利益冲突。
