热毒宁注射液结合更昔洛韦治疗小儿呼吸道合胞病毒感染肺炎的疗效及对其血清炎性因子的影响
2024-03-19李强郝珉
李 强 郝 珉
(1.枣庄市薛城区人民医院儿科,山东 枣庄,277000;2.枣庄市立医院儿科,山东 枣庄,277100)
呼吸道合胞病毒感染肺炎通常是指呼吸道合胞病毒感染引起的呼吸系统病变,以儿童为主要病发群体。患儿初期症状以发热、憋喘、咳嗽、咳痰、喘鸣音为主,如未获得及时治疗,可导致患儿呼吸困难,严重者可发生心力衰竭,危及生命安全[1-2]。临床主要采取拍背吸痰、平喘等基础措施再配以药物进行治疗,其中常用药物为更昔洛韦,该药适用于巨细胞病毒感染,能够抑制病毒DNA多聚酶进入DNA,从而阻止病毒DNA的合成,减少病毒在人体的扩散,改善病毒引起的各项症状,但经过长久的实践发现,该药的临床疗效并不理想[3-4]。近年来,中西医结合的治疗方式逐渐成为研究热点,热毒宁注射液则是常被辅助用于病毒治疗的中药制剂,主要成分为栀子、青蒿与金银花,具有解毒散结、清热疏风之效[5-6]。目前关于热毒宁注射液联合更昔洛韦应用于呼吸道合胞病毒感染肺炎的研究报道较少,基于此,本研究旨在通过分组对照的方式探讨这两种药物的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2020年5月—2023年3月于枣庄市薛城区人民医院进行治疗的86例呼吸道合胞病毒感染肺炎患儿作为研究对象,按随机数表法分为对照组和观察组,各43例。对照组中男患儿22例,女患儿21例;年龄3~8岁,平均年龄(5.71±1.16)岁;病程1~4 d,平均病程(2.19±0.65)d;病毒亚型:A型25例,B型18例;发热程度:高热24例,中热19例。观察组中男患儿25例,女患儿18例,年龄3~9岁,平均年龄(5.65±1.20)岁;病程1~4 d,平均病程(2.23±0.60)d;病毒亚型:A型22例,B型21例;发热程度:高热21例,中热22例。两组患儿一般资料比较,差异无统计学意义(P>0.05),有可比性。本研究经枣庄市薛城区人民医院医学伦理委员会批准,患儿家属对本研究知情并签署同意书。
1.2 纳入与排除标准
纳入标准:①西医符合《诸福棠实用儿科学》(第8版)[7]中相关诊断标准;②中医符合《中医儿科学》[8]中肺炎喘嗽相关标准,证型为毒热闭肺型,高热面赤,咳嗽气喘,痰量多色黄,舌红,苔黄而干,脉数;③血清中均检出呼吸道合胞病毒特异性免疫球蛋白(M);④伴有发热、咳嗽、呼吸困难、咳痰、喘鸣音等症状。
排除标准:①伴有其他肺部疾病;②伴有免疫缺陷;③无沟通能力;④对本研究所用药物过敏。
1.3 方法
入院后,两组患儿均接受相关检查,并给予其吸痰、止咳、平喘等基本治疗措施。对照组在此治疗基础上采取更昔洛韦注射液(生产企业:福安药业集团庆余堂制药有限公司,国药准字H20050578,规格:10 mL∶25 g)治疗,取5 mg/kg更昔洛韦混合于100 mL的5%葡萄糖注射液,静脉滴注,滴注时间需超过1 h,1次/d。观察组在对照组基础上以热毒宁注射液(生产企业:江苏康缘药业股份有限公司,国药准字Z20050217,规格:10 mL)治疗,取0.8 mL/kg热毒宁混合于100 mL的10%葡萄糖注射液,静脉滴注,滴注时间需超过1 h,1次/d。两组用药7 d。
1.4 观察指标
(1)临床疗效。治疗后,患者体温恢复正常,呼吸道合胞病毒检测为阴性,胸片检查显示正常,其他症状基本消失,即为显效;治疗后,患者体温明显消退,其他症状得到缓解,呼吸道合胞病毒检测为阴性,即为有效;治疗后,患者症状无明显变化,呼吸道合胞病毒检测阳性,即为无效。总有效率=(显效+有效)例数/总例数×100%。(2)临床症状消退时间。包括发热、呼吸困难、喘鸣音、咳嗽等症状消退时间。(3)血清炎性因子水平。于治疗前后,取患儿静脉血3 mL,并用全自动生化分析仪(生产企业:深圳市凯特生物医疗电子科技有限公司,粤械准字20122400817,型号:KB-120)检测血清中白细胞介素-6(IL-6)、白细胞介素-1(IL-1)及肿瘤坏死因子α(TNF-α)水平。(4)免疫学指标。于治疗前后,取患儿静脉血3 mL,通过免疫荧光法测定T细胞亚群(CD3+、CD4+、CD8+)及B细胞水平。(5)血气分析指标。于治疗前后采用血气分析仪(生产企业:美国沃芬公司,国械注进20192220141,型号:GEM Premier 5 000)检测两组患儿酸碱度(pH)、动脉二氧化碳分压(PaCO2)和动脉氧分压(PaO2)。(6)不良反应发生情况。记录用药期间出现胃肠道不适、皮疹、白细胞降低等情况。不良反应发生率=(胃肠道不适+皮疹+白细胞降低)例数/总例数×100%。
1.4 统计学分析
采用SPSS 20.0统计学软件分析数据,计量资料 以(±s)表示,符合正态分布,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以[n(%)]表示,用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效比较
观察组总有效率高于对照组,差异有统计学意义(P<0.05),见表1。

表1 临床疗效比较 [n(%)]
2.2 临床症状消退时间
观察组各项症状消退时间均短于对照组,差异有统计学意义(P<0.05),见表2。
表2 临床症状消退时间比较 (±s,d)
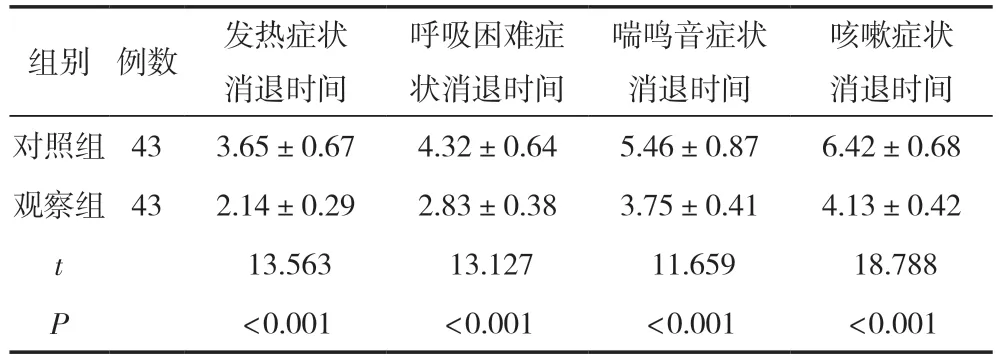
表2 临床症状消退时间比较 (±s,d)
咳嗽症状消退时间对照组433.65±0.674.32±0.645.46±0.876.42±0.68观察组432.14±0.292.83±0.383.75±0.414.13±0.42 t 13.563 13.127 11.659 18.788 P<0.001<0.001<0.001<0.001组别例数发热症状消退时间呼吸困难症状消退时间喘鸣音症状消退时间
2.3 血清炎性因子水平比较
治疗前,两组血清炎性因子水平比较,差异无统计学意义(P>0.05);治疗后,两组IL-6、IL-1、TNF-α水平均降低,且观察组低于对照组,差异有统计学意义(P<0.05),见表3。
表3 血清炎性因子水平比较 (±s)
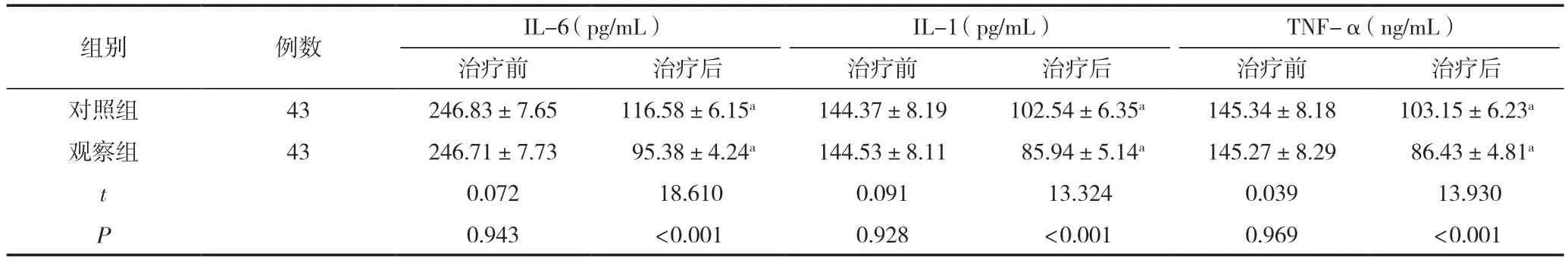
表3 血清炎性因子水平比较 (±s)
注:与同组治疗前比较,aP<0.05。
TNF-α(ng/mL)治疗前治疗后治疗前治疗后治疗前治疗后对照组43246.83±7.65116.58±6.15a144.37±8.19102.54±6.35a145.34±8.18103.15±6.23a观察组43246.71±7.73 95.38±4.24a144.53±8.11 85.94±5.14a145.27±8.29 86.43±4.81a t 0.072 18.6100.091 13.3240.039 13.930 P 0.943<0.0010.928<0.0010.969<0.001组别例数IL-6(pg/mL)IL-1(pg/mL)
2.4 免疫学指标比较
治疗前,两组患儿免疫学指标比较,差异无统计学意义(P>0.05);治疗后,两组患儿CD3+、CD4+均上升,CD8+、B细胞均降低,且观察组CD3+、CD4+高于对照组,CD8+、B细胞低于对照组,差异有统计学意义(P<0.05),见表4。
表4 免疫学指标比较 (±s,%)

表4 免疫学指标比较 (±s,%)
注:与同组治疗前比较,aP<0.05。
B细胞治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后对照组4358.19±4.1961.12±6.14a36.14±2.5740.28±3.64a35.78±3.4630.64±2.73a16.28±1.1313.27±0.84a观察组4358.43±4.2567.26±7.28a36.37±2.4946.21±4.26a35.95±3.4124.53±1.84a16.34±1.2010.15±0.62a t 0.264 4.2280.422 6.9400.230 12.1700.239 19.596 P 0.793<0.0010.675<0.0010.819<0.0010.812<0.001组别例数CD3+CD4+CD8+
2.5 血气分析指标比较
治疗前,两组患儿血气分析比较,差异无统计学意义(P>0.05);治疗后,两组患儿pH、PaO2均上升,PaCO2均降低,且观察组pH、PaO2高于对照组,PaCO2低于对照组,差异有统计学意义(P<0.05),见表5。
表5 血气分析指标比较 (±s)
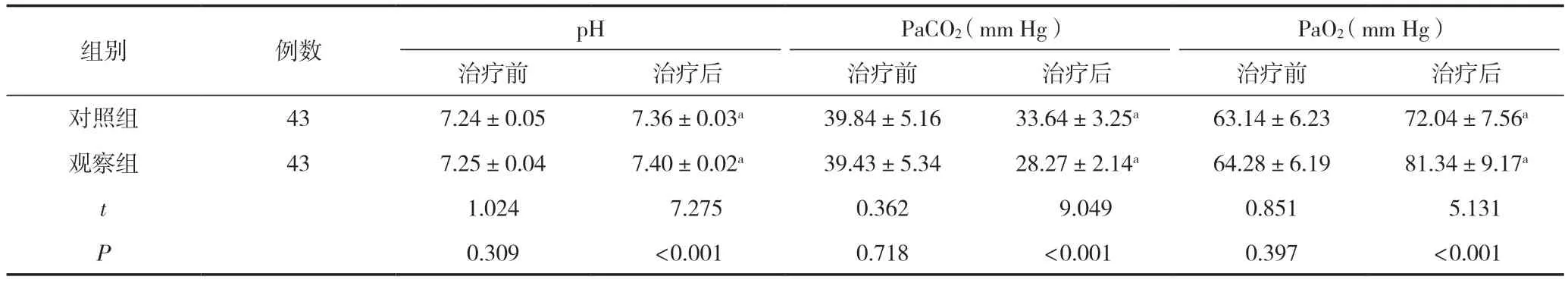
表5 血气分析指标比较 (±s)
注:与同组治疗前比较,aP<0.05;1 mm Hg≈0.133 kPa。
PaO2(mm Hg)治疗前治疗后治疗前治疗后治疗前治疗后对照组437.24±0.057.36±0.03a39.84±5.1633.64±3.25a63.14±6.2372.04±7.56a观察组437.25±0.047.40±0.02a39.43±5.3428.27±2.14a64.28±6.1981.34±9.17a t 1.024 7.2750.362 9.0490.851 5.131 P 0.309<0.0010.718<0.0010.397<0.001组别例数pH PaCO2(mm Hg)
2.6 不良反应发生情况比较
对照组出现3例(6.98%)胃肠道不适,2例(4.65%)皮疹,2例(4.65%)白细胞降低,不良反应总发生率为16.28%(7/43);观察组出现2例(4.65%)胃肠道不适,1例(2.33%)皮疹,2例(4.65%)白细胞降低,不良反应总发生率为11.63%(5/43)。两组不良反应比较,差异无统计学意义(P>0.05)。
3 讨论
肺炎是导致5岁及以下幼儿死亡的主要因素之一。由于儿童机体尚未完全发育,加上免疫力低下等因素,极易受到外界病原菌侵袭,从而引发感染,尤其是呼吸道感染,而其中常见的病原菌则是呼吸道合胞病毒,严重威胁患儿生命健康[9-10]。呼吸道合胞病毒进入机体后能够诱导抗体产生,进而引起T细胞亚群动态失衡,并促使机体释放细胞炎性因子,最终诱发炎性反应[11]。因此,临床治疗呼吸道合胞病毒感染肺炎,不仅要抑制体内病毒的复制,还应减少炎性反应,改善机体的免疫力。
更昔洛韦在临床属于广谱类抗病毒药物,将其用于呼吸道合胞病毒感染肺炎,其可竞争性地抑制病毒DNA与脱氧鸟苷的三价磷酸盐结合,继而导致病毒DNA延长的停止[12]。且更昔洛韦经静脉滴注后在被感染细胞内的浓度要高于未感染细胞,可加强抗病毒作用,但其治疗重点在于抗病毒,对病毒具有高度选择性,对患儿免疫力的改善无明显效果[13]。近年来,药物配伍使用的观念逐渐得到认可,因此可考虑将更昔洛韦与其他药物共同使用,以增强疗效。IL-6与IL-1均属于细胞因子,参与人体炎性反应,机体受到感染时可显著升高;TNF-α是主要的炎性介质,参与人体急性反应的调控。CD3+、CD4+、CD8+是T淋巴细胞的组成部分,其可评估免疫细胞数量的异常,并能直观反映机体免疫情况;B细胞是常在体液中发挥免疫功能的免疫细胞。血气分析可反映肺功能,是临床检验多种呼吸道疾病的指标,呼吸道合胞病毒感染机体后可影响肺部通换气,而pH、PaCO2、PaO2等指标能够精准评价肺部气体交换情况。本研究结果显示,观察组有效率高于对照组,各项临床症状消退时间短于对照组,IL-6、IL-1、TNF-α等炎性因子水平低于对照组,CD3+、CD4+高于对照组,CD8+、B细胞低于对照组,pH、PaO2高于对照组,PaCO2低于对照组,两组不良反应均较少,表明热毒宁注射液与更昔洛韦联合用药,可有效缓解临床症状,抑制炎性反应,提高免疫力,并改善患儿肺部通换气情况,且安全性良好。传统医学认为,呼吸道合胞病毒感染肺炎属于“肺热病”范畴,认为其由风热自口鼻侵入,内犯于肺,且邪气在肺部郁闭,继而出现痰热互结、毒热闭肺等征象,治疗宜以清热解毒为主[14]。热毒宁注射液主要成分为栀子、青蒿、金银花等中药,其中栀子性寒,归心肺经,主治热病、咽痛,具有清热利湿、泻火除烦、凉血解毒之效;青蒿性寒,善治暑热、阴虚发热,具有祛暑透热、凉血除蒸之效;金银花主治咳喘及感染性疾病,具有清热解毒、疏风散热之功,诸药合奏清热解表、解毒凉血之功效[15]。现代药理研究表明[16],栀子中含有的熊果酸、栀子苷等生物成分均具有抗感染作用,保护细胞的完整性,降低病毒对细胞的侵害,继而减轻炎性反应;青蒿中的青蒿素能够有效抑制体内抗体的生成,调节辅助T淋巴细胞-1(Th1)/辅助T淋巴细胞-2(Th2)细胞分化,提高淋巴细胞的转化率,从而增强人体免疫力;金银花含有的环烯醚萜苷、有机酸等成分,能够抑制多种致病菌,同时具有免疫抑制活性,在体外减弱呼吸道合胞病毒的侵袭能力。将热毒宁注射液联合更昔洛韦治疗,不仅在体内抑制病毒DNA复制,消除炎性反应,提高免疫力,还可在体外减弱减弱呼吸道合胞病毒对人体的侵袭,进一步降低病毒对人体的危害。
综上所述,将热毒宁注射液与更昔洛韦联合用药,可有效消除呼吸道合胞病毒感染肺炎患儿症状,抑制炎性因子生成,增强免疫功能,并改善患儿肺部通换气情况,安全性较高,临床优势明显。
