人工智能在睑板腺功能障碍相关干眼中的应用现状及进展
2024-03-15韩亚波综述易全勇审校
韩亚波 综述 易全勇 审校
1宁波大学医学院附属阳明医院,宁波 315040;2宁波市眼科医院,宁波 315040
睑板腺功能障碍(meibomian gland dysfunction,MGD)是蒸发过强型干眼的主要原因,也是眼科常见病[1]。MGD相关干眼可对人们的生活质量产生影响,并可能造成直接或间接公共卫生成本升高以及个人经济负担加重。快速、准确的诊断可以免除不必要的费用及过度治疗引起的潜在不良反应。睑缘和睑板腺开口异常、睑酯分泌异常出现任意一种体征再结合眼部症状可诊断为MGD[2]。由于MGD相关干眼患者症状常表现各异,甚至症状体征分离,因此临床上常联合使用多项测试,包括泪膜破裂时间(tear break-up time,TBUT)、泪腺分泌测试、泪液渗透压和泪河高度、眼表染色、角膜敏感性、瞬目频率、角膜地形图、干涉测量和裂隙灯显微镜图像、红外睑板腺成像技术、活体共聚焦显微镜(invivoconfocal microscopy,IVCM)、问卷记录等[3],这些测试需要在临床上投入大量的时间和资源。人工智能(artificial intelligence,AI)利用机器学习(machine learning,ML)和深度学习(deep learning,DL)技术在医疗领域获得广泛的应用[4]。ML是在算法的基础上,学习大量的历史数据,从而得出预测模型及对应结果[5]。ML包括:(1)监督学习 监督学习算法可以执行回归和分类,其中回归涉及预测数据实例的数值,而分类涉及将数据实例分配给预定义的类别。(2)无监督学习 无监督学习包括聚类算法和降维算法,这种类型的ML通常用于将观察结果分组在一起,检测输入变量之间的关系,以及降维。(3)强化学习 DL是ML研究的一个新领域,很多结构模型都曾应用于医学影像的研究,如卷积神经网络(convolutional neural network,CNN)、栈式自编码器、受限玻尔兹曼机、深度信念网络等[6-7](图1)。基于DL的影像模型可以提高检查的准确性并节省时间,可用于MGD的临床辅助诊断和筛查[8]。AI在眼部疾病中的应用较多,包括糖尿病视网膜病变的筛查、年龄相关性黄斑变性的检测、青光眼和早产儿视网膜病变的诊断等[7,9-11]。AI辅助诊断、评估、随访MGD可节省大量的时间和资源成本,具有重要价值。本文就AI在MGD相关干眼中的应用现状及进展进行综述。
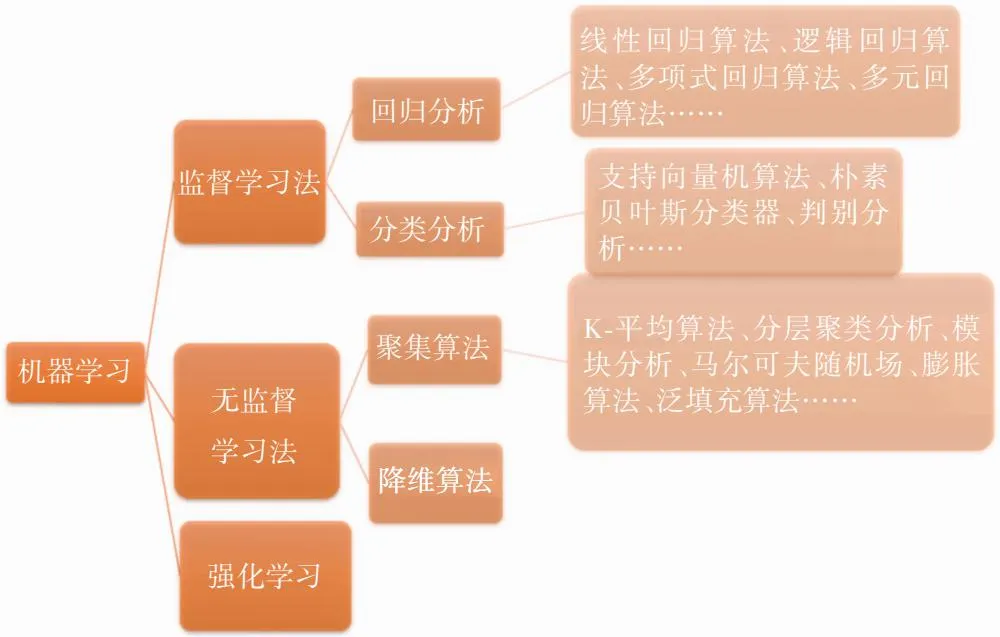
图1 ML具体算法
1 AI技术联合TBUT在MGD相关干眼中的应用
TBUT越短,泪膜越不稳定,发生干眼的概率就越高。TBUT影像中的干燥区域和TBUT可以使用ML来估测[12-14]。与验光师的评估结果相比,利用莱文伯格-马夸特算法探测干燥区域的准确率达到91%[12]。应用马尔可夫随机场,根据视频中泪膜形态的立体变化同时结合多图切割算法来标记估测TBUT,可清晰直观地显示泪膜干燥度随着时间的延长而增加,演算结果较临床医生评估相差2.34 s[14],并充分体现了该算法的可靠性和稳定性。多项式函数也被用来确定干燥区,并在估测TBUT之前对阈值进行微调。基于特异性和敏感性标准,该方法与4位专家的手工测量值进行分析比较,发现90%以上的测量值偏离在±2.5 s的范围内[13]。总之,这些研究表明,与专家相比,使用自动方法获得的TBUT值在可接受范围内。但目前所做研究仅包含少量研究对象,仍需进一步研究来验证相关结果。
2 AI技术联合干涉测量和裂隙灯显微镜图像在MGD相关干眼中的应用
干涉技术是一种高效实用的工具,可以提供泪膜脂质层状态的快照,帮助MGD相关干眼的诊断。ML系统已应用于干涉测量和裂隙灯显微镜图像中,根据睑脂形态进行睑脂分类、脂质层厚度估计、眼红分析和泪河高度的测量[15-24]。
干眼的诊断可以基于以下泪膜的形态特征,如开放网格、闭合网格、波浪、无定形和彩色条纹,大多数研究通过这些特性来使用ML自动分类干涉仪脂质层图像。Remeseiro等[15-16]发现了用于最终分类的各种支持向量机(support vector machine,SVM)模型。使用SVM可分析泪膜脂质干涉仪图像[25]。由于泪膜向上运动的不足,过量的脂质可能聚集在角膜表面的下侧。因此,当由于脂质成分分泌过多和/或水成分不足等条件导致平衡失调时,干涉条纹将呈现出多彩而复杂的外观,从图像中提取的特征被传递到SVM模型,SVM模型将图像分类为健康、水液缺乏型干眼或蒸发过强型干眼。该模型与经验丰富的眼科医生之间的一致性很高,报告的Kappa值为0.82。一个简单的神经网络以96%的精度取得了整体最佳的性能。但是,由于该模型采用留一交叉验证,可能对训练数据拟合过度[26]。da Cruz等[18-19]比较了SVM、随机森林、朴素贝叶斯、多层感知器、随机树和径向基函数网络算法6种不同的ML模型,发现无论采用何种预处理步骤,随机森林都是最好的分类器,获得了高于99%的准确率,标准偏差为0.843%,受试者工作特征曲线下面积为0.999,Kappa值为0.995。在图像预处理阶段研究发现应用Ripley K函数取得了最佳性能,并且Greedy Stepwise技术与ML模型可以同时用于特征选择[19]。由于所有模型都是通过交叉验证来评估的,因此在临床常规使用之前,系统应该在新图像上进行外部评估。
Hwang等[20]研究了泪膜脂质层厚度能否用于区分MGD严重程度。该研究利用ML方法对Lipiscanner眼表分析仪和裂隙灯显微镜影像的厚度进行估算,通过对图像进行预处理,并采用泛光填充算法和canny边缘检测从瞳孔中定位和提取虹膜,发现2种MGD严重程度组间差异有统计学意义,提示该技术可用于MGD的评估。眼表泪膜分析仪也可用于测定泪膜脂质层厚度,通过眼表泪膜分析仪可观察眼表的白光和流动脂质泪膜的干涉颜色,并聚焦于受试者的脂质胶片获得合格的干涉图像,图像分为分割和未分割图像。Fu等[21]采用ImageJ处理图像来确定脂质层厚度,发现估计的泪膜脂质层厚度具有很好的重复性;利用广义线性模型对2种不同的图像分析方法进行比较,发现2种技术之间存在较高的相关性。该研究结果表明,通过对未分割图像分析足以评价泪膜脂质层厚度,但该研究仅纳入了28个研究对象,有待扩大样本量进一步验证。
眼红是干眼的一个重要指标。Rodriguez等[22]进行的回顾性研究描述了用于评估与干眼相关的眼红的自动匹配系统。该研究对26例有干眼病史的受试者采集裂隙灯显微镜图像,采用Sobel算子提取代表眼红强度和水平血管成分的特征,基于提取的特征,训练多元线性回归模型来预测眼红,该系统达到了100%的准确度。
泪河包含75%~90%的泪液,泪河高度可作为蒸发过强型干眼的定量指标。Yang等[23]将新的自动识别软件与ImageJ预测的泪河高度进行比较,结果显示二者相似,两者之间的相关性很高,相关系数为0.626~0.847,显示出较高的准确性和有效性,表明该自动泪河高度测量平台有可能成为干眼筛查和随访的有效工具。
3 AI技术联合IVCM在MGD相关干眼中的应用
近年来的研究发现,IVCM可以在活体内观察睑板腺的微观形态[27-28],且可用于研究MGD的病理生理过程,对MGD的诊断具有重要意义。梁庆丰等[29]采用IVCM观察结果显示,MGD患者睑板腺开口形状不规则、睑板腺腺泡囊样扩张或萎缩、腺泡间炎症细胞浸润及纤维化改变,对MGD的诊断具有潜在的应用价值。高分辨率IVCM图像可用于评估阻塞性MGD[30]。使用五折交叉验证对9个不同CNN的组合进行训练并在图像上进行测试,将模型分类与3位眼睑专家的诊断进行比较,结果显示VGG16、DenseNet-169、DenseNet-201、InceptionV3 4种不同模型组合效果最好,曲线下面积、灵敏度和特异性均较高,分别为0.981、92.1%和98.8%,表明该模型可以用来区分健康的睑板腺图像和阻塞性MGD图像,具有很高的准确性,未来可以对患者进行自动阻塞性MGD诊断。CNN的优点是不需要在分析之前从图像中提取特征,由模型自动执行即可。虽然使用ML来解释IVCM图像的结果很有前景,但仍需更大规模的临床研究来验证这些结果。
4 AI技术联合睑板腺成像技术在MGD相关干眼中的应用
睑板腺成像是诊断MGD的常用技术[31]。在评估图像时,重要的是将像素区分为3类,即属于腺体、腺体间区域(即没有腺体的健康组织)和组织丢失区域。Koh等[32]针对从图像中提取的特征训练SVM,预处理包括图像灰度转换、中值滤波、去除不均匀光照和归一化,结果显示模型的敏感性为0.979,特异性为0.961。然而,与其他图像分析方法相比,该方法在图像传递到系统之前需要手动操作。将大津(Otsu)方法与骨架化和分水岭算法相结合,可以自动量化睑板腺,该方法比眼科医生的诊断速度更快,灵敏度为0.993,特异性为0.975[33]。Xiao等[34]先后应用Prewitt算子、Graham扫描、碎片化和骨架化算法进行图像分析以量化睑板腺腺体,模型预测结果与眼科医生的一致性较高,Kappa值大于0.8,假阳性率低(<0.06),假阴性率为0.19,提示该方法遗漏了部分腺体,但同时由于样本量小使研究结果可信度欠佳。另一项研究采用Sobel算子、多项式函数、碎片化算法和Otsu方法对MGD的严重程度进行自动分级,虽然该方法速度更快,但结果与临床医生的评估结果明显不同,需要进一步的临床研究验证[35]。
Wang等[36]采用SqueezeNet、resnet 18、resnet 34、resnet 50 4种不同的CNN算法来测定睑板腺萎缩,结果显示resnet50在评价数据集上具有最佳的算法性能。CNN可以用来识别睑板腺萎缩的区域,并在一组图像中估计萎缩的百分比,同时具有高精度、可重复性和低可变性,在很大程度上优于临床医生。在国内一项应用Mask RCNN构建模型的临床研究中,模型评价每幅图像仅需0.499 s,与临床医师的评估结果无显著差异,可用于MGD相关疾病的临床辅助诊断和筛查[7]。Yeh等[37]开发了一种评估睑板腺萎缩的方法,在应用K-nearest neighbors模型分配睑板评分之前,使用一种特殊类型的无监督CNN从睑板图像中提取特征,该系统达到了80.9%的准确性,优于临床团队的评估。此外,提取的CNN特征的层次聚类可以显示睑板腺图像之间的关系。Khan等[38]使用GAN结构对睑板腺的红外3D图像进行测试,以评估MGD,模型输出与真实标签比较结果显示,其性能得分优于现有的分割方法,新自动化方法与2名临床医生的相关系数分别为0.962和0.968。
5 AI技术联合蛋白质组学分析在MGD诊断中的应用
Grus等[39]报道了结合判别分析检测最重要的蛋白质和深度神经网络进行分类的方法,结果显示其有较高的准确性、敏感性和特异性。Gonzlez等[40]也采用判别分析方法对泪液蛋白质组进行了分析,该研究选取最重要的蛋白质检测人工神经网络,将泪液样本分类为水液缺乏型干眼、MGD和健康对照,结果显示该模型总体精度为89.3%;主成分分析显示,健康对照、水液缺乏型干眼和MGD数据点分离良好,表明蛋白质是分类这3种对象的良好候选者,该系统达到了所有已综述的蛋白质组学研究的较高准确率。
6 展望
鉴于我国人口老龄化和医疗保健支出比例的不断增加,改善人口的总体健康状况、降低医疗费用和改善患者就医体验成为目前医疗卫生建设的主要目标。AI是解决这些问题有潜力的解决方案之一,可能会给我们的生活方式和医疗模式带来革命性的改变。尽管目前要在医疗领域增加AI的应用还有不少亟待攻克的问题,如模型开发和评估的执行、不同模型间的比较、不同类型绩效分数的比较等,但仍可能会在未来几十年迅速改变这一领域。此外,数据和代码共享的缺失使得结果具有不可重复性。因此,未来重点应该放在建立数据和代码共享作为一个标准程序上。总之,在模型开发、临床测试和标准化方面还有很多工作要做,不同研究ML模型的结果表明其很有潜力。AI在与MGD相关干眼的许多不同应用中均有很大潜力,包括MGD自动检测和分类、MGD相关干眼的病因和危险因素研究,以及潜在的生物标志物检测。应当努力为模型开发过程,特别是模型评价,制定共同的指导方针。
利益冲突所有作者均声明不存在任何利益冲突
