基于分子模拟技术筛选具有潜在治疗非小细胞肺癌的ROS1激酶抑制化合物
2024-03-15刘飞远梁佳龙孙智勇陈伟刘建青
刘飞远 梁佳龙,2 孙智勇△ 陈伟 刘建青
(1.中国人民解放军陆军第946医院,新疆 伊宁 835000;2.空军军医大学药学院,陕西 西安 710032;3.包头师范学院生物科学与技术学院,内蒙古 包头 014030)
受体酪氨酸激酶的胰岛素受体家族是一个庞大的家族,其中肉瘤致癌因子c-ros(ROS proto-oncogene 1,ROS1)是家族成员之一,该因子参与调节细胞的存活、细胞分化、细胞转化、细胞增殖、细胞迁移和细胞凋亡等生命各个过程。不但在非小细胞肺癌(non-small cell lung cancer, NSCLC)中发现ros1基因重排可以使ROS1激酶被持续激活,从而使ros1基因陆续在直肠癌、卵巢癌、胃癌、胆管癌等恶性肿瘤中发现重排,最终使RAS/MAPK、JAK/STAT、PI3K/AKT 等多种信号通路受到干扰,导致肿瘤发生。因此,ROS1激酶已经被确定为肿瘤治疗的重要靶点[1]。本文旨在通过分子模拟方法筛选出能够抑制ROS1的先导化合物。
1 材料与方法
1.1 数据来源波士顿塔夫茨大学医学院Al Charest[2]课题组的研究表明,PF-06463922 是最有效和最具选择性的新一代小分子ROS1抑制剂。文中详细阐述了两者之间的结合作用模式,其中的小分子抑制剂见图1。在RCSB PDB蛋白质数据库中,该化合物与ROS1激酶的复合物晶体结构编号为4UXL。
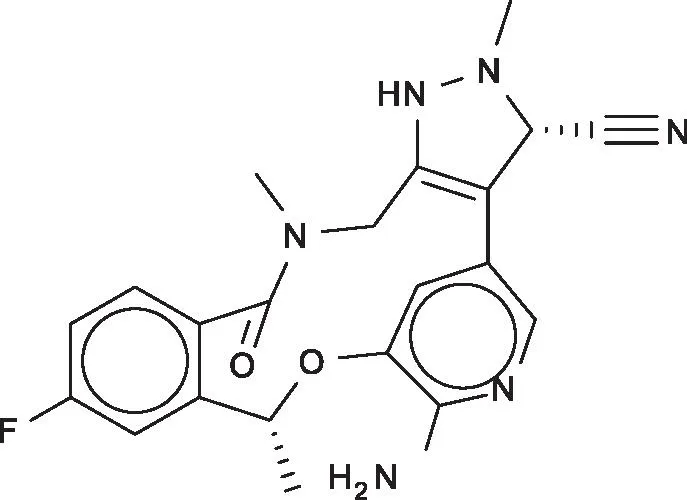
图1 PF-06463922
1.2 实验条件分子模拟实验在联想P920塔式工作站上进行,该服务器搭载双路英特尔至强5218CPU、英伟达P5000计算加速卡、内存配备128G、Windows10操作系统,分子模拟实验在Discovery Studio 3.5中进行。
1.3 构建药效团模型T.M.Kumar等[3]的研究阐明[3],药效团模型具有良好的筛选准确性和药物制备性,在众多药效团模型构建方法中,本研究采用了当前主流的药效团模型构建方法,即基于配体和受体相互作用的药效团模型。解析4UXL中ROS1融合蛋白与PF-06463922之间的相互作用,构建配体—受体的药效团模型,用于后续的先导化合物筛选。
1.4 虚拟筛选使用Discovery Studio3.5-build 3D database工具进行虚拟筛选。实验以加州大学旧金山分校药化系设计、更新的ZINC15数据库为基础,该数据库是全球最大的化合物数据库[4],被各大药物研发机构用于虚拟筛选[5]。本课题组选用可购买的全部化合物数据库,用于构建药效团模型,并进行虚拟筛选。
1.5 分子对接本课题组通过对4UXL晶体复合物结构中PF-06463922小分子抑制剂与受体蛋白之间进行对接预实验,分别对Discovery Studio3.5软件中的CDOCKER、Libdock、Ligandfit三种对接方法进行了可靠性验证[6-7]。
1.6 分子动力学模拟[8]该方法可有效反映配体药物分子与受体靶蛋白之间的关系[9-10],从而以最佳对接构象当做起始状态,使用Discovery Studio3.5软件中的solvation计算方法,溶剂化的初始条件是以对接结果最佳的化合物和受体蛋白间的结合作用模式为标准。使用标准动力学流注算法(SDC算法)进行分子动力学模拟,基准温度为300K,恒温恒压,时间间隔2fs,持续时间500 ps[11-12]。
2 结 果
2.1 PF-06463922与ROS1激酶相互作用模式和药效团模型本研究将4UXL晶体结构进行解析可知PF-06463922与ROS1激酶之间形成的多种相互作用关系,其三维结构见图2。PF-06463922下端的氨基基团与Glu2027形成了一组氢键相互作用,距离为1.97 Å;杂环与Met2029形成了两组氢键,距离分别为1.97 Å、2.19 Å;远端杂环上的N与Glu2030形成了一组氢键,距离为2.60 Å;上端甲基基团与Leu1951形成了一组氢键,距离为2.96 Å。以该结构中PF-06463922与ROS1激酶之间的相互作用模式,构建出1种药效团模型,其结构如图3所示。其中包含,合计4个药效团模型特点。
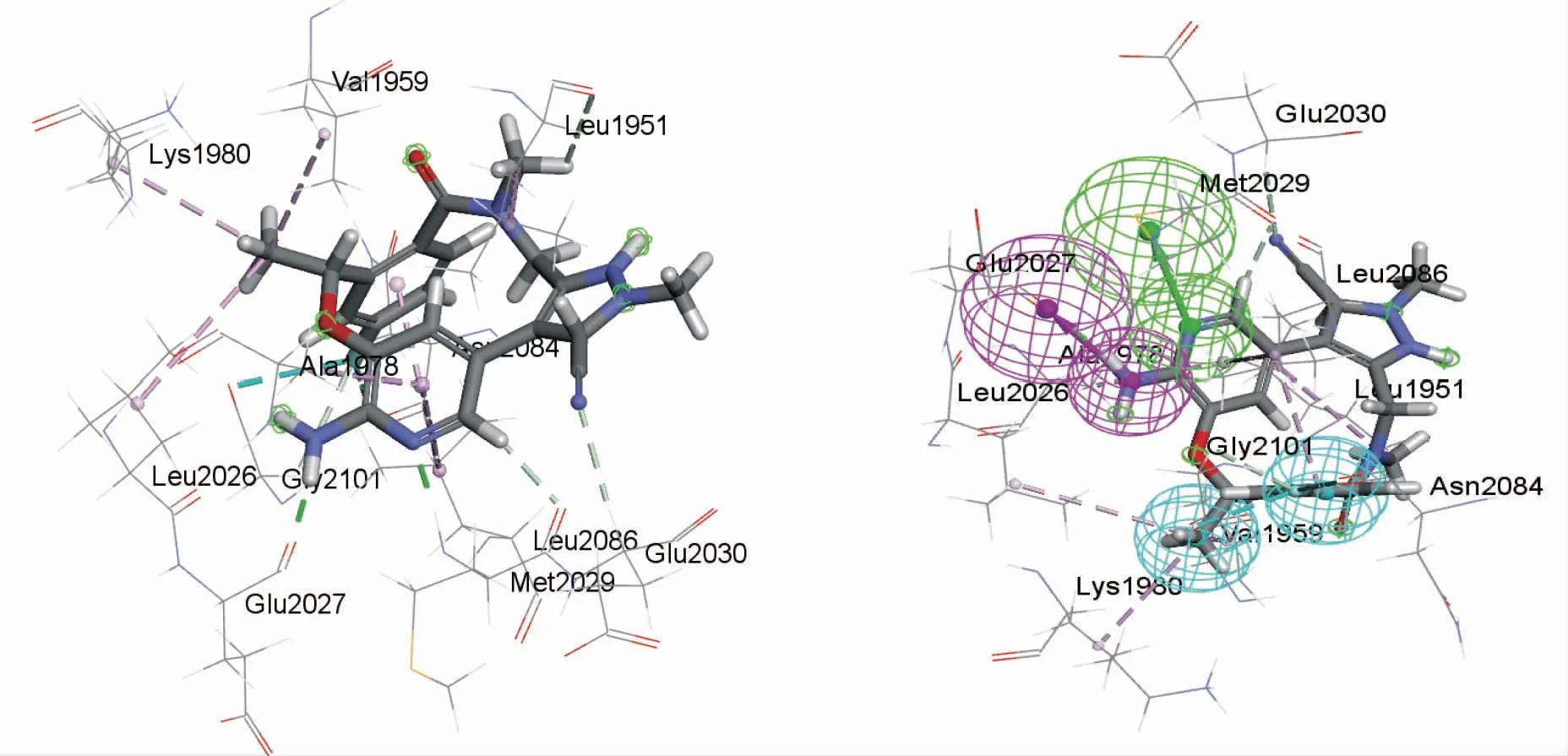
图2 PF-06463922与ROS1激酶相互作用结构 图3 PF-06463922与ROS1激酶药效团模型
2.2 基于虚拟筛选的结果共得到符合药效团模型的化合物611 0340个,再以药效团打分分数自高向低排序,选择得分前100名的化合物。
2.3 分子对接方法评估与对接结果选用重现4UXL复合物中配体受体结合作用模式最优的CDOCKER的对接方法,将表1中的化合物逐一与4UXL受体蛋白进行对接。对接结果发现:75号化合物在打分函数最高的前10个构象之中占了8个,得分最高构象见图4。该化合物上端杂环与Arg2083、Asn2084、Asp2102形成了五组氢键,距离分别为2.66 Å、2.91 Å、2.29 Å、2.53 Å、2.77 Å;近端的O与Lys1980形成了一组氢键,距离为2.43 Å;下端与Gly2101形成了一组氢键,距离为2.59 Å;上端的O与Gly2032、Asp2033号形成两组氢键,距离分别是2.88 Å、2.94 Å;上端杂环与Asp2102形成了一组盐桥,距离为2.05 Å。
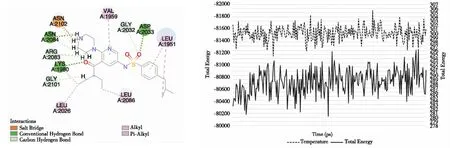
图4 化合物ZINC000065025270与ROS1激酶相互作用结构 图5 分子动力学温度能量图
2.4 分子动力学模拟结果在500 ps的全过程过程中,75号化合物与4UXL蛋白结合态的整体能量在-80,156.10~-81,259.50 kcal/mol间波动,体系温度在294.623~305.527 K间波动,模拟过程中温度、体系能量波动见图5。可发现含297个氨基酸受体蛋白与75号化合物结合能量波动较小,说明该模拟所确定的初始状态相对稳定。受体蛋白的各氨基酸残基均方根涨落(RMSF)值见图6。RMSF值较小,说明结合作用是稳定的,动力学模拟的500 ps期间,活性袋中化合物75呈现稳定状态,各帧构象中化合物75母核结构与受体蛋白之间结合作用模式稳定,整体RMSD在5 Å以内,可见化合物75与4UXL之间的结合作用模式是稳定可靠的(图7)。
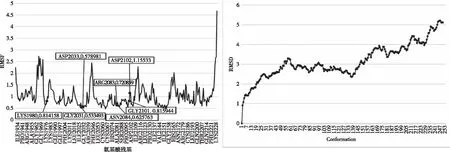
图6 受体蛋白各氨基酸残基均方根涨落(RMSF)图 图7 受体蛋白均方根偏差(RMSD)图
3 讨 论
肺癌是常见致病、致命癌症之一,在我国非小细胞肺癌在肺癌中最为常见,约占发病的80%~85%[13],近年来,非小细胞肺癌主要以靶向药物吉非替尼为主要治疗手段,但该类药物的靶基因主要针对的是EGFR和ALK,一旦产生了耐药性或基因发生了突变,靶向药物的治疗效果也将大打折扣,因此亟待找到一种可能代替吉非替尼的新型药物, ROS1相对于EGFR和ALK的阳性率较低,但它可为肺癌患者的靶向治疗提供新的靶点,且迅速成为研究热点[14]。
课题组通过实验得到的75号化合物可能是潜在的ROS1抑制剂,但受限于实验环境,目前仅进行了分子模拟的实验,亟需进一步的生物活性实验验证。如可对ROS1进行定点氨基酸突变:对4UXL蛋白进行定点突变,对Lys1980、Gly2032、Asp2033、Arg2083、Asn2084、Gly2101、Asp2102等氨基酸进行定点突变,观测突变前后75号化合物与受体蛋白之间的亲和力变化,通过复合物晶体结构的电泳实验进行衡量:如结合较好,则复合物较重,反之则较轻。
虽然75号化合物在对接结果、分子动力学模拟等方面都展现出了其在抑制ROS1活性方面可能具有一定的效果,但这种结果仅仅是基于计算机模拟的结果,到底是否具有药理活性,还需要进行包括动物实验在内的大量后续研究来进行验证,新型抗癌药物的研发需要长期不懈的研究,往往花费巨大,耗时漫长,本研究最大的意义在于尝试利用计算机的辅助筛选技术来寻找新药,从而达到降低研究时间和成本,提高新药发现的概率的目的。特别需要指出的是,本研究的结果不是盲目的,是基于药效团模型的理性设计,尤其是随着学术界对ROS1的蛋白质晶体结构的深入广泛研究,在一定程度上为我们发现并精准筛选的ROS1抑制剂化合物方面提供了保证。
化合物75的分子量约为473.26,具有良好的成药性,但其结构之中具有季铵盐的结构特征,极性较大易溶于水,且其结构之中包含两个容易水解的结构,化合物在体液内的稳定性还有待进一步的研究和确认。接下来的活性验证可着重对其稳定性进行理性设计和改造。
对于ROS1抑制剂的研究,本课题组在现有基础上,下一步将对得到的75号化合物开展更加深入的理论研究,如:如分子轨道能量、关键氨基酸残基的能量差异以及作用力特征等信息,从而对新药研发提供更多的理论支撑,尽早开展动物活性实验也是必不可少的工作。
利益冲突说明/Conflict of Intetests
所有作者声明不存在利益冲突。
伦理批准及知情同意/Ethics Approval and Patient Consent
本研究不涉及伦理批准及知情同意。
