HPLC-MS/MS 法同时测定清开灵口服液中7 种成分的含量
2024-03-05吴锦云蔡凯伟陈红英王家祺潘碧妍谢智勇廖琼峰广州中医药大学中药学院广东广州50006广州白云山明兴制药有限公司广东广州5050中山大学药学院深圳广东深圳58406
吴锦云,蔡凯伟,陈红英,王家祺,潘碧妍,谢智勇,廖琼峰[. 广州中医药大学中药学院,广东广州 50006;. 广州白云山明兴制药有限公司,广东广州 5050;. 中山大学药学院(深圳),广东深圳 58406]
清开灵口服液处方来源于“温病三宝”中的安宫牛黄丸,是由胆酸、猪去氧胆酸、珍珠母、水牛角、栀子、板蓝根、金银花和黄芩苷制成的中药制剂,具有清热解毒、镇静安神的功效,用于外感风热时毒、火毒内盛所致发热、咽喉肿痛、舌质红绛、苔黄、脉数者。针对当前新冠疫情流行现状,临床上也有将其应用于新型冠状病毒感染的治疗[1]。因此,清开灵口服液具有较高的临床使用价值和良好的经济效益。2020 年版《中国药典》(一部)规定对清开灵口服液中的胆酸、栀子苷和黄芩苷进行含量测定[2]。但对于一个由5 味中药及3 种中药成分组成的制剂,仅测定其中的3种成分,难以全面控制制剂的质量。目前已有报道[3-5]清开灵口服液中一种或多种成分的含量测定方法。同时清开灵其他剂型的含量测定亦有较多报道[6-9]。但其中应用高效液相色谱(HPLC)法测定的时间较长,应用高效液相色谱-质谱联用(HPLC - MS/MS)法则未对板蓝根中的有效成分进行含量测定。相关文献表明,清开灵口服液中的猪去氧胆酸[10-11]、板蓝根成分腺苷[12-13]、金银花成分绿原酸和咖啡酸[14-15]均具有抗炎、抗病毒等药理活性。因此,本研究基于成分有效性及可测性原则,根据清开灵口服液的处方组成,选择了《中国药典》中规定的3 种成分胆酸、栀子苷、黄芩苷,同时增加了猪去氧胆酸、绿原酸、咖啡酸和腺苷4 种成分,采用HPLC-MS/MS 技术建立清开灵口服液的含量测定方法,以期为其质量控制提供参考。
1 仪器和材料
1.1 仪器 Agilent 1260 高效液相色谱-6460 三重四级杆质谱联用仪(美国Agilent Technologies 公司);Vortex Mixer XW-80A 型涡旋振荡器(海门市其林贝尔仪器制造有限公司);KQ-250B 型超声波清洗器(昆山市超声仪器有限公司);AS62.R2型十万分之一电子天平(波兰RADWAG 公司);JA/YP 型万分之一电子天平(瑞士METTLER TOLEDO 有限公司)。
1.2 药物和试剂 16 批清开灵口服液(广州白云山明兴制药有限公司,批号分别为1221020、1230510、1230511、1230515、1230602、1230603、1230604、1230606、1230608、1230609、1230610、1230611、1230612、1230613、1230614、12300615)。腺苷、绿原酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸(含量均≥98.0%,中国食品药品检定研究所,批号分别为110879-202204、110753-202119、110749-201919、110715-202223、100087-201411 和100078-201808);咖啡酸(含量≥98.0%,上海源叶生物科技有限公司,批号:M27GB143417);甲醇(色谱纯,德国默克化学试剂有限公司);乙酸铵(色谱纯,上海晶纯生化科技股份有限公司);甲酸(色谱纯,天津市科密欧化学试剂有限公司);其余试剂均为分析纯。
2 方法与结果
2.1 色谱和质谱条件
2.1.1 色谱条件 色谱柱:Waters ACQUITY UPLC BEH C18色谱柱(2.1 mm×10 mm,1.7 μm);流动相:含10 mmol·L-1乙酸铵和0.1%甲酸的水溶液(A)-甲醇(B),梯度洗脱(0~3.5 min,80%A;3.5~5 min,80%A→10%A;5~12.2 min,10%A);柱温:30 ℃;流速:0.15 mL·min-1;进样量:5 μL。
2.1.2 质谱条件 离子源采用电喷雾离子源(ESI),正/负离子模式进行扫描,多反应监测模式(MRM)进行分析,干燥气(氮气)温度为300 ℃,干燥气流速为5 L · min-1,雾化气(氮气)压力为45 psi,鞘气(氮气)温度为300 ℃,鞘气流速为11 L·min-1,毛细管电压为3 500 V,喷嘴电压为500 V。7 种化合物的裂解电压及碰撞能量等质谱参数见表1。
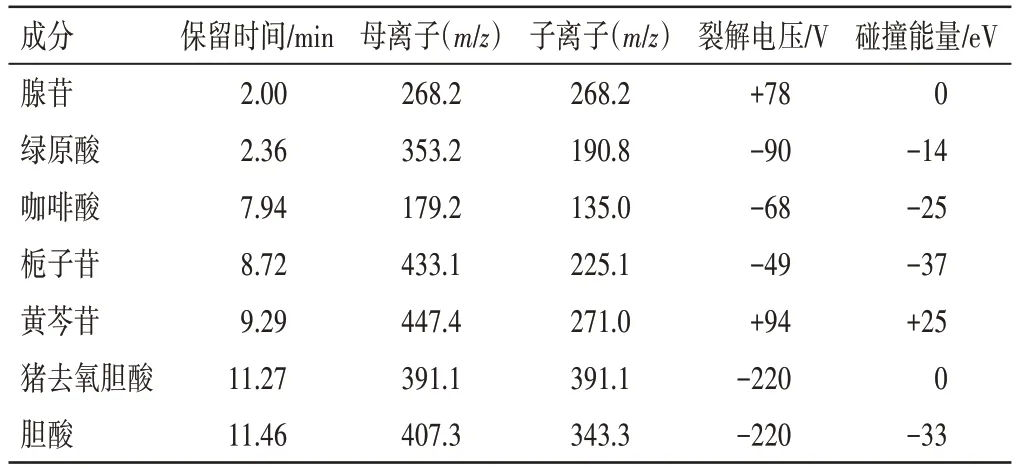
表1 清开灵口服液中7 种化合物的质谱测定参数Table 1 The mass spectral parameters of 7 components in Qingkailing Oral Liquid
2.2 溶液的配制
2.2.1 样品溶液的制备 分别精密量取15个批次的清开灵口服液0.25 mL,置于10 mL 的容量瓶中,加入50%甲醇稀释至刻度,摇匀,0.22 μm 微孔滤膜过滤,取续滤液,即得15个批次供试品溶液。
2.2.2 对照品储备液及混合对照品储备溶液的制备分别取腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸对照品适量,精密称定,分别置于7 个10 mL 容量瓶中,加甲醇溶解并稀释至刻度,摇匀,配成质量浓度分别为1.004、0.998、0.998、0.996、1.002、1.005 和1.037 mg·mL-1的对照品储备液。分别精密量取各对照品储备液适量,用50%甲醇配成质量浓度分别为4.016、14.97、3.992、24.90、501.0、50.25 和155.5 μg·mL-1的混合对照品储备溶液。
2.3 方法学研究
2.3.1 专属性试验 精密量取“2.2.2”项下的混合对照品储备溶液2 mL,置于10 mL 容量瓶中,用50%甲醇稀释至刻度,摇匀,0.22 μm 微孔滤膜过滤,得混合对照品溶液。取混合对照品溶液及“2.2.1”项下的样品溶液,按“2.1”项下条件分别进样分析,结果显示,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸在各自的离子通道内均能出峰,且无干扰,表明该方法的专属性良好。MRM 图谱见图1。
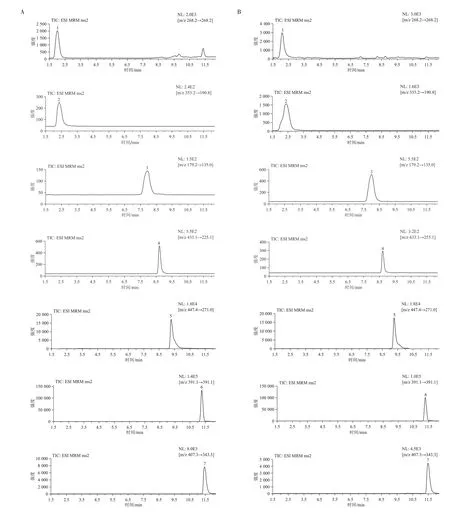
图1 清开灵口服液中7 种成分的MRM 提取离子流图Figure 1 The MRM chromatograms of 7 investigated components in Qingkailing Oral Liquid
2.3.2 线性关系考察 精密量取“2.2.2”项下的混合对照品储备溶液0.25、0.5、1、2、4、6、8 mL,置于10 mL 容量瓶中,加50%甲醇水稀释至刻度,摇匀,0.22 μm 微孔滤膜过滤,即得系列浓度的混合对照品溶液,按“2.1”项下条件进样分析,记录峰面积。以浓度(X)为横坐标,峰面积(Y)为纵坐标进行线性回归,每个成分取5 个浓度点,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸的线性范围、回归方程、相关系数(r)见表2。

表2 清开灵口服液中7 种成分的线性范围和回归方程Table 2 Linear ranges,regression equations of 7 components in Qingkailing Oral Liquid
2.3.3 精密度试验 取“2.3.1”项下的混合对照品溶液,按“2.1”项下条件连续进样6 次分析,计算峰面积的RSD。结果显示,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸峰面积的RSD分别为1.53%、2.48%、0.91%、1.66%、1.65%、2.03%和1.09%,表明该仪器精密度良好。
2.3.4 重复性试验 按照“2.2.1”项下方法平行制备供试品溶液(批号:1221020)6 份,按“2.1”项下条件进样测定,计算峰面积的RSD。结果显示,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸峰面积的RSD 分别为2.89%、2.14%、1.99%、1.28%、1.73%、1.53%和1.61%,表明该方法重复性良好。
2.3.5 稳定性试验 取同一份供试品溶液(批号:1221020),分别于0、2、4、8、12、24 h 按“2.1”项下条件进行测定,计算峰面积的RSD。结果显示,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸峰面积的RSD分别为1.81%、2.99%、2.26%、1.06%、3.00%、2.41%和0.62%,表明24 h 内供试品溶液稳定性良好。
2.3.6 回收率试验 精密量取已知含量的清开灵口服液6 份(批号:1221020),每份0.125 mL,分别加入腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸质量浓度分别为5.02、16.69、9.98、37.85、501.00、70.35 和186.66 μg·mL-1的混合对照品溶液1 mL,按“2.2.1”项下方法平行制备供试溶液。按“2.1”项下条件进样分析,并计算回收率。结果显示,腺苷、绿原酸、咖啡酸、栀子苷、黄芩苷、猪去氧胆酸和胆酸的平均回收率分别为100.9%、98.74%、 101.2%、 100.2%、 100.8%、 99.97% 和98.94%,RSD 分别为1.58%、0.59%、1.78%、1.25%、0.65%、1.69%和1.07%。见表3。
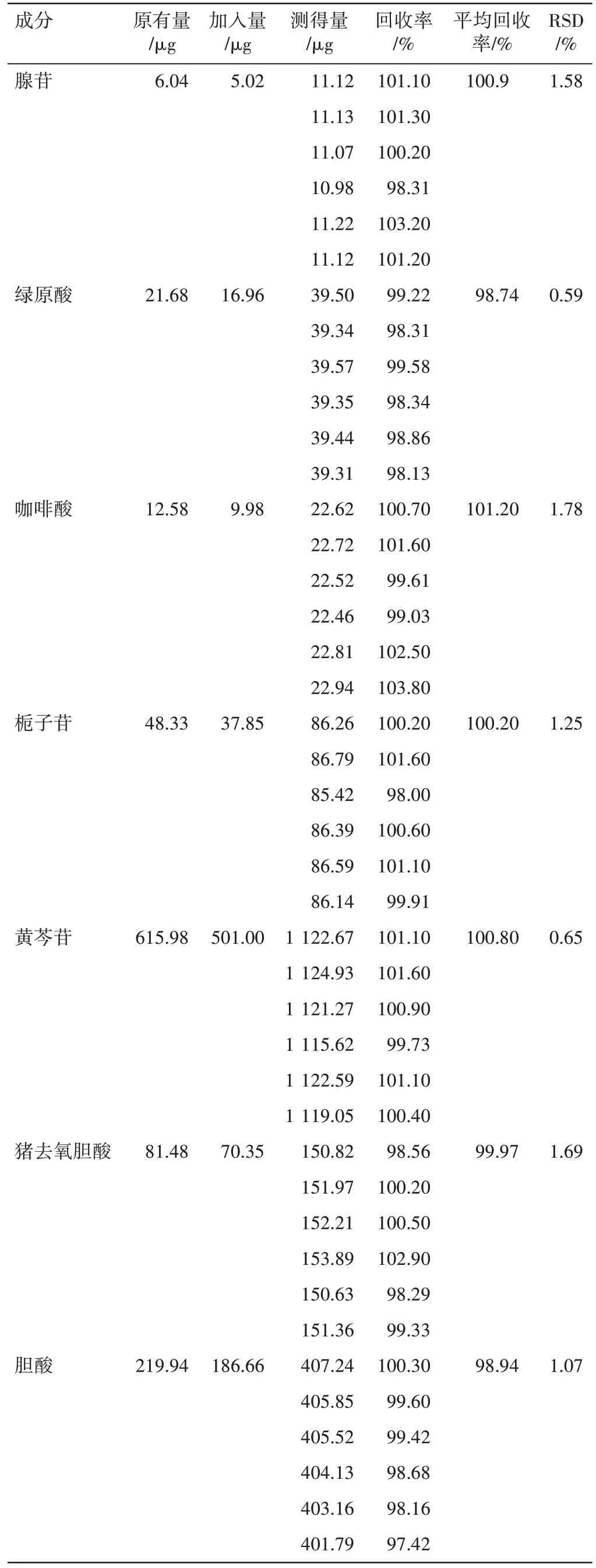
表3 清开灵口服液的回收率试验结果(n=6)Table 3 The results of recovery rate of Qingkailing Oral Liquid(n=6)
2.4 样品测定 取15批清开灵口服液样品各3份,分别按“2.2.1”项下方法制备供试品溶液,按“2.1”项下条件进样分析,使用外标法计算7 种成分的含量。结果见表4。

表4 清开灵口服液中7 种成分的含量测定结果(mg·mL-1,n=3)Table 4 Contents of 7 components in of Qingkailing Oral Liquid(mg·mL-1,n=3)
3 讨论
清开灵口服液处方中含8 味药,成分复杂,采用HPLC-UV 法进行检测时,所需分析时间长,色谱峰干扰较多[6-7],且处方中黄芩苷和栀子苷属于黄酮类化合物,与有机酸类化合物绿原酸、咖啡酸和核苷类化合物腺苷的最大吸收波长不同,而胆酸、猪去氧胆酸仅有末端吸收,因此用HPLC-UV 法难以满足上述成分的定量测定需求。HPLC-MS/MS 法专属性强,灵敏度高,故选择此方法进行测定。
本实验中考察了不同流动相对色谱峰峰型及响应的影响,使用甲醇作为有机相时,各成分色谱峰响应均优于使用乙腈;在水中分别添加0.1%甲酸、5 mmol·L-1乙酸铵、10 mmol·L-1乙酸铵、0.1%甲酸和10 mmol·L-1乙酸铵进行测定,结果表明,使用0.1%甲酸时,黄芩苷、腺苷色谱峰拖尾严重,使用5 及10 mmol·L-1乙酸铵时,黄芩苷及腺苷的峰型得到改善,而加入0.1%甲酸和10 mmol·L-1乙酸铵后,响应值提高,峰型对称,因此选择甲醇-含10 mmol·L-1乙酸铵和0.1%甲酸的水作为流动相进行梯度洗脱。
2020 年版《中国药典》 规定清开灵口服液“1 mL 含胆酸应为1.50~3.50 mg,1 mL 含栀子苷不得少于0.2 mg,1 mL 含黄芩苷不得少于3.5 mg”。本研究15 批样品中胆酸、栀子苷和黄芩苷的含量测定结果均符合规定。腺苷、绿原酸、咖啡酸和猪去氧胆酸在《中国药典》的清开灵口服液质量标准中无相应限度规定,本研究15批样品含量测定结果表明,腺苷、绿原酸、咖啡酸和猪去氧胆酸各批次之间的含量较为接近,提示这4种成分可以考虑纳入新的质量控制标准中。
综上所述,本研究建立了清开灵口服液中7 种成分的含量测定方法,对其质量进行较为全面的评价。本研究中测定的猪去氧胆酸、绿原酸、咖啡酸、腺苷在清开灵口服液中含量均较为接近,可为清开灵口服液的质量控制和后续研究提供参考。
