基于烯烃碳-氢键活化的碳-碳交叉偶联反应
2024-03-04颜瑞陈虎赵明
颜瑞,陈虎,赵明,*
1 合肥师范学院化学与制药工程学院,安徽省药食同源天然资源开发与利用工程实验室,合肥 230601
2 中国科学技术大学中国科学院软物质化学重点实验室,合肥 230026
烯烃是大学有机化学课程中的重点学习内容,烯烃中的碳碳双键(由一个σ键和一个π键组成)是反应的中心,富电子的碳-碳双键易受亲电试剂进攻,π键打开,形成两个σ键,能够与卤素、卤化氢、水、硫酸、次卤酸、硼烷等试剂发生亲电加成反应[1]。由于烯烃的碳-氢键具有较高的键能,往往不易发生断裂,然而在过渡金属催化条件下,基于碳-氢键活化,能够实现烯烃碳-氢键的官能团化,成功地构建各种碳-碳键[2–4](图1)。烯烃碳-氢键官能团化策略,步骤简单且具有较高的原子经济性,已成为有机化学中非常重要的合成手段。在本文中,我们介绍基于烯烃碳-氢键活化策略,通过碳-碳交叉偶联反应构建各类碳-碳键。
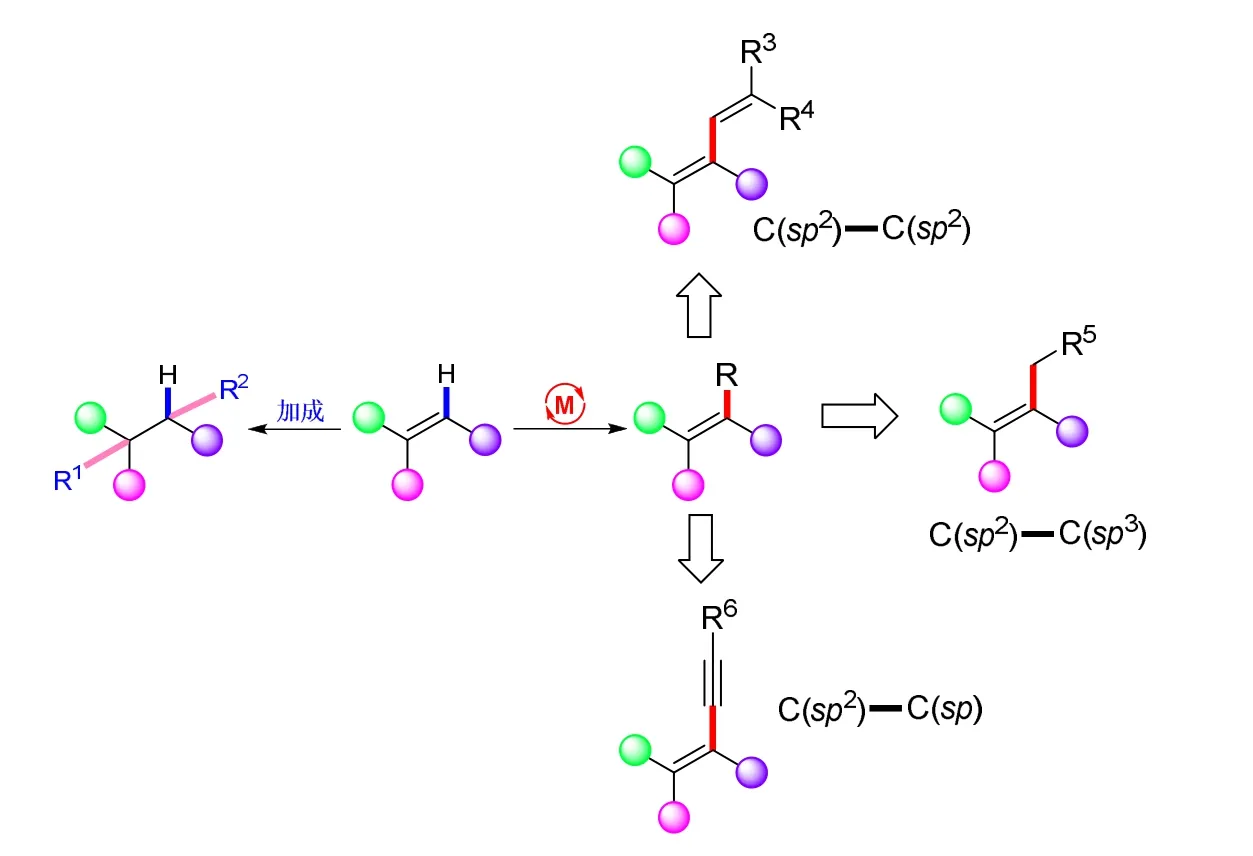
图1 烯烃反应
1 基于烯烃碳-氢活化构建碳(sp2)-碳(sp)键
烯炔结构在天然产物中广泛存在,同时也是有机化学及材料科学中非常重要的官能团[5–8]。近年来,人们在一些抗癌类维生素内也发现了烯炔的结构单元。基于烯烃碳-氢活化,共轭烯炔可由烯烃与炔基化试剂反应得到。
2015年,Nachtsheim课题组[9]报道了铑催化OH辅助的2-乙烯基苯酚烯烃碳-氢键与改良的高价碘(III)试剂(TIPS-EBX*)的炔基化反应。反应在非常温和的条件下顺利进行,具有较高的官能团兼容性、优异的化学选择性和较好的立体选择性。通过该反应,可以合成多种高度取代的1,3-烯炔类化合物(图2)。关于该反应机理,作者提出首先在铑催化剂作用下,发生烯烃碳-氢活化及配体交换,然后得到环状中间体1,随后炔基试剂(TIPS-EBX*)插入到中间体1中得到八元环状铑中间体后,发生α-消除得到关键中间体2,并释放出2-碘-6-甲基苯甲酸根,最后中间体2发生分子内1,2-协同迁移及配体交换,得到目标产物并释放出铑(III)催化剂(图3)。
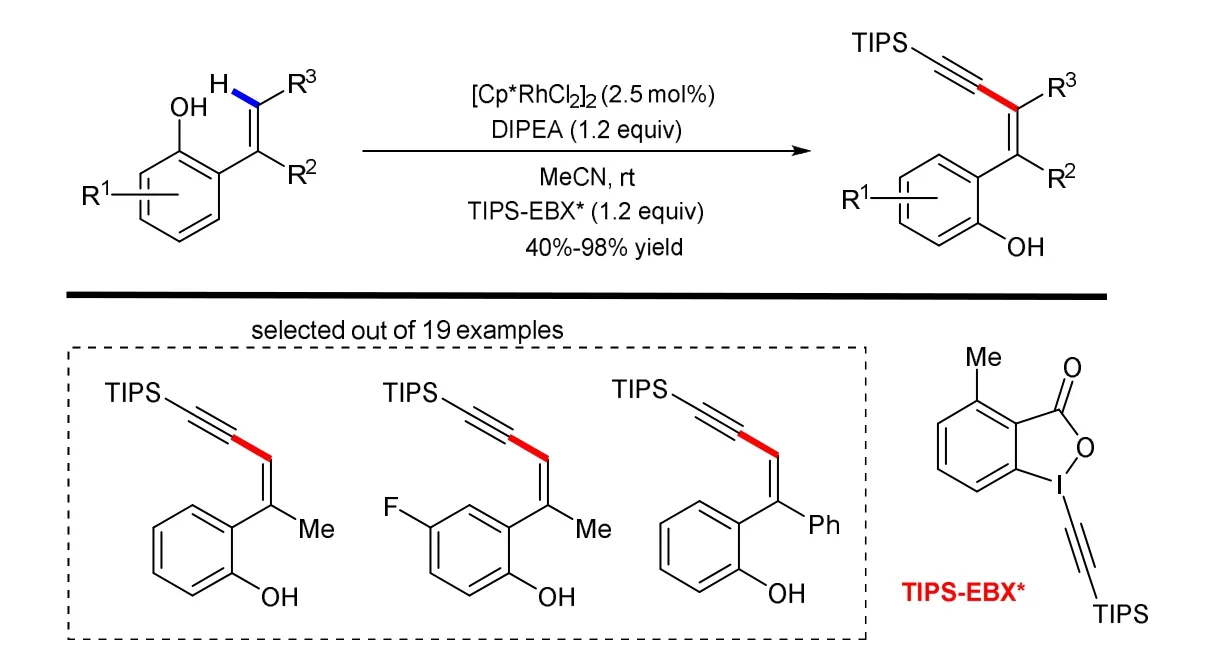
图2 2-乙烯基苯酚的炔基化反应

图3 2-乙烯基苯酚的炔基化反应机理
2017年,该课题组[10]又实现了Ir(III)催化的游离NH2导向的2-乙烯基苯胺的碳-氢键的炔基化反应。该反应以TIPS-EBX作为炔基化试剂,以最高97%的收率,较高的立体选择性合成高纯度Z-1,3-烯炔。反应具有广泛的底物范围,通过该方法可以得到多种非常有用的1,3-烯炔,而后者可以发生进一步转化得到五元和六元杂环化合物,为合成五元和六元杂环化合物提供了新的思路和方法(图4)。

图4 2-乙烯基苯胺的炔基化反应
罗德平教授课题组在合成共轭烯炔方面做了许多重要的工作[11,12]。2014年,罗德平教授课题组[11]利用铑(III)催化剂,成功实现了胺基导向的丙烯酰胺的炔基化反应。该反应具有操作简单、反应条件温和、产物收率高的优点。反应用TIPS-EBX作为炔基化试剂,在最优条件下,不同取代基取代的丙烯酰胺均能与炔基试剂发生反应,得到目标化合物。作者指出,对甲苯磺酰亚胺基作为弱配位导向基团,在该反应中起到了至关重要的作用(图5)。
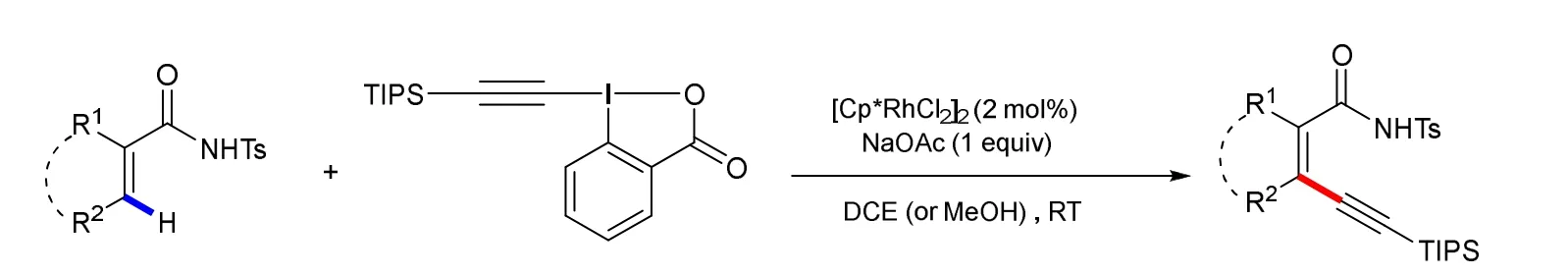
图5 丙烯酰胺的炔基化反应
2 基于烯烃碳-氢活化构建碳(sp2)-碳(sp2)键
共轭二烯及多烯类化合物是天然产物及药物分子中非常常见的分子骨架[13–16]。通过过渡金属催化的烯烃碳-氢活化,可以实现烯烃与烯烃的交叉偶联反应。其中最常见的是钯催化的偶联反应以及导向基辅助的铑、钌、铱等过渡金属催化的烯烃碳-氢键的烯基化反应[17–19]。
对于钯催化的烯烃碳-氢活化,其机理一般是:钯催化剂首先与富电子烯烃结合生成乙烯基钯中间体3,该中间体随后与缺电子烯烃发生络合,随后该烯烃双键发生迁移插入到碳-钯键之间,得到σ-钯中间体4,中间体4发生β-消除得到二烯烃类产物,释放出的钯物种5被氧化后重新得到活性钯催化剂,进入到下一个催化循环(图6a)。对于导向基辅助的烯烃碳-氢活化反应机理,过渡金属通过与导向基络合活化烯烃碳-氢键,得到乙烯基金属中间体6,随后缺电子烯烃中的双键插入到中间体6的C―M键中间,得到的中间体7,接着中间体7发生β-消除得到目标产物(图6b)。
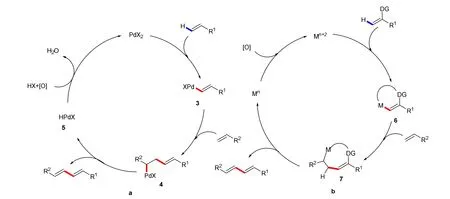
图6 (a) 钯催化的烯烃交叉偶联反应历程;(b) 导向基辅助的烯烃交叉偶联反应历程
罗德平教授课题组在2009年首次实现了两种不同的简单烯烃之间的交叉偶联反应[20]。通过利用不同烯烃的空间位阻与电子性质,成功实现了α-取代的苯乙烯与丙烯酸酯的交叉偶联反应(图7)。该反应用钯作催化剂,在温和条件下以较高收率得到偶联产物。随后,该课题组将该催化策略进一步应用到茚类化合物与缺电子烯烃的交叉偶联反应中[21],该反应催化剂Pd(OAc)2用量为10 mol% (图8)。

图7 苯乙烯与丙烯酸酯的交叉偶联反应

图8 茚类化合物与缺电子烯烃的交叉偶联反应
此后几年,众多研究人员相继报道了许多类似的工作。2012年,柳忠全教授课题组[22]成功发展了Pd(OAc)2催化的简单烯烃碳-氢键活化得到1,3二烯烃的反应。该反应用α位置没有被取代的苯乙烯和一系列未活化的脂肪族烯烃进行反应,以较为优秀的产率得到1,3丁二烯类化合物。略显不足的是,该反应需要用15 mol%的催化剂和2.5倍摩尔当量的AgOAc作为添加剂(图9)。
除了上面讨论的简单烯烃的碳-氢键官能化反应外,多年来,人们还致力于导向基辅助的烯烃碳-氢活化。2014年,Glorius教授课题组[23]用Rh(III)催化剂,实现了烯醇衍生物与简单烯烃的交叉偶联反应。该反应选用含有碳酸酯导向基的芳基或脂肪族烯烃,与简单烯烃反应,以较高收率得到共轭二烯烃。此外,反应产物在特定条件下,还可以脱掉碳酸酯导向基,得到β,γ-不饱和酮(图10)。
2017年,罗德平教授课题组[24]报道了钯催化的简单烯烃之间的氧化交叉偶联反应。反应具有立体选择性高、反应条件温和等优点。该方法利用羟基作为导向基,烯烃与缺电子烯烃反应得到多取代烯烃产物。研究发现,羟基除了作为导向基外,还可以提高偶联产物中Z构型的比例(图11)。
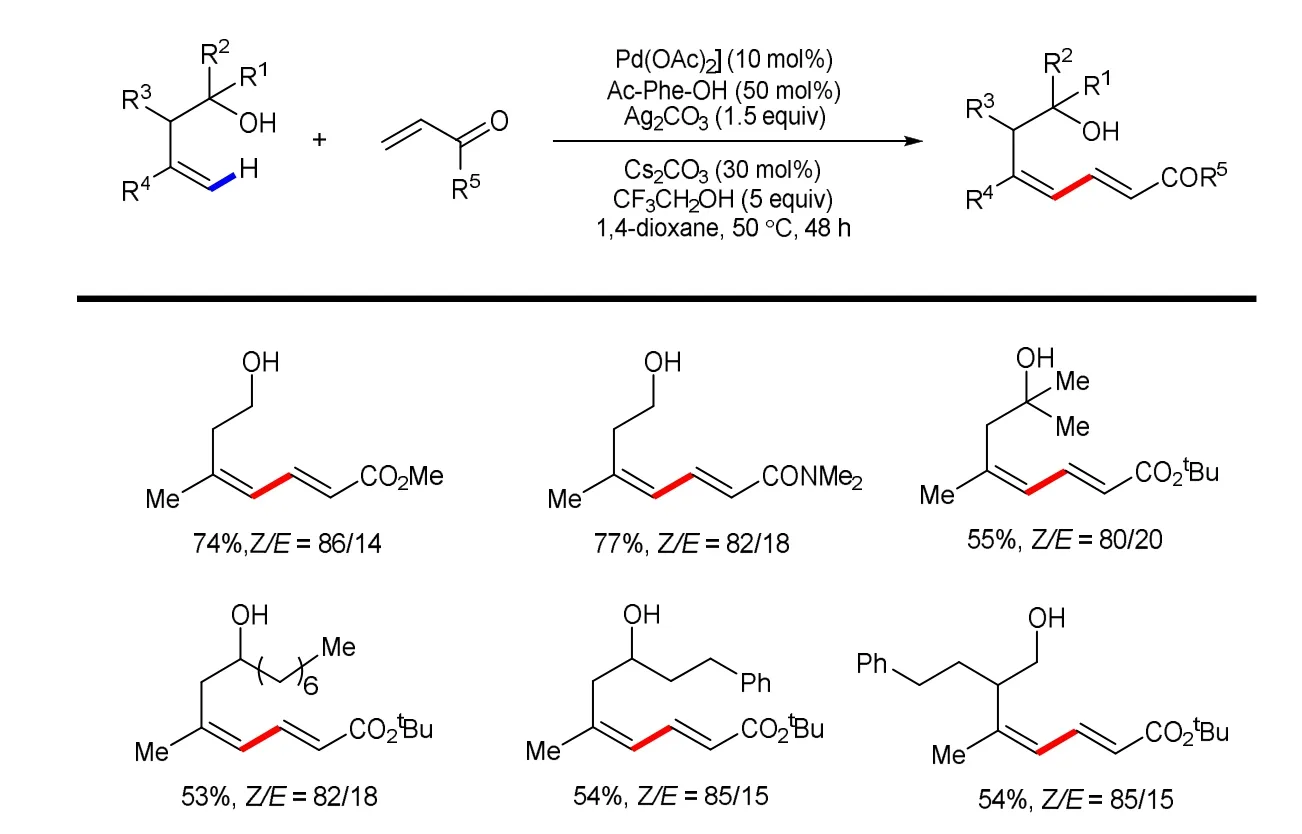
图11 烯丙醇与烯烃的交叉偶联反应
3 基于烯烃碳-氢活化构建碳(sp2)-碳(sp3)键
基于烯烃碳-氢活化,也可以构建碳(sp2)-碳(sp3)键,本文主要介绍烯烃碳-氢键的烯丙基化反应。烯丙基化反应是有机合成中非常有用的反应之一,烯丙基可以进一步反应得到许多其他有用的官能团[25]。
2015年,Glorius教授课题组[26]实现了酰胺导向的烯烃碳-氢键的烯丙基化反应。反应用较为便宜的Cp*Co(III)作催化剂,丙烯酰胺和烯丙基碳酸酯反应,以较高收率得到烯丙基化的产物(图12)。此外,Kim教授课题组[27]也报道了类似的工作,不同的是,Kim教授课题组用Ru作为催化剂,并以中等收率得到了烯丙基化产物。

图12 丙烯酰胺的烯丙基化反应
2018年,纪海涛教授课题[28]组报道了Ru(II)催化的烯烃的烯丙基化反应。值得注意的是,该反应用廉价易得的烯丙醇作为烯丙基试剂,相比于烯丙基酯、烯丙基卤化物等具有原子经济性高等优点。反应用N-甲氧基氨基甲酰基作为导向基,各种缺电子的丙烯酰胺均能与烯丙醇反应,得到1,4-二烯。反应具有较高的官能团兼容性,产物具有较好的立体基区域选择性(图13)。
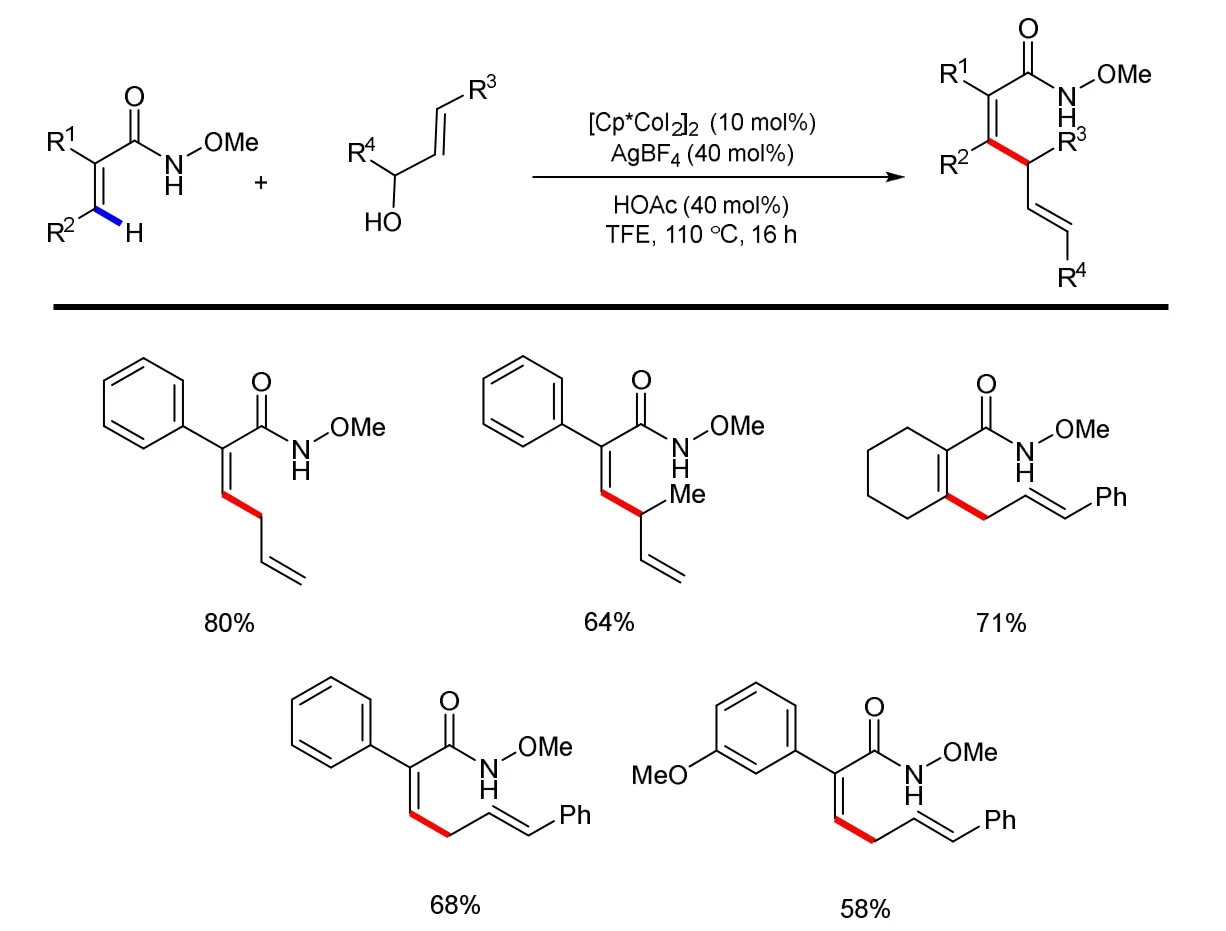
图13 丙烯酰胺与烯丙醇的烯丙基化反应
4 结语
本文主要介绍了基于烯烃碳-氢键活化策略构建各类碳-碳键。在过渡金属催化剂作用下,烯烃碳-氢键可发生活化断裂,进一步与其他试剂发生交叉偶联反应,得到含有碳(sp2)-碳(sp)、碳(sp2)-碳(sp2)、碳(sp2)-碳(sp3)键的产物。过去几十年间,烯烃碳-氢键活化获得了长足发展,人们相继报道了许多重要的催化方法。然而目前仍存在很多挑战,例如大部分反应需要用到钯、铑等贵金属作为催化剂,且催化剂用量相对较高。因此发展廉价过渡金属如铁、铜等催化的或无金属催化的新型烯烃碳-氢活化,是未来的重点研究方向。此部分内容拓展了本科教学中烯烃的知识点,帮助学生们开阔视野,培养学生们的科研兴趣,激发学生们对未知世界的探索欲。
