不同剂量右美托咪定对脑外科手术全身麻醉患者术后认知功能及TGF-β/Smad通路的影响*
2024-02-28马晓梅马万杨海燕杨莉
马晓梅,马万,杨海燕,杨莉
(宁夏医科大学总医院 麻醉与围术期医学科,宁夏 银川 750004)
脑外科手术一般指神经外科用以解决颅脑系统疾病的手术,脑肿瘤、脑血管病、脑外伤等均可进行脑外科手术[1]。术后认知功能障碍(postoperative cognitive dysfunction, POCD)是指麻醉手术后患者出现人格、社交能力、认知能力等方面受损,表现为精神错乱、记忆力下降等[2-3]。外科手术后患者发生POCD的现象并不少见,在老年患者中更易发生,围手术期血流动力学变化、术中创伤、低血压等也可能导致POCD发生[4-6]。因此,围手术期麻醉管理关系到患者术后是否发生POCD。不同麻醉药物、不同药物剂量对患者围手术期血流动力学、术后应激反应、认知功能的影响也不尽相同[7-8]。右美托咪定是全身麻醉手术中气管插管与机械通气的常用麻醉药物,镇静和镇痛效果较好[9-10]。转化生长因子-β(transforming growth factor-β, TGF-β)信号通路关系到多种生理过程,如调控干细胞活性及细胞生长发育等,Smad蛋白是TGF-β受体下游的信号转导分子[11-12]。本研究在脑外科全身麻醉手术中应用不同剂量右美托咪定进行麻醉,观察不同剂量右美托咪定对术后认知功能、TGF-β/Smad通路表达等的影响,为临床治疗提供帮助。
1 资料与方法
1.1 研究对象
选取2020年1月—2023年1月宁夏医科大学总医院收治的114例行血肿清除术患者为研究对象。本研究经医院医学伦理委员会批准,患者及其监护人均签署知情同意书。
1.2 纳入与排除标准
1.2.1 纳入标准 ①具有血肿清除术手术指征;②美国麻醉师协会(American Society of Anesthesiologists, ASA)分级[13]为Ⅰ、Ⅱ级;③年龄35~55岁。
1.2.2 排除标准 ①术前1个月内服用过镇痛、镇静类药物;②术前合并精神类疾病;③合并心、肝等器官功能严重不全;④凝血功能障碍;⑤对研究中所用药物严重过敏;⑥合并脑外科手术禁忌证。
1.3 药物
右美托咪定(湖南科伦制药有限公司,批准文号:国药准字H20183150,规格:1 mL∶100 μg),阿托品(福建汇天生物药业有限公司,批准文号:国药准字H35020368,规格:2 mL∶1 mg),咪达唑仑(江苏九旭药业有限公司,批准文号:国药准字H20153019,规格:3 mL∶15 mg),顺苯磺酸阿曲库铵(江苏恒瑞医药股份有限公司,批准文号:国药准字H20183042,规格:5 mL∶10 mg),舒芬太尼(宜昌人福药业有限责任公司,批准文号:国药准字H20054171,规格:1 mL∶50 μg),丙泊酚(四川国瑞药业有限责任公司,批准文号:国药准字H20040079,规格:10 mL∶0.1 g)。
1.4 分组及治疗方法
将患者分为A、B、C组,每组38例。患者入室后监测生命体征,建立静脉通道。麻醉诱导前10 min,A、B、C组均予以静脉泵注右美托咪定,负荷剂量为0.6 μg/(kg·h),然后分别以0.2、0.4、0.8 μg/(kg·h)维持泵注至手术结束前40 min。麻醉诱导:阿托品0.5 mg + 咪达唑仑0.5 mg/kg +顺苯磺酸阿曲库铵0.15 mg/kg + 舒芬太尼0.2 mg/kg +丙泊酚1.5 mg/kg。气管插管:设置潮气量为8~10 mL/kg,通气频率为10~15次/min,氧流量为1 L/min,呼气与吸气比为1∶2,呼气末二氧化碳分压为35~45 mmHg。以微量注射泵双通道模式按4~12 mg/(kg·h)输注丙泊酚,7~12 μg/(kg·h)输注瑞芬太尼,术中依据血流动力学水平调整丙泊酚和瑞芬太尼用量。按照出血量与失液量补充相应胶体、晶体及血制品。
1.5 观察指标
1.5.1 一般资料 性别、年龄、体质量指数(body mass index, BMI)、ASA分级、血肿量、手术类型。
1.5.2 围手术期指标 手术时间、麻醉时间、丙泊酚用量、自主呼吸恢复时间。
1.5.3 血流动力学 麻醉前(T0)、给药后10 min(T1)、拔管时(T2)的心率(heart rate, HR)、血氧饱和度(nlood oxygen saturation, SpO2)、收缩压(systolic blood pressure, SBP)。
1.5.4 镇痛、镇静、认知功能评分 在拔管后15 min(T3)、拔管后30 min(T4)采用视觉模拟评分法(visual analog score, VAS)[14]评估患者疼痛程度;采用Ramsay镇静评分[15]评估患者躁动程度;术前、术后3 d、术后7 d采用蒙特利尔认知评估量表[16](Montreal cognitive assessment, MoCA)评估患者认知功能。
1.5.5 TGF-β1、Smad2蛋白相对表达量 Western blotting检测病变脑组织中TGF-β1、Smad2蛋白相对表达量,通过SDS-PDGE电泳、转膜、封闭,4 ℃下孵育一抗过夜,洗膜后孵育二抗1 h,曝光成像,以Image Lab软件分析。
1.5.6 不良反应 观察患者不良反应发生情况,并根据不同情况给予相应药物以减轻不良反应。
1.6 统计学方法
数据分析采用SPSS 22.0统计软件。计量资料以均数±标准差(±s)表示,比较用t检验或方差分析或重复测量设计的方差分析,两两比较用LSD-t检验;计数资料以构成比或率(%)表示,比较用χ2检验,两两比较用Bonferroni法,调整检验水准α=0.017。P<0.05为差异有统计学意义。
2 结果
2.1 3组患者一般资料比较
研究共筛选120例患者,最终入组114例。3组患者性别构成、年龄、BMI、ASA分级、血肿量、手术类型比较,经χ2检验或方差分析,差异均无统计学意义(P>0.05)。见表1。
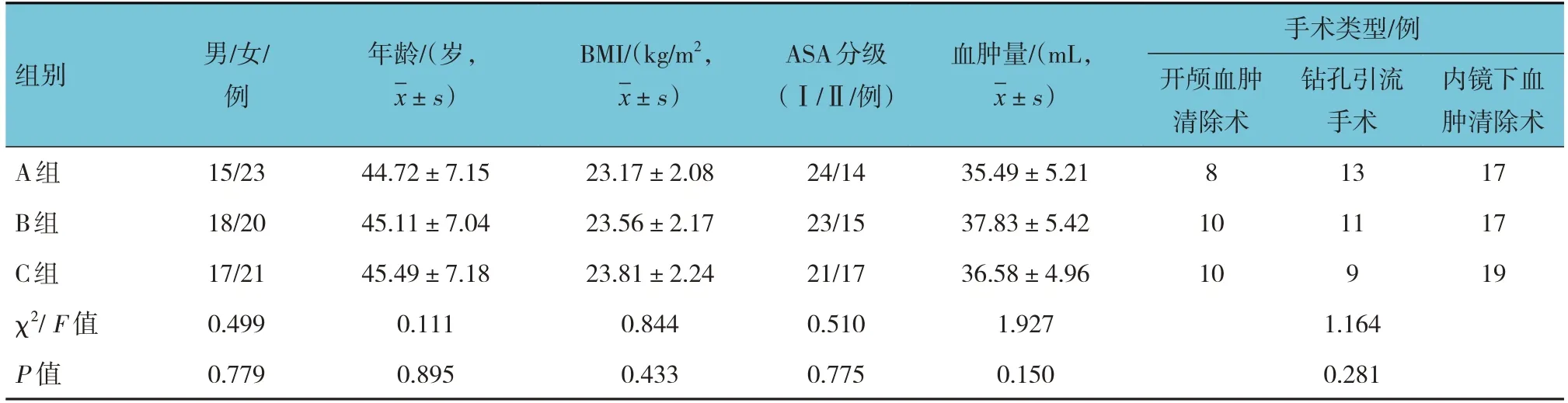
表1 3组患者一般资料比较 (n =38)
2.2 3组患者围手术期指标比较
3组患者手术时间、麻醉时间、自主呼吸恢复时间比较,经方差分析,差异均无统计学意义(P>0.05)。3组患者丙泊酚用量比较,经方差分析,差异有统计学意义(P<0.05);与A、B组比较,C组丙泊酚用量低,与A组相比,B组丙泊酚用量低。见表2。
表2 3组患者围手术期指标比较 (n =38,±s)
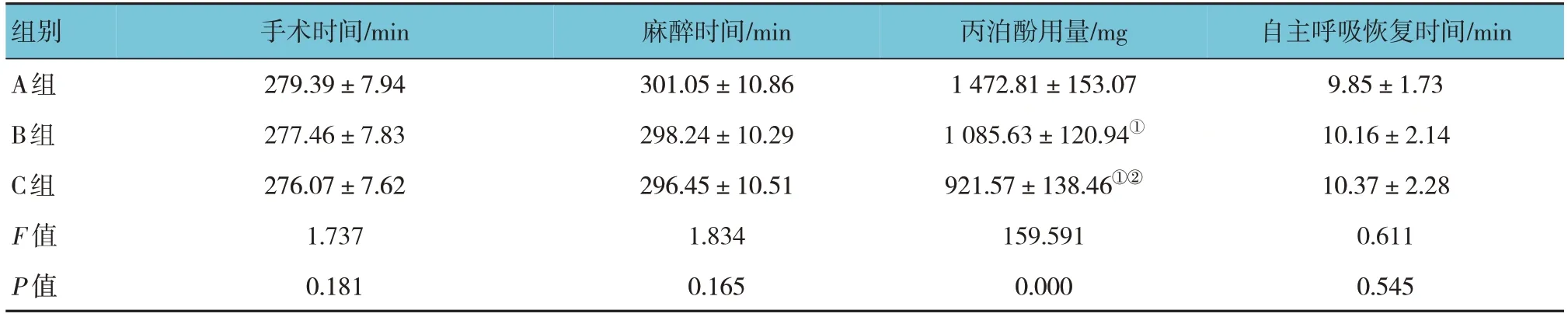
表2 3组患者围手术期指标比较 (n =38,±s)
注:①与A组比较,P<0.05;②与B组比较,P<0.05。
组别A组B组C组F 值P 值自主呼吸恢复时间/min 9.85±1.73 10.16±2.14 10.37±2.28 0.611 0.545手术时间/min 279.39±7.94 277.46±7.83 276.07±7.62 1.737 0.181麻醉时间/min 301.05±10.86 298.24±10.29 296.45±10.51 1.834 0.165丙泊酚用量/mg 1 472.81±153.07 1 085.63±120.94①921.57±138.46①②159.591 0.000
2.3 3组患者不同时间点血流动力学比较
3组患者T0、T1、T2时HR、SpO2、SBP比较,采用重复测量设计的方差分析,结果:①不同时间点HR、SpO2、SBP比较,差异均有统计学意义(F=62.351、101.964和83.926,均P=0.000);②3组HR、SpO2、SBP比较,差异均有统计学意义(F=72.365、59.813和64.549,均P=0.000),C组T2时HR、SpO2、SBP水平较A组均降低,C组T1、T2时SpO2水平较B组均降低(P<0.05),血流动力学更稳定;③3组HR、SpO2、SBP随时间变化趋势比较,差异均有统计学意义(F=21.354、18.240和14.683,均P=0.000)。见表3。
表3 3组患者不同时间点血流动力学比较 (n =38,±s)
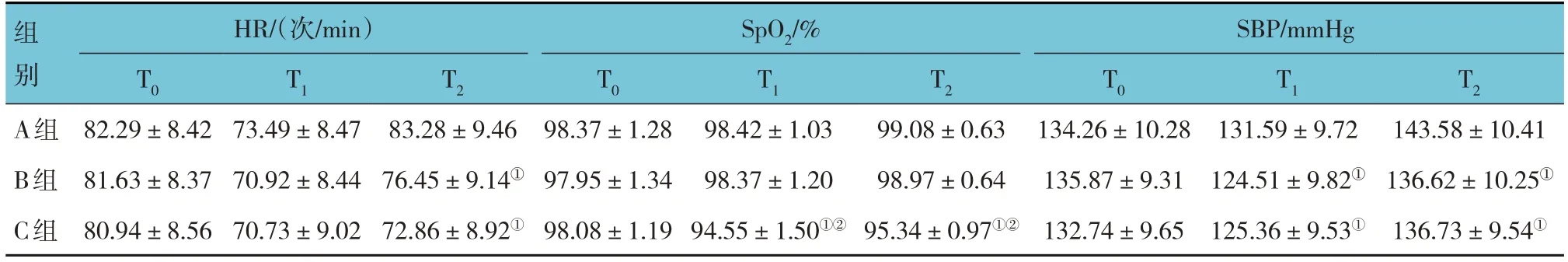
表3 3组患者不同时间点血流动力学比较 (n =38,±s)
注:①与A组比较,P<0.05;②与B组比较,P<0.05。
组别A组HR/(次/min)SpO2/%SBP/mmHg T1 T2 T1 T2 T1 T2 B组C组T0 82.29±8.42 81.63±8.37 80.94±8.56 T0 98.37±1.28 97.95±1.34 98.08±1.19 T0 134.26±10.28 135.87±9.31 132.74±9.65 143.58±10.41 136.62±10.25①136.73±9.54①73.49±8.47 70.92±8.44 70.73±9.02 83.28±9.46 76.45±9.14①72.86±8.92①98.42±1.03 98.37±1.20 94.55±1.50①②99.08±0.63 98.97±0.64 95.34±0.97①②131.59±9.72 124.51±9.82①125.36±9.53①
2.4 3组患者不同时间点镇痛、镇静、认知功能评分比较
3组患者T3、T4时VAS、Ramsay评分及术前、术后1 d、术后3 d MoCA评分比较,采用重复测量设计的方差分析,结果:①不同时间点VAS、Ramsay、MoCA评分比较,差异均有统计学意义(F=24.382、15.217和18.493,均P=0.000);②3组VAS、Ramsay、MoCA评分比较,差异均有统计学意义(F=32.189、29.843和37.462,均P=0.000),B、C组T3时VAS评分均低于A组,Ramsay评分均高于A组(P<0.05),C组T4时VAS评分低于A组,Ramsay评分高于A组(P<0.05),B、C组术后1 d、术后3 d时MoCA评分均高于A组(P<0.05);③3组VAS、Ramsay、MoCA评分随时间变化趋势比较,差异均有统计学意义(F=5.356、4.297和39.465,均P=0.000)。见表4。
表4 3组患者镇痛、镇静、认知功能评分比较 (n =38,分,±s)

表4 3组患者镇痛、镇静、认知功能评分比较 (n =38,分,±s)
注:†与A组比较,P<0.05。
组别MoCA T4 T4 A组B组C组VAS T3 2.01±0.57 1.40±0.45†1.25±0.41†Ramsay T3 1.96±0.60 2.34±0.68†2.48±0.89†术后3 d 23.31±2.41 24.75±2.58†24.91±2.61†2.15±0.61 1.81±0.86 1.59±0.72†1.89±0.58 2.10±0.67 2.35±0.71†术前26.63±2.82 26.94±2.75 26.71±2.86术后1 d 21.26±2.37 23.59±2.46†23.73±2.61†
2.5 3组患者TGF-β1、Smad2蛋白相对表达量比较
3组患者术前、术后7 d的TGF-β1、Smad2蛋白相对表达量比较,采用重复测量设计的方差分析,结果:①不同时间点TGF-β1、Smad2相对表达量比较,差异均有统计学意义(F=27.384和128.659,均P=0.000),②3组术后7 d时TGF-β1、Smad2相对表达量比较,差异均有统计学意义(F=40.826和32.418,均P=0.000),B、C组TGF-β1、Smad2蛋白相对表达量均低于A组,C组TGF-β1、Smad2蛋白相对表达量低于B组(P<0.05)。③3组TGF-β1、Smad2蛋白相对表达量随时间变化趋势比较,差异均有统计学意义(F=30.492和83.627,均P=0.000)。见表5。
表5 3组患者TGF-β1、Smad2蛋白相对表达量比较(n =38,±s)
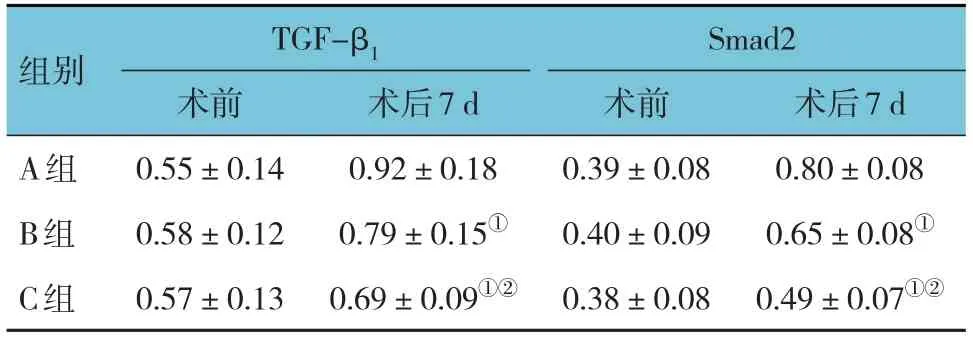
表5 3组患者TGF-β1、Smad2蛋白相对表达量比较(n =38,±s)
注:①与A组比较,P<0.05;②与B组比较,P<0.05。
组别TGF-β1术前0.55±0.14 0.58±0.12 0.57±0.13 A组B组C组Smad2术前0.39±0.08 0.40±0.09 0.38±0.08术后7 d 0.80±0.08 0.65±0.08①0.49±0.07①②术后7 d 0.92±0.18 0.79±0.15①0.69±0.09①②
2.6 3组患者不良反应情况
3组患者心动过缓、低血压、呼吸抑制发生率比较,经χ2检验,差异均无统计学意义(P>0.05)。3组患者恶心、呕吐发生率比较,经χ2检验,差异有统计学意义(P<0.05),C组恶心、呕吐发生率低于A组(χ2=0.013,P<0.017)。见表6。
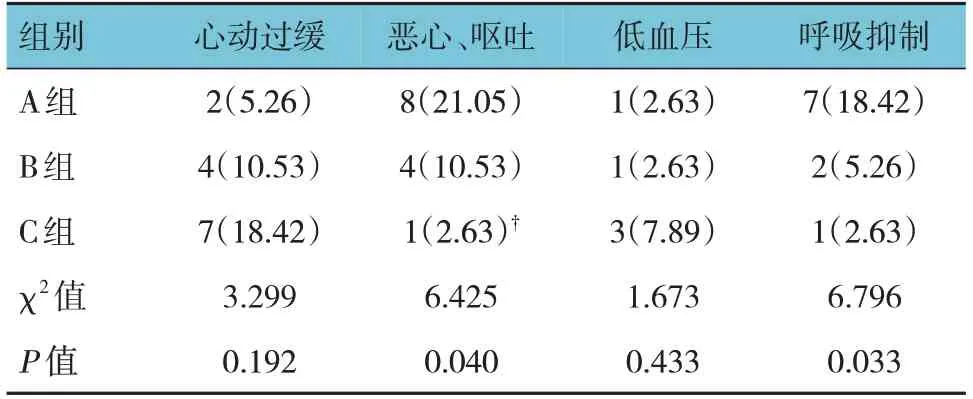
表6 3组患者不良反应比较 [n =38,例(%)]
3 讨论
POCD的发生受多种因素影响,高龄、营养不良、心理因素等内因易使其发生率上升,术中出血、应激反应、术后疼痛等外因也有可能导致POCD发生。有研究报道,麻醉方式、麻醉药物种类、麻醉深度等会均影响患者术后认知功能[17-18]。不同麻醉药物对中枢神经系统、血流动力学的影响不尽相同,因此在脑外科手术中,需选择合适的麻醉药物及药物剂量,最大程度地减少术后并发症的发生。
本研究结果显示,C组丙泊酚用量低于A、B组,B组丙泊酚用量低于A组;C组T2时HR、SpO2、SBP水平较A组均降低,C组T1、T2时SpO2水平较B组均降低;B、C组T3时VAS评分均低于A组,Ramsay评分高于A组,C组T4时VAS评分低于A组,Ramsay评分高于A组。提示以0.8 μg/(kg·h)速率维持泵注右美托咪定能够减少丙泊酚用量,保持围手术期血流动力学稳定,且具有更好镇痛、镇静效果。多项研究表明,右美托咪定的镇痛镇静效果及对血流动力学等影响具有剂量依赖性[19-20]。右美托咪定是一种相对选择性α2-肾上腺素受体激动剂,α2受体存在于神经突触前膜及后膜,右美托咪定通过激动前膜α2受体,能够抑制去甲肾上腺素释放,阻滞疼痛传导,因此具有较好的镇痛、镇静作用;激动后膜α2受体,能够抑制交感神经活性,减少因术中刺激引起的血流动力学波动,因而具有稳定血流动力学的作用[21-23]。此外,右美托咪定可与其他麻醉药物发挥协同作用,因此可减少麻醉诱导所需药物剂量及术中麻醉药物剂量,进而减少其他麻醉药物带来的不良反应[24]。
本研究结果显示,术后1 d、3 d时B、C组MoCA评分均高于A组,术后7 d时B、C组TGF-β1、Smad2蛋白相对表达量均低于A组,C组TGF-β1、Smad2蛋白相对表达量低于B组,提示以0.8 μg/(kg·h)速率维持泵注右美托咪定能够减轻POCD,其可能与右美托咪定抑制TGF-β1、Smad2表达有关。有研究报道,POCD患者TGF-β、Smad1、Smad3、Smad7水平高于正常水平,认为POCD与TGF-β/Smad信号通路参与有关[25]。应激及创伤会激活下丘脑-垂体-肾上腺皮质轴功能亢进和免疫系统,引起乙酰胆碱、5-羟色胺等内分泌紊乱并提高炎症细胞因子表达水平,引起精神紊乱[26]。TGF-β可由免疫细胞产生,广泛存在于组织细胞中,是调节细胞生长分化、免疫等生理功能的多功能因子,Smad蛋白是TGF-β超家族信号传递的重要调控分子,受I型受体诱导发挥转录调控作用[27]。当机体存在炎症时,局部血小板释放的TGF-β放大炎症反应,其水平升高。而临床研究证实,右美托咪定能够抑制肿瘤坏死因子-α等炎症因子水平[28]。推测右美托咪定能够改善术后认知功能的原因可能是,右美托咪定能够减轻炎症,从而减轻炎症因子对中枢神经系统的损害,同时维持机体内分泌稳定,改善认知功能。胡凯等[29]研究报道,术后炎症反应抑制程度与右美托咪定呈剂量依赖性。据此推测右美托咪定对认知功能的改善也具有一定剂量依赖性,这与本研究结果相符。刘华琴等[30]报道,对胃肠恶性肿瘤根治术后患者夜间输注不同剂量右美托咪定,结果显示,较高剂量右美托咪定可减少患者POCD发生,与本研究存在相似之处。
本研究对3组不良反应进行观察,结果显示,C组恶心呕吐发生率低于A组,提示以0.8 μg/(kg·h)速率维持泵注右美托咪定能够减少不良反应发生。推测其原因可能是,较高剂量右美托咪定的应用可显著减少术中丙泊酚用量,而丙泊酚会引起恶心、呕吐等不良反应[31]。因此,减少丙泊酚用量后可减少恶心、呕吐发生率。
综上所述,脑外科术中以0.8 μg/(kg·h)速率维持泵注右美托咪定可明显减少术中丙泊酚用量及不良反应,保持血流动力学稳定,具有较好镇痛、镇静作用,且能够改善患者术后认知功能,其可能与抑制TGF-β/Smad通路表达有关。本研究不足之处,所纳入样本量较少,研究结果可能发生偏差,不同剂量右美托咪定对认知功能的影响及其机制仍需要后续深入探讨。
