放射性粒子125I体外实验模型的发展和现状
2024-02-26韩莹波杨泽成董红梅孙雅敏张舵舵
韩莹波,杨泽成*,董红梅,孙雅敏,张舵舵
(1.吉林大学第二医院 胃肠外科,吉林 长春130022;2.吉林大学第一医院 胸外科,吉林 长春130021)
放射性粒子125I植入术作为临床治疗肿瘤的重要手段之一,近些年已在临床应用越来越广泛,并取得了令人瞩目的效果[1-5]。在我国,临床上主要使用的125I放射性粒子为6711型,结构见图1[6],半衰期59.6天,主要发射光子能量为 27.4 keV、31.4 keV 的X射线和光子能量为35.5 keV的γ射线,半价层为0.025 mmPb。放射性粒子植入术属于近距离放射治疗范围,不同于其他放射治疗方法,是采用极低剂量率持续照射肿瘤来获得治疗效果的。因此,在生物学机制方面有其自身的特点,国内外已有很多相关的研究。本文将就关于125I放射性粒子体外实验使用的模型的发展和现状进行介绍。

图1 放射性粒子I-125 6711型 结构图
1 模型设计的发展和现状
1.1 布源规则
关于125I放射性粒子的体外实验模型设计的文献相对较少,尽管各有不同,但就布源思路基本一致,均是按曼特斯特系统(也称为Paterson-Parker系统)规则进行平面布源,达到照射平面的剂量分布接近一致。按照曼彻斯特系统,模型设计中布源应遵循以下规则[7]:1)圆形布源。将放射源均匀地放置在圆周。在圆周上尽可能多布源,但是如果相邻源头尾之间的距离不超过源平面与照射平面的距离(h),可以少布置一些。2)如果照射平面的直径(d)小于源平面与照射平面之间的距离(h)3倍的情况下,即d/h<3,一个粒子圆环就足够了。如果3
1.2 分类介绍实验模型和特点
除了布源方式以外,放射性粒子体外实验模型设计还涉及细胞培养皿的因素,实验模型根据使用细胞培养皿的不同有明显差别。下面将根据细胞培养皿类型不同来分别介绍。
第一种是使用最常见的皮氏细胞培养皿(petri dish)设计的模型。这种模型出现较早,目前使用也最普遍。
1982年纽约哥伦比亚大学癌症研究所GOLDHAGEN等[8]为研究125I和137Cs的相对生物学效应,设计了一种放射性粒子体外细胞实验辐照模型。如图2。具体方案是使用了15枚约12倍于临床常用活度的125I放射性粒子,其中14枚等距分布于直径35 mm的圆周,剩下的1枚至于圆的中心,粒子使用聚酯胶带固定。在粒子盘的上方叠加放置3个细胞培养皿,粒子盘的下方叠加放置2个细胞培养皿。实验中使用了盘型离子室测量培养皿中细胞的受到的剂量率,并与理论公式计算出的结果做了比较(计算方法为:|理论值-测量值|÷测量值×100%,下同),除1例结果相差16%,其余均在10%以内,平均相差5.67%,证明了这种模型的可行性。实验设计者对于一些细节考虑比较周密-实验中为了减少培养皿与培养基之间的界面效应(interface effect),培养皿材料使用了聚四氟乙烯(PVDF)。不过这种模型的缺陷也很明显,根据曼彻斯特系统布源规则,距离布源平面远近不同的照射平面,d/h发生了变化,使用同一种布源方式无法保证不同照射平面剂量分布的均一性都理想。尽管此实验未进行剂量均一性的测量,后来也有学者验证了这种缺陷,YUE等[9]通过AAPM TG-43推荐公式[10]计算了将125I粒子(设定粒子表观活度为: 1 mCi)以在直径3 cm的圆周上均匀布置8枚粒子和圆中心布置1枚粒子的方式进行布源的周围剂量分布的情况,最后证明了距离布源平面越远,剂量分布均一性越好,距离布源平面越近则相反。
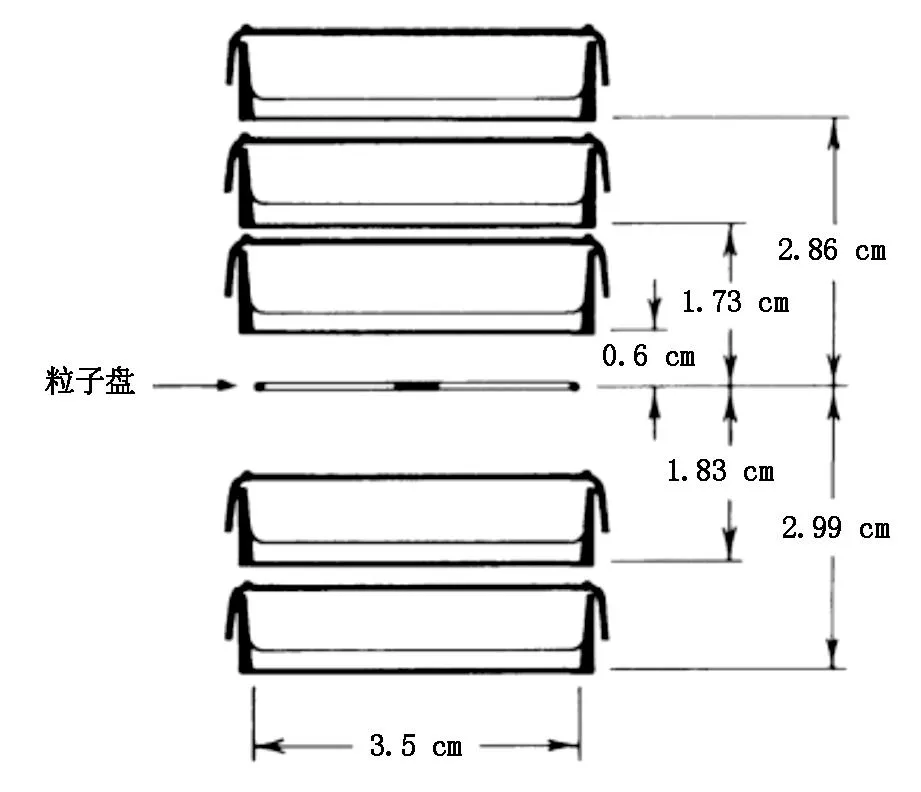
图2 Goldhagen等学者为研究125I和137Cs的相对生物学效应,设计的一种放射性粒子体外细胞实验辐照模型
2001年,英国弗农山医院医学物理科ARID等学者设计了一种比较经典的125I放射性粒子体外辐照实验模型,目前很多实验参照这个模型进行实验模型的设计[11-14],如图3。在ARID等设计的模型中,有一套聚苯乙烯材料制作的圆柱形模具,直径5 cm,分为上下两层。粒子盘也是聚苯乙烯材料制作,直径3 cm,粒子盘放在两层中间,呈“三明治”结构。在模具的上方放置直径3 cm(d)的细胞培养皿,粒子盘与培养皿之间存在一个厚度为6 mm(h)的聚苯乙烯层,这样d/h=5。粒子盘粒子排布为圆周均匀放置8颗,中心1颗。实验也使用TLD进行了剂量验证,同时使用AAPM TG-43推荐公式进行了剂量计算,实际测量结果与理论计算结果相差最大值为6.6%,平均为3.1%,实际测量剂量分布均一性为1.54(照射平面测的剂量率最高点与最低点的比值)。此实验设计优点在于:第一,在放射源与照射平面之间为填充聚苯乙烯材料,因为细胞培养皿使用的也是聚苯乙烯材料,这样放射源的射线达到照射平面经过的介质均一,干扰因素小,最后理论计算结果可以转换为聚苯乙烯介质条件下的结果,更精确。第二,提出在预定照射时间进行一半时,将细胞培养皿旋转22.5度,可以使照射平面受量更均匀。缺点是没有考虑聚丙乙烯材料培养皿与细胞培养基之间的界面效应。

图3 ARID等学者设计了一种比较经典的125I放射性粒子体外辐照实验模型
因为ARID等设计的模型中的聚苯乙烯模具也不易获得,需要特殊定制,所以为了解决这个问题,2008年复旦放射研究所陈红红等学者设计了一种相近的实验模型[15],区别在于粒子盘与照射平面之间的间隙使用液态水为填充介质。根据YUE等[9]的研究,1 mm厚的聚苯乙烯材料对125I粒子在水介质中的剂量率分布无影响。因此,使用聚苯乙烯细胞培养皿不会对实验结果产生影响。同时,对于照射平面吸收剂量的计算,使用了其自主研发的基于AAPM TG-43公式的放射性粒子植入计划系统(FudanTPS2.0)进行照射平面吸收剂量的计算。这种模型最大程度的还原了使用AAPM TG-43公式时所要求的液态水环境。
第二种是使用插入式细胞培养皿或悬挂式细胞培养皿。
1995年纽约纪念斯隆凯特琳癌症中心LING等学者为了研究125I和103Pd粒子相对生物学效应[16],设计了不同于上述的放射性粒子体外细胞辐照模型。如图4。实验中使用了Millicell插入式细胞培养皿,于培养皿上方放置粒子盘,放置14颗活度相同的125I粒子,按直径33 mm(d)的圆周均匀排布,粒子使用双面胶固定,粒子盘与培养皿的距离是12 mm(h),培养皿圆心与粒子盘圆心对应,d/h=2.8。在小室的底部有固体水膜,散在放置数枚TLD芯片(3 mm×3 mm×0.75 mm)。实验也比较了理论计算和实际测得培养皿内细胞受到的剂量率,两者相差最大在6%范围,平均为4.2%。不过实验并未测量剂量分布均一性。这种模型优点在于避免了培养基与培养皿之间的界面效应。文中指出,因为细胞正处于这个平面,这个效应会直接反应在细胞上,影响细胞的吸收剂量。因为该实验使用的是水等价的纤维基质膜,这层膜80%的空间已被细胞培养基填充,基本上避免了这一效应。这是使用这种培养皿的一个优势。
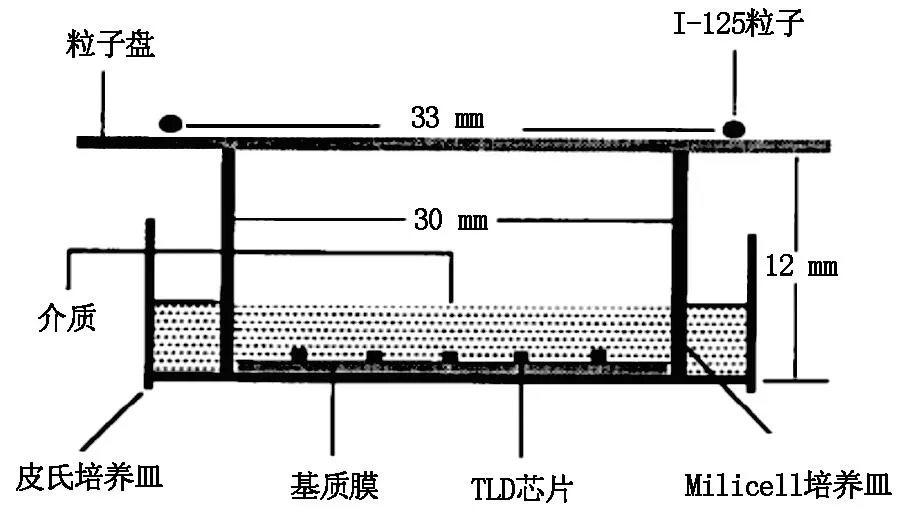
图4 LING等学者为了研究125I和103Pd粒子相对生物学效应[17],设计了不同于上述的放射性粒子体外细胞辐照模型
虽然Arid等设计的模型比较成熟,但受限于实验器材,这种模型不能研究细胞迁移、侵袭能力,而悬挂式培养皿可以进行相关研究。2014年由GUANG等[17]在研究肝癌细胞侵袭转移能力时设计了一种新型放射性粒子体外辐照模型。如图5。模型中使用Transwell(Corning,NY,USA)培养系统。在培养皿的底座放置粒子,周边7颗,中心1颗,活度为22.2 MBq(0.6mCi)。悬挂小室用于培养细胞。小室直径2.4 mm,底部为有直径8 mm微孔的聚碳酸脂膜,小室底部上表面至培养皿底部上表面的距离为3 mm。因为Transwell 培养系统可以用来研究细胞共培养、细胞趋化、细胞迁移、细胞侵袭等传统培养皿无法实现的研究项目,所以该实验模型进一步扩展了放射性粒子体外实验的研究范围。

图5 GUANG等设计的一种新型放射性粒子体外辐照模型
除这些模型以外,也有将放射性粒子直接放入细胞培养容器中的方案[18]。这样的方案弊端在于:如果采用的容器较大,细胞受照剂量率差别较大,达不到剂量学均一性要求;如果容器较小,很可能会存在实验后存活细胞数量不够、对照组细胞很快长满容器-影响实验观察时间、相邻容器内粒子互相干扰等问题。因此,可以做较简单的观察项目,并不适于较为深入的机制方面的研究。
2 展望
经过多年的发展,放射性粒子体外辐照模型已发展相对成熟,然而仍需在剂量分布均一性方面进行改善。按照目前的模型,改善剂量分布均一性的办法是可以增加放射源与照射平面的距离,不过增加距离会导致照射平面受到的剂量率降低,同时也会增大理论计算值与实际测量值之间的误差[19]。另外,在理论计算照射平面受照剂量时,如何避免干扰因素(比如界面效应)、如何还原计算公式所要求的条件、如何使用更精确的剂量测量设备验证模型照射平面的实际受照剂量等细节问题也需要进一步思考。随着细胞培养技术、材料学技术和剂量学研究的进步,以后可能有更好的解决方案问世。
