未破裂主动脉窦动脉瘤合并房间隔缺损误诊血性囊肿1例
2024-02-26付启航王小丛
佟 琳,付启航,王小丛,姜 舒,徐 卉
(吉林大学第一医院 超声诊断中心,吉林 长春130021)
1 临床资料
患者女,17岁,就诊前半月,活动期间出现胸闷、气短,伴有脸色苍白、嘴唇发紫,蹲踞休息数分钟后症状缓解,在当地医院行心脏彩超检查,提示:心脏肿物。为进一步诊治就诊于吉林大学白求恩第一医院。入院时查体:体温36.6℃,呼吸20次/min,脉搏98次/min,血压102/83 mmHg,身高142 cm,体重35.8 Kg,尚未初潮,心率规整,瓣膜听诊区未闻及病理性杂音。实验室检查未见明显异常。经胸壁超声心动图(transthoracic echocardiography,TTE)检查:EF:70%。各房室内径大小正常,右心比例偏大。室间隔、左室后壁厚度正常。室间隔运动不协调。右心近三尖瓣瓣环处可见一34 mm×33 mm的近似囊性回声肿物,位于三尖瓣前方,因巨大肿物遮挡三尖瓣结构显示不清(图1),三尖瓣瓣口血流偏心,最大流速127 cm/s。肿物内部可见血流信号,受声窗条件限制,未能明确探查血流来源。TTE提示:右房室瓣环处囊性占位性病变,不除外血性囊肿,建议进一步检查。右心声学造影检查:右房、右室顺序显影,三个心动周期后左房、左室内可见大量微泡回声,右心肿物内亦可见造影剂回声,微泡浓度与左心类似(图2)。提示卵圆孔未闭、右心肿物与心腔或血管之间有血流相通。为进一步确诊行磁共振心脏功能增强检查:右心可见一类圆形异常信号,与三尖瓣瓣环关系密切,随心动周期在右房与右心室之间往复运动,黑血序列显示不清,亮血序列呈稍高信号,T2WI-FS呈明亮高信号,边界清楚,首过灌注病灶可见快速渐进性强化,延迟增强呈均匀一致高信号,与血池信号接近。核磁提示右心房与右心室之间占位性病变,考虑血管瘤可能性大(图3)。另行冠状动脉CTA检查,未见明确异常(图4)。家属及本人一致决定行手术治疗。术前为进一步获取肿物信息,行经食管超声心动图(transesophageal echocardiography,TEE)检查:提示房间隔中部不连续,缺损处可见左向右分流;食管中段右室流出道切面显示囊性肿物囊壁似与左冠状窦、无冠状窦壁相连,心室舒张期可见右心血流绕行肿物(图5),心室收缩期见有五彩血流经窦口射入窦瘤内(图6)。最终TEE超声提示为主动脉窦动脉瘤合并房间隔缺损。
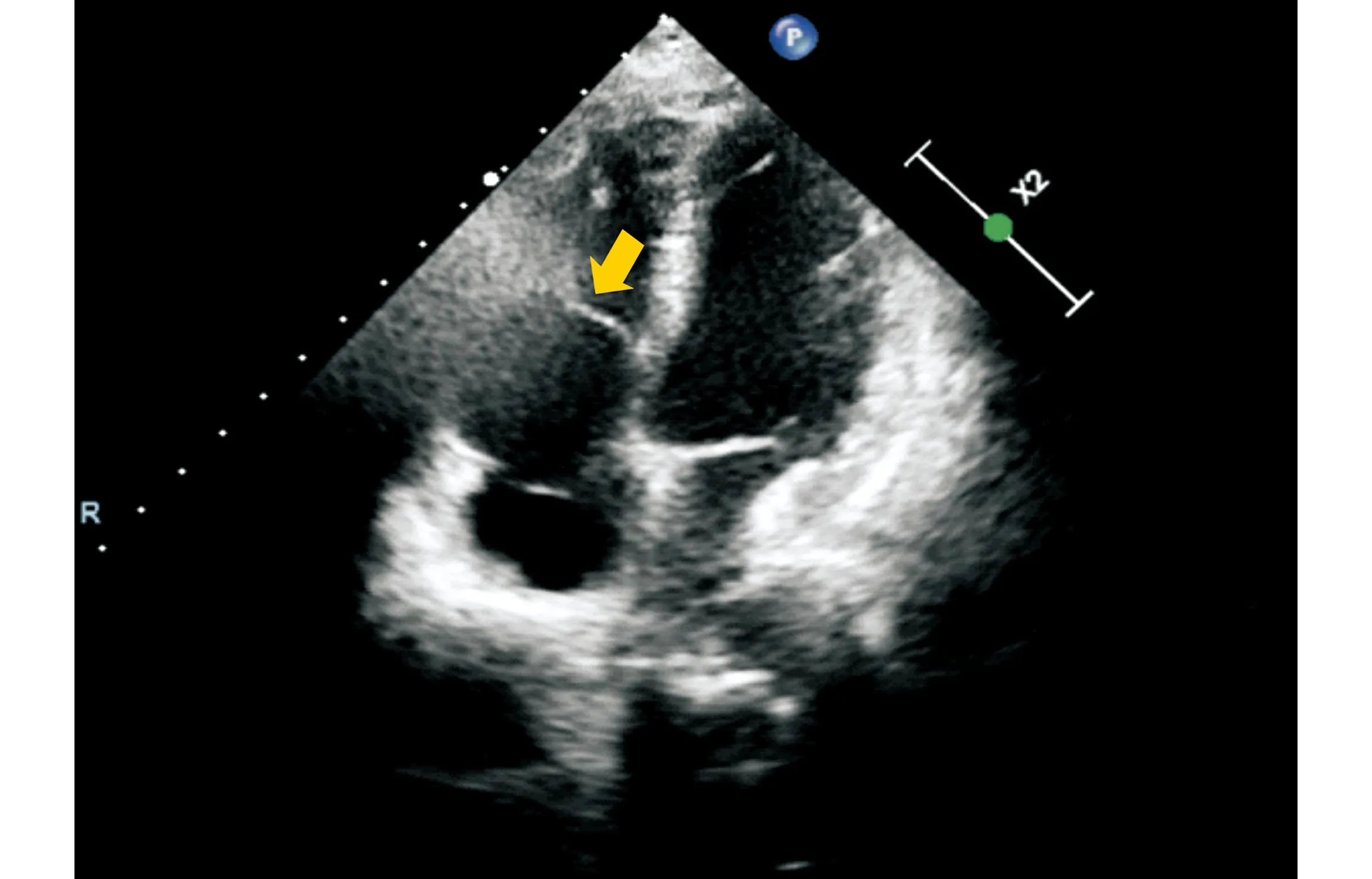
图1 心尖四腔心切面,囊性肿物遮挡三尖瓣结构

图2 注入右心造影剂后,肿物内见微泡回声,浓度与左心类似

图3 增强CMR显示病灶与血池信号接近

图4 冠脉CTA未见明显异常
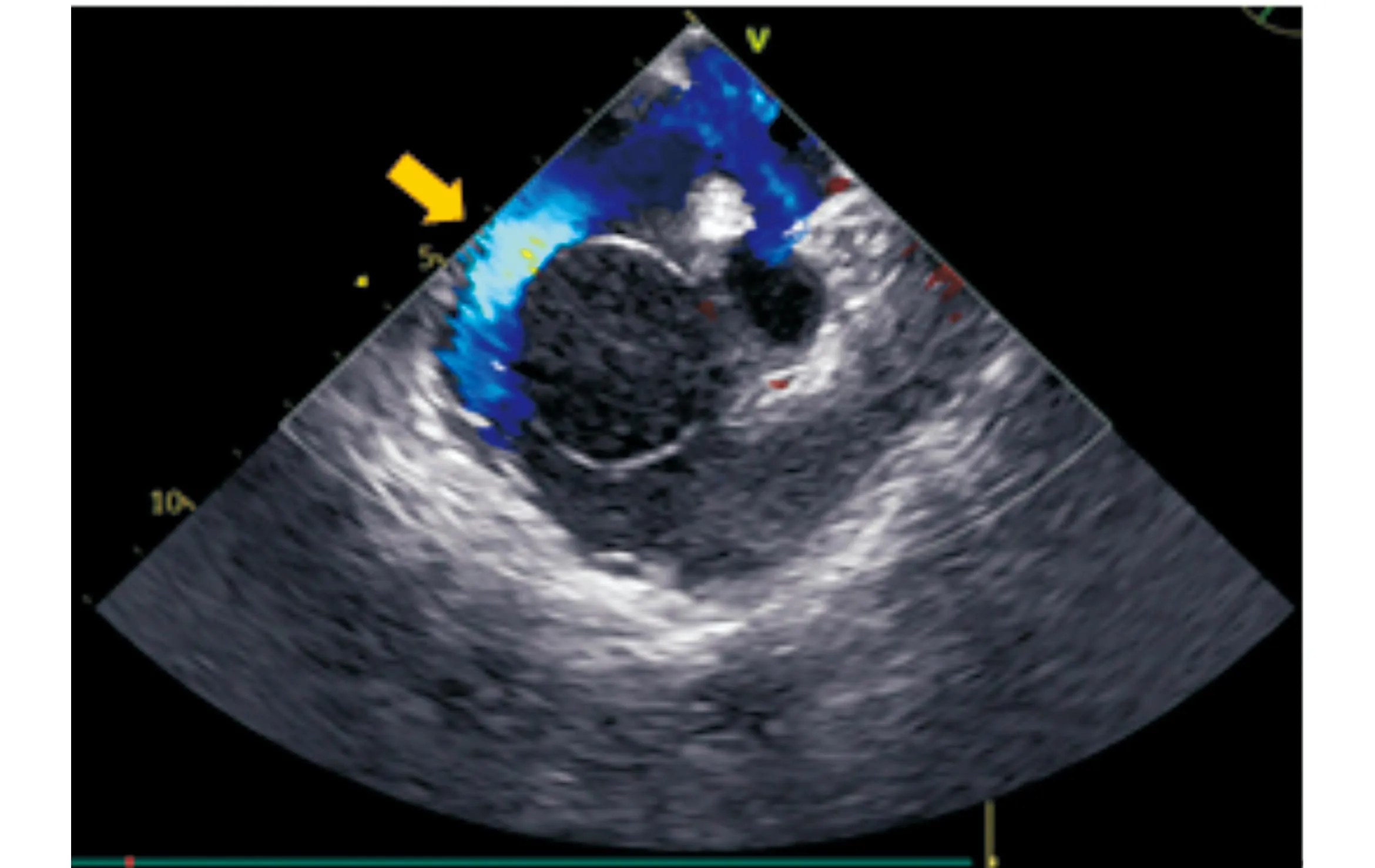
图5 心室舒张期可见右心血流绕行肿物
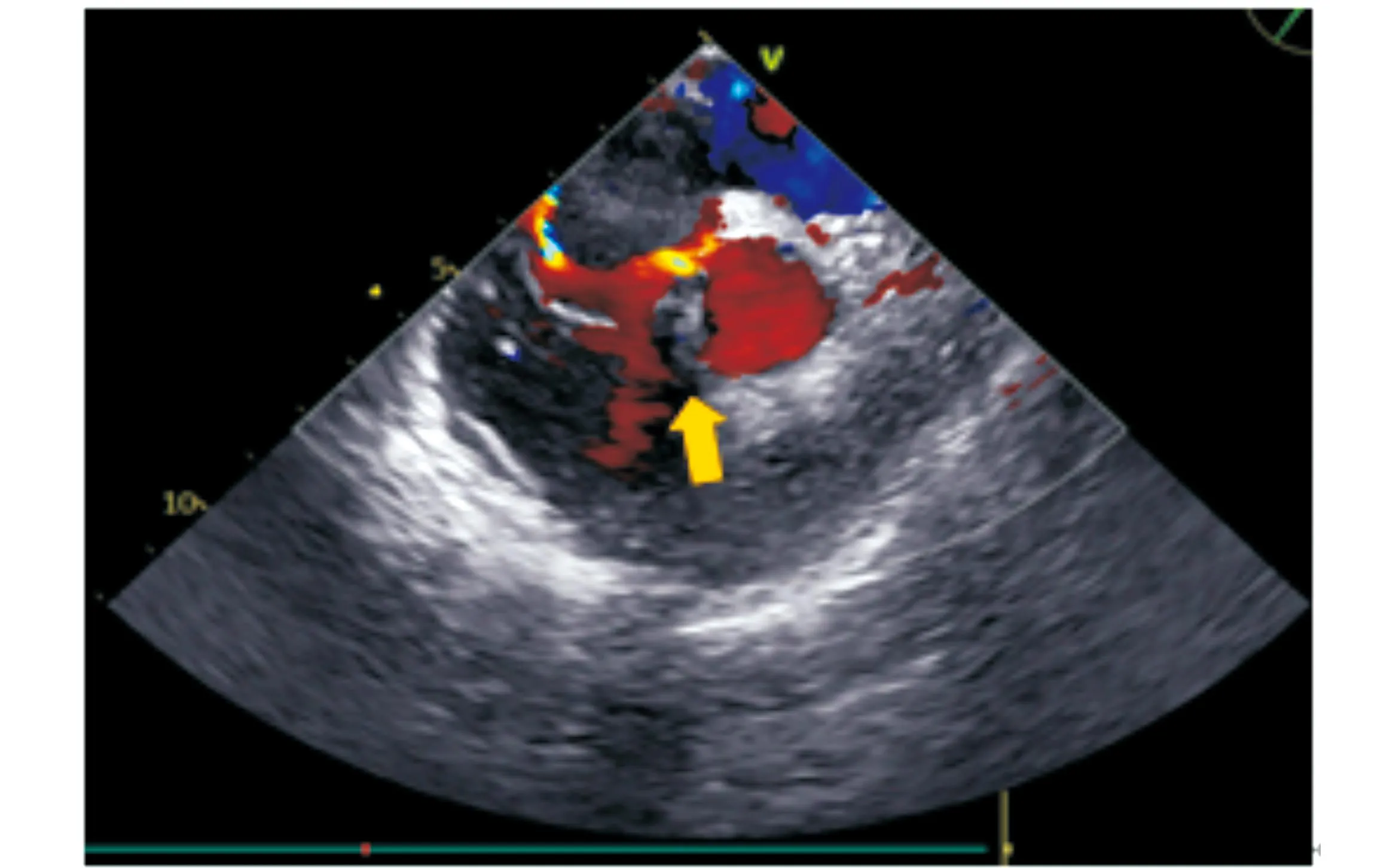
图6 TEE食管中段右室流出道切面:肿物囊壁与主动脉窦相连,心室收缩期见有五彩血流经窦口射入窦瘤内
术中切开右心房,内见囊状肿物,与周围组织无黏连,可自由通过三尖瓣瓣口,根部位于三尖瓣前叶、隔叶交界处右房侧,切开肿物根部见大量血液流出,考虑为巨大主动脉窦动脉瘤,行主动脉窦成形术。另见中央型房间隔缺损,行房间隔缺损修补术。最终术后病理诊断:动脉壁组织呈囊性扩张,伴纤维组织增生、玻璃样变性及局灶钙化,该肿物符合主动脉窦动脉瘤特征(图7、8)。

图7 SOVA瘤壁囊壁样组织,总体积3.5 cm×2 cm×1.5 cm,壁厚0.1 cm,内壁淡褐色、尚光滑
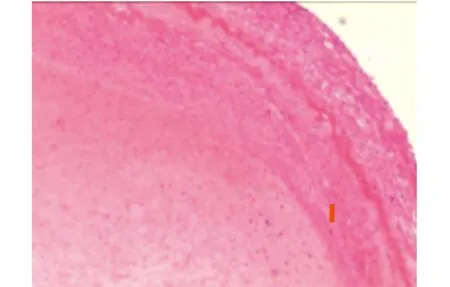
图8 光镜所见:动脉壁组织呈囊性扩张伴纤维组织增生、玻璃样变性及局灶钙化
患者住院期间病情平稳,术后6日出院。
2 讨论
主动脉窦动脉瘤(Sinus of Valsalva aneurysms,SOVA)指主动脉瓣环和窦管交界处之间的主动脉根部异常膨出,是一种罕见的心脏血管缺陷疾病[1],好发于亚洲男性。尸检研究表明,SOVA在西方国家普通人群中的发生率不到 0.1%,仅为亚洲人群发病率的1/5[2]。SOVA可由多种病因引起,分为先天性和后天性两大类。先天性SOVA通常由于主动脉壁弹力纤维与主动脉瓣环融合异常,主动脉窦壁结构薄弱,在高压血流作用下形成囊样窦瘤突入心腔,严重者甚至破裂[3]。后天性SOVA通常与结缔组织损伤有关,如大动脉炎、马凡综合征、梅毒、感染性心内膜炎等,也可继发于外源性或医源性损伤[4]。本例患者17岁,身高142 cm,体重35.8 Kg,尚未初潮,发育迟缓,实验室检查未见明显异常,故考虑先天发育异常导致的SOVA。
1962年,SAKAKIBARA[5]首次将SOVA根据起源及破入位置分成4型,Ⅰ型起源于右冠状窦左侧,于肺动脉瓣下突入右心室,突出的瘤体可阻碍右室流出道,造成漏斗部狭窄,此型最常见且易合并室间隔缺损,产生左向右分流,继发主肺动脉增宽、左心增大;Ⅱ型窦瘤从右冠状窦中部突入右心室;Ⅲ型起自右冠状窦右部,根据破入右心室、右心房又分为Ⅲv型和Ⅲa型;Ⅳ型主动脉窦瘤更为少见,起自无冠状窦突入右心房。LUO[6]为将分型更适用于临床手术,对其进行了改良并将其他罕见情况如突至左心房、肺动脉、左心室或其他结构的主动脉窦瘤定义为V型。本例患者属于少见的IIIa型SOVA合并房间隔缺损。
未破裂的SOVA常因无明显临床症状而不易被发现,少数患者由于并发主动脉瓣狭窄或反流、右心室流出道梗阻伴三尖瓣反流、冠状动脉供血不足、急性肺水肿,而出现非特异性的心绞痛、心律失常、呼吸困难等症状[7]。随着瘤体渐进性增大,窦壁继续变薄甚至破裂,可引发急性充血性心衰等严重后果[8]。有研究统计,SOVA破裂且未经治疗的预后极差,预计寿命仅为1年[4]。为防止病情进一步的恶化甚至死亡,早期诊断和及时的手术干预十分关键[9]。TTE是SOVA筛查的首选方法[10],二维图像上可观察到未破裂的主动脉窦壁局部呈“风袋样”外膨[11],边界完整,未与心腔有异常相通。窦瘤破裂后,多普勒成像可见破口处存在全期左向右的五彩湍流信号,由于血流动力学变化,心腔、动脉出现相应增大增宽。TEE由于其更好的声窗条件、更高的图像质量,对心内精细结构的成像更有优势,可以为TTE结果不明确的患者提供进一步评估[12]。
本例患者窦瘤自三尖瓣前叶和隔叶之间的薄弱处突入右心房,巨大的SOVA通过三尖瓣启闭侵入右心室。而因房间隔缺损而产生的左向右分流可能增加了三尖瓣功能性狭窄对右心造成的容量负荷,加快了右心腔增大的进程。受声窗条件限制和巨大瘤体遮挡,TTE中未能明确显示肿物的囊壁与主动脉窦之间的结构关系,故误诊为血性囊肿。TEE检查更精确地评估了SOVA于心内的结构、与瓣膜之间的位置关系,心脏瓣膜受损的程度,同时检出SOVA的合并症——房间隔缺损,最终于术前做出了正确的诊断,为后续治疗奠定了坚实的基础。
SOVA超声表现与心内血性囊肿相似,两者应相鉴别。二维图像上,SOVA位于主动脉瓣上,呈囊袋状,未破裂前瘤体内可探及舒张期五彩镶嵌样的湍流信号,破裂后可于窦瘤瘤壁探及双期连续性左向右分流信号[13]。声学造影时瘤体内造影剂灌注程度与主动脉窦内相似。血性囊肿呈灯泡状,多单发,位于二尖瓣及三尖瓣瓣叶,是由内皮细胞形成的囊壁及内部潴留的血液构成的良性囊肿,少数囊肿内腔可与心室通过内皮细胞形成的管道相互沟通[14],胡文文[15]收集了13例心腔内血性囊肿的患者,仅有一例瘤颈与周围小血管相通。多数瘤体声学造影其内无造影剂充盈信号。
由于SOVA潜在的恶性结果,尽早诊断并手术干预尤为重要。TTE是快速诊断疾病的首选方法,TEE可补充TTE的短板,并在术中引导、术后长期复查周边有无异常血流及评价心脏整体血流动力学情况中起到重要作用。评价预后的过程对超声十分依赖,超声在整个诊疗过程中均发挥不可替代的重要作用。
