基于UHPLC-Q-TOF-MS/MS技术的百蕊颗粒入血成分研究
2024-02-26周思倩谭金桃王雅静龙红萍
周思倩,方 艳,谭金桃,王雅静,吴 娟,邵 乐,龙红萍*
1湖南中医药大学第一附属医院;2湖南省儿童医院药学部,长沙 410007;3湖南中医药大学,长沙 410208
百蕊颗粒是由百蕊草单味药组成的颗粒制剂,具有抗菌消炎、清热解毒、止咳之功效,现代临床上多用于治疗小儿扁桃体炎、支气管炎及各种呼吸道感染等症[1,2]。中药有效成分多以血液为介质输送到靶点(肠道直接起作用及外用药除外)从而发挥作用,因此分析口服中药后体内活性成分对于中药药效物质基础研究十分重要[3-5]。本课题组前期已采用液质联用技术对百蕊草醇提物的化学成分进行系统性分析[6],发现百蕊草中存在许多有效成分,如黄酮类、生物碱类等化合物,既往的文献研究多为单味药的化学成分和质量控制研究,缺少对百蕊颗粒体内入血成分和体内代谢过程的研究,且药效物质基础尚不明确。
四极杆飞行时间质谱技术因其灵敏度高、分辨率高的特点,可以快速高效地对中药中的化学成分进行分析,已广泛运用在中药药效物质基础研究等领域[7,8]。因此,本课题组在前期研究基础上继续采用超高效液相色谱-四极杆飞行时间质谱(UHPLC-Q-TOF-MS/MS)技术,对百蕊颗粒入血成分和代谢过程进行分析,为药效物质基础研究提供参考依据,对于中成药的质量控制和开发利用具有重要意义。
1 材料与方法
1.1 仪器
Agilent 1290UPLC-6540 Q-TOF色谱-质谱联用仪(美国Agilent科技公司);超声波清洗机(上海科导超声仪器有限公司),S-23高速台式离心机(湖南湘仪仪器有限公司);电子分析天平(日本SHIMADZU公司);LABCONCO CentriVap型离心浓缩仪(Labconco,美国)。
1.2 材料
百蕊颗粒购于安徽九华华源药业有限公司(批号为Z20090694);色谱级甲醇、质谱级乙腈均购于德国(Merck Millipore公司);蒸馏水(深圳屈臣氏蒸馏水有限公司);甲酸铵(质谱级,美国Fisher公司)。健康SPF级雄性SD大鼠,体质量(180~220)g,购自湖南斯莱克景达实验动物有限公司,常规饲养于湖南中医药大学第一附属医院医学创新中心动物中心,动物许可证号为SCXK(湘)2019-0004,经湖南中医药大学第一附属医院动物伦理审查,伦理审批号为ZYFY2021040701。
1.3 方法
1.3.1 灌胃药液制备
将百蕊颗粒置于研钵研至粉末状,准确称量144 g百蕊颗粒粉末,加100 mL纯水溶解,超声溶解30 min后,配制成质量浓度为0.850 5 g/mL的混悬液(按照临床剂量折算成大鼠灌胃给药剂量每天8.50 g/kg),摇匀静置,储存至4 ℃冰箱中,备用。
1.3.2 供试品溶液制备
精密称量百蕊颗粒粉末2 g,置25 mL容量瓶,加20 mL甲醇溶解,超声提取30 min,取上清液离心5 min(8 000 r/min),用0.22 μm微孔滤膜过滤,待测。
1.3.3 血清样品制备
大鼠随机分为空白对照组和给药组,每组各6只,给药组灌胃百蕊颗粒灌胃液,空白组生理盐水灌胃,每天2次,连续灌胃5 d,在最后一次给药1 h后,对大鼠腹腔注射30 mg / kg 戊巴比妥麻醉,腹主动脉取血,静置1 h后,4 000 r/min离心10 min分离血清。取大鼠空白和给药血清各2 mL,分别加入3倍量甲醇沉淀蛋白,涡旋10 min后,置于冰浴中10 min,低温离心10 min,5 000 r/min。吸取上清液,用离心浓缩仪挥干;残渣加200 μL甲醇复溶,于12 000 r/min下离心5 min,取上清液用0.22 μm微孔滤膜过滤,待测。
1.3.4 色谱条件
Agilent ZORBAX Eclipse Plus C18(3.0 mm×100 mm,1.8 μm);流动相为0.1%甲酸水(A)-乙腈(B),梯度洗脱(0~5 min,5%→15%B;5~10 min,15%→35%B;10~20 min,35%→65%B;20~40 min,65%→85%B);进样量:2 μL;流速:0.4 mL/min。
1.3.5 质谱条件
采用电喷雾离子化源(ESI),正、负离子模式同时检测,扫描范围m/z100~1 700;干燥气温度325 ℃,流速为6.8 L/min;鞘气温度为350 ℃;毛细管电压为4.0 kV;Fragment电压为150 V;二级质谱扫描检测范围:m/z50~1 000;Fragment电压:10、20、40 V。
1.3.6 数据分析
采用Agilent MassHunter软件(B.07.00版) 采集正、负离子模式下各组数据,使用Agilent Masshunter Qualitative Analysis工作站中的分子特征提取(MFE)功能提取主要成分相关的特征离子,比对空白组及给药组血清的提取离子流图,再结合前期所分析的体外成分二级质谱信息、裂解规律、文献报道的分子式、保留时间等分析百蕊颗粒的入血成分。
2 结果
本研究通过比对分析百蕊颗粒含药血清及空白血清的质谱图信息数据,查阅数据库和文献报道,并结合分析质谱裂解规律,对大鼠口服百蕊颗粒后血清中的化学成分进行分析,在大鼠血清中共推测鉴定了30个成分,其中原型成分和代谢产物分别为20个和10个(见表1),其正、负离子模式下含药血清和空白血清总离子流图(total ion chromatogram,TIC)见图1,入血成分提取离子流图见图2。
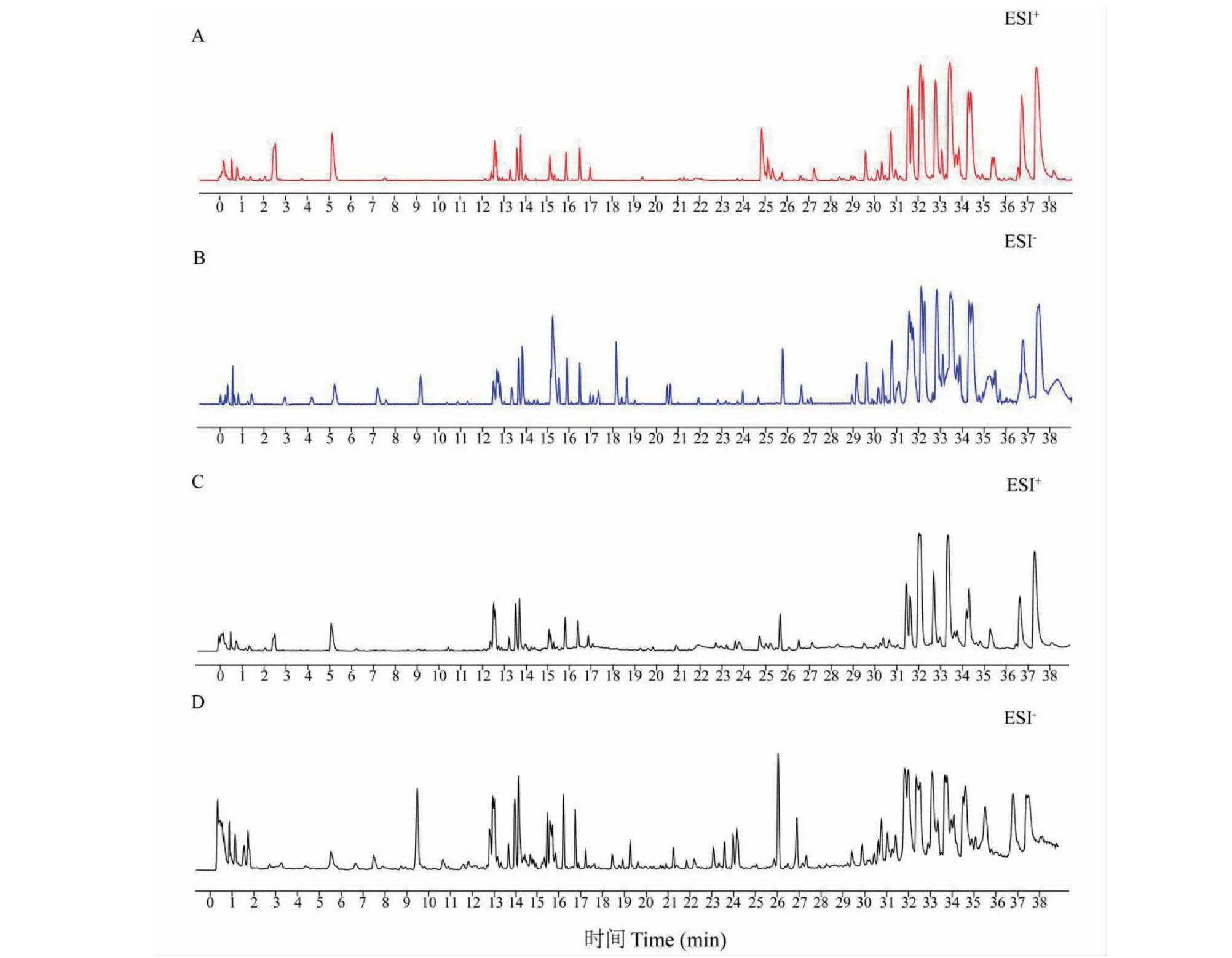
图1 正、负离子模式下各样品的TIC图
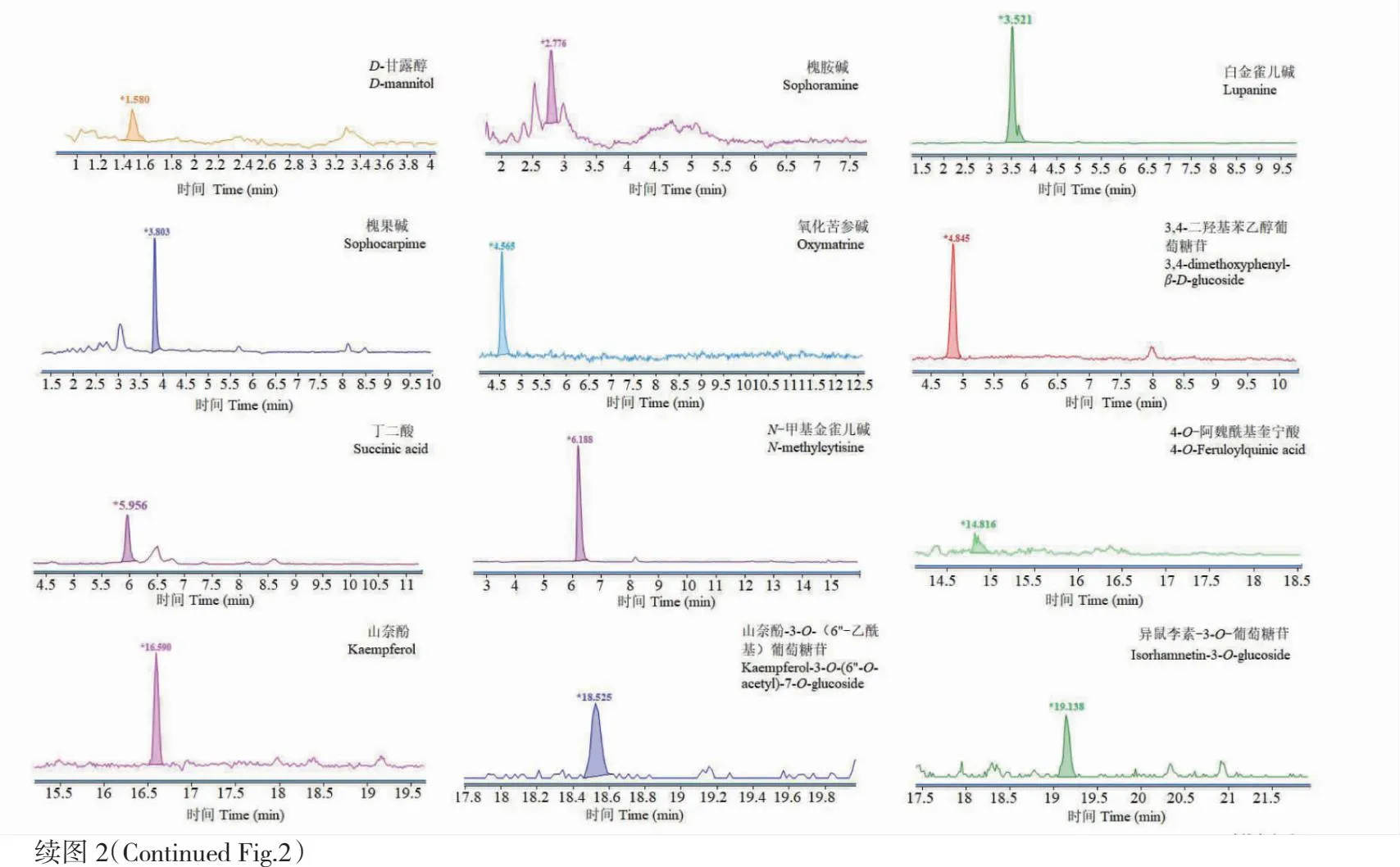
图2 百蕊颗粒20个原型成分在正、负离子模式下的提取离子流图
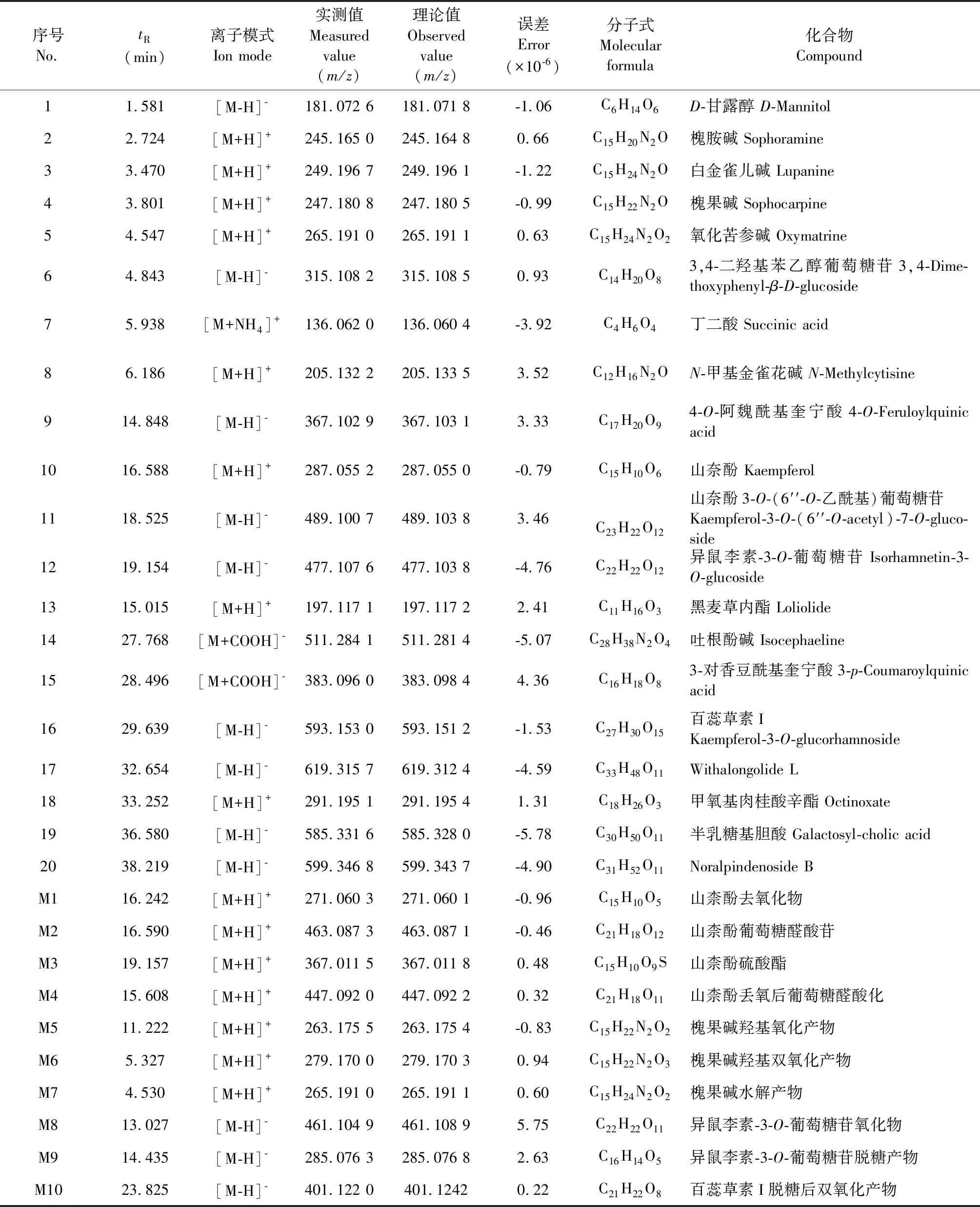
表1 大鼠灌胃百蕊颗粒后血清中的原型成分及代谢产物
3.1 原型成分分析
采用液质联用技术采集百蕊颗粒空白血清和含药血清数据,与前期鉴定出的体外化学成分进行比对,共检测到20个原型成分,包括6个生物碱类化合物和4个黄酮类化合物,3个有机酸类,2个糖苷类,2个萜类,1个内酯类,2个其他类,其原型成分结构图见图3。

图3 百蕊颗粒20个原型成分化学结构
以化合物8和11为例来进行解析。化合物8(tR为6.186 min)在正离子模式下检测到准分子离子[M+H]+为m/z205.132 2,其碎片离子包括[M+H-H2O]+(m/z186.995 8)、[M+H-C3H11N]+(m/z146.062 0)和[M+H-C6H7NO]+(m/z110.098 1),据文献报道,m/z146是金雀花碱型生物碱的特征碎片离子,为金雀花碱型生物碱C环裂解产生,同时金雀花碱型生物碱B环裂解产生m/z110.098 1的碎片离子,根据其碎片离子信息和相关文献报道[9],推测其为N-甲基金雀花碱(C12H16N2O),其MS/MS质谱图和可能裂解途径见图4和图5。化合物11(tR为18.525 min)在负离子模式下检测到准分子离子峰[M-H]-为m/z489.100 7,其二级碎片离子包括[M-H-C3H8O2]+(m/z412.249 3)、[M-H-C9H18O7]+(m/z284.035 8)和[M-H-C6H7NO]+(m/z266.726 0),m/z284.035 8分别失去H2O、CO基团得到m/z266.726 0和m/z256.036 2,根据其碎片离子信息和相关文献报道[10],推测其化合物11为山奈酚3-O-(6′′-O-乙酰基)葡萄糖苷(C23H22O12),其MS/MS质谱图和可能裂解途径见图6和图7。

图4 N-甲基金雀花碱质谱图
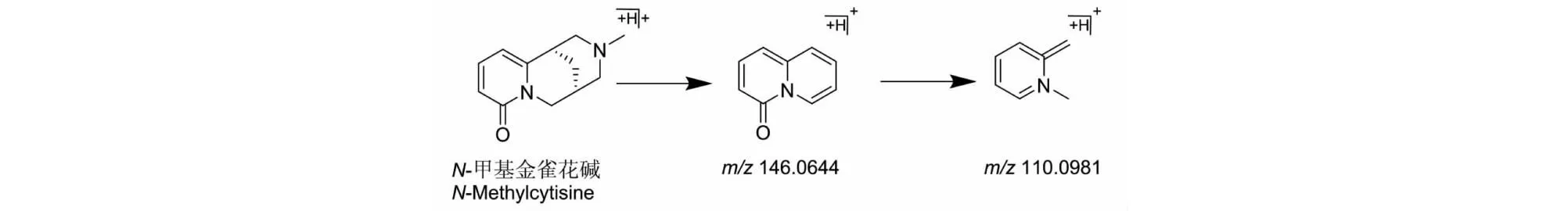
图5 N-甲基金雀花碱可能质谱裂解途径

图6 山奈酚3-O-(6′′-O-乙酰基)葡萄糖苷质谱图
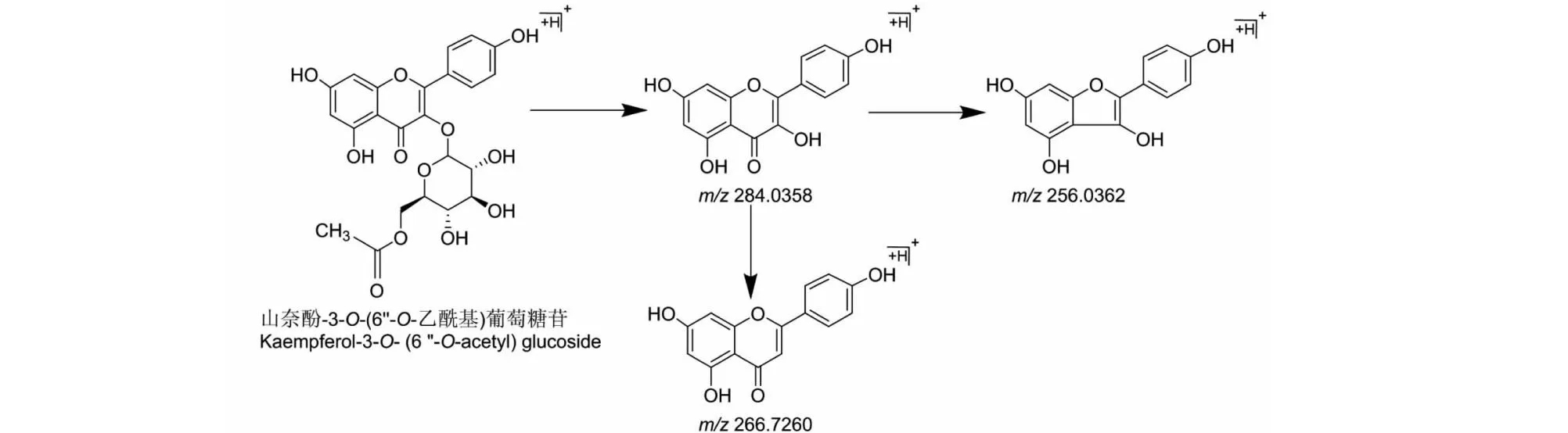
图7 山奈酚-3-O-(6′′-O-乙酰基)葡萄糖苷可能质谱裂解途径
3.2 代谢产物分析
通过Agilent Masshunter软件分析结合相关文献报道,在原型成分的基础上检测到10个代谢产物,其中代谢途径包括还原反应和水解反应、硫酸化反应和葡萄糖醛酸结合反应,见图8和图9。
图8 体内10个代谢产物的提取离子色谱图
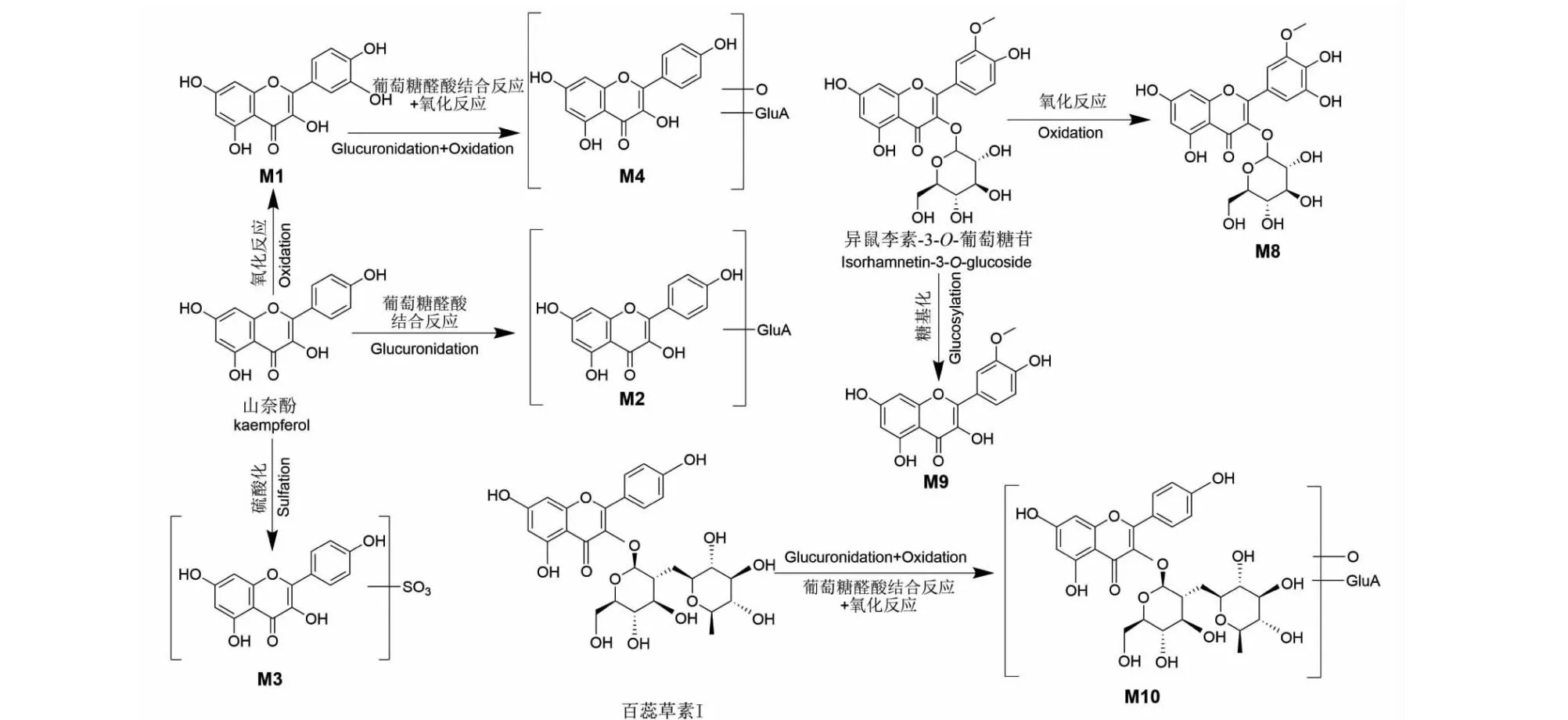
图9 百蕊颗粒中黄酮类化合物体内代谢途径
代谢产物M1、M2(tR分别为16.242、16.590 min),正离子模式下其准分子离子峰分别为m/z271.060 1和463.087 3[M+H]+,代谢产物M1准分子离子峰相比山奈酚准分子离子m/z287.055 2[M+H]+少了16 Da,推测代谢产物M1可能为山柰酚去氧化产物;代谢产物M2准分离子离子峰相比山奈酚准分子离子m/z287.055 2[M+H]+多了176 Da,推测M2可能为发生葡萄糖醛酸反应的产物,根据软件计算M1分子式为C15H10O5,M2分子式为C21H18O12。
代谢产物M3、M4(tR分别为19.157 min和15.608 min),正离子模式下准分子离子峰分别为m/z367.011 5和447.092 0[M+H]+,代谢产物M3准分子离子峰与山奈酚准分子离子m/z287.055 2 [M+H]+多了80 Da,推测M3为与硫酸盐结合的产物,M4准分子离子峰与山柰酚准分子离子m/z287.055 2[M+H]+多了160 Da,推测M4可能为山柰酚发生还原反应后的糖基化产物,根据软件计算该分子式为C15H10O9S和C21H18O11,推测M3、M4分别为山奈酚的硫酸酯和山奈酚丢氧后葡萄糖醛酸化产物。
代谢产物M5~M7(tR分别为11.222、5.327、4.530 min),正离子模式下的准分子离子峰分别为 [M+H]+m/z263.175 5、279.170 0和265.191 0。代谢产物M5准分子离子峰与槐果碱母离子相差16 Da,推测可能为槐果碱氧化反应的代谢产物;代谢产物M6准分子离子峰与槐果碱母离子相差32 Da,推测可能为槐果碱双氧化反应的代谢产物;代谢产物M7准分子离子峰与槐果碱母离子相差18 Da,推测可能为槐果碱水解反应的代谢产物,根据软件计算M5~M7分子式C15H22N2O2、C15H22N2O3和C15H24N2O3,推测M5为槐果碱羟基氧化物,M6为槐果碱羟基双氧化物,M7为槐果碱水解产物。
代谢产物M8、M9(tR为13.027、14.435 min),负离子模式下准分子离子峰分别为m/z461.104 9和285.076 3 [M-H]-。代谢产物M8准分子离子峰与异鼠李素-3-O-葡萄糖苷母离子相差16 Da,推测可能为异鼠李素-3-O-葡萄糖苷氧化反应的代谢产物;代谢产物M9准分子离子峰与异鼠李素-3-O-葡萄糖苷母离子相差162 Da,推测可能为异鼠李素-3-O-葡萄糖苷发生去糖基化反应的代谢产物,根据软件计算该分子式为C22H22O11和C16H14O5,推测M8和M9分别为异鼠李素-3-O-葡萄糖苷氧化物和脱糖产物。
代谢产物M10(tR为23.825 min),负离子模式下准分子离子峰为 [M-H]-m/z401.122 0,与百蕊草素I准分子母离子相差192 Da,推测可能为百蕊草素I发生葡萄糖醛酸反应后的氧化代谢产物,根据软件计算该分子式为C21H22O8,推测M10为百蕊草素I葡萄糖醛酸化后氧化产物。
大鼠口服灌胃百蕊颗粒后,在其含药血清的原型成分中发现苦参碱类和金雀花碱类生物碱均被检测到,推测苦参碱类和金雀花碱类生物碱能直接入血发挥药效作用;原型成分中黄酮类化合物主要以山柰酚苷元为主,然而在给药后大鼠血清中原型成分未检测到芦丁等黄酮-O-双糖苷类化合物的质谱信号,推测黄酮-O-双糖苷类化合物可能在动物体内水解成苷元,导致其主要以代谢产物形式存在于体内;在代谢产物中,I相代谢产物主要以氧化产物为主,II相代谢产物尤以硫酸化、葡萄糖基化、葡萄糖醛酸化。
3 讨论与结论
本研究采用UHPLC-Q-TOF-MS/MS技术对百蕊颗粒吸收入血成分进行分析,从大鼠血清中共检测到20个原型成分和10个代谢产物。其中分析出的体内原型成分主要为白金雀儿碱、槐果碱等生物碱类化合物以及山柰酚、百蕊草素I等黄酮类化合物;体内代谢产物主要是山柰酚经氧化、葡萄糖醛酸化反应生成和槐果碱经氧化、水解反应生成,表明生物碱类和黄酮类是进入体内的主要成分,也可能是发挥药效的潜在活性成分。
现代药理学研究表明黄酮类和生物碱类化合物具有抗炎、抗菌、抗病毒、抗氧化等药理功能[11,12],先前研究报道百蕊草中山奈酚衍生物抗炎作用与有效抑制细胞内活性氧的产生以及p38 MAPK和活化蛋白1的激活有关[13],山柰酚作为一种天然黄酮醇,在抑制炎症细胞功能以及抑制促炎细胞因子和趋化因子的表达方面有着强大作用[14]。百蕊草素I可以通过作用于NF-κB和MAPK通路抑制炎性细胞因子TNF-α、IL-6、IL-1β等的表达,从而改善感染肺炎的小鼠肺部的肺水肿[15,16]。生物碱类化合物能明显抑制大肠杆菌、金黄色葡萄球菌等微生物的生长[17],槐果碱具有较强的抗炎镇痛作用,可通过抑制NF-κB信号通路来减少炎症的发生[18]。氧化苦参碱可通过抑制NF-κB信号通路,降低炎症因子IL-6和IL-8的表达,从而发挥抗炎作用[19]。
综上所述,本研究通过采用UHPLC-Q-TOF-MS/MS技术阐明了百蕊颗粒的入血成分及代谢产物,这些化合物可能与百蕊颗粒抗炎抗菌等药效密切相关,对于明确中药药效物质基础研究和中药质量标准的提升具有重要意义,为进一步了解其作用机制和临床应用提供参考依据。
