弱碱性吸收剂碳捕集及CO2富液生物再生性能
2024-02-22赵敏楠张佳音张新妙栾金义陆丁香赵鹏宇陈湘泽武振康
赵敏楠,张佳音,张新妙,徐 恒,栾金义,陆丁香,赵鹏宇,陈湘泽,武振康
(1.中国矿业大学(北京) 化学与环境工程学院,北京 100089;2.中石化(北京)化工研究院有限公司,北京 100013)
0 引 言
随着全球人口增加和经济发展,人类社会对能源需求量不断增加,煤炭、石油等化石能源的使用造成大量CO2排放,CO2过量排放是导致全球气温上升并引起系列气候变化的重要原因之一。为应对气候问题、减少碳排放,2020年,我国提出“双碳”目标。虽然我国太阳能、风能等可再生能源发展迅速,但化石能源在一次能源消费中仍占82.7%[1],其中煤炭消费量占能源总消费量的56.2%[2],且在未来很长一段时间内,煤炭等化石能源仍是保障我国能源安全的稳定器和压舱石[1]。为实现双碳目标,在化石能源利用过程中开展CO2捕集、利用与封存(CCUS)十分必要[3]。
基于醇胺的化学吸收法具有吸收速率快、工艺简单、适于处理低浓度CO2等优点,是目前应用最广泛的技术[4-5],但运行成本高,尤其在CO2富液再生环节,能耗在3.5~4.0 GJ/t(以CO2计),占总运行成本的60%~80%[5-6]。新型CCUS工艺开发是解决吸收剂再生能耗高的重要途径之一。碳捕集转化一体化工艺可直接对CO2富液进行转化,同时实现吸收剂再生,省去分子态CO2分离环节,有望大幅降低捕集转化整体成本[7]。碳捕集转化一体化工艺中的转化过程可通过矿化[8]、电化学还原[9]、生物转化等方法实现。其中,生物转化具有反应条件温和、CO2转化利用率高、副产物少、绿色经济等优点,近年来受到广泛关注[10-11]。如邱依婷[12]以氨水、K2CO3作为吸收剂捕集CO2,并利用微藻将吸收液中的CO2转化为微藻生物质。除微藻转化外,生物甲烷化过程同样具有与碳捕集过程相耦合的潜力[13]。首先,利用碳酸盐、碳酸氢盐、微生物营养液配制弱碱性吸收剂(pH=10),并进行CO2吸收,吸收剂中的活性组分碳酸盐与CO2反应生成碳酸氢盐;其次利用甲烷化微生物和绿氢将吸收液中的碳酸氢盐转化为易与水溶液分离的产物CH4和碳酸盐[14],吸收剂再生,CH4作为一种典型的碳、氢储运载体,应用前景广阔[15]。
为评价碳捕集耦合生物甲烷化工艺的可行性,笔者在填料塔中考察弱碱性吸收剂在流通模式和循环模式下模拟烟气CO2的吸收性能;对CO2吸收富液开展生物甲烷化试验,结合微生物群落分析,考察弱碱性吸收剂的生物再生性能。
1 试 验
1.1 试验材料
模拟烟气为N2和CO2组成的混合气,N2和CO2体积分数分别为85%和15%。弱碱性吸收剂为4.2 g/L NaHCO3、6.0 g/L Na2CO3、微生物营养液配制成pH=10溶液。微生物营养液主要由以下物质组成:NaCl (0.25 g/L)、NH4Cl (1.00 g/L)、CaCl2·2H2O(0.01 g/L)、MgCl2·6H2O (0.01 g/L)、KH2PO4(0.11 g/L)、K2HPO4·3H2O (0.22 g/L)、Na2SO4(0.02 g/L)、微量元素母液1 mL/L[16-17]以及维生素母液5 mL/L[16-17]。
填料塔由高硼硅玻璃加工而成,高1.5 m,内径50 mm,填料为6 mm×6 mm×2 mm的陶瓷拉西环,比表面积为789 m2/m3,空隙率为73%,填料高度1.2 m。接种污泥取自北京市某污水处理厂,其总固体为15.9 g/L,挥发性固体为6.9 g/L。采用5 mm×5 mm×5 mm海绵材料,堆积密度为0.03 g/cm3,比表面积为35.5 m2/g,空隙率为89.4%。
1.2 试验过程
1.2.1 弱碱性吸收剂吸收CO2试验
1)流通模式。弱碱性吸收剂吸收CO2试验系统流通模式如图1(a)所示,模拟烟气经质量流量控制器调节流量后从填料塔底部进入,贫液罐内吸收剂(由于流通模式下吸收剂用量大,此处用自来水代替微生物营养液配制吸收剂)经蠕动泵从填料塔顶部喷淋而下,气体和液体在填料表面发生气-液传质,CO2吸收富液由塔底部排入富液罐,净化后的气体从塔顶部排出。液体和气体流量分别设置为0.5~1.3、0.4~1.2 L/min(本文所有气体流量均为标准状况下气体流量)。每个试验工况的第0、5、10、15、20 min从塔顶部气体出口处采集气体,测定气体组分,计算CO2去除率、体积总传质系数KGaV;待气体组分稳定后,采集CO2吸收富液,测定其pH,并计算NaHCO3、Na2CO3浓度。每个试验工况重复2次。
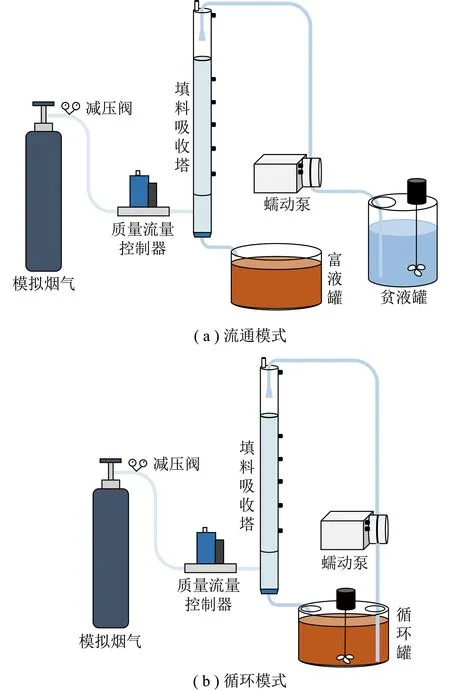
图1 弱碱性吸收剂吸收CO2试验系统示意
2)循环模式。弱碱性吸收剂吸收CO2试验系统循环模式如图1(b)所示,基于流通模式试验结果,选择气体流量0.6 L/min、液体流量0.7 L/min工况开展循环吸收试验,液体循环周期设置为10 min。循环罐中初始吸收剂体积为7 L,循环罐的液体经蠕动泵从填料塔顶部喷淋而下,形成的CO2吸收富液从塔底部排回循环罐。试验进行第0、2.5、5、10、20、30、40、50、60 min从塔顶部气体出口处采集气体,测定气体组分,并于第0、10、20、30、40、50、60 min采集吸收富液,测定其pH,并计算NaHCO3、Na2CO3浓度和溶解的总无机碳量。循环吸收试验重复2次。
1.2.2 CO2吸收富液生物再生试验

2)循环CO2化学吸收-富液生物再生试验。采用有效容积67 mL的厌氧瓶作为反应器,设置2个平行试验。首先进行CO2化学吸收,向各厌氧瓶内充入定量CO2,放入水浴振荡器内振荡反应30 min(35 ℃、130 r/min);待吸收剂吸收饱和后,检测瓶内剩余CO2量,计算CO2吸收量。之后进行富液生物再生,对各厌氧瓶进行氮气吹脱5 min,排出瓶内剩余CO2;根据上一步试验得出的CO2吸收量,计算再生试验所需全部H2投加量(CO2吸收量×4),并分4次注入厌氧瓶内,每次注入H2后,将厌氧瓶放入水浴振荡器中(35 ℃、130 r/min)。每12 h检测瓶内气体组分,计算CH4产量;待注入的H2消耗完后,进入下一周期CO2化学吸收和富液生物再生试验,共计5个周期。
1.3 分析与计算方法
通过pH测定仪(哈希HQ40d)测定pH。利用气相色谱仪(Shimadzu GC-2014)测定[18]气体组分(H2、CH4和CO2)。
1)通过测定填料塔进、出气口处CO2体积分数,计算其物质的量比和CO2去除率η:
η=(Yin-Yout)/Yin,
(1)
式中,Yin为进气口CO2物质的量比;Yout为出气口CO2物质的量比。
2)体积总传质系数计算方法[19]为:根据双膜理论,在气液接触稳态过程中,CO2传质速率NA可用总传质系数KG、气相总压p和平衡推动力表示:
NA=KGp(y-y*),
(2)
根据质量守恒定律,对于填料高度dZ的传质单元,有以下微分方程:
NAaVdZ=-VdY,
(3)
整理得体积总传质系数KGaV为
(4)

(5)
方程两边同时积分,得
(6)
式中,y为CO2在气相中体积分数;y*为与液相主体中CO2浓度成平衡的气相体积分数;aV为单位体积填料的有效传质面积,m2/m3;Z为填料高度,m;V为惰性气体流量,mol/(m2·h)。
3)溶解的总无机碳量(Tic)计算方法[20]:假设在平衡状态下,相同化学组分代表溶解的总无机碳:
(7)
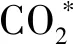
(8)
(9)
(10)
(11)
(12)
α0、α1和α2作为pH和反应平衡常数k1、k2的函数,计算公式为
(13)
(14)
(15)
式中,C(H+)=10-pH。
Tic无法测量,但可用总碱度(ηALCC)代替,即
(16)
因此,
Tic=ηALCC/(α1+2α2)。
(17)
采用滴定法计算ηALCC,即采用C(HCl)=0.1 mol/L 的HCl标准溶液滴定水样(15 mL),总碱度滴定终点为pH=3.7,记录滴定所用HCl体积V(HCl),ηALCC计算公式为
(18)
4)高通量测序分析。对需分析的生物膜样品进行DNA提取和PCR扩增。细菌PCR扩增采用338F_806R为引物,引物序列分别为ACTCCTACGGGAGGCAGCAG和GGACTACHVGGGTWTCTAAT;古菌采用巢式PCR扩增法,第1轮引物为Arch340F_Arch1000R,引物序列分别为CCCTAYGGGGYGCASCAG和GGCCATGCACYWCYTCTC,第2轮引物为Arch349F_Arch806R,引物序列分别为GYGCASCAGKCGMGAAW和GGACTACVSGGGTAT-CTAAT。最后使用Illumina MiSeq高通量测序平台进行基因测序。
2 结果与讨论
2.1 流通吸收性能
2.1.1 CO2去除率
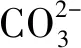

图2 不同试验工况下CO2去除率和CO2吸收量
2.1.2 体积总传质系数KGaV
体积总传质系数KGaV是衡量填料塔传质性能的重要参数之一[24]。根据每组吸收试验运行稳定后测得尾气中CO2含量,计算体积总传质系数KGaV,结果如图3所示。气体流量0.4~1.2 L/min下,随液体流量增加KGaV变化趋势基本一致,由初始14 mol/(h·kPa·m3)逐渐上升并稳定在17~19 mol/(h·kPa·m3)。与气体流量相比,液体流量对CO2传质性能影响更大。以1.0 L/min气体流量为例,液体流量由0.5 L/min增至0.9 L/min时,KGaV由14.3 mol/(h·kPa·m3)增至18.2 mol/(h·kPa·m3),提高液体流量能增加填料层的有效传质面积aV,进而提高传质效果[19,25];液体流量由0.9 L/min增至1.1 L/min时,KGaV仅由18.2 mol/(h·kPa·m3)增至18.3 mol/(h·kPa·m3),说明进一步提高液体流量可能会增加液膜厚度和液膜传质阻力,降低总传质系数KG,导致KGaV并未随液体流量增加而发生明显变化。

图3 不同试验工况下的体积总传质系数KGaV
2.1.3 CO2吸收过程NaHCO3、Na2CO3变化量

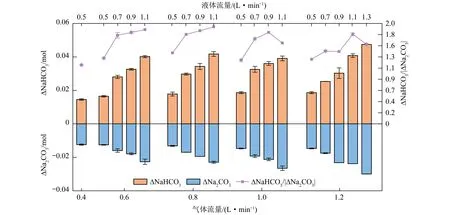
图4 不同试验工况下1 min内ΔNaHCO3、ΔNa2CO3及二者比值
2.2 循环吸收性能
选取CO2去除率较高的试验工况(气体流量0.6 L/min、液体流量0.7 L/min)开展循环吸收试验,如图5所示。液体循环周期设置为10 min,总计循环6次,持续60 min。由图5(a)可知,CO2去除率随循环时间增加逐渐降低,第5分钟时,尾气中CO2体积分数仅0.48%,CO2去除率高达97.28%,第60分钟时,CO2去除率降至80.1%。若设置CO2去除率目标为80%,本试验工况下吸收剂可实现6次循环吸收。此外,随循环次数增加,溶液pH由10.00降至8.82,Na2CO3物质的量浓度由0.038 mol/L降至0.004 mol/L,Na2CO3利用率达89.5%;溶液中NaHCO3、Tic逐渐增加并分别稳定在0.122和0.127 mol/L左右。GONZLEZ-LPEZ等[26]证实,营养液pH在8~10、Tic小于0.167 mol/L时,CO2生物转化过程不受溶液pH和盐含量影响;营养液Tic在0.083 mol/L左右时,微生物生长速率最高。本循环试验结束时,富液中Tic为0.127 mol/L,pH为8.82,预计能为生物甲烷化微生物提供适宜的生长环境。

图5 CO2去除情况及富液特性随循环时间的变化
2.3 CO2吸收富液生物再生性能

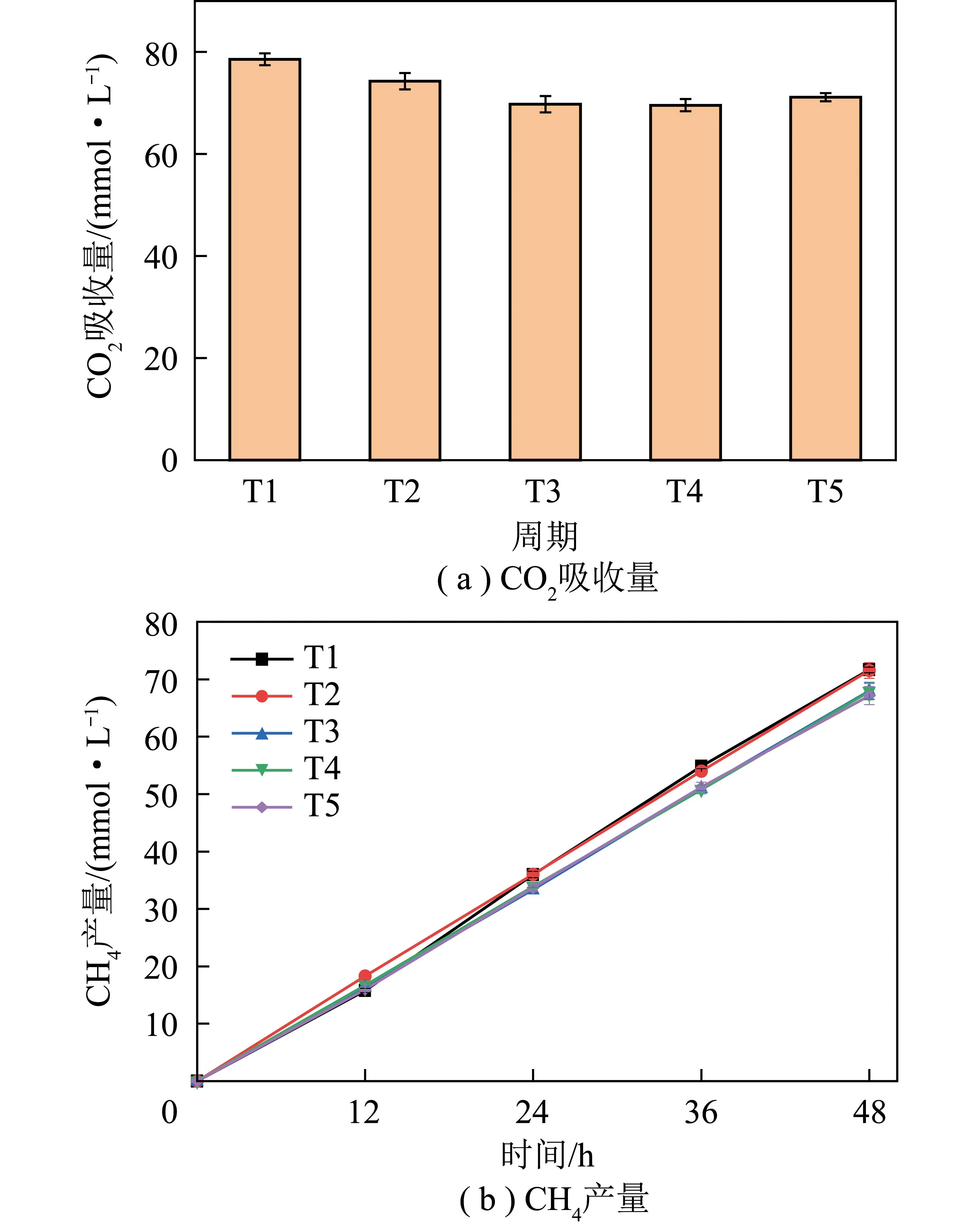
图6 每个吸收-再生周期的CO2吸收量和CH4产量
为识别参与富液生物再生过程的主要微生物种类,对5个循环CO2化学吸收-富液生物再生试验前后厌氧瓶内生物膜进行高通量测序分析,结果如图7所示。门水平细菌群落中相对丰度较高的微生物菌群主要包括Firmicutes(厚壁菌门)、Bacteroidota(拟杆菌门)、Proteobacteria(变形杆菌门)、Actinobacteriota(放线菌门)、Synergistota(互养菌门)、Desulfobacterota(脱硫菌门)。其中,Firmicutes可产生大量与有机物降解密切相关的水解酶,且由于其厚壁特性,耐酸耐碱性能更好[27];Bacteroidota、Proteobacteria、Actinobacteriota能将蛋白质降解转化为氨基酸等小分子有机物,且可以分解多糖等有机物[28-30];Desulfobacterota是一种硫酸盐还原菌,可将有机物不完全氧化为乙酸[31];Synergistota可与氢营养型甲烷菌进行互养代谢,促进甲烷菌进行H2还原CO2的反应[32]。由于生物再生试验在弱碱性条件下进行,Bacteroidota、Proteobacteria可能无法适应该环境而衰减,相对丰度分别由16.6%、7.1%降至11.8%、1.6%,衰减的细胞可作为Firmicutes、Actinobacteriota等耐碱性细菌的底物,使其相对丰度分别由50.5%、10.0%增至54.5%、22.1%。虽然循环试验前后门水平细菌种类没有明显变化,但耐碱性微生物占比提高。属水平古菌群落中,相对丰度较高的菌群主要包括unclassified_f_Methano-bacteriaceae(甲烷杆菌科未分类属)、Methanobacterium(甲烷杆菌属)、Methanobrevibacter(甲烷短杆菌属)。Methanobacterium、Methanobrevibacter、Methanobacteriaceae均是典型的氢营养型产甲烷菌,以H2、CO2为底物生成CH4[28,33-36]。生物再生试验前后氢营养型产甲烷菌均占绝对主导地位,相对丰度之和均接近99%。然而,再生试验后,Methanobrevibacter的相对丰度降低了19.5%,unclassified_f_Methanobact-eriaceae增加了18.7%,说明氢营养型产甲烷菌群可通过调整自身结构以适应弱碱性试验条件。
3 结 论
1)由碳酸盐、碳酸氢盐、微生物营养液配制的弱碱性吸收剂(pH=10)在流通模式下对模拟烟气CO2吸收效果良好,适宜的气体和液体流量应分别不高于1.0和0.9 L/min,此时CO2去除率可保持在80%以上,最高达96.6%;填料塔体积总传质系数稳定在17~19 mol/(h·kPa·m3);吸收液中NaHCO3增量和Na2CO3消耗量比值平均为1.6。
3)5个周期的循环CO2吸收-富液生物再生性能具有良好的可重复性,每个周期的CO2吸收量和CH4产量分别在69.6~78.6 mmol/L和67.2~71.6 mmol/L,生物甲烷化生物膜可通过自身菌群结构的调整适应弱碱性富液环境,初步证实了碳捕集耦合生物甲烷化工艺的可行性。
