Al含量对含铝奥氏体不锈钢在高温超临界二氧化碳中均匀腐蚀性能的影响研究
2024-02-20龙家琛郭相龙张乐福
刘 珠,龙家琛,高 阳,郭相龙,张乐福
(上海交通大学,上海 200240)
超临界二氧化碳(supercritical carbon dioxide, sCO2)由于具有高密度、高压缩性、高导热系数等属性,被视为新一代能源动力系统的潜在工质,可应用于核电、火电、太阳能等诸多领域,发展前景广阔[1]。其中,以sCO2为冷却剂的核反应堆更因其高能量转化效率、低空间占有率、高经济性等优势,受到国内外多家研究机构的广泛关注[2]。与第二、三代核反应堆相比,sCO2核反应堆的运行温度更高(500~700 ℃),材料在服役过程中更易失效,发生严重的氧化、渗碳[3-6]。相比于其他结构材料,燃料包壳管在反应堆中的服役环境最恶劣(高温、辐照),其特有的薄壁结构更提高了材料对耐腐蚀性能的要求,因此,燃料包壳管的选材工作成为sCO2核反应堆设计和建造过程中亟待解决的关键问题之一。
由于兼具较好的高温耐腐蚀性及较高的中子经济性,奥氏体不锈钢被视为燃料包壳管的主要候选材料。奥氏体不锈钢中较高的Cr含量(>18wt%)能促进保护性Cr2O3氧化膜的生成[7],然而,Yang等[8]的研究结果表明,在sCO2环境中,温度升高(500 ℃→600 ℃)将导致奥氏体不锈钢表面连续Cr2O3氧化膜失效,保护性较差的Fe3O4氧化物将在表面生成。此外,Young等[9]的研究结果表明,在高温CO2环境中C仍能通过Cr2O3氧化膜中的晶界向基体扩散,造成材料渗碳。为进一步优化奥氏体不锈钢的耐氧化和渗碳属性,含铝奥氏体(alumina-forming austenitic, AFA)不锈钢的概念应运而生。其中,更高的Al含量能促进保护性Al2O3形成,致密的Al2O3氧化膜能有效抑制金属元素及氧化/渗碳介质的扩散,进而降低材料的腐蚀速率、减缓材料氧化和渗碳的程度[10-11]。然而,AFA不锈钢在不同环境中形成保护性Al2O3氧化膜所需的Al含量存在较大差异。Yamamoto等[10]的研究结果表明,Fe-14Cr-20Ni-2.5Al不锈钢可在800 ℃水蒸气中形成连续的Al2O3氧化膜,而He等[12]的研究结果表明,Fe-14Cr-25Ni-3.5Al不锈钢在550 ℃以上的sCO2环境中表面生成了多层氧化膜,腐蚀增重量显著增加。因此,研究Al含量对AFA不锈钢在sCO2中腐蚀行为的影响,将为AFA不锈钢在高温sCO2中的应用提供可靠的数据支撑。
本工作通过实验研究3种不同Al含量的AFA不锈钢及无Al基材(Fe-xAl-19Cr-26Ni-1Si-2Mn-1.5Cu-4Mo-1Nb-0.08C,x=0/1.5/2.5/3.5)在650 ℃/20 MPa的sCO2环境下的均匀腐蚀行为,分析讨论Al含量对材料氧化、渗碳行为的影响。
1 实验方法
1.1 材料
实验采用的3种AFA不锈钢及基材名义成分为Fe-xAl-19Cr-26Ni-1Si-2Mn-1.5Cu-4Mo-1Nb-0.08C(x=0/1.5/2.5/3.5),实测成分列于表1。其中,无Al基材A0中测得较低Al含量(0.036wt%)的主要来源为熔炼过程中引入的杂质。所有材料在冶炼后均采取热处理的加工方式,具体处理如下:1) 1 200 ℃固溶1 h;2) 700 ℃时效100 h。

表1 实验材料实测成分
材料微观组织结构示于图1,其中,所有材料中均存在微米级NbC析出相(亮白色颗粒,相应的元素分布及衍射花样结果示于图1e、f),该种析出相形成于材料冶炼过程中。A0基材中还存在纳米级针状析出相(亮灰色析出相,红色箭头),存在形式为Laves相,主要成分富Si/Nb/Mo。A1和A2材料中均存在3种析出相,即亮灰色纳米级析出相(红色箭头,Laves相,富Si/Nb/Mo)、暗灰色纳米级析出相(蓝色箭头,NiAl相,富Ni/Al)、亮灰色微米级析出相(黄色箭头,Sigma相,富Fe/Cr/Mo/Si)。A3材料中除上述3种析出相(Laves、Sigma、NiAl)外,还存在一定尺寸的BCC相,该BCC相中仍存在Laves相(红色箭头)和NiAl相(蓝色箭头)。由于Al元素作为铁素体强化元素,A3材料中较高的Al含量(3.5wt%)导致了其基体中BCC区域的形成[13]。

a——A0;b——A1;c——A2;d——A3;e——图a~d中标出点的EDS结果;f——A0材料中NbC面扫及SAED结果
1.2 实验及分析方法
均匀腐蚀实验样品采用片状挂片,长、宽、厚分别为20、10、2 mm,实验前采用不同牌号SiC水砂纸(180#至2000#)打磨样品表面,再采用5、1、0.3 μm氧化铝抛光悬浊液逐级进行机械抛光,最后采用0.03 μm二氧化硅抛光悬浊液进行振动抛光,以去除表面加工痕迹及表面应力层。样品用镍铬丝悬挂于实验段中,试样之间用氧化铝陶瓷片进行分隔。
腐蚀实验系统由气体供给系统、高温实验系统、数据采集与控制系统组成,具体设计方案及系统流程见文献[14]。本次实验温度为(650.0±0.5) ℃,压力为(20.0±0.5) MPa,实验用二氧化碳(CO2)纯度为99.99%。实验前通过多次交替抽真空及充入CO2的方式进行洗气处理,以除去系统中气体杂质。
实验前使用游标卡尺对样品实际尺寸进行测量,实验前后均采用电子天平(精度为0.01 mg)对样品进行称重。通过计算腐蚀增重情况,拟合腐蚀增重曲线,进而分析材料的腐蚀动力学规律,量化腐蚀速率。称重周期设定为24、100、300、500、700、1 000 h,留样周期为24、100、500、1 000 h。采用X射线荧光光谱(XRF)仪及高频红外碳硫分析仪对原始材料的成分进行了测定。采用配备背散射探头(BSE)、电子背散射衍射探头(EBSD)及能谱仪(EDS)的扫描电子显微镜(SEM)对腐蚀前后材料进行微观形貌及成分表征。采用选区电子衍射法(selected area electron diffraction, SAED)对析出相结构进行判定。通过辉光放电光发射光谱(glow discharge optical emission spectroscopy, GDOES)的方法分析腐蚀后材料的渗碳程度。
2 实验结果
2.1 腐蚀增重
图2为3种AFA材料及其基材在650 ℃/20 MPa的sCO2中腐蚀1 000 h后的腐蚀增重曲线及拟合结果。图2a表明,4种材料的腐蚀增重量从大到小排序依次为A0>A1>A2>A3。其中,最高Al含量(3.236wt%)的A3材料腐蚀增重量最低,1 000 h时的腐蚀增重量仅0.022 mg/cm2;无Al元素(0.036wt%)的A0基材腐蚀增重量最高,1 000 h时的腐蚀增重量可达0.283 mg/cm2,约为A3材料腐蚀增重量的13倍。这表明随着Al元素含量的升高,材料的腐蚀增重量显著下降,基体中Al元素的存在将有效降低材料的腐蚀速率。其中,A2、A3材料的腐蚀增重量在1 000 h后仍低于文献中多种传统高Cr奥氏体不锈钢(316LN[15]、800HT[16]、310S[17])、镍基合金(600[16]、690[18])在相同测试环境中的腐蚀增重量,这进一步说明了增加材料中Al含量将明显提升材料的耐腐蚀性能。此外,图2a中腐蚀增重结果也表明了腐蚀初期(0~100 h),材料的腐蚀增重量具有较快的增长速率,随着腐蚀时间的延长,不同材料腐蚀增重量的变化均趋于平缓。腐蚀初期,材料表面氧化膜较薄,氧化物形成元素(Fe、Cr等)能较快通过氧化膜向外扩散,此时,材料具有较快腐蚀增重速率,界面反应控制了该阶段的腐蚀增重速率;腐蚀中后期(100~1 000 h),材料表面氧化膜厚度增加,较厚氧化膜的存在抑制了氧化膜形成元素的向外扩散,减缓了腐蚀反应发生的速率,元素扩散成为该阶段中材料表面腐蚀产物生长的控制因素[6]。图2b中对100 h后腐蚀增重量的拟合结果也进一步证实了4种实验材料在该阶段的腐蚀增重量随时间的变化趋势均近似服从抛物线规律,说明此时材料表面腐蚀产物的生长速率主要由元素扩散控制[19]。

a——增重量与腐蚀时间的关系;b——增重量与根号下腐蚀时间的关系
2.2 氧化及渗碳行为
图3为材料腐蚀24 h和1 000 h时的表面形貌。腐蚀24 h时,颗粒状氧化物在所有材料表面均匀分布。其中,所有材料表面氧化物的衬度与基体中晶粒(红色、蓝色箭头)及相(黄色箭头)的分布情况存在一定的关联性。元素在不同取向的晶粒中具有不同的扩散速度[20],且不同相中化学成分及微观结构的差异同样影响了元素的扩散速度[21],进而导致了不同取向晶粒及不同相表面形成的氧化膜在成分及厚度方面存在差异,最终造成了不同区域氧化物衬度不同的现象。当腐蚀时间延长到1 000 h时,A0及A1材料表面氧化物颗粒较为突出,而A2、A3材料表面氧化物颗粒相对平坦,这说明A0及A1材料表面氧化物具有更快的生长速率,A2及A3材料表面氧化物生长速率较为缓慢,与前文中腐蚀增重情况相吻合。此外,与24 h腐蚀行为相比,4种材料表面氧化物颗粒尺寸略有增加,部分区域发生粘连,这在一定程度上表明了样品表面的腐蚀行为仍在进行。

a——A0,24 h;b——A0,24 h;c——A0,1 000 h;d——A1,24 h;e——A1,24 h;f——A1,1 000 h;g——A2,24 h;h——A2,24 h;i——A2,1 000 h;j——A3,24 h;k——A3,24 h;l——A3,1 000 h
为研究材料腐蚀后的氧化膜结构,在对腐蚀1 000 h的样品进行表面镀镍保护后,制备了截面样品进行观察分析。如图4a所示,A0材料腐蚀1 000 h后的表面氧化膜厚度范围在3~6 μm之间,线扫结果证实该氧化膜为双层结构(区域Ⅱ),外层富Fe、内层富Fe/Cr,氧化膜下方还存在一定厚度的富Ni区(区域Ⅲ),该层富Ni区产生的主要原因是Fe、Cr元素的向外扩散[15]。此外,A0材料的表面氧化膜中存在较多孔洞(黄色箭头),该种缺陷可作为扩散通道,导致氧化、渗碳反应的进一步进行[22]。A1材料腐蚀1 000 h后的表面氧化膜形貌见图4c,其厚度范围在2~5 μm之间,同样为双层结构(区域Ⅱ),外层富Fe、内层富Fe/Cr。与A0材料不同的是,A1材料表面氧化膜下边缘相对平整,其下基体中存在一层不连续的内氧化区域(区域Ⅲ,富Cr/Al)。相比于表面生成的富Fe氧化物,A1材料内氧化区域中富Cr/Al氧化物的所占体积相对较小,其对腐蚀增重的提升程度也有限。与A0材料相似,该内氧化区域下方同样存在一定厚度的富Ni区。此外,A1材料表面氧化膜中的孔洞密度相对较低(黄色箭头),其保护性略好于A0材料表面氧化膜,这也在一定程度上解释了相同取样时间A1的腐蚀增重量要低于A0。
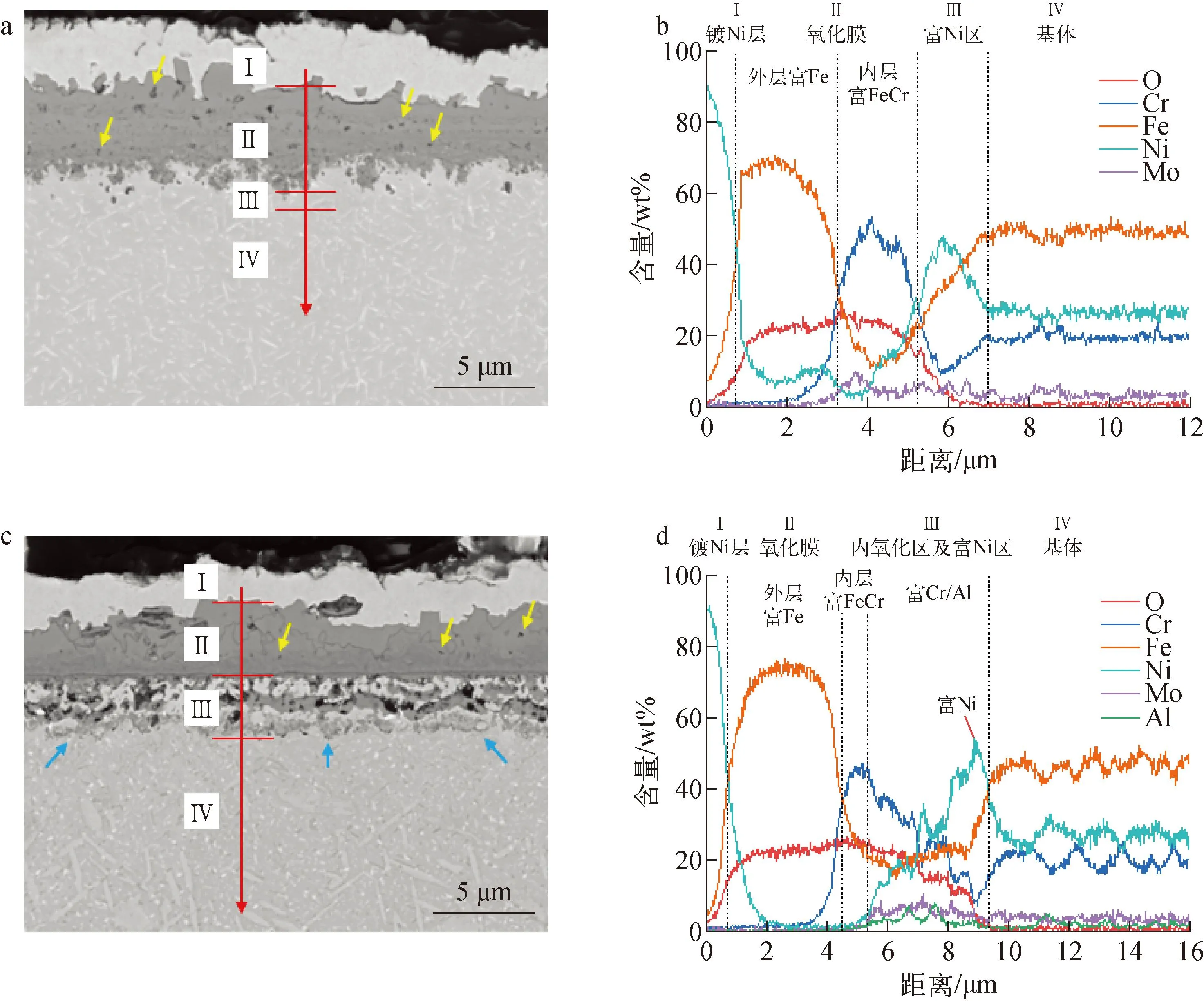
a——A0的截面形貌;b——A0的线扫结果(图a中红色箭头区域);c——A1的截面形貌;d——A1的线扫结果(图c中红色箭头区域)
A2、A3材料腐蚀1 000 h后的截面形貌如图5a、b、c所示,A2表面氧化膜厚度约1 μm,A3材料不同区域(FCC和BCC)表面氧化膜的厚度均小于0.5 μm,与前文中A3材料具有最低的腐蚀增重量结果相吻合。图5d、e、f中线扫结果表明,A2、A3材料表面氧化膜均为双层结构,外层富Cr、内层富Al,未在表面观察到无保护性的富Fe氧化物。上述结果表明Al含量高于2.5%时,材料表面形成了保护性的富Cr和富Al氧化膜,阻碍了Fe的向外扩散,提升了材料的耐腐蚀性能。
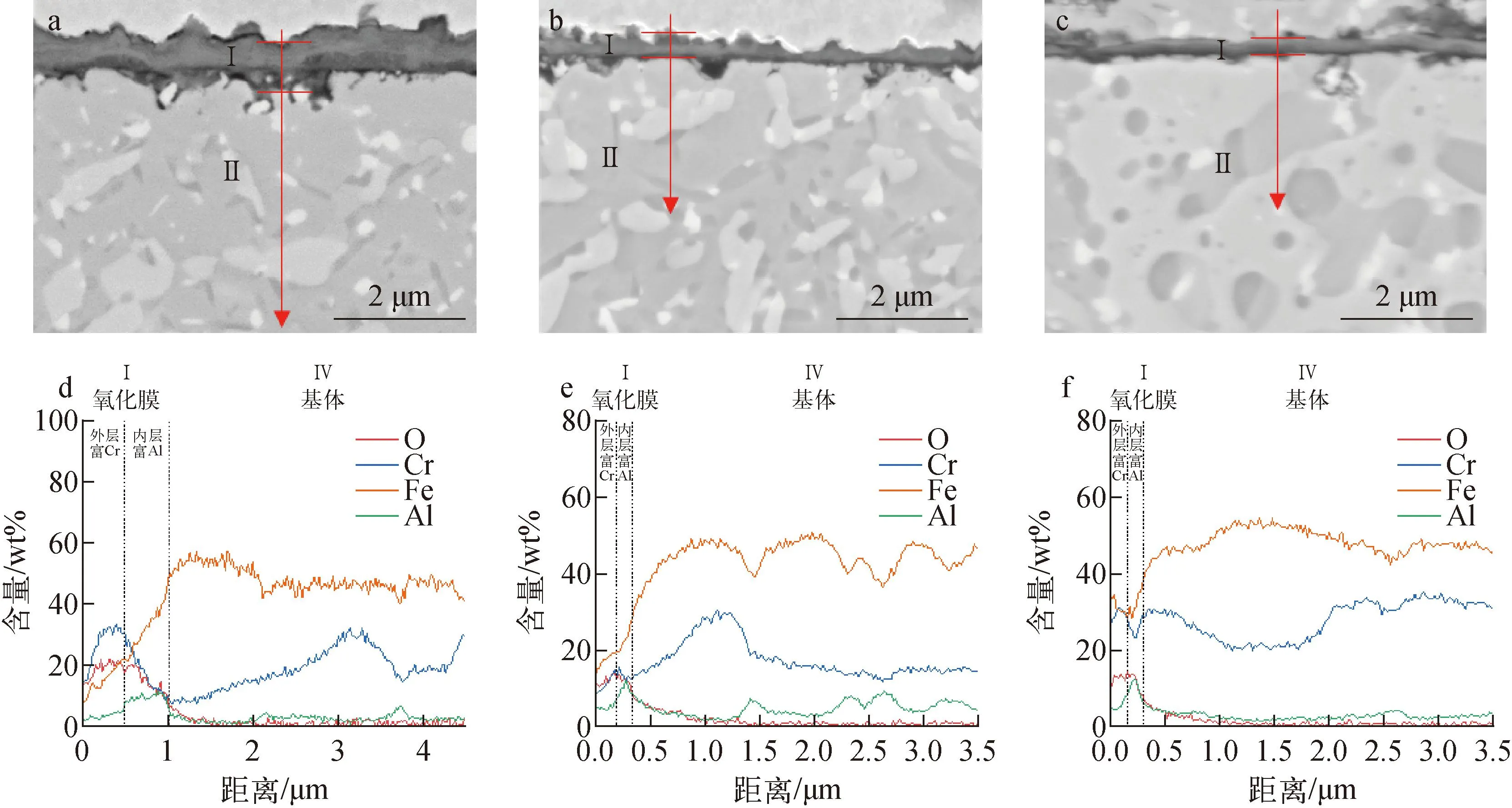
a——A2的截面形貌;b——A3中FCC区域的截面形貌;c——A3中BCC区域的截面形貌;d——A2的线扫结果(图a中红色箭头区域);e——A3中FCC区域的线扫结果(图b中红色箭头区域);f——A3中BCC区域的线扫结果(图c中红色箭头区域)
为分析材料的渗碳情况,对腐蚀1 000 h后的A0和A2材料进行GDOES分析。如图6a所示,A0材料中最大渗碳深度可达12 μm,C含量在氧化膜外表面达到峰值(约7.5wt%)。随着距离氧化膜外表面深度的增加,C含量逐渐降低。除氧化膜外,A0基体中仍然存在一定厚度的渗碳区域,该区域最大C含量约为0.3wt%。A2材料中渗碳行为与A0存在显著差异,如图6b所示,A2材料中最大渗碳深度约为6 μm,C含量同样在氧化膜外表面达到峰值(约6wt%)。前文对氧化膜结构的表征中发现,A2材料腐蚀后表面生成的氧化膜为外层富Cr、内层富Al的双层结构。GDOES分析结果表明C元素也在富Cr与富Al氧化膜的交界面发生富集,该处C含量约为0.9wt%。该现象表明相对于富Cr氧化膜,富Al氧化膜能够更好的阻碍C向内的进一步扩散。除氧化膜外,A2基体中同样存在一定厚度的渗碳区域,该区域C含量峰值约为0.15wt%,略低于腐蚀后A0材料基体中的渗碳区域的C含量,说明了A2材料表面形成的Al膜虽然具有较好的耐渗碳属性,但未能完全阻碍C的向内扩散。

图6 A0及A2腐蚀1 000 h后的GDOES结果
3 分析与讨论
sCO2环境中,含有较低Al含量的A0和A1材料表面生成了双层结构的富Fe氧化膜,以A0为例,其氧化膜及基体中发生明显渗碳,渗碳深度可达12 μm;而含有2.5wt%及以上Al含量的A2和A3材料表面生成了外层富Cr、内层富Al的双层氧化膜,保护性较好,以A2为例,其氧化膜及基体中仍发生渗碳,渗碳深度约为6 μm。不锈钢在高温sCO2中发生氧化和渗碳行为的方式主要有以下几种[16]:不锈钢中的金属元素可直接通过式(1)、式(2)与高温CO2发生反应生成表面氧化物;式(1)中的反应产物CO也可通过式(3)进一步氧化金属元素,生成氧化物;除氧化行为外,式(2)和式(3)中的另一反应产物C可通过氧化膜中的缺陷(孔洞、裂纹等)进一步向基体扩散,使材料发生渗碳;如式(4)所示,C的生成还可由式(1)中的反应产物CO直接通过Boudouard反应获得。
xM+yCO2=MxOy+yCO
(1)
xM+yCO2=MxO2y+yC
(2)
xM+yCO=MxOy+yC
(3)
2CO=CO2+C
(4)
其中,M为Fe,Cr,Al。
在不锈钢的常见化学成分中,Al元素的亲氧性远高于Cr和Fe元素,Al的氧化物将优先在材料表面生成[23]。然而,基体中的Al含量能否达到形成向外生长的Al膜和维持该种Al膜所需的临界Al含量将对表面形成的氧化膜种类起决定性作用[24]。对不含Al和低Al含量的材料而言,由于基体中的Al含量低于临界Al含量,这使得该类材料表面形成了保护性差的Al氧化物,难以阻碍Cr、Fe元素的向外扩散,进而导致了材料表面生成了双层富Fe氧化物。富Fe氧化物对C的阻碍作用非常有限,这使得反应过程中产生的C可以通过氧化物的晶界、孔洞等通道进一步向基体扩散,造成较大的渗碳深度[25]。此外,富Fe氧化物中存在的缺陷对氧化介质(CO2、CO等)的阻碍作用同样有限,由于Al元素具有更高的亲氧性,氧化介质向内扩散将优先与Al元素反应,导致内氧化区域的形成。对较高Al含量的材料而言,基体中的Al含量高于临界Al含量,保护性的富Al氧化物可形成于材料表面。由于材料中的Cr含量远高于Al含量,Cr元素浓度梯度更大且扩散速度更快,这使得该类材料表面氧化膜外层富Cr、内层富Al[26]。由于富Al氧化膜比富Cr氧化膜的耐渗碳属性更为优异[27],C可通过富Cr氧化膜晶界向内部扩散[9],因此,在外层富Cr氧化膜与内层富Al氧化膜界面出现C的富集现象。然而,由于富Al氧化膜的生长速率相对较慢[28],C在连续富Al氧化膜形成前可向基体进行扩散,导致该类材料基体中仍存在一定的渗碳层。
4 结论
本文对3种不同Al含量的含铝奥氏体不锈钢及其不含Al基材在650 ℃/20 MPa的SCO2中的均匀腐蚀行为进行分析,得到以下结论。
1) 650 ℃/20 MPa的sCO2环境中,不同Al含量材料的腐蚀增重均服从抛物线生长规律,腐蚀增重量随Al含量的升高而降低。
2) 不含Al或低Al含量的材料表面生成了无保护性的双层氧化物,外层富Fe、内层富Fe/Cr,含有2.5wt%及以上Al含量的材料表面生成了保护性较好的双层氧化物,外层富Cr、内层富Al。材料中较高的Al含量能够促进富Cr、Al氧化膜的形成,进而抑制无保护性富Fe氧化物在材料表面形成。
3) 腐蚀后,不含Al或低Al含量的材料表面氧化膜及基体中均发生渗碳,渗碳深度可达12 μm;较高Al含量的材料表面氧化膜及基体中同样发生渗碳,渗碳深度相对较浅,仅为6 μm,且在其内外氧化膜交界处发生明显的碳富集现象。保护性富Al氧化膜的形成使得较高Al含量的材料具有更好的耐渗碳属性,Al元素含量高于2.5wt%时能够促进表面连续富Al氧化膜的形成。
感谢上海交通大学分析测试中心提供的微观结构分析技术支持。
