HPLC 多指标成分定量联合化学计量学评价不同产地茜草
2024-01-29姜云乔春凤刘华乔亚红李俊涛
姜云,乔春凤,刘华,乔亚红,李俊涛
1.郑州颐和医院 药学部,河南 郑州 450047
2.河南省医药科学研究院 药物研究所,河南 郑州 450052
茜草是茜草科植物茜草Rubia cordifoliaL.的干燥全草,可凉血、祛瘀、止血、通经,临床上主要用于吐血、衄血、崩漏、外伤出血、瘀阻经闭、关节痹痛、跌扑肿痛[1]。蒽醌及其苷类化合物、萘醌类、萘氢醌、黄酮类、环己肽类、多糖类和微量元素等是茜草中主要药效成分[2-4]。现代研究表明,茜草具有抗肿瘤、升高白细胞、免疫调节、护肝、抗炎、抗风湿、抗氧化、止血等作用[5-7],并且现代研究还证明,蒽醌类成分茜草素在体外对沙门菌、大肠埃希菌、金黄色葡萄球菌、绿脓杆菌和变形杆菌等都具有明显的抑制作用[4],还用于治疗婴幼儿病毒性腹泻[5,8]。茜草收载于《中国药典》2020 年版一部,标准中规定大叶茜草素不得少于0.40%,羟基茜草素不得少于0.10%。对于茜草质量研究文献仅限指纹图谱[9-12]和1~2 个成分的定量[13-15]。中药是复杂的个体,所含成分多而杂,少数指标成分不能诠释其内在整体质量。主成分分析(PCA)和正交偏最小二乘判别分析(OPLS-DA)是化学计量学常用的技术手段,通过对含量数据分析挖掘,查找共性和不同,对样品分组分类,发现决定产品质量的标志性成分,预测精度高[16-19]。灰色关联度分析(GRA)可客观地对各组数据相似程度进行因素间相互关联分析,是解决多目标之间复杂关系问题的有力工具[20-22]。PCA、OPLS-DA 和GRA 均不存在主观因素,客观地对大量数据进行分析,非常适用于所含成分繁多的中药。本研究收集陕西、河南、安徽、河北、山东、青海、四川和西藏8 省区共18个批茜草药材,采用HPLC 法同时测定新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素10 种成分,通过化学计量学结合GRA 法进行综合质量评价,希望为茜草质量总体评价和新标准的提升、制定提供数据。
1 材料
1.1 试药
新橙皮苷(批号111857-202305,质量分数99.6%)、山柰酚(批号110861-202214,质量分数97.4%)、羟基茜草素(批号111898-202004,质量分数98.8%)、大叶茜草素(批号110884-202107,质量分数99.5%)、β-谷甾醇(批号110851-201909,质量分数92.7%)对照品均购自中国食品药品检定研究院;茜草素(批号CFS202301,质量分数98.2%)、异茜草素(批号CFS202201,质量分数98.5%)、1,3,6-三羟基-2-甲基蒽醌(批号CFS202201,质量分数98.9%)、去氢-α-拉杷醌(批号CFS202201,质量分数98.0%)、异落叶松脂素(批号CFS202201,质量分数98.5%)对照品均购自武汉天植生物技术有限公司;乙腈(色谱纯,VSA 公司),磷酸(色谱纯,Fisher 公司),水为纯净水,甲醇(分析纯,天津市大茂化学试剂厂);茜草经河南省医药科学研究院李俊涛研究员鉴定为正品,产地信息见表1。
1.2 仪器
LC-20A HPLC 仪(日本岛津);CP225D 型电子分析天平(北京赛多利斯),SB-5200 DTD 超声波发生器(宁波新芝生物科技股份有限公司)。
2 方法与结果
2.1 对照品溶液的制备
精准称取新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素10个对照品适量,用60%甲醇溶解并制成质量浓度分别为0.028、0.492、0.610、0.064、1.370、1.878、4.730、0.092、0.128、0.236 mg/mL 的混合贮备液,再将混合贮备液用同一溶剂稀释20 倍,即得混合对照品溶液(含新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇和异落叶松脂素1.40、24.60、30.50、3.20、68.50、93.90、236.50、4.60、6.40、11.80 μg/mL)。
2.2 供试品溶液的制备
将茜草样品干燥、粉碎(过二号筛),取粉末约1.0 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇25 mL,称定质量,加热回流45 min,放冷,再称定质量,用提取溶剂补足质量,摇匀,0.45 μm滤膜滤过,即得。
2.3 色谱条件
Alltima C18色谱柱(250 mm×4.6 mm,5 μm);流动相0.2%磷酸(A)-乙腈(B),梯度洗脱(0~12 min,20.0% B;12~19 min,20.0%→28.0% B;19~40 min,28.0%→45.0% B;40~53 min,45.0%→80.0% B;53~60 min,80.0%→20.0% B);检测波长:254 nm(0~40 min,新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌)、210 nm(40~60 min,β-谷甾醇、异落叶松脂素);体积流量1.0 mL/min;柱温30 ℃;进样量10 μL。在上述色谱条件下,供试品溶液中10 种成分色谱峰的保留时间与对照品一致,且峰形对称,与相邻色谱峰分离良好(分离度均≥1.5),色谱图见图1。
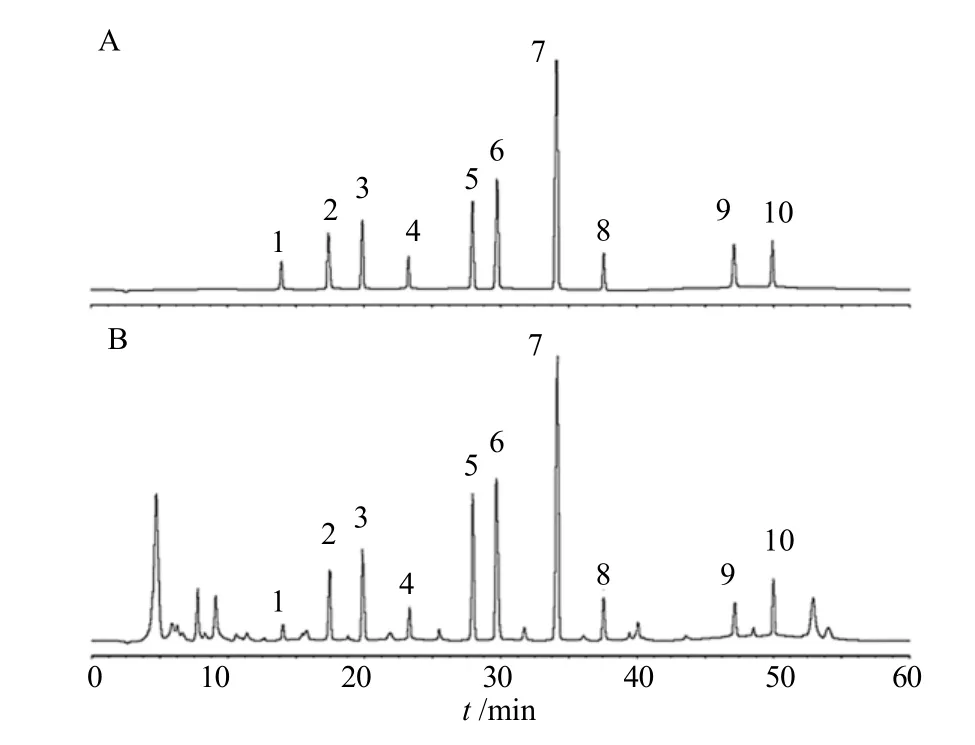
图1 对照品(A)和茜草供试品(B)的高效液相色谱图Fig.1 HPLC chromatograms reference substances (A)and Rubiae Radix samples (B)
2.4 方法学考察
2.4.1 线性关系考察 精密吸混合贮备溶液,分别用60%甲醇按照4、10、20、40、100、200 倍稀释成从高到低的6 个质量浓度,进样测定,用得到的色谱峰峰面积作线性回归处理。逐步稀释各对照品溶液,进样测定,计算主峰峰高与基线噪音的比值(S/N)。以S/N 为3 时的质量浓度计为检测限浓度;S/N 为10 时的质量浓度计为定量限浓度。结果见表2。可见10 个成分在各自范围内线性关系良好。

表2 线性关系考察Table 2 Linear relationship investigation
2.4.2 精密度试验 取混合对照品溶液连续进样6次,记录新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素色谱峰峰面积,计算得10 个成分峰面积的RSD 值分别为1.45%、1.06%、0.98%、1.23%、0.56%、0.50%、0.39%、1.32%、1.18%、1.22%。
2.4.3 稳定性试验 称取1 份茜草(S1)样品,制成供试品溶液,分别在0、2、5、9、14、20、24 h进样,计算得新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素峰面积的RSD 值分别为1.95%、1.66%、1.08%、1.74%、0.78%、0.92%、0.67%、1.62%、1.88%、1.76%,结果表明茜草供试品溶液在24 h 内稳定性良好。
2.4.4 重复性试验 称取茜草(S1)6 份,制备供试品溶液,进样,结果新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素的平均质量分数分别为0.032、0.549、0.836、0.073、1.922、2.537、6.561、0.098、0.136、0.253 mg/g,RSD 值分别为1.98%、1.86%、1.35%、1.60%、1.02%、0.89%、0.63%、1.57%、1.79%、1.81%。
2.4.5 回收率试验 取茜草(S1)细粉(过二号筛)9 份,每份0.5 g,精密称定,分别加入混合对照品溶液(含新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素0.017、0.271、0.426、0.039、0.965、1.263、3.251、0.048、0.069、0.124 mg/mL)0.8、1.0、1.2 mL,制备供试品溶液,进样测定峰面积,计算得10 种成分的平均回收率分别为96.97%、97.68%、98.05%、97.54%、100.10%、99.09%、100.18%、97.15%、97.38%、98.05%,RSD 值分别为0.93%、1.43%、1.34%、1.06%、0.76%、1.38%、0.69%、1.51%、1.13%、1.91%。
2.5 样品测定
精密吸取18 批茜草样品,制备供试品溶液,进样测定,记录峰面积,采用外标法计算新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素的质量分数,结果见表3。
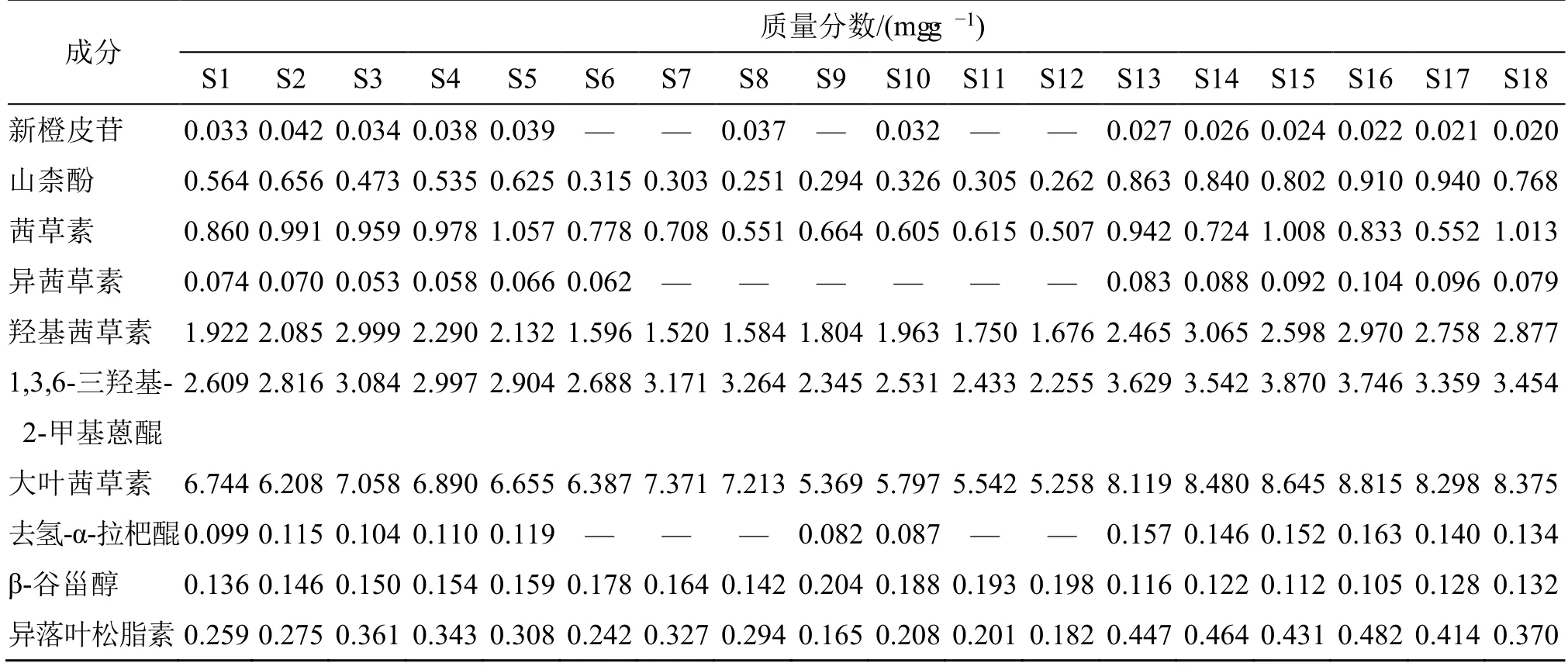
表3 茜草中新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素的测定结果(n=3)Table 3 Determination of neohesperidin,kaempferol,alizarin,xanthopurpurin,purpurin,1,3,6-trihydroxy-2-methylanthraquinone,mollugin,dehydro-α-lapachone,β-sitosterol and isolariciresinol from Rubiae Radix (n=3)
2.6 主成分分析(PCA)
应用SIMCA 14.1 软件对18 批茜草样品中新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素质量分数数据建立PCA模型,得图2。提取出2 个主成分,其中模型系数R2X=0.820,18 批茜草样品分为3 组,S1~S5 为1组,S6~S12 为2 组,S13~S18 为3 组,聚为相同组的样品来自1 个产区,说明相同产区的茜草,质量较接近,且所有散点均在95%置信区间内,表明检测数据未出现异常。
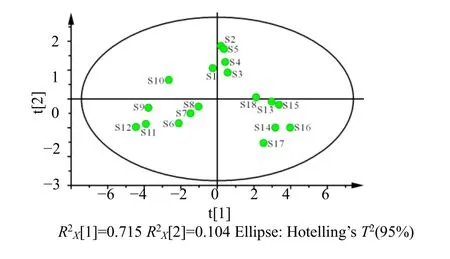
图2 PCA 得分图Fig.2 PCA score chart
2.7 正交偏最小二乘法-判别分析(OPLS-DA)
运行OPLS-DA 程序,结果见图3,模型参数R2X=0.990、R2Y=0.935、Q2=0.753,均大于0.5,表明建立的模型稳定可靠、预测能力强[16]。再以变量重要性投影(VIP)值>1 为显著影响[18],共找到4 个差异性标志成分,影响显著性为大叶茜草素>茜草素>1,3,6-三羟基-2-甲基蒽醌>羟基茜草素,VIP 值分别为1.810 3、1.366 7、1.240 5、1.226 4,结果见图4。

图3 茜草的OPLS-DA 模型得分图Fig.3 Score chart of OPLS-DA model for Rubiae Radix

图4 茜草的VIP 图Fig.4 VIP images of Rubiae Radix
2.8 灰色关联度分析(GRA)
采用均值变换法对18 批茜草中10 个成分新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇、异落叶松脂素的质量分数数据进行规格化处理(表4)。以处理后每个成分的最大值为最优参考序列,最小值为最差参考序列,分别计算各评价单元与最优参考序列的关联系数、与最差参考序列的关联系数(表5、6)[20],最后计算相对关联度[20]。以相对关联度为测度,对茜草样品进行质量优劣排序(表7)。结果18 批茜草的相对关联度在0.327 6~0.592 7,S16、S15、S14、S13、S18、S17 分别位于排名前6 位,S3、S5、S2、S4、S1 位于排名中间位置,S12、S9、S11、S6、S8、S10、S7位于排名后7 位。结果表明陕西、河南和安徽所产的茜草整体质量较好,其次为河北和山东产地。
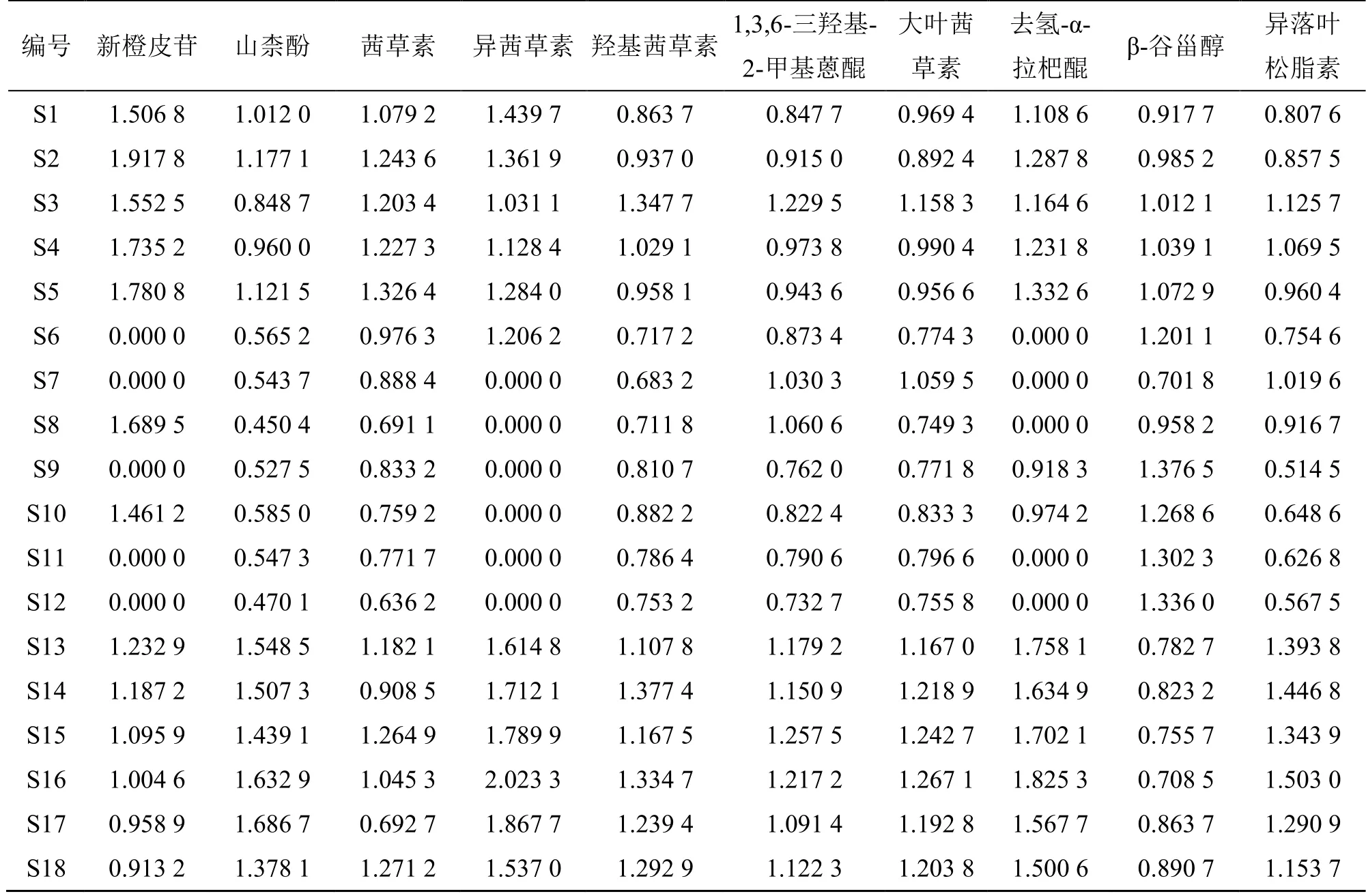
表4 数据规格化处理结果Table 4 Results of data contents

表5 各指标与最优参考序列的关联系数Table 5 Correlation coefficient between each index and the optimal reference sequence

表6 各指标与最差参考序列的关联系数Table 6 Correlation coefficient between each index and the worst reference sequence

表7 各样品相对关联度及质量优劣排序Table 7 Relative correlation degree and quality ranking of the samples
3 讨论
3.1 目标成分的选择
茜草中主要药效成分为蒽醌及其苷类化合物、萘醌类、萘氢醌、黄酮类、环己肽类、多糖类等,现代研究表明萘醌类和蒽醌及其苷类化合物类为茜草中最主要的活性成分,与其抗氧化、抗炎、抗肿瘤功能密切相关用[5],以茜草素、羟基茜草素、1-羟甲基蒽醌、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、异茜草素、山柰酚、新橙皮苷的含量较高;甾醇类是一类天然化合物,以β-谷甾醇含量较高。故本实验以上述10 种成分作为目标成分,采用HPLC法同时测定。
3.2 流动相和供试品溶液的处理方式确定
考察了洗脱能力较强的有机相乙腈,水相选择0.1%磷酸、0.2%磷酸、0.5%磷酸、0.1%甲酸、水。综合色谱峰对称情况、基线平稳情况、成分间的分离度、出峰时间等,最终确定流动相为乙腈-0.2%磷酸溶液。由于本实验中待测成分涵盖了黄酮类、萜类、蒽醌类、甾醇类化合物,各类物质极性不同,在供试品的预处理时,以新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇和异落叶松脂素的综合提取率、杂质峰为指标,通过对提取溶剂(45%甲醇、60%甲醇、75%甲醇)进行对比,发现以60%甲醇提取色谱峰数目多,且峰的纯度高。通过对提取方式(超声、加热回流)和时间(30、45、60 min)进行了考察,最终确定以60%甲醇加热回流提取45 min 为茜草供试品溶液的最佳提取方式。
3.3 测定结果和化学计量学分析结果评价
本实验对不同产地的18 批茜草中新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇和异落叶松脂素进行了检测,结果显示部分产地茜草中未检出新橙皮苷、异茜草素和去氢-α-拉杷醌,大叶茜草素和羟基茜草素质量分数分别在5.258~8.815 mg/g 和1.520~3.065 mg/g,符合《中国药典》2020 年版一部的要求。采用化学计量学中最常用的PCA 和OPLS-DA 对全国8 个省产地的18 批茜草中新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇和异落叶松脂素共10个成分的质量分数数据进行分析,结果显示大叶茜草素、茜草素、1,3,6-三羟基-2-甲基蒽醌和羟基茜草素是影响茜草质量的主要物质,提示对茜草的研究应着重关注上述4 个成分,而且这4 个成分的质量分数结果显示S13~S18 明显高于其他批次。同时GRA 结果显示,陕西、河南和安徽产地的茜草整体质量较好,与文献报道[6,9,12]相符,为茜草的道地性研究指明了方向。
本研究检测的10 个成分新橙皮苷、山柰酚、茜草素、异茜草素、羟基茜草素、1,3,6-三羟基-2-甲基蒽醌、大叶茜草素、去氢-α-拉杷醌、β-谷甾醇和异落叶松脂素涵盖了黄酮类、蒽醌类、甾体类和木脂素类,方法便捷、准确,易于推广,可以更全面、更系统地评价茜草的质量,为茜草药材的综合评价、产地道地性评价提供了参考。
利益冲突所有作者均声明不存在利益冲突
