人羊膜填塞与内界膜翻转填塞对高度近视黄斑裂孔性视网膜脱离疗效比较
2024-01-23王楚翘周激波姚腾腾王泽淇高慧芹汪朝阳
王楚翘 周激波 姚腾腾 王泽淇 高慧芹 汪朝阳
上海交通大学医学院附属第九人民医院眼科 上海市眼眶病眼肿瘤重点实验室,上海 200011
黄斑裂孔性视网膜脱离(macular hole retinal detachment,MHRD)是高度近视的严重并发症之一,好发于中老年女性,通常会导致严重的视力损害。高度近视MHRD发病机制尚不明确,可能与眼轴增长所致的后巩膜葡萄肿及玻璃体黄斑区所受的前后及切线方向持续牵拉等因素有关[1-2]。自1982年玻璃体切割术(pars plana vitrectomy,PPV)首次被应用于MHRD以来[3],MHRD的手术方式已由PPV联合气体或硅油填充术逐步改良至PPV联合内界膜剥除、PPV联合内界膜填塞及PPV联合内界膜翻转填塞术等。2010年,Michalewska等[4]首次采用内界膜翻转覆盖术治疗裂孔直径>400 μm的特发性黄斑裂孔(macular hole,MH),术后MH的愈合率及患眼视力均有所提高。随后有研究者将该技术改良至将翻转过的内界膜插入MH中,以防止内界膜瓣与裂孔脱离,从而更加有效闭合MH[5]。Rizzo等[6]提出利用视网膜下人羊膜填塞的方法来治疗复发性MH或复杂性视网膜脱离患者,并认为该方法可有效提高MH闭合率及视网膜复位率,且术后患眼功能有明显改善。内界膜或人羊膜等组织填塞裂孔并与视网膜组织黏附,有助于在裂孔处形成相对封闭的解剖环境,从而促进闭孔的愈合[4,7]。但目前关于人羊膜在MH填塞中的临床应用仅有少数几例,其解剖和功能预后仍有待进一步研究。本研究拟比较PPV术中人羊膜填塞与内界膜填塞对高度近视MHRD的疗效和安全性。
1 资料与方法
1.1 一般资料
采用非随机对照临床研究方法,纳入2020年7月至2021年8月在上海交通大学医学院附属第九人民医院接受PPV的高度近视MHRD患者15例16眼,其中男2例2眼,女13例14眼;年龄27~74岁,平均(58.93±11.07)岁。纳入标准:(1)屈光度数≤-6.00 D或眼轴长度≥26 mm;(2)经裂隙灯显微镜联合前置镜、光学相干断层扫描(optical coherence tomography,OCT)和眼部B型超声扫描等检查明确诊断为MHRD;(3)行PPV联合人羊膜填塞术或内界膜翻转填塞术。排除标准:增生性玻璃体视网膜病变、外伤等其他因素引起的MH者。根据术中MH填塞材料的不同将患者分为人羊膜填塞组7例7眼和内界膜填塞组8例9眼。2个组患者性别构成、年龄、眼别构成、眼轴长度、术前最佳矫正视力(best corrected visual acuity,BCVA)、术前眼压及术前屈光度比较,差异均无统计学意义(均P>0.05)(表1)。人羊膜填塞组中有6例6眼既往有PPV手术史,术眼晶状体状态均为缺如或人工晶状体在位;内界膜填塞组均为初次行PPV手术患者,有1例患者既往有白内障手术史。本研究遵循《赫尔辛基宣言》,且研究方案经上海交通大学医学院附属第九人民医院伦理委员会审核批准(批文号:SH9H-2021-T322-2)。所有患者术前均签署知情同意书。
1.2 方法
1.2.1手术方法 采用标准经睫状体平坦部三切口23G PPV,手术均由同一位经验丰富的术者完成。切割所有患者中央区玻璃体后注射40 mg/ml曲安奈德(昆明积大制药股份有限公司)0.05 ml,行玻璃体染色以明确清除玻璃体后皮质和周边残留玻璃体,笛针吸出视网膜下液,后极部视网膜前注射5 mg/ml吲哚菁绿(丹东医创药业有限责任公司)0.1 ml辅助内界膜染色。(1)人羊膜填塞术 黄斑区玻璃体后皮质剥除后,取组织库的新鲜人羊膜组织贴片,剪成合适大小(约2 mm×2 mm),用内界膜镊将其经由套管伸入玻璃体腔中并小心展平,经过MH将羊膜片填塞至视网膜下间隙,保持羊膜的绒毛膜层面向视网膜色素上皮(retinal pigment epithelium,RPE)层,并小心调整羊膜位置,使其中心位于MH区域,立刻行气液交换防止羊膜移位(视频)。(2)内界膜翻转填塞术 在距裂孔范围不超过2个视盘直径的血管旁区域行内界膜剥离(注意保留MH边缘的内界膜),并将内界膜的游离瓣翻折填塞至视网膜下间隙。手术结束时根据视网膜脱离程度及裂孔大小综合评估以明确眼内填充物,其中人羊膜填塞组及内界膜填塞组内各有1例1眼玻璃体腔内填充C3F8气体,其余术眼均填充硅油。视患者晶状体混浊程度行晶状体超声乳化及人工晶状体植入术。
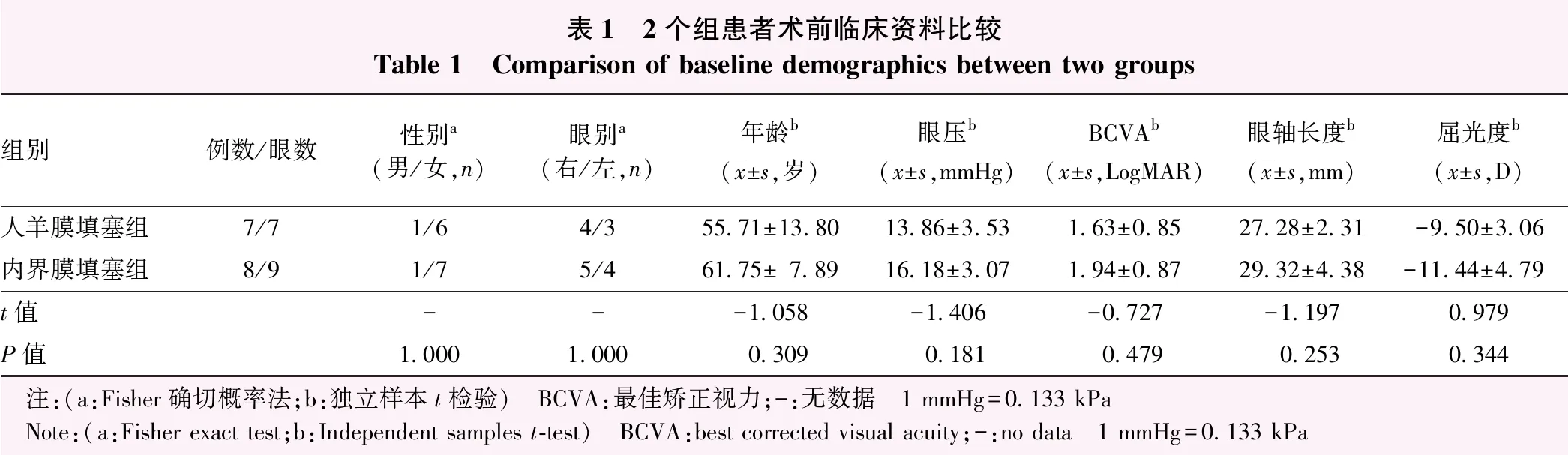
表1 2个组患者术前临床资料比较Table 1 Comparison of baseline demographics between two groups组别例数/眼数性别a (男/女,n)眼别a(右/左,n)年龄b(x±s,岁)眼压b(x±s,mmHg)BCVAb(x±s,LogMAR)眼轴长度b(x±s,mm)屈光度b(x±s,D)人羊膜填塞组7/71/64/355.71±13.8013.86±3.531.63±0.8527.28±2.31-9.50±3.06内界膜填塞组8/91/75/461.75±7.8916.18±3.071.94±0.8729.32±4.38-11.44±4.79t值---1.058-1.406-0.727-1.1970.979P值1.0001.0000.3090.1810.4790.2530.344 注:(a:Fisher确切概率法;b:独立样本t检验) BCVA:最佳矫正视力;-:无数据 1 mmHg=0.133 kPa Note:(a:Fisher exact test;b:Independent samples t-test) BCVA:best corrected visual acuity;-:no data 1 mmHg=0.133 kPa
1.2.2随访及评价指标 于手术前及术后1周、1个月、3个月、6个月对患者进行检查。采用标准对数视力表行BCVA检查,记录最小分辨角对数(logarithm of minimal angle resolution,LogMAR)视力,其中光感换算为4.0 LogMAR,手动换算为3.0 LogMAR,指数根据10 cm、20 cm及50 cm测量距离分别记作2.7 LogMAR、2.4 LogMAR和2.0 LogMAR;采用非接触眼压计(CT-1P,日本Topcon公司)测量眼压;采用裂隙灯显微镜(BM900,瑞士Haag-Streit公司)检查眼前节;采用欧堡激光扫描检眼镜[Daytona(P200T),英国Optos公司]及复方托吡卡胺滴眼液[参天制药(中国)有限公司]扩瞳后采用裂隙灯显微镜联合前置镜(90D,美国Ocular公司)检查眼底情况;采用Spectralis OCT仪(德国Heidelberg公司)行眼底结构检查。术后通过OCT检查结果判定MH闭合及视网膜复位情况,其中MH边缘消失或边缘贴近视网膜上皮层,视网膜上皮层暴露/未暴露认作MH完全性闭合或裸露性闭合,均认定为MH愈合;裂孔边缘翘起或未贴近视网膜上皮层且视网膜上皮层暴露为MH未愈合。视网膜神经上皮层与RPE层之间的间隙消失视为视网膜复位;MH未闭合致视网膜再脱离需手术再次干预视为视网膜未复位。
1.3 统计学方法
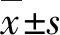
2 结果
2.1 2个组术眼MH闭合及视网膜复位眼数比较
人羊膜填塞组6眼初次手术后视网膜即复位,1眼于术后1个月出现视网膜再脱离;内界膜填塞组所有术眼初次手术后即复位。人羊膜填塞组2眼MH初次手术后未闭合,其中1眼于术后3个月再次行人羊膜填塞,术后6个月随访时MH已恢复闭合状态;内界膜填塞组术后1眼初次手术后MH未闭合,2个组患者术后MH初次闭合率比较差异无统计学意义(P=0.550)。
人羊膜填塞组MH闭合患者OCT图像显示,术后1周破损的视网膜组织黏附在人羊膜贴片上,术后3个月可见人羊膜贴片上视网膜断裂边缘的视网膜向内生长,部分视网膜组织分层(图1,2)。
图1 1例59岁女性高度近视MHRD患者右眼PPV联合人羊膜填塞术前后OCT图像 A:术前OCT图像 B:术后1周OCT图像 C:术后3个月OCT图像 红色箭头示视网膜下人羊膜贴片边缘

图2 1例61岁女性高度近视MHRD患者右眼人羊膜填塞术前后OCT图像 A:术前OCT图像 B:术后1周OCT图像 C:术后3个月OCT图像 红色箭头示视网膜下人羊膜贴片边缘
2.2 2个组术眼手术前后不同时间点BCVA比较
患者手术前后不同时间点术眼BCVA总体比较差异有统计学意义(F时间=4.420,P<0.05);各组术后1、3和6个月BCVA优于术前值,但差异均无统计学意义(均P>0.05)。2个组间BCVA总体比较差异无统计学意义(F组别=0.183,P=0.676)(表2)。
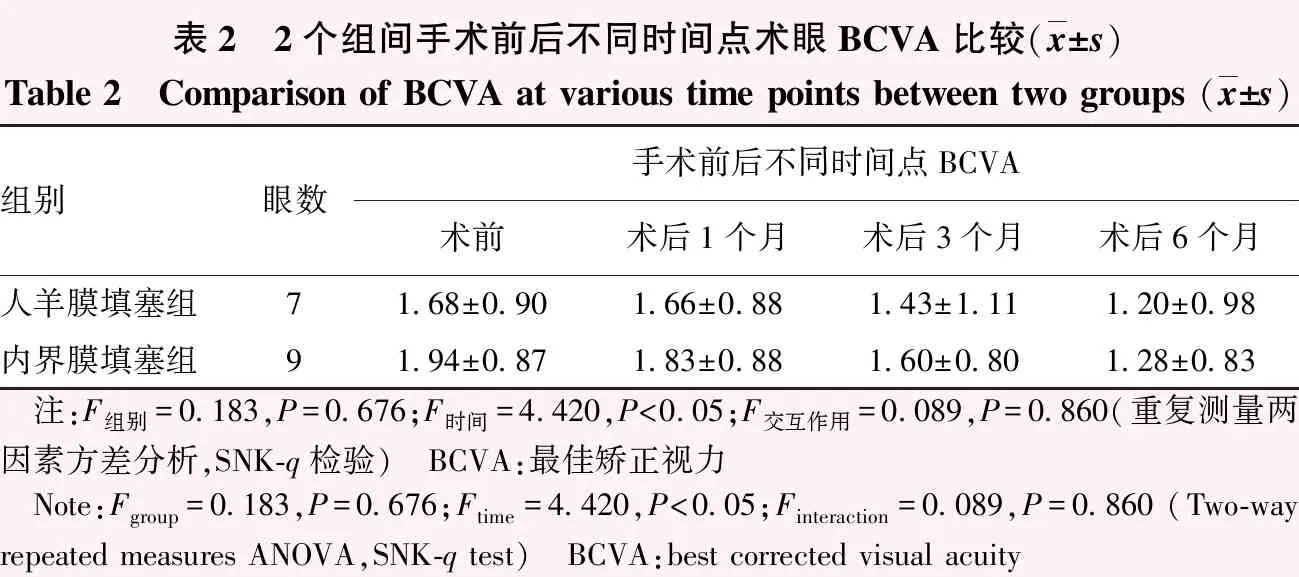
表2 2个组间手术前后不同时间点术眼BCVA比较(x±s)Table 2 Comparison of BCVA at various time points between two groups (x±s)组别眼数手术前后不同时间点BCVA术前术后1个月术后3个月术后6个月人羊膜填塞组71.68±0.901.66±0.881.43±1.111.20±0.98内界膜填塞组91.94±0.871.83±0.881.60±0.801.28±0.83 注:F组别=0.183,P=0.676;F时间=4.420,P<0.05;F交互作用=0.089,P=0.860(重复测量两因素方差分析,SNK-q检验) BCVA:最佳矫正视力 Note:Fgroup=0.183,P=0.676;Ftime=4.420,P<0.05;Finteraction=0.089,P=0.860 (Two-way repeated measures ANOVA,SNK-q test) BCVA:best corrected visual acuity
2.3 2个组术眼术后并发症比较
共6眼出现术后一过性眼压升高,其中人羊膜填塞组2眼,内界膜填塞组4眼,采用降眼压滴眼液点眼治疗1周后复查眼压均恢复正常。2个组均未发生角膜水肿、眼内炎、视网膜前膜、玻璃体出血及继发性青光眼等术后并发症。
3 讨论
2016年Holden等[8]通过对1995年以来发表的数据进行系统性回顾及meta分析,估算出全球近20亿人(约占全球总人口的28.3%)患有近视,其中高度近视约2.77亿人(约占全球总人口的4.0%)。随着眼轴的进行性延长,高度近视患者眼底会出现一系列退行性病变并多伴随或导致白内障、后巩膜葡萄肿、黄斑病变以及视网膜脱离等严重并发症的出现。预计在未来几十年内高度近视的患病率将继续上升[8],这意味着与高度近视相关的眼部并发症和视力丧失也将进一步增多。MH是高度近视中常见的并发症,其发生和发展与严重的视力障碍有关。MHRD是较难治疗的视网膜脱离类型之一,与非近视患者相比,高度近视患者MHRD视网膜复位和MH闭合率较低,且手术后视力恢复情况更差,一直是临床工作中亟待解决的难题。
2010年,Michalewska等[4]首次对内界膜翻转覆盖术进行了描述,随后Kuriyama等[9]即提出将其应用于高度近视MHRD的治疗中。翻转覆盖的内界膜不会完全从视网膜上移除,而是留有部分附着在MH的边缘,相比于单纯的内界膜剥除以及游离内界膜填塞而言,该项技术可使MH修复在短期内有更显著的效果[10]。但是仅覆盖在MH上的内界膜组织缺乏底层结构支撑,气液交换时视网膜下液体快速流动可能导致覆盖的内界膜在术中或术后脱位,故改进的内界膜翻转填塞技术将剥离的内界膜组织塞入裂孔内,填塞的内界膜组织不仅提供框架支撑,还充当填塞物,从而增加了结构的稳定性[5]。
然而,在MHRD患者脱离的视网膜组织中剥离翻转足够大小的内界膜组织需要更复杂的手术操作,并可能会导致一些额外的眼内并发症,例如视网膜脱离及玻璃体积血[11]。相比之下,人羊膜贴片更容易获取和制备,且可以根据MH的尺寸轻松调整大小,是一个很好的替代选择。羊膜是由单层立方上皮、基膜以及间质层组成的胎盘最内层无血管结构[12],具有结构透明、抗菌、抗炎、抗纤维化、抗新生血管及低免疫原性等优点[13-17]。1940年,人羊膜作为替代结膜的理想材料首次应用于眼表重建中[18],随后即广泛应用于多种眼表疾病的治疗。近年来,体外研究表明RPE细胞可在人羊膜上附着和生长[19],且人羊膜有利于RPE细胞分化的诱导及上皮表型的保留[20];同时,动物模型也证明视网膜下人羊膜植入耐受性良好,并可促进损伤的修复[21]。基于此,Rizzo等[6]展开了关于人羊膜填塞治疗复发性MH或复杂性视网膜脱离的临床研究;Caporossi等[22-23]随后将其应用于复发性MHRD的治疗中。以上研究表明,羊膜不仅可以在解剖层面封闭裂孔,还可以刺激视网膜增生和组织分层。目前,关于人羊膜在高度近视MHRD的临床应用鲜有报道[22]。本研究创新性地聚焦于人羊膜填塞术和内界膜翻转填塞术对高度近视性MHRD疗效的对比,不仅为人羊膜填塞术在高度近视MHRD治疗的临床研究中增加了一些研究病例,同时强调了人羊膜填塞术在伴有更复杂眼底情况的高度近视MHRD患者中具有与内界膜翻转填塞术相当的疗效。
本研究中,人羊膜填塞组较内界膜填塞组眼底情况更加复杂。内界膜填塞组既往无PPV手术史,而人羊膜填塞组7例中有6例既往存在PPV手术史,其中4例为视网膜脱离术后,2例为黄斑前膜术后;此外2个组间基线数据比较差异无统计学意义。2个组视网膜复位及MH闭合情况均良好,且2个组间MH术后初次闭合率比较差异无统计学意义。其中内界膜填塞组数据与既往研究一致[5,24-25],而既往关于人羊膜填塞治疗复发性MHRD的研究皆显示全部视网膜复位及MH闭合[6-7,22-23],本研究也仅存在1例术后裂孔未闭合且视网膜未复位的患者。该患者术前眼部基本情况较差,数年前有外伤性白内障史且术前3个月于外院行PPV治疗视网膜脱离(具体术式不详),术后2个月复诊OCT示裂孔再次形成,术后3个月复诊可见继发性视网膜脱离。人羊膜填塞组另有1例初次手术后MH未闭合患者,该患者于术后3个月再次行人羊膜填塞治疗,二次手术后3个月随访时MH恢复为闭合状态,且术后视力由0.7 LogMAR提高至0.4 LogMAR。我们考虑MH初次未闭合是由于人羊膜贴片尺寸未完全贴合裂孔尺寸导致。随访OCT可见术后1周人羊膜贴片溶解至略小于视网膜断裂尺寸,断裂边缘视网膜组织未能完全黏附于人羊膜贴片上;术后2个月可见人羊膜明显溶解,裂孔边缘翘起。故我们分析人羊膜贴片需在MH边缘下方均匀且完整地铺展以确定裂孔边缘的视网膜组织可黏附在人羊膜贴片上,进而确保RPE细胞可在人羊膜贴片上均匀增生。
本研究结果显示,人羊膜填塞组和内界膜填塞组患者手术前后不同时间点术眼BCVA总体比较差异有统计学意义,但各组术后各时间点与术前比较差异无统计学意义。考虑本研究纳入部分病例眼底情况极差,随访至术后6个月时,仍有患者眼底情况不适合将硅油取出,其中人羊膜填塞组3例,内界膜填塞组4例,这可能对术后视力的评估造成一定影响。同时2个组间BCVA总体比较差异无统计学意义,可见将人羊膜或内界膜填塞入视网膜下间隙,可以提高其与RPE的相互作用,刺激组织增生和视网膜断裂闭合,从而进一步改善视力。人羊膜填塞还有助于吸收裂孔周围的视网膜下液体,在更复杂的情况下也能保持相似的解剖和功能结果,进一步强调了人羊膜在高度近视MHRD治疗中的实用性。
综上所述,PPV联合人羊膜填塞术或内界膜翻转填塞术均为治疗高度近视MHRD安全有效的手术方式,且伴随更复杂的眼底既往病史时人羊膜填塞术也能保持良好的视网膜解剖学复位及功能恢复。人羊膜贴片可以刺激视网膜向内生长,且新生的视网膜存在时间依赖的结构分化;同时相比内界膜翻转填塞而言,人羊膜贴片更容易获取和制备,手术操作相对简单,是一个很好的替代选择。由于高度近视MHRD的病例临床上较少见,本研究入选的病例数较少,因此结果存在一定的局限性,仅为人羊膜填塞术治疗MHRD增加极少的病例资料,未来仍需要更多临床数据来分析人羊膜填塞这种新技术的有效性以及更多研究来探讨羊膜和视网膜之间的相互作用。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明王楚翘:研究设计及实施、分析数据、文章撰写及修改;周激波:解释数据、对文章的知识性内容作批评性审阅;姚腾腾:研究设计、统计分析、文章修改;王泽淇:实施研究、采集数据;高慧芹:采集数据;汪朝阳:研究设计、文章修改及定稿
