质谱离子源内裂解和重排可能会为化学反应中间体的捕获带来错误信息
2024-01-20赵玲玲梁驰予张新星
赵玲玲,梁驰予,汪 杰,张新星
(南开大学化学学院,天津 300071)
鉴定化学反应中间体并解析其结构对于阐明反应机理至关重要。反应中间体通常具有活性高、寿命短、难以分离等特点,需要使用化学方法捕获后进行表征,或使用原位方法从反应混合物中直接识别中间体的特征信号,这对分析方法的特异性和样品的兼容性提出了更高要求。质谱(MS)依据离子的质荷比(m/z)确定样品成分,能够全面获得反应体系中底物、中间体和产物的信息,具有分辨率高、响应速度快、灵敏性好等优势,非常适用于中间体的检测;得益于串联质谱(MS/MS)技术以及离子裂解技术,质谱还具有一定的结构分析能力;并且,随着大气压离子化(API)和敞开式离子化技术的发展,质谱能够兼容的样品形态更加丰富,制样过程进一步简化,甚至可以省略样品前处理步骤直接测定反应体系,最大程度地维持反应体系原貌,保持中间体信息[1-3]。基于这些优势,质谱技术越来越多地用于化学反应监测与中间体鉴定[4-9],如:1) 监测Claisen重排[10-11]、Smiles重排[12]、串联有机催化反应[13-14]等小分子有机反应并鉴定重要中间体;2) 醇氧化和乙酸的选择性分解[15]、碳-氢/碳-碳键活化[16]、烯烃复分解[17-18]等过渡金属介导的反应中配合物中间体的鉴定;3) 电化学反应的质谱监测[19-22];4) 蛋白质组装过程的中间体[23-24]、杂原子-酶共价键合不稳定中间体[25-26]的鉴定;5) 在原子水平上实时监测单个金原子向银纳米团簇的动态团簇内扩散的过程[27]等。
在开发基于喷雾的敞开式离子化方法过程中,研究者们发现,细小的雾滴由于具有巨大的比表面积,将受到界面效应的显著影响,从而表现出独特的反应性质。2011年,Girod等[28]利用解吸电喷雾质谱(DESI-MS)对可的松等甾酮和肼(Girard T)的成腙反应进行监测,首次报道了微液滴体系中的反应加速现象,拉开了微液滴领域研究的序幕。后续研究表明,水微液滴除了能够加速反应2~6个数量级外[29-33],还能够触发自发的氧化还原反应[34-39]。微液滴表面的特殊环境,包括极端的酸性环境[28,31,40-42]、强大的界面电场[43-45],以及在电场作用下产生的丰富的羟基自由基和水合电子[35-37,46-48],均对微液滴的独特性质具有重要贡献。这种特殊环境能够稳定许多高活性、短寿命中间体,使它们能够被在线质谱捕获、检测[48-53]。
使用质谱表征喷雾形式的微液滴体系时,微液滴既是离子化载体,又充当反应容器;相应地,质谱条件不再仅是检测条件,也将作为反应条件,在很大程度上影响反应过程,甚至导致副产物的生成。最显著的影响因素集中在质谱的大气压接口处,Page等[54]考察了进样毛细管长度对离子传输效率的影响及分析结果可能的偏差;Banerjee等[55]报道了微液滴反应会受到进样毛细管温度的影响,在高温下,液滴蒸发带来的冷却效应和喷射出的离子受到的加热效应互相竞争,对不同反应有着不同影响,表现为加速或抑制;Venter等[56]在使用DESI-MS分析蛋白质的过程中发现,管透镜电压(tube lens offset)这一参数的高低对蛋白质的相对信号强度具有重要影响。因此,进行微液滴实验时,需要充分考虑仪器参数的影响,在研究反应机理和捕获中间体时,应当更加谨慎。
近期,Banerjee课题组[50-51]使用DESI-MS监测水微液滴体系中的消除、取代、氧化等多种反应,观察到高活性的碳正离子中间体。此前,相关研究表明,成腙反应[28]、Pomeranz-Fritsch异喹啉合成反应[42]等需要强酸催化的反应能够在不添加外来酸的微液滴中以极高的速度进行,证实了微液滴表面存在极端的酸性环境。基于这一现象,参考Olah等[57-58]使用超强酸体系捕获烷基碳正离子的开创性研究,Banerjee等[50]推测他们观察到的碳正离子是由微液滴表面极端酸性环境捕获得到的。商用电喷雾离子源(ESI)的喷雾距离较短,且在气流的辅助下快速脱除溶剂,可在较短的时间内将样品离子化,能够淬灭反应体系,排除微液滴界面效应的影响[32-33,59]。本工作拟使用ESI-MS测定上述研究涉及的一系列前体物质溶液,观察在特定仪器参数下是否生成碳正离子,并通过调整进样毛细管温度及管透镜电压分析碳正离子的来源。
1 实验部分
1.1 主要仪器与试剂
LTQ-XL线性离子阱质谱仪:美国Thermo Fisher Scientific公司产品,配有ESI源和注射泵,以及Xcalibur数据处理系统。
1-金刚烷胺盐酸盐(纯度99%):北京百灵威科技有限公司产品;2-金刚烷胺盐酸盐(纯度98%):Sigma-Aldrich(上海)贸易有限公司产品;2-氨基降冰片烷胺盐酸盐(纯度99%)、叔丁胺(纯度98%)、胆固醇(纯度99%)、叔丁醇(纯度≥99.5%)、1-溴金刚烷(纯度>97%):上海麦克林生化科技有限公司产品;外-降冰片(纯度98%):东京化成工业株式会社产品;4-叔丁基环己醇(纯度98%):上海迈瑞尔生化科技有限公司产品;1-氯金刚烷(纯度98%):上海浩鸿生物医药科技有限公司产品。
甲醇(色谱级):上海阿拉丁生化科技股份有限公司产品;超纯水:由Purelab Quest超纯水系统制备,英国Elga LabWater公司产品;高纯氮气:液化空气(天津)有限公司产品。
1.2 实验条件
1.2.1溶液配制 首先用甲醇溶解各待测物,再用超纯水稀释至100 μmol/L,备用。
1.2.2电喷雾质谱测试条件 喷雾气压强69 kPa,喷雾电压4.5 kV,毛细管电压0 V,毛细管温度275 ℃,管透镜电压0 V或140 V,进样速度15 μL/min。
2 结果与讨论
2.1 毛细管温度和管透镜电压共同影响碳正离子的生成
2.1.1桥头碳正离子的生成 为探究毛细管温度以及管透镜电压对中间体检测的影响,首先使用ESI-MS表征1-金刚烷胺盐酸盐溶液,结果示于图1。当毛细管温度为275 ℃、管透镜电压为140 V时,m/z152、135离子的信号同时出现,分别是质子化的1-金刚烷胺和1-金刚烷基碳正离子,示于图1a;保持毛细管温度不变、关闭管透镜电压(图1b),或保持管透镜电压不变、降低毛细管温度至45 ℃(图1c)时,谱图中均只出现1-金刚烷胺离子m/z152峰,而观察不到1-金刚烷基碳正离子。对比这3组质谱结果可以发现,只有在毛细管高温且施加管透镜电压的条件下,谱图中才会出现碳正离子信号。分别对上述条件下的1-金刚烷胺离子(m/z152)进行碰撞诱导裂解(CID)实验,均产生了1-金刚烷基碳正离子m/z135,示于图1d,证实碳正离子可以由碎裂得到(中性丢失17 u,对应NH3)。结合以上结果,本研究推测高温和管透镜的共同作用将引发1-金刚烷胺离子的源内裂解,产生桥头碳正离子。

注:a.毛细管温度275 ℃,管透镜电压140 V;b.毛细管温度275 ℃,管透镜电压0 V;c.毛细管温度45 ℃,管透镜电压140 V图1 1-金刚烷胺盐酸盐溶液的质谱图(a~c)以及m/z 152的二级质谱图(d)Fig.1 Mass spectra of 1-adamantane hydrochloride (a-c) and MS/MS spectrum of m/z 152 cations (d)
对2-金刚烷胺盐酸盐溶液进行了相同的实验,结果表明,在毛细管高温和管透镜电压的共同作用下,才能在谱图中观察到碎裂生成的碳正离子,示于图2。2-金刚烷基正离子的稳定性比1-金刚烷基正离子差,且由于其二面角接近90°,受空间结构的限制,很难发生重排。图2a中碳正离子的相对丰度显著低于图1a,该现象与这2种碳正离子的稳定性关系一致。

注:a.毛细管温度275 ℃,管透镜电压140 V;b.毛细管温度275 ℃,管透镜电压0 V;c.毛细管温度45 ℃,管透镜电压140 V图2 2-金刚烷胺盐酸盐溶液的质谱图(a~c)以及m/z 152的二级质谱图(d)Fig.2 Mass spectra of 2-adamantane hydrochloride (a-c) and MS/MS spectrum of m/z 152 cations (d)
除金刚烷胺外,卤代金刚烷也能够作为金刚烷基碳正离子的前体。使用ESI-MS分别表征1-溴金刚烷和1-氯金刚烷,结果示于图3。当毛细管温度275 ℃、管透镜电压140 V时,出现较强的m/z135峰信号,推测为1-金刚烷基碳正离子。在该条件下,溴/氯代金刚烷的碳-卤键发生异裂,溴、氯以负离子形式离去,生成碳正离子。降低毛细管温度或关闭管透镜电压时,正离子模式下仅能观察到较弱的金刚烷基碳正离子信号,进一步表明这2个仪器参数对碳正离子的生成有着重要影响。

图3 1-溴金刚烷(a)和1-氯金刚烷(b)的ESI-MS谱图Fig.3 ESI-MS spectra of 1-bromo adamantane (a) and 1-chloride adamantane (b)
2.1.2非经典碳正离子的生成 非经典碳正离子(nonclassical carbocations)通常含有三中心二电子键,通过σ键参与等方式稳定正电荷中心,比对应的孤立碳正离子形式的稳定性更高[60-62],其中,2-降冰片基正离子是一种具有代表性的非经典碳正离子。本研究以2-氨基降冰片烷胺盐酸盐水溶液作为前体物种,采用ESI-MS检测可能的非经典碳正离子,结果示于图4。与前述现象相似,在毛细管高温及管透镜电压的共同作用下,样品分子能够碎裂得到目标碳正离子,并以非经典形式存在,即谱图中的m/z95峰,示于图4a;当毛细管温度降至45 ℃或关闭管透镜电压后,谱图中仅能观察到m/z112峰,即2-氨基降冰片烷胺正离子,示于图4b,4c;CID实验证明了母离子碎裂生成非经典碳正离子的可能性,示于图4d。

注:a.毛细管温度275 ℃,管透镜电压140 V;b.毛细管温度275 ℃,管透镜电压0 V;c.毛细管温度45 ℃,管透镜电压140 V图4 2-氨基降冰片烷盐酸盐溶液的质谱图(a~c)以及m/z 112的二级质谱图(d)Fig.4 Mass spectra of 2-aminonorbornane hydrochloride (a-c) and MS/MS spectrum of m/z 112 cations (d)
2.1.3叔碳正离子的推测 采用ESI-MS表征100 μmol/L叔丁胺溶液,结果示于图5。当调节毛细管温度为275 ℃、管透镜电压为140 V时,除观察到m/z74对应的叔丁胺正离子外,还观察到m/z57对应的叔丁基正离子,示于图5a;当毛细管温度为45 ℃,或管透镜电压为0 V时,仅能观察到叔丁胺正离子(m/z74)。这再次说明在高温与较高管透镜电压的共同作用下,前体物种易发生源内裂解得到碳正离子。
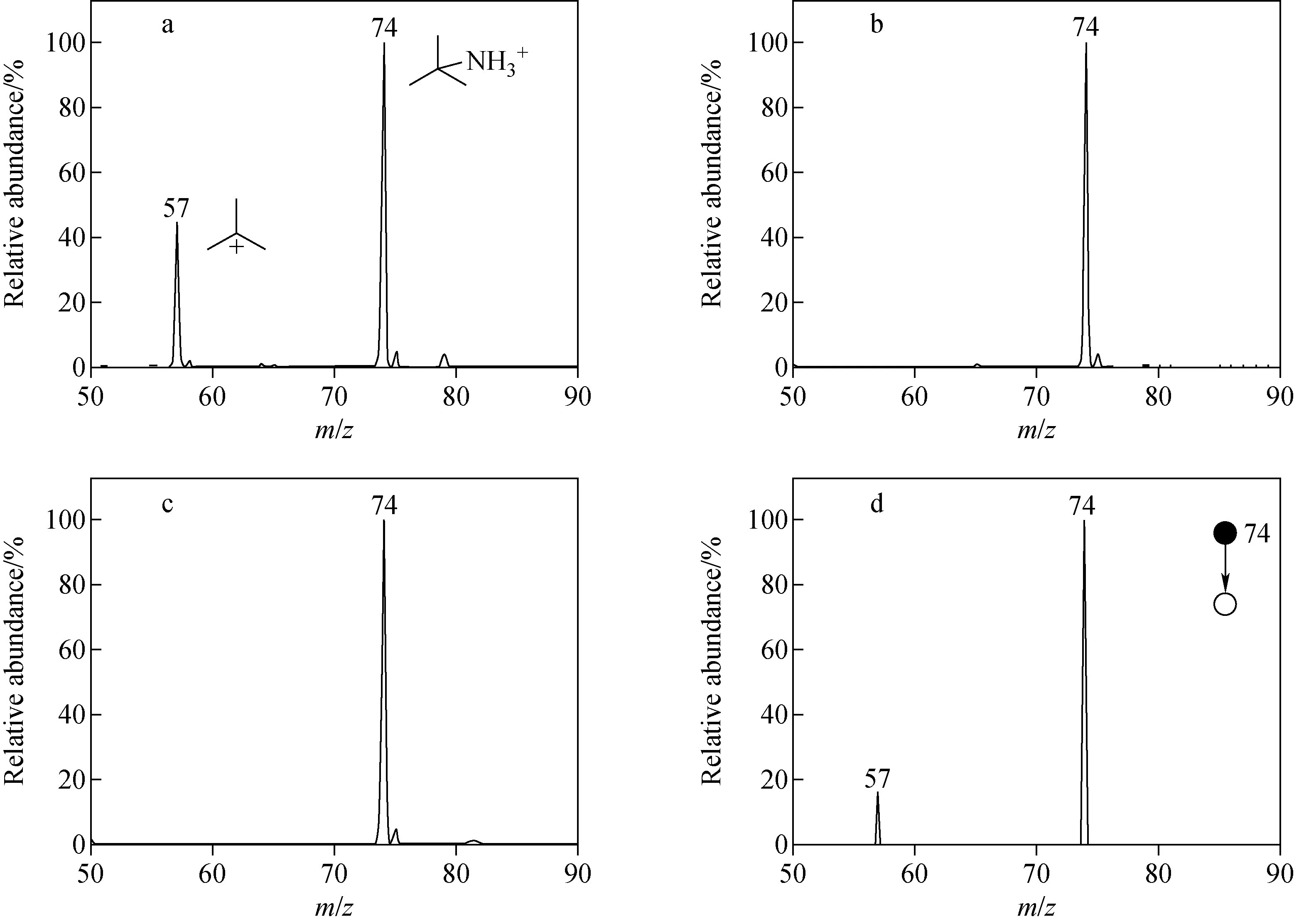
注:a.毛细管温度275 ℃,管透镜电压140 V;b.毛细管温度275 ℃,管透镜电压0 V;c.毛细管温度45 ℃,管透镜电压140 V图5 叔丁胺溶液的质谱图(a~c)以及m/z 74的二级质谱图(d)Fig.5 Mass spectra of tert-butylamine (a-c) and MS/MS spectrum of m/z 74 cations (d)
2.1.4含羟基化合物作为碳正离子前体 使用ESI-MS检测胆固醇、外-降冰片、4-叔丁基环己醇、叔丁醇等含羟基物质的溶液,当同时存在较高的进样毛细管温度和管透镜电压这2个条件时,这些物质均能够形成对应的碳正离子,推测可能经历了质子化后脱水的过程,没有观察到前体分子的羟基质子化后形成的离子,示于图6。去除高温或管透镜电压的条件后,则无法观察到碎裂形成的碳正离子,也观察不到质子化的前体分子。其中,胆固醇对应的碳正离子可能发生了重排,形成了更稳定的烯丙基碳正离子,示于图6a。
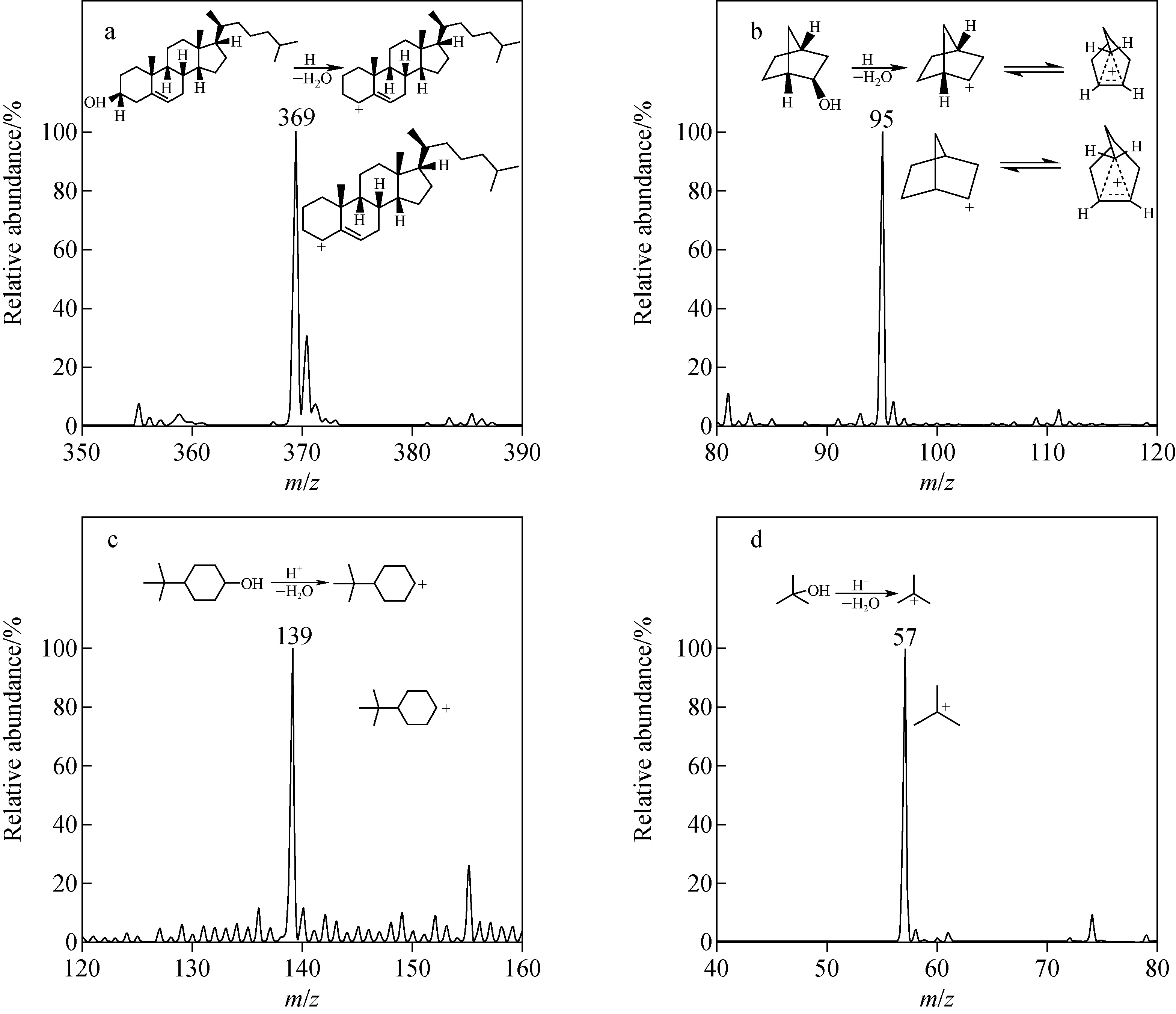
图6 毛细管温度275 ℃、管透镜电压140 V时,100 μmol/L胆固醇(a)、外-降冰片(b)、4-叔丁基环己醇(c)、叔丁醇(d)溶液的电喷雾质谱图Fig.6 ESI-MS spectra of 100 μmol/L cholesterol (a), exo-2-norbornol (b), 4-tert-butylcyclohexanol (c) and tert-butanol (d) at the capillary temperature of 275 ℃ and the tube lens voltage of 140 V
2.2 管透镜电压引发源内裂解
电喷雾电离等大气压电离方法在常压下产生离子,而质量分析器处于高真空环境,需要通过大气压接口实现离子的传输。在通过毛细管、小孔等传输方式限制进气量的同时,许多离子随气体一起被真空系统抽走;同时,受离子电荷排斥的影响,离子传输效率将非常低。因此,需要使用离子光学系统辅助离子传输,如采用静电透镜、离子漏斗等部件对离子聚焦[63]。LTQ-XL质谱仪采用多级差分真空系统[64],管透镜(tube lens)和撇渣器(skimmer)被设置在第1级真空(~133 Pa)到第2级真空(~0.133 Pa)的入口处,示于图7。施加合适的管透镜电压能够保证更多离子进入锥孔,提高离子传输效率。然而,该区域的气体密度较高,在电压的影响下,极有可能发生气体-离子反应,引发离子的源内裂解[65]。

注:a摘自LTQ-XL仪器硬件手册图7 LTQ-XL质谱大气接口结构(a)及差分真空系统示意图[64](b)Fig.7 Schematic diagrams of atmosphere pressure interface (a) and differential pumping stages[64] (b) on LTQ-XL spectrometer
Garrett等[66]研究了四极杆离子阱质谱(QIT-MS)中质子化磷脂分子及钠离子加和磷脂分子的解离,分别利用脆弱离子在进样毛细管温度诱导下发生热解离(TID)和管透镜电压诱导碎裂的现象,评估了多种离子的“脆性”。
Kulyk等[67]使用Velos Pro离子阱质谱仪研究了苄胺醇离子在离子化和传输过程中的碎裂现象,发现离子传输毛细管温度和离子光学部件S-透镜组(S-lens)的射频电压将显著影响碎裂产物离子的分布。Raji等[68]采用全因子实验设计的方法考察了离子传输部件电压、喷雾电压、离子传输毛细管温度、毛细管电压等仪器参数的主效应及它们之间的交互作用。其中,对于Thermo LCQ Deca XP质谱仪和Shimadzu LCMS 2010质谱仪,离子传输部件分别是管透镜和四极杆阵列(Q-array)。离子传输部件的电压对这2种质谱仪的检测结果均有重要影响,且对于Thermo LCQ Deca XP质谱仪而言,毛细管温度及其与管透镜电压的交互作用的影响均是主要因素。
2.3 碎片离子干扰中间体捕获研究和机理分析
使用微液滴体系捕获反应中间体时,需要考虑分析条件是否影响目标离子,以避免误将碎片离子归属为反应中间体。本课题组在研究微液滴中吡啶与碘甲烷的反应时,曾意外观察到m/z79正离子,数值与吡啶的分子质量相同。起初,将该离子归属为吡啶自由基正离子,但在后续的研究中发现,只有在高温和施加管透镜电压共同作用的条件下才能观察到m/z79。本工作表征了包含预期产物离子——甲基吡啶正离子的甲基吡啶鎓六氟磷酸盐,发现当高温和管透镜电压这2个条件共存时才能够观察到m/z79峰,由此确定该峰并不是奇特的反应中间体,而仅是由甲基化产物在特定分析条件下裂解得到的碎片离子。基于这一现象和上述讨论,我们认为在运用微液滴体系研究中间体时,尤其需要注意分析条件的影响,以免得到错误结论。
3 结论
本工作使用电喷雾质谱法分析了一系列碳正离子的前体分子,通过改变毛细管温度以及管透镜电压,发现在毛细管高温和管透镜电压共同作用下,前体物质会发生碎裂形成碳正离子。这一系列碳正离子的形成不需要微液滴提供的极端酸性条件,也并不是反应过程的活性中间体。此前,在本课题组关于微液滴条件下电子介导的氧化还原过程的综述[39]中分别提到了进样毛细管温度和离子光学部件对表征结果的不利影响,本工作进一步探究了这2个因素共同存在时对检测结果的重要影响,同时也证明了相关报道[50]结论的系统性错误。
质谱仪的分析参数繁多复杂,为达到理想的分析效果,往往需要协同调整多个离子光学系统的参数。在使用质谱监测反应或捕获中间体的过程中,这些参数可能会使飞行中的离子发生解离或重排。这些变化并非液滴内反应导致的,而是离子光学系统所加电压导致的。因此,在使用质谱进行反应机理研究,尤其是中间体捕获研究时,需要注意各分析条件及它们之间交互作用的影响,避免这些条件引起对化学反应机理研究的误判。
