低品位铜镍电镀污泥还原硫化熔炼低冰镍①
2024-01-20周兆安刘小文毛谙章李加兴
周兆安, 刘小文, 李 俊, 毛谙章, 李加兴
(1.广东飞南资源利用股份有限公司,广东 肇庆 526233; 2.广东省工业固废含铜污泥资源综合利用工程技术研究中心,广东 肇庆 526233)
铜镍电镀污泥来源于电镀行业,一般含有大量的重金属(Ni、Cu、Cr、Fe、Zn、Pb、Cd 等),且含量远远超过国家环境标准,因此被列为危险废弃物(HW17)[1]。电镀污泥中的重金属化学性质不稳定,容易造成二次污染[1-2],但同时电镀污泥也极具回收价值,是金属资源的一种重要补充。
目前,铜镍电镀污泥资源化处理主要分为火法工艺和湿法工艺。 常规火法工艺主要有铜镍污泥直接熔炼法[3-5]、矿化-选矿法[6-7]、焙烧-浸出法[2,8]等。 常规湿法工艺主要有酸浸法[9-11]和氨浸法[12]等。 铜镍电镀污泥还原硫化熔炼法[5]是将HW17 类铜镍含量较低的含镍危险废物经过预处理后,经高温还原硫化熔炼生产低冰镍,该方法具有原料适应性好、铜镍及贵金属回收率高、产品可直接与新能源产业衔接等优点,但在危险废物处理领域针对该工艺的基础理论研究薄弱,鲜有相关报道。 本文采用HSC Chemistry 6.0 热力学软件[13],研究了铜镍电镀污泥还原硫化熔炼低冰镍过程物相演变规律,分析了硫化熔炼过程的主要影响因素,为铜镍电镀污泥还原硫化熔炼技术发展与生产实践提供理论指导。
1 实验原料
实验原料铜镍电镀污泥取自广东某环保公司。 原料先在80 ℃下干燥,再用密封式化验制样机(南昌永平化验设备有限公司,YP-400-1)细磨,筛分取-0.074 mm粒级物料待用。 铜镍电镀污泥化学组成见表1,其主要成分有CuO、NiO、Fe2O3、CaO、ZnO、Al2O3、SiO2和一些硫酸盐或硫化物,另有少量的MgO、Cr2O3等。

表1 铜镍电镀污泥化学组成(质量分数) %
2 研究方法
参考表1 中铜镍电镀污泥化学组成设定还原熔炼物料数据模型,利用HSC Chemistry 6.0 热力学软件,模拟铜镍电镀污泥还原硫化熔炼过程中主要金属的物相演变。 HSC Chemistry 软件Lpp-Diagrams 模块Me-S-O优势区域图可以清晰揭示物相的转变路径;使用HSC Chemistry 6.0 软件Equilibrium Compositions 模块数据库模拟计算物质稳定存在区域[13-14],得出体系多相反应平衡时的产物组成情况,再通过数据处理计算相关产物与温度、气氛等变量之间的对应关系,并绘制相关图表。
3 铜镍污泥还原硫化熔炼低冰镍理论分析
根据一般铜镍污泥中铜镍铁等元素的赋存状态特点[8],为了尽可能准确表达反应机理和简化复杂的冶金反应过程,用NiO、CuO 和Fe2O3来表示铜镍电镀污泥中Ni、Cu、Fe 的存在形式。
3.1 硫化熔炼过程物相转变路径
利用HSC Chemistry 软件Lpp-Diagrams 模块计算并绘制了1 250 ℃下Cu/Ni/Fe-O-S 优势区域图,如图1所示。 从Cu-O-S 优势区域图的计算数据可以得出,P(SO2)<1.01×105Pa、P(O2)<5.61×105Pa 时,铜氧化物转变历程为:CuO→Cu2O→Cu→Cu2S。 从Ni-O-S优势区域图中可得出,P(SO2)=1.26×104~1.01×105Pa、P(O2)<16.02 Pa 时,镍氧化物转变历程为:NiO→Ni3S2;P(SO2)<1.26×104Pa、P(O2)<7.94 × 10-3Pa时,镍氧化物转变历程为:NiO→Ni→Ni3S2。 从Fe-O-S优势区域图中可得出,P(SO2)=3.37×102~1.01×105Pa、P(O2)=2.55×10-5~3.30×103Pa 时,铁氧化物转变途径为:Fe2O3→Fe3O4→FeS;P(SO2)=1.02 ~3.37×102Pa、P(O2)=5.33×10-7~3.30×103Pa 时,铁氧化物转变途径为:Fe2O3→Fe3O4→FeO→FeS;P(SO2)<1.02 Pa、P(O2)<3.30×103Pa 时,铁氧化物转变历程为:Fe2O3→Fe3O4→FeO→Fe→FeS。
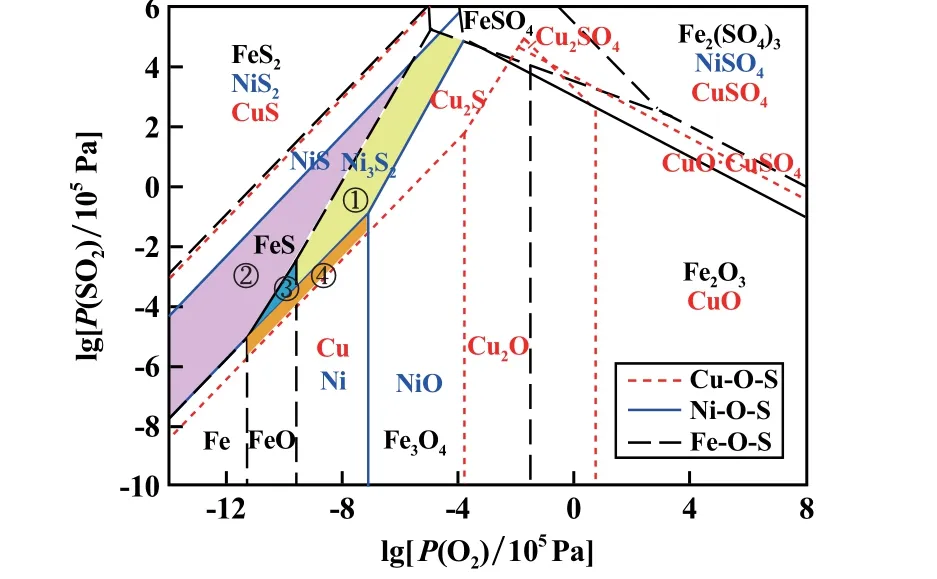
图1 1 250 ℃下Cu/Ni/Fe-O-S 优势区域图
图1 中①、②、③、④区域分别表示Cu2S+Ni3S2+Fe3O4、Cu2S+Ni3S2+FeS、Cu2S+Ni3S2+FeO、Cu2S+Ni+Fe3O4,若想实现铜镍电镀污泥中CuO、NiO 的选择性硫化回收,需要将熔炼氧分压和硫分压控制在①、②、③、④区域内,优选②、③区域,因为熔炼过程中产生过多Fe3O4是不利的[15]。 从图1 也可得到金属亲硫性强弱顺序为:Cu>Ni≈Fe,金属亲氧性强弱顺序为:Fe>Ni>Cu。
3.2 硫化熔炼过程还原硫化反应
在工业生产中,铜镍污泥还原硫化过程温度可控制在1 423~1 623 K(1 150 ~1 350 ℃),采用炭基还原剂,以硫酸钙为硫化剂,选用CaO-FeOx-SiO2渣系进行高温还原熔炼。 熔炼产物主要有炉渣和铜镍锍,由图1可知,铜镍电镀污泥中主要化合物在还原硫化熔炼过程中可能发生的化学反应为:
由反应式(4)~(6)可以看出,一定温度下的还原硫化过程主要反应热力学平衡常数均与P(CO2)/P(CO)、P(SO2)相关,同时硫化物和合金的比例又与硫化剂的用量相关。 因此,整个还原硫化过程和产物情况主要由反应温度T、反应气氛P(CO2)/P(CO)和硫化剂用量决定。
3.3 硫化熔炼过程热力学计算
利用HSC Chemistry 软件的Equilibrium Compositions模块,计算不同反应温度、硫化剂用量和熔炼气氛下的多相反应平衡情况,再进行数据处理,得出单因素的结果。
计算条件为:参考表1 数据,设定铜镍污泥铜镍品位分别为6%和4%,预配硅铁钙渣型组成为Fe ∶SiO2∶CaO=15 ∶30 ∶28(质量比),模拟计算参数设定值见表2。
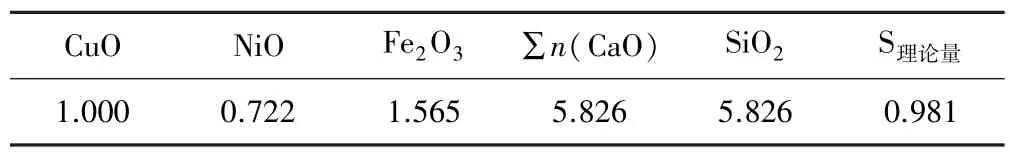
表2 模拟计算参数设定值 kmol
基于表2 数据,通过调节CaSO4和CaO 的参数变化,可以模拟计算不同硫化剂用量(S实际用量/S理论量)条件,利用设定不同的CO 和CO2比例来模拟不同的还原反应气氛,最终利用HSC 软件计算得到反应平衡时产物的组成,并由此展开相关计算。 为了方便计算分析,作如下假设:①在计算产物组成时合金相、锍相和渣相之间互不相溶;②铜镍还原硫化过程中烟尘率较小,热力学计算过程中不考虑铜镍在烟尘中的损失;③预估渣铜、渣镍和铜镍金属回收率时仅将铜镍的所有氧化物形态算入渣中,不考虑硫化物相和合金相在渣中的溶解和物理夹带。
3.3.1 不同反应温度时的平衡组成及热力学计算
基于表2 参数,并设定n(CaSO4)=0.981 kmol,n(CaO)=4.845 kmol,S实际用量/S理论量=1.0,使用HSC Chemistry 软件Equilibrium Compositions 模块进行多相反应平衡模拟计算,选取反应平衡终点P(CO)/[P(CO)+P(CO2)]=50%,得出不同反应温度时的平衡组成结果如图2 所示。
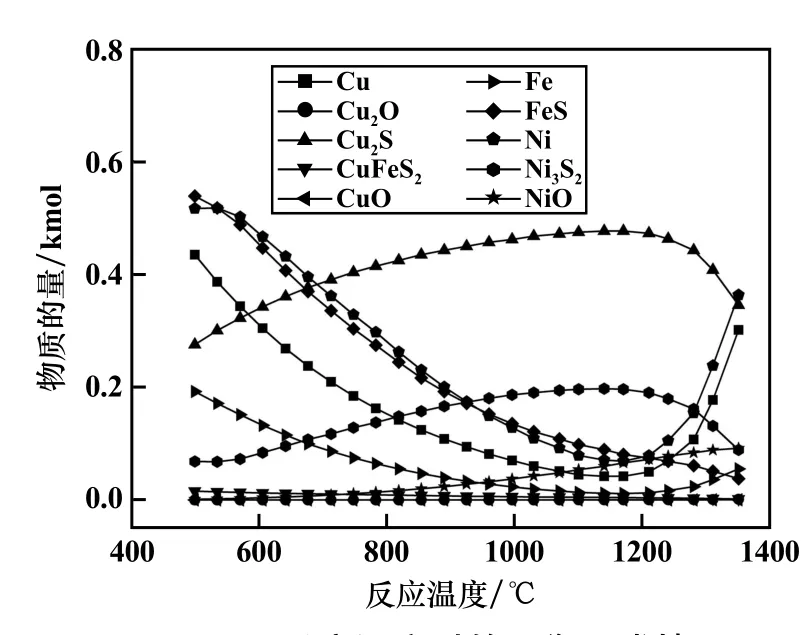
图2 不同反应温度时的平衡组成情况
由图2 可以看出,随着温度升高,NiO 含量增加,这不利于Ni 的回收,铜镍硫化物基本在1 200 ℃左右达到高峰值,随后金属相开始增加,硫化物相开始减少,锍相合金化开始加重。 由此可知,1 200 ℃时整体有利于获得低合金化的冰镍。 但如果兼顾冶炼过程的操作难易度和炉渣黏度,选择1 250 ℃更为合理。
3.3.2 不同反应气氛时的平衡组成及热力学计算
基于表2 参数,并设定T=1 250 ℃,n(CaSO4)=0.981 kmol,n(CaO)=4.845 kmol,S实际用量/S理论量=1.0,进行多相反应平衡模拟计算,得出不同反应气氛时的平衡组成结果如图3~5 所示。

图3 不同反应气氛时的铁物相分布和产物(合金+锍相)含铁量情况
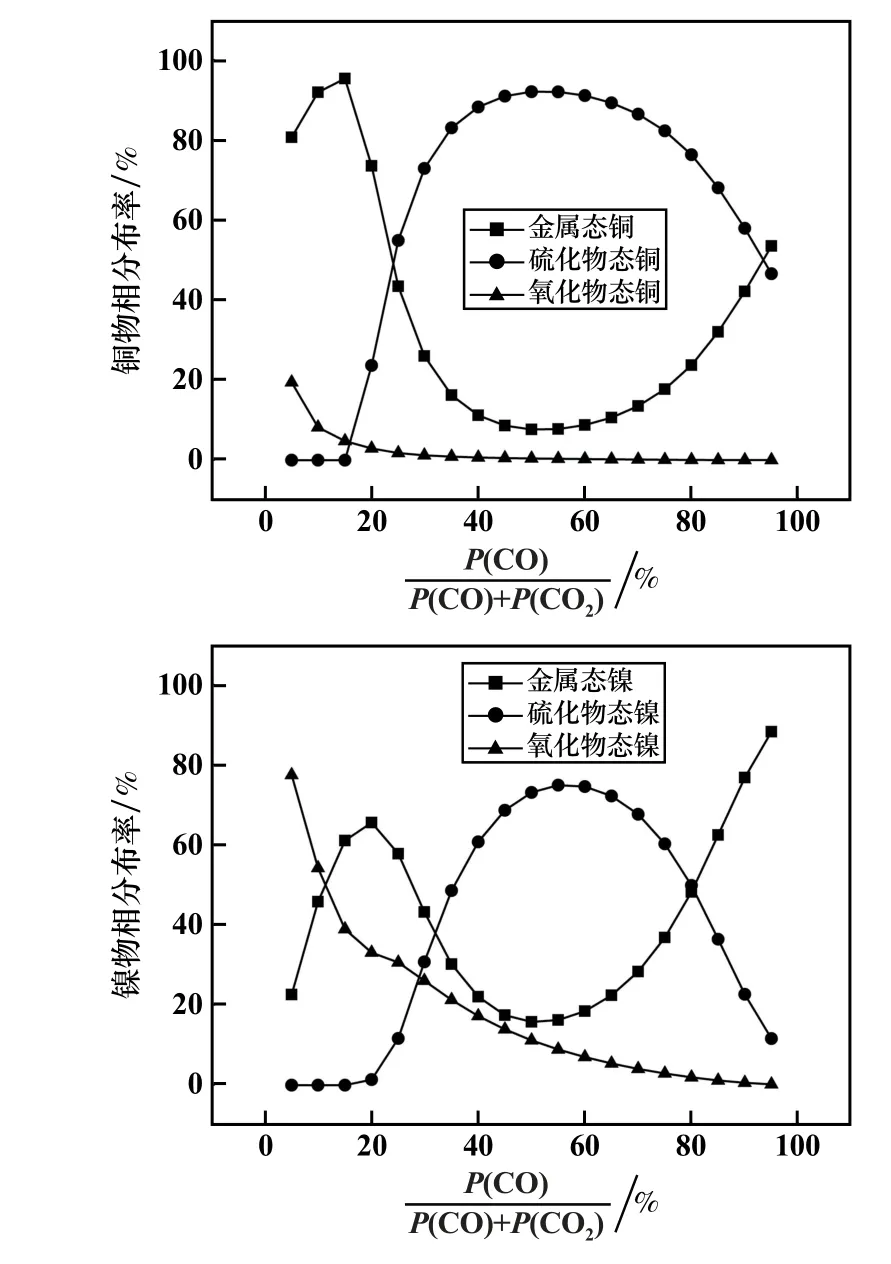
图4 不同反应气氛时铜、镍物相分布情况

图5 不同反应气氛时铜镍直收率及渣铜、渣镍情况
由上述理论计算结果可知,随着P(CO)/[P(CO)+P(CO2)]值升高,铁物相呈现氧化态物相逐渐减少、金属态和硫化物态物相逐渐增多的趋势,尤其是当P(CO)/[P(CO)+P(CO2)]≥80%之后。 随着P(CO)/[P(CO)+P(CO2)]值升高,铜和镍的物相均表现为金属相先增后减然后再增加,硫化物相则先增后减,氧化物相一直在减少,大的拐点分别发生在P(CO)/[P(CO)+P(CO2)]值10%~20%和50%左右。P(CO)/[P(CO)+P(CO2)]值为10% ~20%是获得金属态产物最好的区域,P(CO)/[P(CO)+P(CO2)]值50%左右可以获得低合金化的锍相。
此外,随着P(CO)/[P(CO)+P(CO2)]值升高,渣铜渣镍进一步降低,对应的金属直收率逐渐提高,当P(CO)/[P(CO)+P(CO2)]为50%左右时,预期渣铜和渣镍分别为0.029%和0.525%,此时铜和镍直收率分别为99.58%和88.83%。 随着P(CO)/[P(CO)+P(CO2)]值进一步提高,将会有大量铁进入金属相或锍相,导致产物中铁含量急剧升高。
综上所述,为了获得低合金化的铜镍锍,宜选择P(CO)/[P(CO)+P(CO2)]为50%左右。
3.3.3 不同硫化剂用量时的平衡组成及热力学计算
基于表2 参数,并设定T=1 250 ℃,平衡点P(CO)/[P(CO)+P(CO2)]=50%,得出不同硫化剂用量时的平衡组成结果如图6~8 所示。

图6 不同硫化剂用量时的平衡组成和产物(合金+锍相)含铁量情况
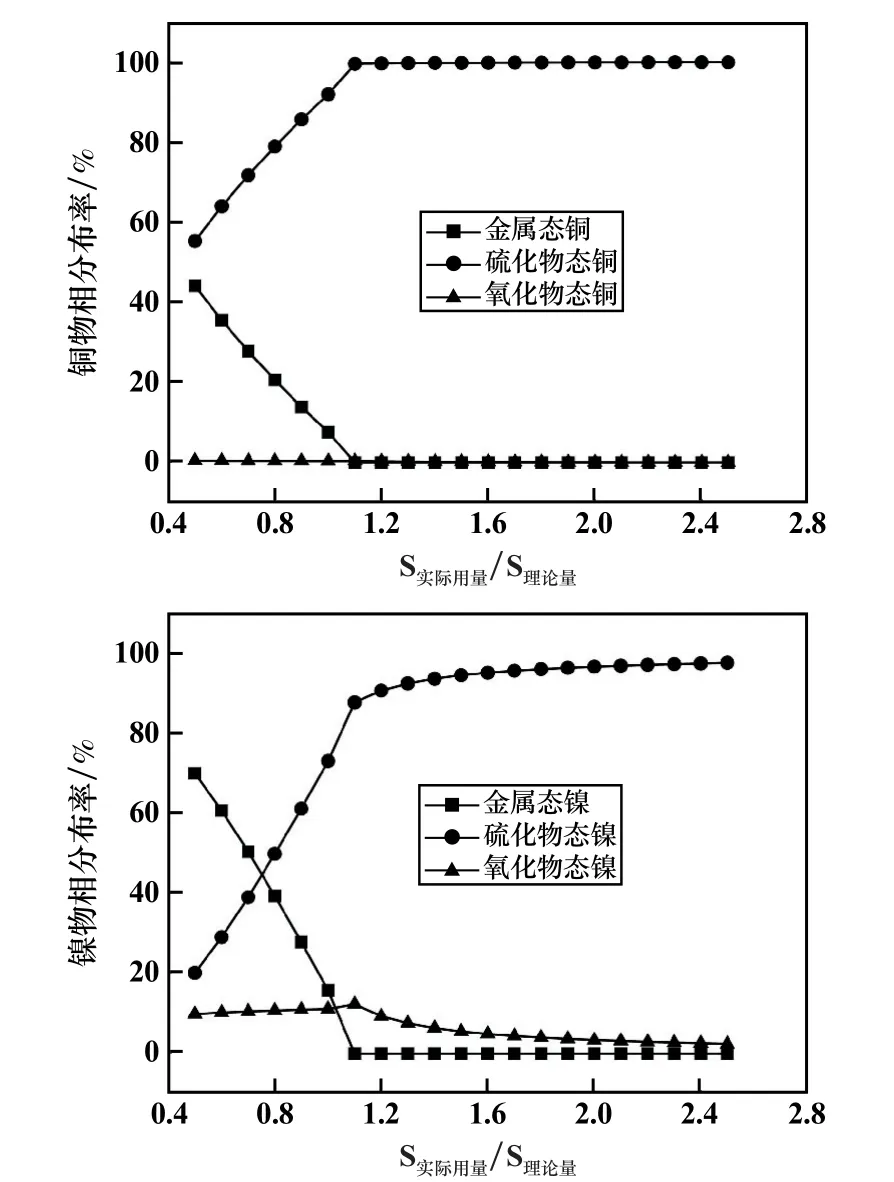
图7 不同硫化剂用量时铜、镍物相分布情况
由上述理论计算结果不难看出,S实际用量/S理论量≤1时,随着S实际用量/S理论量不断增加,铜镍硫化物相比例几乎以线性方式快速增加,而金属相比例则呈近似负线性关系降低;S实际用量/S理论量>1 后,铜镍物相比例几乎不再变化。 铁的物相比例在S实际用量/S理论量≤1 时变化幅度微弱,S实际用量/S理论量>1 后,铁的硫化物相增加,与此同时,氧化态的铁比例降低。 这主要是因为:S实际用量/S理论量≤1 时,硫的总量不足,优先硫化铜镍,S实际用量/S理论量>1 之后,铜镍硫化几乎完成,过量的硫主要用于硫化铁,进而导致铜镍锍中的铁含量升高。
另外,由图8 可以看出,硫的用量直接关系到铜镍直收以及渣中铜镍的品位,尤其是对镍的影响较大,通过加入足量的硫可以将渣中铜镍降低到较低水平,使渣不具有选矿的经济性,进而采用水淬法处理炉渣,并有望使其达到《固体废物玻璃化处理产物技术要求》(GB/T 41015—2021)[16]中有关玻璃态产物的处理要求。 综上所述,优选S实际用量/S理论量≥1.8,可使渣中铜镍品位均低于0.2%。

图8 不同硫化剂用量时的铜镍直收率及渣铜、渣镍情况
3.3.4 热力学计算的优化还原硫化条件
在铜镍电镀污泥铜镍品位分别为6%和4%时,经热力学计算,在1 250 ℃下,以CaSO4为硫化剂,配料调节S实际用量/S理论量=2.0,控制熔炼平衡时P(CO)/[P(CO)+P(CO2)]=50%,熔炼产出低冰镍的品位(Cu+Ni)为57.2%,熔炼渣中的铜和镍品位均低于0.2%,铜和镍直收率分别达到99%和96%以上,固硫率77.20%,具体工艺技术指标如表3 所示。

表3 熔炼工艺技术指标
4 生产实践
目前,含有价金属类危险废物资源化处理领域主要采用还原熔炼炉和熔池熔炼炉生产技术,其中还原熔炼炉借鉴传统冶金鼓风炉,因其物料适应性强、操作简易、设备投资少等特点,在含铜危险废物火法处理领域得到广泛应用,鼓风炉还原熔炼技术在铅、铜、锌和镍等有色冶金领域成熟应用,为其在铜镍电镀污泥还原硫化熔炼低冰镍提供了借鉴经验。
铜镍电镀污泥还原硫化熔炼低冰镍模型如图9 所示。 铜镍电镀污泥经预处理成块料,再与还原剂、硫化剂和造渣剂一起投入熔炼炉内,控制体系的氧分压和硫分压位于低冰镍稳定区域,在高温下经还原硫化熔炼生产低冰镍和炉渣。 某公司近期完成了铜镍电镀污泥还原硫化熔炼生产低冰镍的技术改造,现已投产运行,其生产过程如图10 所示,产出的低冰镍样品组成如表4 所示,低冰镍的品位(Cu+Ni)达43.32%,Cu/Ni质量比为1.334。 炉渣(水淬渣)组成及理化性质如表5 所示,炉渣中铜镍含量均低于0.2%,水淬渣满足GB/T 41015—2021[16]中玻璃态物质的技术要求。
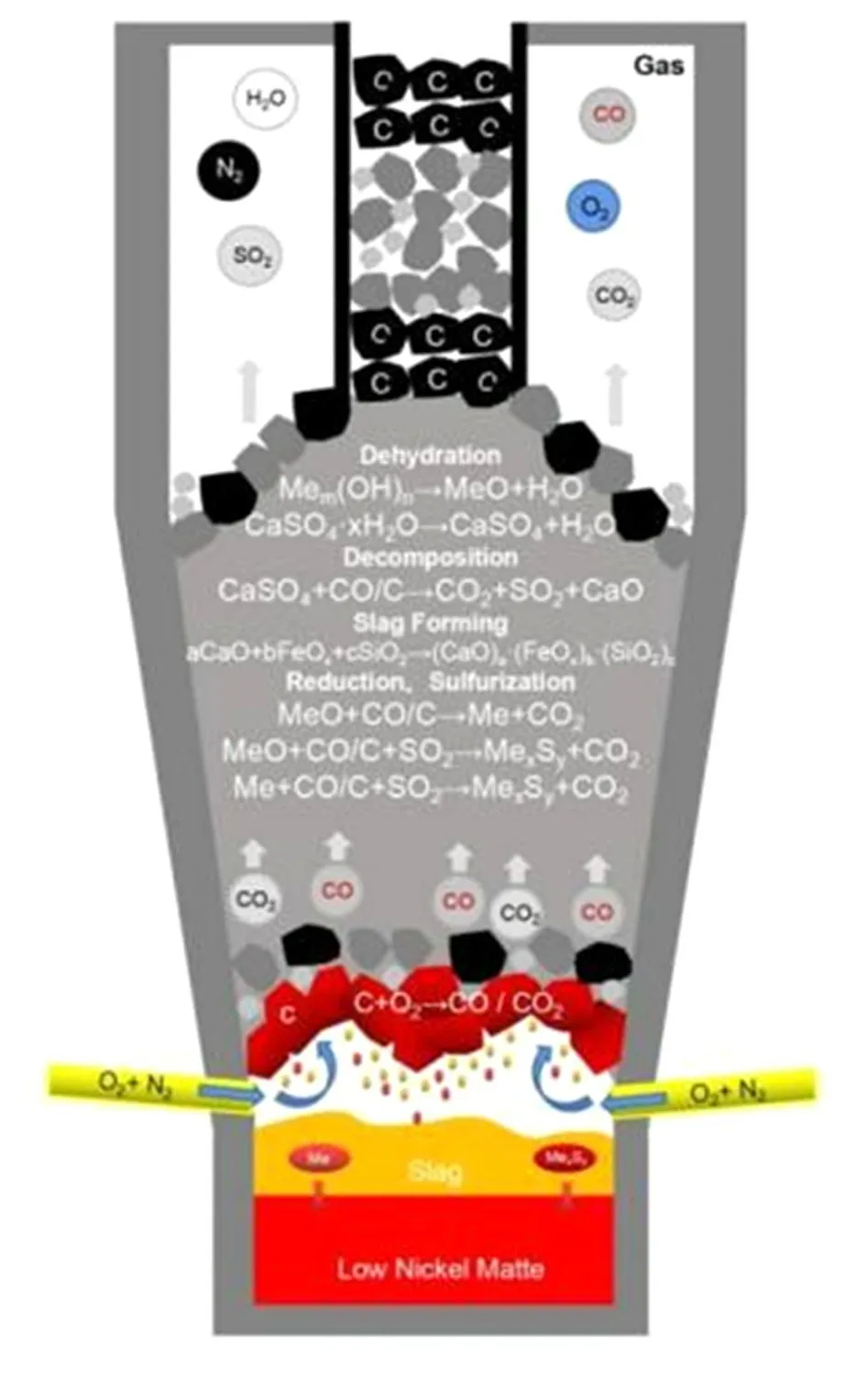
图9 铜镍污泥硫化熔炼反应模型

图10 铜镍电镀污泥硫化熔炼生产过程
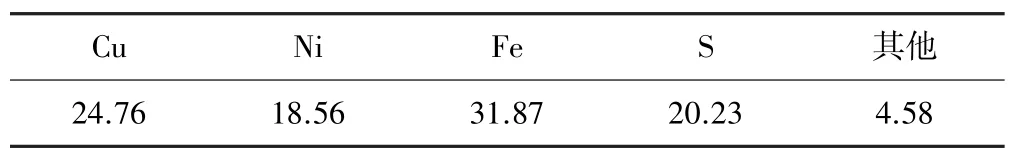
表4 低冰镍主要化学组成(质量分数) %
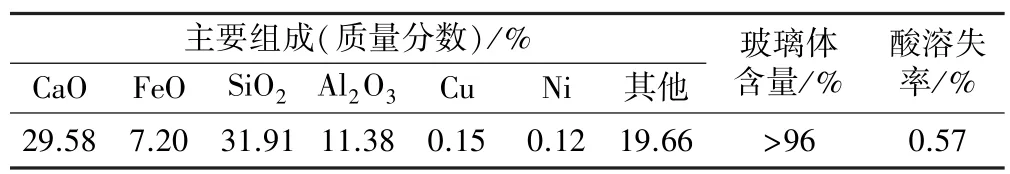
表5 炉渣(水淬渣)主要组成及理化指标
铜镍电镀污泥还原硫化熔炼低冰镍的成功工业化应用打通了从HW17 类危险废物到新能源电池原料的新技术路径,相较于常规湿法回收工艺[17-19],具有铜镍和贵金属回收率高、处理量大、处理成本低,对原料适应性强,无废水、废盐产出等诸多优点,具有显著的技术优势。
5 结 论
1) 铜镍电镀污泥还原硫化熔炼生产低冰镍过程中,铜镍污泥中铜氧化物转变历程为:CuO→Cu2O→Cu→Cu2S,镍氧化物转变历程为:NiO→Ni3S2或NiO→Ni→Ni3S2,铁氧化物转变途径为:Fe2O3→Fe3O4→FeS,Fe2O3→Fe3O4→FeO→FeS 或Fe2O3→Fe3O4→FeO→Fe→FeS。 金属亲硫性强弱顺序:Cu>Ni≈Fe;金属亲氧性强弱顺序:Fe>Ni>Cu。
2) 经热力学理论计算,铜镍污泥还原硫化熔炼的优化工艺条件为:当铜镍含量分别为6%和4%时,采用硫石膏作为硫化剂,S实际用量/S理论量=2.0,熔炼气氛P(CO)/[P(CO)+P(CO2)] =50%,此时产出低冰镍的品位(Cu+Ni)可达57.2%,铜、镍在渣中品位均低于0.2%,铜和镍直收率分别可以达到99%和96%以上,固硫率77.20%。
3) 铜镍电镀污泥还原硫化熔炼生产低冰镍的生产实践中,渣铜渣镍接近理论值,该工艺的产业化应用打通了从HW17 类危险废物到新能源材料的新技术路径,相较于传统工艺,具有显著的技术优势。
